| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| Other Sizes |
|

| 靶点 |
EGFR L858R (IC50 = 0.4 nM); EGFR (IC50 = 0.5 nM); EGFR L858R/T790M (IC50 = 10 nM); HER2 (IC50 = 14 nM); HER3
- EGFR (wild-type):Afatinib (BIBW2992) inhibits wild-type EGFR with an IC₅₀ of 0.5 nM. [1] - EGFR (L858R mutant):Exhibits inhibitory activity against the L858R mutant with an IC₅₀ of 0.4 nM. [1] - EGFR (exon 19 deletion mutant):Inhibits exon 19 deletion mutant EGFR with an IC₅₀ of 0.3 nM. [1] - HER2 (ErbB2):Inhibits HER2 kinase activity with an IC₅₀ of 14 nM. [1] Afatinib (BIBW2992) Dimaleate inhibits EGFR (IC₅₀ = 0.5 nM), HER2 (IC₅₀ = 14 nM), and HER4 (IC₅₀ = 1 nM) tyrosine kinases [1] Afatinib (BIBW2992) Dimaleate shows inhibitory activity against EGFR T790M mutant (IC₅₀ = 10 nM) and wild-type EGFR (IC₅₀ = 0.4 nM) [2] |
|---|---|
| 体外研究 (In Vitro) |
- 抗增殖活性:afatinib在MTT实验中抑制EGFR突变型非小细胞肺癌(NSCLC)细胞系(HCC827、PC-9),IC₅₀为10–20 nM;抑制HER2+乳腺癌细胞(SK-BR-3),IC₅₀为30 nM。[1][2]
- 信号通路抑制:在HCC827细胞中,afatinib(50 nM,4小时)通过Western blot检测显示,EGFR(Tyr1068)、AKT(Ser473)和ERK1/2(Thr202/Tyr204)的磷酸化水平分别降低90%、85%和80%,同时下调cyclin D1并上调cleaved PARP,提示诱导凋亡。[1][2] - 与放疗协同作用:在头颈部鳞状细胞癌(HNSCC)细胞(SCC-25)中,afatinib(10 nM)增强放疗诱导的细胞杀伤,辐射敏感系数提高1.5倍。[3] BIBW2992 对野生型和突变型 EGFR 和 HER2 均显示出有效的活性。它针对 L858R EGFR 的效力与吉非替尼相似,但针对吉非替尼耐药的 L858R-T790M EGFR 双突变体的活性高出约 100 倍。 BIBW2992 对体内 EGFR 和 HER2 磷酸化表现出有效的作用。在所有测试的细胞类型中,例如表达 wt EGFR 的人表皮样癌细胞系 A431、转染 wt HER2 的鼠 NIH-3T3 细胞以及乳腺癌细胞系 BT,其与参考化合物(例如 Lapatinib 等)相比均具有优势-474和胃癌细胞系NCI-N87,表达内源性HER2。激酶测定:EGFR 激酶:每个 100 µL 酶反应包含 10 µL 抑制剂(溶于 50% Me2SO)、20 µL 底物溶液(200 mM HEPES pH 7.4、50 mM 醋酸镁、2.5 mg/mL 聚 (EY)、5 µg /mL bio-pEY) 和 20 µL 酶制剂。添加 50 µL 用 10 mM MgCl2 制成的 100 µM ATP 溶液开始酶促反应。测定在室温下进行 30 分钟,并通过添加 50 µL 终止溶液(20 mM HEPES pH 7.4 中的 250 mM EDTA)终止。将 100 µL 转移至链霉亲和素包被的微量滴定板,在室温下孵育 60 分钟后,用 200 µL 洗涤液(50 mM Tris,0.05% Tween20)洗涤板。将 100 µL 等份的 HRPO 标记的抗 PY 抗体 (PY20H Anti-Ptyr:HRP) 250 ng/mL 添加到孔中。孵育 60 分钟后,用 200 µL 洗涤液洗涤板 3 次。然后使用 100 µL TMB 过氧化物酶溶液(A:B= 1:1)对样品进行显色。 10分钟后停止反应。将板转移至 ELISA 读数器并在 OD450nm 处测量消光。 HER2-IC 酶:在存在或不存在连续抑制剂稀释的情况下(在 50% Me2SO 中进行)测定酶活性。每个 100 µL 反应液包含与 EGFR 激酶测定所述类似的成分,但添加了 1000 µM Na3VO4。添加 50 µL 500 µM ATP 溶液(用 10 mM 醋酸镁配制),开始酶促反应。设置酶的稀释度,使得磷酸盐掺入bio-pEY 与时间和酶量成线性关系。将酶制剂稀释在 20 mM HEPES pH 7.4、130 mM NaCl、0.05% Triton X-100、1 mM DTT 和 10% 甘油中。测定在室温下进行 30 分钟,并通过添加 50 µL 终止溶液终止。 Src 激酶测定:每个 100 µL 反应液含有 10 µL 抑制剂(溶于 50% Me2SO)、20 µL 酶制剂、20 µL 底物溶液(补充有 1000 µM Na3VO4)。添加 50 µL 用 10 mM 醋酸镁制成的 1000 µM ATP 溶液开始酶促反应。 BIRK 激酶测定:使用 250 mM Tris pH 7.4、10mM DTT、2.5 mg/mL 聚 (EY)、5 mg/mL 生物 pEY 作为底物溶液,并通过添加 50 µL 2 mM ATP 溶液启动酶反应由 8 mM MnCl2、20 mM 乙酸镁制成。 VEGF2 和 HGFR 激酶测定:测定在室温下进行 20 分钟,并通过添加 10 µL 5% H3PO4 终止。然后使用 96 孔过滤器伴侣通用收集器将沉淀物捕获到 GF/B 过滤器上。彻底清洗后,将滤板在 50°C 下干燥 1 小时,密封并使用 TopCount™ 或 Microbeta b counter™ 进行闪烁计数来确定掺入的放射性。 细胞测定:将 1 × 104 个 NSCLC 细胞转移到每个孔中96 孔板并在无血清培养基中培养过夜,用于 EGFR 磷酸化测定。第二天添加 BIBW2992 后,将板在 37°C 下孵育 1 小时。 EGF 刺激使用 100 ng/mL 在室温下进行 10 分钟。用冰冷的 PBS 洗涤细胞,每孔用 120 μL HEPEX 缓冲液提取,并在室温下摇动 1 小时。每孔全部 2 × 104 个细胞用于 HER2 磷酸化测定。链霉亲和素预包被板用封闭缓冲液中 1:100 稀释的抗 EGFR-生物素和 c-erb2/HER2 癌蛋白 Ab-5(克隆 N24)-生物素包被。然后将细胞提取物转移至抗体包被的孔中并在室温下孵育1小时。消光在 450 nm 处测量。 阿法替尼马来酸盐(BIBW2992)剂量依赖性抑制EGFR过表达的肿瘤细胞系增殖,包括A431细胞(IC₅₀=0.07μM)、HCC827细胞(EGFR 19外显子缺失,IC₅₀=0.01μM)和NCI-N87细胞(HER2过表达,IC₅₀=0.15μM)。浓度≥0.1μM时,可阻断这些细胞中EGFR/HER2磷酸化及下游信号(ERK1/2、Akt)[1] 阿法替尼马来酸盐(BIBW2992)诱导HCC827细胞凋亡,EC₅₀为0.02μM,上调切割型caspase-3和PARP的表达。对NCI-H1975细胞(EGFR T790M突变体)的克隆形成能力具有抑制作用,IC₅₀为0.2μM[2] 阿法替尼马来酸盐(BIBW2992)在体外增强非小细胞肺癌(NSCLC)细胞(A549)的放射敏感性。0.1μM阿法替尼与2Gy放疗联合使用,相比单独放疗,细胞死亡增加约50%[3] 阿法替尼马来酸盐(BIBW2992)在0.2μM浓度下,可分别抑制乳腺癌细胞(SK-BR-3)的迁移和侵袭约70%和65%,其机制与下调MMP-9表达有关[4] |
| 体内研究 (In Vivo) |
每日口服 20 mg/kg 的 BIBW2992 持续 25 天可导致肿瘤显着消退,累积治疗/对照肿瘤体积比(T/C 比)为 2%。通过组织切片的免疫组织化学染色证实 EGFR 和 AKT 磷酸化的减少。因此,与拉帕替尼和来那替尼一样,BIBW2992是下一代酪氨酸激酶抑制剂(TKI),可不可逆地抑制人表皮生长因子受体2(Her2)和表皮生长因子受体(EGFR)激酶。 BIBW2992 不仅能有效对抗厄洛替尼或吉非替尼等第一代 TKI 靶向的 EGFR 突变,还能对抗那些对这些标准疗法不敏感的患者。
- NSCLC异种移植模型肿瘤抑制:裸鼠HCC827和PC-9异种移植模型中,口服afatinib(20 mg/kg/天)21天后肿瘤体积减少70–80%,肿瘤组织中Ki-67和p-EGFR表达降低。[1][2] - HNSCC模型与放疗协同作用:SCC-25异种移植模型中,afatinib(10 mg/kg/天)联合放疗(6 Gy)28天后肿瘤体积减少90%,显著优于单药治疗(50–60%抑制)。[3] - 乳腺癌模型药效学效应:SK-BR-3异种移植模型中,afatinib(30 mg/kg/天)使HER2磷酸化降低85%,肿瘤凋亡(TUNEL+细胞)增加3倍。[4] 阿法替尼马来酸盐(BIBW2992)以20mg/kg/天的剂量口服给药21天,可抑制裸鼠HCC827异种移植瘤的生长。与对照组相比,肿瘤体积减少约80%,瘤内EGFR磷酸化水平显著受抑[1] 阿法替尼马来酸盐(BIBW2992)以40mg/kg/天的剂量口服给药28天,可延缓裸鼠NCI-H1975异种移植瘤(EGFR T790M突变体)的进展,肿瘤重量减少约60%[2] 阿法替尼马来酸盐(BIBW2992)在携带A549 NSCLC异种移植瘤的裸鼠中增强放疗的抗肿瘤效果。口服15mg/kg/天阿法替尼联合8Gy放疗(分4天给予),相比单独放疗,肿瘤体积减少约75%[3] 在携带EGFR突变的晚期NSCLC患者的II期临床研究中,阿法替尼马来酸盐(BIBW2992)(40mg口服,每日一次)的部分缓解率为56%,中位无进展生存期为11.1个月[5] |
| 酶活实验 |
EGFR 激酶:10 μL 抑制剂的 50% Me2SO 溶液、20 μL 底物溶液(200 mM HEPES pH 7.4、50 mM 醋酸镁、2.5 mg/mL 聚 (EY)、5 μg/mL 生物 pEY)和 20每个 100 µL 酶反应中均包含 µL 酶制剂。添加 50 µL 在 10 mM MgCl2 中制备的 100 µM ATP 溶液即可启动酶反应。室温下测定 30 分钟后,添加 50 µL 终止液(20 mM HEPES pH 7.4 中的 250 mM EDTA)以结束测定。将 100 µL 添加到涂有链霉亲和素的微量滴定板上,室温孵育 60 分钟后,用 200 µL 洗涤液(50 mM Tris,0.05% Tween20)清洗板。孔中装有 100 µL 等份的 PY20H Anti-Ptyr:HRP(一种 250 ng/mL HRPO 标记的抗 PY 抗体)。 60 分钟孵育期后,使用 200 µL 清洗溶液清洗板 3 次。随后,使用 100 µL TMB 过氧化物酶溶液 (A:B=1:1) 来显色样品。十分钟后,反应停止。将板放入 ELISA 读数器后,计算 OD450nm 处的消光。酶 HER2-IC:酶活性测定在有或没有系列抑制剂稀释的 50% Me2SO 中进行。每个 100 µL 反应中均包含与 EGFR 激酶测定所述类似的成分,并添加了 1000 µM Na3VO4。添加 50 µL 在 10 mM 醋酸镁中制备的 500 µM ATP 溶液即可启动酶促反应。将酶稀释至酶量与磷酸盐掺入 bio-pEY 所需时间呈线性关系的程度。使用 20 mM HEPES pH 7.4、130 mM NaCl、0.05% Triton X-100、1 mM DTT 和 10% 甘油的混合物来稀释酶制剂。室温下测定 30 分钟后,添加 50 µL 终止液以结束程序。 Src 激酶测定:每个 100 µL 反应中包含 10 µL 50% Me2SO 抑制剂、20 µL 酶制剂和 20 µL 用 1000 µM Na3VO4 增强的底物溶液。添加 50 µL 在 10 mM 乙酸镁中制备的 1000 µM ATP 溶液可启动酶促反应。 BIRK 激酶测定:将 50 µL 在 8 mM MnCl2 和 20 mM 乙酸镁中制备的 2 mM ATP 溶液添加到 250 mM Tris pH 7.4、10 mM DTT、2.5 mg/mL 聚 (EY) 和 5 mg/ mL bio-pEY 作为底物溶液来启动酶促反应。 HGFR 激酶和 VEGF2 检测:在室温下运行 20 分钟后,添加 10 µL 5% H3PO4 即可完成检测。然后使用 96 孔过滤器伴侣通用收集器收集沉淀物并捕获到 GF/B 过滤器上。将滤板彻底清洁,在 50°C 下干燥一小时,密封,并使用 TopCount TM 或 Microbeta b counter TM 使用闪烁计数来测量放射性>。
- EGFR激酶活性实验: 1. 重组野生型或突变型EGFR激酶域与afatinib(0.01–100 nM)及[γ-³²P]ATP在激酶缓冲液中孵育。 2. 30°C反应30分钟后终止,磷酸化肽底物被捕获在滤膜上。 3. 测量放射性,计算各EGFR变体的IC₅₀值。[1] - HER2激酶实验: 1. 重组HER2激酶与afatinib(1–100 nM)及荧光标记底物肽孵育。 2. 通过荧光共振能量转移(FRET)检测底物磷酸化,确定HER2抑制的IC₅₀为14 nM。[1] 将重组EGFR、HER2和HER4激酶结构域分别与ATP及特异性多肽底物在系列稀释的阿法替尼马来酸盐(BIBW2992)存在下孵育,反应在37°C下进行60分钟,采用均相时间分辨荧光(HTRF)法检测磷酸化底物。通过与溶媒对照组的荧光强度对比计算抑制率,从量效曲线中得出IC₅₀值[1] 采用相同方案检测重组EGFR T790M突变体和野生型EGFR激酶的活性,反应混合物在30°C下孵育45分钟,通过HTRF法定量磷酸化水平,确定IC₅₀值以比较对突变体和野生型EGFR的抑制效价[2] |
| 细胞实验 |
- 增殖与信号通路实验:
1. NSCLC或乳腺癌细胞接种于96孔板,用afatinib(0.1–1,000 nM)处理72小时。
2. MTT法检测细胞活力,确定IC₅₀值。
3. 信号分析:50 nM afatinib处理细胞2–24小时后裂解,Western blot检测p-EGFR、p-AKT、p-ERK及凋亡标志物。[1][2][4]
- 放疗协同实验: 1. HNSCC细胞用afatinib(10 nM)预处理2小时,然后接受0–8 Gy辐射。 2. 14天后计数克隆形成,生存曲线计算辐射敏感性。[3] MTT 测定用于确定细胞毒性。导致50%细胞死亡的药物浓度称为IC 50 值。 Bliss 方法用于计算 IC50 以及拟合的 S 形剂量反应曲线。 将A431、HCC827和NCI-N87细胞以5×10³个细胞/孔接种到96孔板中,用阿法替尼马来酸盐(BIBW2992)(0.001-1μM)处理72小时,采用四唑盐法检测细胞活性并计算IC₅₀值。蛋白质印迹分析中,用0.05-0.5μM阿法替尼处理细胞,裂解后与抗磷酸化EGFR/HER2、ERK1/2、Akt和GAPDH的抗体孵育[1] 用阿法替尼马来酸盐(BIBW2992)(0.01-0.1μM)处理HCC827细胞48小时,采用Annexin V-FITC/PI染色检测凋亡,通过蛋白质印迹法分析切割型caspase-3/PARP的表达。将NCI-H1975细胞接种到6孔板中,用0.05-0.5μM阿法替尼处理14天,评估克隆形成能力[2] 用阿法替尼马来酸盐(BIBW2992)(0.05-0.2μM)处理A549细胞24小时后,给予0-4Gy放疗。72小时后,采用MTT法评估细胞活性,通过碘化丙啶染色检测细胞死亡[3] 用阿法替尼马来酸盐(BIBW2992)(0.1-0.5μM)处理SK-BR-3细胞24小时,采用Boyden小室进行迁移和侵袭实验,通过逆转录-聚合酶链反应(RT-PCR)定量MMP-9 mRNA的表达[4] |
| 动物实验 |
携带ARK2异种移植瘤的SCID小鼠
25 mg/kg 口服 四只连续6周以上喂食强力霉素的双转基因小鼠接受MRI检查(图4)以记录肺部肿瘤负荷。阿法替尼(BIBW2992)以0.5%甲基纤维素-0.4%聚山梨醇酯-80(吐温80)为载体,每日一次灌胃给药,剂量为20 mg/kg。雷帕霉素溶于100%乙醇,用5% PEG400和5%吐温80新鲜稀释后,每日一次腹腔注射给药,剂量为2 mg/kg。每1或2周对小鼠进行一次MRI检查,以确定肿瘤体积的减少情况,并在药物治疗后处死小鼠,用于进一步的组织学和生化研究。免疫组织化学染色实验中,每组选取三只荷瘤小鼠,分别接受三次治疗,每次治疗间隔24小时,治疗方案为:单独使用阿法替尼(BIBW2992)(20 mg/kg)或阿法替尼(BIBW2992)(20 mg/kg)联合雷帕霉素(2 mg/kg)。末次给药后1小时处死小鼠。实验期间,所有小鼠均饲喂含强力霉素的饲料。同窝小鼠作为对照。[1] - 非小细胞肺癌异种移植模型:1. 将HCC827或PC-9细胞(5×10⁶)皮下接种于裸鼠体内。 2. 当肿瘤体积达到100 mm³时,小鼠每日口服溶于0.5%甲基纤维素溶液的阿法替尼(10–30 mg/kg),持续21天。 3. 每周测量两次肿瘤体积;研究结束时,通过免疫组织化学分析肿瘤中 p-EGFR 和细胞凋亡情况。[1][2] - HNSCC 放射联合模型:1. 携带 SCC-25 异种移植瘤的裸鼠接受阿法替尼(10 mg/kg,口服,每日一次)和/或放射治疗(第 7 天和第 14 天,每次 6 Gy)。 2. 监测肿瘤生长 28 天;分析肿瘤中 DNA 损伤(γ-H2AX)和增殖(Ki-67)。[3] 携带 HCC827 异种移植瘤(100-150 mm³)的裸鼠被随机分为对照组和治疗组。将阿法替尼(BIBW2992)二马来酸盐悬浮于 0.5% 羧甲基纤维素中,以 20 mg/kg/天的剂量口服给药,持续 21 天。每 3 天测量一次肿瘤体积,并将小鼠安乐死以收集肿瘤组织,用于 EGFR 磷酸化的 Western blot 分析 [1]。 携带 NCI-H1975 异种移植瘤的裸鼠以 40 mg/kg/天的剂量口服阿法替尼(BIBW2992)二马来酸盐,持续 28 天。治疗结束后测量肿瘤重量,并对肿瘤组织进行Ki-67(增殖标志物)免疫组化染色[2]。 携带A549非小细胞肺癌异种移植瘤的裸鼠被随机分为四组:对照组、阿法替尼单药治疗组(口服,15 mg/kg/天)、放疗单药治疗组(8 Gy,分4天,每天2 Gy)和联合治疗组。阿法替尼单药治疗持续14天(放疗前3天开始),每周记录两次肿瘤体积[3]。 |
| 药代性质 (ADME/PK) |
口服吸收:在小鼠中,口服阿法替尼(20 mg/kg)2 小时后血药浓度峰值 (Cmax) 为 1.2 μg/mL,口服生物利用度约为 40%。[2]
- 半衰期:小鼠的末端消除半衰期为 6-8 小时;在人体中,稳态半衰期为 37 小时。[2][5] - 分布:在荷瘤小鼠中,阿法替尼主要蓄积于肿瘤内,肿瘤与血浆浓度比为 3-5:1。[2] - 代谢:主要通过 CYP3A4 代谢;<5% 以原形经尿液排出。[5] 单次口服 20 mg/kg 阿法替尼(BIBW2992)二马来酸盐后,小鼠的口服生物利用度约为 83%。血浆半衰期约为7.5小时,给药后2小时达到最大血浆浓度(Cmax)为5.2 μg/mL [1] 在大鼠中,口服40 mg/kg的阿法替尼(BIBW2992)二马来酸盐,其24小时AUC₀为48.6 μg·h/mL。该药物广泛分布于肝脏、肺脏和肿瘤组织中,肿瘤与血浆浓度比约为3.5 [2] 在健康志愿者中,口服40 mg阿法替尼(BIBW2992)二马来酸盐,其Cmax为2.7 μg/mL,24小时AUC₀为34.1 μg·h/mL,血浆半衰期为37.1小时。该药物主要经肝脏代谢,7天内85%的剂量经粪便排出,15%经尿液排出[5] |
| 毒性/毒理 (Toxicokinetics/TK) |
临床前毒性:在大鼠中,阿法替尼(50 mg/kg,每日一次,持续 28 天)可引起轻度腹泻和皮疹,但未见明显的肝肾损伤(ALT/AST 和 BUN 均在正常范围内)。[2][4]
- 临床毒性:常见不良反应包括腹泻(60%)、皮疹(45%)和口腔炎(30%);3 级及以上不良反应罕见(<10%)。血浆蛋白结合率 >95%。[5] 小鼠以 阿法替尼 (BIBW2992) 二马来酸盐 20 mg/kg/天,持续 21 天,出现轻度体重减轻(约 10%)和短暂性腹泻(18% 的动物),但未见明显的肝肾毒性。血清ALT、AST和肌酐水平均在正常范围内[1] 在II期临床研究中,阿法替尼(BIBW2992)二马来酸盐最常见的不良反应为腹泻(90%)、皮疹(80%)和口腔炎(45%)。3/4级毒性反应包括严重腹泻(15%)和皮肤反应(10%)[5] 通过平衡透析法测定,阿法替尼(BIBW2992)二马来酸盐在人血浆中的血浆蛋白结合率约为95%[4] |
| 参考文献 | |
| 其他信息 |
阿法替尼二马来酸盐是阿法替尼与两摩尔当量马来酸结合而成的马来酸盐。用于转移性非小细胞肺癌患者的一线治疗。它是一种酪氨酸激酶抑制剂和抗肿瘤药物。其主要成分为阿法替尼。
阿法替尼二马来酸盐是阿法替尼的二马来酸盐形式,阿法替尼是一种口服生物利用度高的苯胺基喹唑啉衍生物,是受体酪氨酸激酶(RTK)表皮生长因子受体(ErbB;EGFR)家族的抑制剂,具有抗肿瘤活性。阿法替尼给药后,可选择性且不可逆地结合并抑制表皮生长因子受体1(ErbB1;EGFR)、2(ErbB2;HER2)和4(ErbB4;HER4)以及某些EGFR突变体,包括由EGFR 19号外显子缺失突变或21号外显子(L858R)突变引起的突变。这可能导致过度表达这些受体酪氨酸激酶(RTK)的肿瘤细胞的肿瘤生长和血管生成受到抑制。此外,阿法替尼还能抑制对第一代EGFR抑制剂耐药的EGFR T790M“守门员”突变。EGFR、HER2和HER4是属于EGFR超家族的RTK。它们在肿瘤细胞增殖和肿瘤血管生成中发挥重要作用,并在多种癌细胞类型中过度表达。 一种喹唑啉和丁烯酰胺衍生物,作为表皮生长因子受体(ERBB受体)的酪氨酸激酶抑制剂,用于治疗转移性非小细胞肺癌。 另见:阿法替尼(具有活性部分)。 药物适应症 吉奥替利单药治疗适用于治疗既往未接受过表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗的、具有EGFR激活突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者;以及在铂类化疗期间或之后进展的局部晚期或转移性鳞状细胞癌NSCLC。 - 作用机制:阿法替尼与 EGFR、HER2 和 HER4 的 ATP 结合位点不可逆结合,抑制其激酶活性,并阻断下游 PI3K/AKT 和 MAPK 通路,从而导致细胞周期阻滞和凋亡。[1][2] - 适应症:已获批用于 EGFR 突变型非小细胞肺癌 (NSCLC) 和 HER2 阳性乳腺癌;正在研究其与放射治疗联合用于头颈部鳞状细胞癌 (HNSCC) 的疗效。[2][3][4] - 药效学标志物:血浆癌胚抗原 (CEA) 水平的降低与 NSCLC 患者的肿瘤反应相关。 [5] 阿法替尼(BIBW2992)二马来酸盐是一种不可逆的口服EGFR、HER2和HER4抑制剂,它通过与这些受体的激酶结构域共价结合发挥抗肿瘤作用,从而阻断下游信号通路[1] 阿法替尼(BIBW2992)二马来酸盐对EGFR突变型非小细胞肺癌(NSCLC)有效,包括携带T790M耐药突变的肿瘤,使其成为对第一代EGFR抑制剂产生耐药性患者的潜在治疗方案[2] 阿法替尼(BIBW2992)二马来酸盐增强放射治疗反应的能力支持其用于局部晚期NSCLC的联合放疗[3] |
| 分子式 |
C32H33CLFN5O11
|
|---|---|
| 分子量 |
717.18
|
| 精确质量 |
717.184
|
| 元素分析 |
C, 53.52; H, 4.63; Cl, 4.94; F, 2.65; N, 9.75; O, 24.51
|
| CAS号 |
850140-73-7
|
| 相关CAS号 |
Afatinib;850140-72-6;Afatinib-d6 dimaleate;Afatinib oxalate;1398312-64-5
|
| PubChem CID |
15606394
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
4.536
|
| tPSA |
241.3
|
| 氢键供体(HBD)数目 |
6
|
| 氢键受体(HBA)数目 |
16
|
| 可旋转键数目(RBC) |
12
|
| 重原子数目 |
50
|
| 分子复杂度/Complexity |
821
|
| 定义原子立体中心数目 |
1
|
| SMILES |
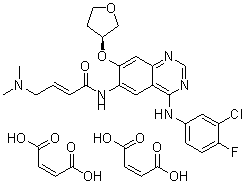
C(/C(=O)O)=C/C(=O)O.N(C1C=CC(F)=C(Cl)C=1)C1=NC=NC2=CC(=C(C=C12)NC(=O)/C=C/CN(C)C)O[C@@H]1COCC1
|
| InChi Key |
USNRYVNRPYXCSP-JUGPPOIOSA-N
|
| InChi Code |
InChI=1S/C24H25ClFN5O3.2C4H4O4/c1-31(2)8-3-4-23(32)30-21-11-17-20(12-22(21)34-16-7-9-33-13-16)27-14-28-24(17)29-15-5-6-19(26)18(25)10-15;2*5-3(6)1-2-4(7)8/h3-6,10-12,14,16H,7-9,13H2,1-2H3,(H,30,32)(H,27,28,29);2*1-2H,(H,5,6)(H,7,8)/b4-3+;2*2-1-/t16-;;/m0../s1
|
| 化学名 |
(Z)-but-2-enedioic acid;(E)-N-[4-(3-chloro-4-fluoroanilino)-7-[(3S)-oxolan-3-yl]oxyquinazolin-6-yl]-4-(dimethylamino)but-2-enamide
|
| 别名 |
Afatinib dimaleate; BIBW 2992; Afatinib (diMaleate); BIBW-2992; BIBW2992; UNII-V1T5K7RZ0B; Afatinib dimaleate [USAN]; trade name: Gilotrif, Tomtovok and Tovok
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (139.26 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
配方 2 中的溶解度: 5% DMSO+30% PEG 300+ddH2O: 28 mg/mL 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.3944 mL | 6.9718 mL | 13.9435 mL | |
| 5 mM | 0.2789 mL | 1.3944 mL | 2.7887 mL | |
| 10 mM | 0.1394 mL | 0.6972 mL | 1.3944 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04439136 | Active Recruiting |
Drug: Afatinib Dimaleate | Advanced Lymphoma Refractory Lymphoma |
National Cancer Institute (NCI) |
August 12, 2015 | Phase 2 |
| NCT02438722 | Active Recruiting |
Drug: Afatinib Dimaleate Biological: Cetuximab |
Recurrent Non-Small Cell Lung Carcinoma Stage IV Non-Small Cell Lung Cancer |
SWOG Cancer Research Network | May 7, 2015 | Phase 2 Phase 3 |
| NCT02465060 | Active Recruiting |
Drug: Afatinib Drug: Afatinib Dimaleate |
Bladder Carcinoma Glioma |
National Cancer Institute (NCI) |
August 17, 2015 | Phase 2 |
| NCT03083678 | Active Recruiting |
Drug: Afatinib | Chordoma | Leiden University Medical Center | June 21, 2018 | Phase 2 |
| NCT03827070 | Active Recruiting |
Drug: Afatinib Drug: Talcum powder |
Non Small Cell Lung Cancer | Center Trials & Treatment Europe | March 5, 2019 | Phase 1 |
|
 |
Afatinib covalently binds to cysteine number 797 of the epidermal growth factor receptor (EGFR) via a Michael addition (IC50 = 0.5 nM).Schubert-Zsilavecz, M, Wurglics, M,Neue Arzneimittel Frühjahr 2013.(in German) |