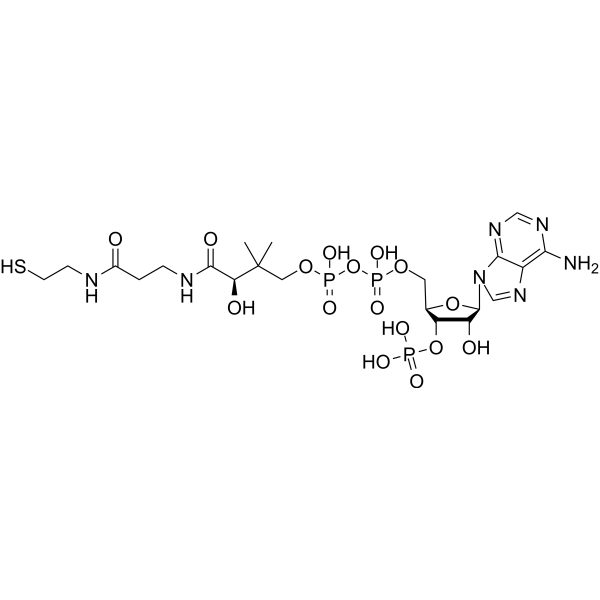
| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|

| 靶点 |
This study identifies that Coenzyme A covalently modifies specific cysteine residues on a wide range of proteins, a process termed protein CoAlation. In Staphylococcus aureus, mass spectrometry analysis revealed 356 CoAlated proteins. Specific targets identified include:
- Glyceraldehyde-3-phosphate dehydrogenase (SaGAPDH), modified at the catalytic Cys151 [1]. - Transcriptional regulators: SarR, CtsR, AgrA (CoAlated on Cys6 and Cys199), PerR (CoAlated on Cys142), and SarS [1]. - Antioxidant proteins: thioredoxin (Trx), alkyl hydroperoxide reductase C (AhpC), thiol peroxidase (Tpx, CoAlated on active site Cys60), malate: quinone oxidoreductases 1 and 2 (Mqo1/2), and others [1]. - Many ribosomal proteins, including L12, S12, L14, S18, L32, L33 (RpmG3), and L36 (RpmJ) [1]. - Numerous metabolic enzymes: succinate-CoA ligase, acyl-CoA ligase, HMG-CoA synthase, acetyl-CoA carboxylase, acyl-CoA dehydrogenase, glyceraldehyde-3-phosphate dehydrogenase 2 (GapA2), pyruvate kinase (Pyk), ATP-dependent 6-phosphofructokinase (PfkA), acetate kinase (AckA), alcohol dehydrogenase (Adh), and others [1]. Coenzyme A itself is not a drug targeting specific receptors but rather an obligate cofactor for hundreds of enzymes in intermediary metabolism. Its primary molecular targets include acyl-CoA synthetases, carnitine O-acetyltransferase, citrate synthase, and 3-hydroxy-3-methylglutaryl-coenzyme A reductase (HMGCR), among many others. CoA also binds to the acyl-CoA-binding protein (ACBP), which serves as an intracellular carrier and pool former for acyl-CoA esters. In addition, CoA acts as the source of the 4′-phosphopantetheine prosthetic group for carrier proteins in fatty acid, polyketide, and nonribosomal peptide synthases. |
|---|---|
| 体外研究 (In Vitro) |
- SaGAPDH的体外CoAlation: 将重组His标签SaGAPDH与2 mM 辅酶A二硫化物(CoASSCoA)共同孵育。这种处理导致其酶活性被抑制90%。这种抑制效应可通过添加10 mM 二硫苏糖醇(DTT)完全逆转 [1]。
- 防止过度氧化: 在暴露于10 mM 过氧化氢(H₂O₂)之前对SaGAPDH进行体外CoAlation,随后用10 mM DTT处理,可使其酶活性恢复近100%。这表明CoAlation可保护催化位点Cys151免受不可逆的过度氧化 [1]。 - H₂O₂的抑制作用: 将重组SaGAPDH暴露于10 µM H₂O₂,其催化活性降低约50%。1 mM H₂O₂导致95%的抑制,而10 mM H₂O₂则完全阻断其活性。由10 mM H₂O₂引起的失活仅部分可逆,10 mM DTT仅能恢复40%的活性 [1]。 体外研究表明,辅酶A是多种酶促反应(包括丙酮酸生成乙酰辅酶A、脂肪酸氧化和柠檬酸循环)的必需辅因子。在细胞培养模型中,细胞外辅酶A不能提高细胞内辅酶A水平,因为在细胞存在下它会完全降解为泛酸。例如,当辅酶A(10 µM)与C3A细胞共孵育20小时后,它完全转化为泛酸,表明细胞不直接摄取外源性辅酶A,而是利用其降解产物进行从头合成。辅酶A还被证明可以调节AMPK活性,棕榈酰辅酶A在体外激酶测定中可激活AMPK。 |
| 体内研究 (In Vivo) |
- 在细菌中的诱导: 在正常生长条件下,革兰氏阴性菌(大肠杆菌)和革兰氏阳性菌(巨大芽孢杆菌、金黄色葡萄球菌)中蛋白质CoAlation的基础水平较低。用氧化剂(包括10-100 mM 过氧化氢、2 mM diamide和100-150 µM 次氯酸钠)处理30分钟,可强烈诱导其发生 [1]。
- 代谢胁迫诱导: 葡萄糖饥饿(将细菌转移到缺乏葡萄糖的培养基中培养60-120分钟)可强烈诱导大肠杆菌、巨大芽孢杆菌和金黄色葡萄球菌中的蛋白质CoAlation。这种CoAlation可通过重新添加20 mM 葡萄糖并孵育30分钟而被逆转 [1]。 - 可逆性: 在大肠杆菌、巨大芽孢杆菌和金黄色葡萄球菌中,diamide诱导的蛋白质CoAlation是一种可逆的翻译后修饰 [1]。 - SaGAPDH的体内CoAlation: 在过表达His-SaGAPDH的大肠杆菌中,用2 mM diamide处理可强烈诱导该蛋白的CoAlation。响应100 µM 次氯酸钠时观察到的CoAlation最强,而在用10 mM 过氧化氢处理的细胞中检测到较弱的信号 [1]。 在体内,辅酶A在大脑能量代谢、脂肪酸氧化和神经递质合成中发挥关键作用。在泛酸激酶相关神经退行性疾病(PKAN)小鼠模型中,大脑辅酶A缺乏与运动功能障碍相关,通过泛酸激酶激活剂BBP-671治疗恢复大脑辅酶A水平可改善运动和生存率。Pank1fl/fl,Pank2fl/fl SynCre+神经元敲除小鼠表现出持久的大脑辅酶A缺乏和明确的运动功能障碍,证明了辅酶A在神经元功能中的重要作用。在尤卡坦微型猪中,局部应用4-羟基视黄酸(一种依赖于辅酶A介导的酰基转移的代谢物)可诱导表皮增生 |
| 酶活实验 |
- GAPDH酶活性测定: 通过测量340 nm处NADH生成引起的吸光度变化,在25°C下测定重组SaGAPDH的活性。反应在150 µl的混合物中进行,包含20 mM Tris-HCl(pH 8.7)、0.36 µM SaGAPDH、1.25 mM NAD⁺、1.25 mM EDTA和15 mM 砷酸钠。通过添加0.25 mM 3-磷酸甘油醛启动反应。通过测定反应最初80秒曲线线性部分的斜率来计算初始反应速率。在失活实验中,将SaGAPDH与1 µM、10 µM、100 µM或10 mM H₂O₂预孵育10分钟,或与10 mM CoASSCoA预孵育30分钟,然后测量剩余活性 [1]。
- Nudix 7水解酶测定: 将重组His-Nudix 7水解酶(1.7 µg)在总体积100 µl的溶液(含50 mM (NH₄)HCO₃和0.2 mM CoASSG(辅酶A-谷胱甘肽混合二硫化物))中,于37°C下孵育20分钟,反应体系中存在或不存在5 mM MgCl₂。通过HPLC分析反应产物和底物,洗脱监测波长为205 nm [1]。 典型的辅酶A非细胞实验使用生化试剂盒测量其浓度或酶活性。例如,辅酶A检测试剂盒(ab102504)利用多步酶促反应,其中游离辅酶A被特异性转化生成产物,与OxiRed探针反应产生颜色(λ = 570 nm)和荧光(Ex/Em = 535/587 nm)。该检测的线性范围为2.5–250 µM,灵敏度>2.5 µM。或者,可以使用带有通过SILEC(细胞培养中必需营养素稳定同位素标记)生成的稳定同位素标记内标的LC-MS/MS对辅酶A及其硫酯衍生物进行定量。对于酶活性测定,通常将辅酶A与目标酶、适当的底物(例如用于乙酰转移酶的乙酰辅酶A)和针对特定反应优化的缓冲条件共同孵育。 |
| 细胞实验 |
- 用于蛋白质CoAlation分析的细菌培养和处理: 将细菌种类(大肠杆菌、巨大芽孢杆菌、金黄色葡萄球菌)在富集培养基中过夜培养(大肠杆菌和金黄色葡萄球菌使用Luria Bertani培养基;巨大芽孢杆菌使用营养肉汤3)。将过夜培养物以1:100的比例稀释到相同的培养基中,孵育至600 nm处的光密度(OD₆₀₀)达到0.7。然后,在37°C下用氧化剂处理细胞30分钟或不处理:过氧化氢(10和100 mM)、diamide(2 mM)和次氯酸钠(150 µM)。为了诱导代谢胁迫,将OD₆₀₀为0.7的细菌培养物通过离心收集,并重新悬浮在补充或不补充葡萄糖作为碳源的M9基本培养基中 [1]。
- 细胞裂解和蛋白质提取: 对于大肠杆菌和巨大芽孢杆菌,将沉淀重悬于含有100 mM Tris-HCl(pH 7.5)、100 mM NaCl、100 mM NEM(以防止体外修饰)和蛋白酶抑制剂的缓冲液中。加入SDS至终浓度1%,匀浆后超声处理,然后在室温下以21,000g离心10分钟。对于金黄色葡萄球菌,将沉淀重悬于类似的缓冲液中,加入溶葡萄球菌酶(22 U/ml)以溶解细胞壁蛋白,在37°C下孵育30分钟,然后加入SDS并进行超声处理 [1]。 辅酶A的体外细胞实验通常涉及在含有透析或活性炭处理胎牛血清的培养基中培养细胞,以消除未标记的泛酸污染。为了生成同位素标记的辅酶A标准品,将细胞(例如Hepa 1c1c7小鼠肝癌细胞或果蝇S2细胞)在补充有[13C315N]-泛酸(1 mg/L)而非未标记泛酸的培养基中传代3-5次。传代3次后,约98-99%的细胞辅酶A被标记。对于辅酶A定量,裂解细胞,使用LC-中性丢失扫描m/z = 507分析裂解物,该扫描可检测辅酶A衍生物的特征性碎裂模式。细胞辅酶A水平可以通过添加特定脂肪酸(例如丙酸盐生成丙酰辅酶A)或使细胞经受各种代谢扰动来调节。 |
| 动物实验 |
辅酶A的体内动物研究通常使用Pank1fl/fl,Pank2fl/fl SynCre+泛酸激酶相关神经退行性疾病(PKAN)小鼠模型,该模型表现出大脑辅酶A缺乏和运动功能障碍。通常通过口服灌胃每天给予动物测试化合物(例如泛酸激酶激活剂BBP-671),剂量范围为0.1至30 mg/kg,持续7天,以评估药代动力学和药效学性质。在指定时间点(例如最后一次给药后4小时)收集组织样本(血浆、肝脏、大脑和脑脊液),并使用LC-MS/MS分析总辅酶A浓度。终点包括测量血液、肝脏和大脑中的辅酶A水平,以及评估运动功能和体重变化。
|
| 药代性质 (ADME/PK) |
辅酶A本身由于口服生物利用度差和快速降解而不作为治疗药物给药。外源性辅酶A在细胞存在下会定量降解为泛酸,如在C3A细胞培养研究中所示,与细胞共孵育20小时的辅酶A(10 µM)完全转化为泛酸。在体内,辅酶A通过五步酶促途径从泛酸(维生素B5)内源性合成:泛酸 → 4′-磷酸泛酸 → 4′-磷酸泛酰巯基乙胺 → 去磷酸辅酶A → 辅酶A。细胞内辅酶A浓度通过酰基辅酶A对泛酸激酶的反馈抑制进行严格调控。组织辅酶A水平差异显著;例如,在葡萄糖上生长的大肠杆菌的辅酶A池约为400 µM,而在氨基酸上生长的细菌约为100 µM。
|
| 毒性/毒理 (Toxicokinetics/TK) |
根据安全数据表,辅酶A被分类为引起皮肤刺激(类别2)、严重眼刺激(类别2)和特异性靶器官毒性——单次暴露(类别3),可能引起呼吸道刺激。预防措施包括佩戴防护手套、护目镜和在通风良好的区域工作。在动物研究中,辅酶A本身未报告引起显著全身毒性,但辅酶A生物合成异常与人类疾病相关。例如,PANK2基因(编码泛酸激酶2)的突变导致泛酸激酶相关神经退行性疾病(PKAN),这是一种罕见的常染色体隐性遗传病,以肌张力障碍、帕金森症和早逝为特征。尽管辅酶A在生理水平下通常被认为是安全的,但高剂量或长期暴露可能引起接触部位的局部刺激。
|
| 参考文献 |
[1]. Protein CoAlation and antioxidant function of coenzyme A in prokaryotic cells. Biochem J. 2018 Jun 6;475(11):1909-1937.
[2]. https://pubchem.ncbi.nlm.nih.gov/compound/87642 |
| 其他信息 |
- 辅酶A硫醇的背景信息: 已发现辅酶A可形成辅酶A二硫化物(CoASSCoA)以及与其他低分子量硫醇(如辅酶A-半胱氨酸和辅酶A-谷胱甘肽混合二硫化物CoASSG)的混合二硫化物。CoASSG异源二聚体已从细菌、酵母、人心肌组织和甲状旁腺中分离出来。在培养的血管平滑肌细胞中观察到CoASSG具有强效的血管收缩和增殖作用,并且它还被证明能抑制细菌RNA聚合酶的活性 [1]。
- 蛋白质CoAlation的机制: 当半胱氨酸硫醇基团被活性氧(ROS)氧化为不稳定的亚磺酸中间体时,它可以与附近的硫醇反应,导致与低分子量硫醇(如CoA)形成混合二硫化物。形成的二硫化物是可逆的调节事件,其作用是保护不稳定的亚磺酸免于过度氧化为亚磺酸和磺酸 [1]。 - 在氧化应激中的作用: 该研究得出结论,蛋白质CoAlation是细菌中一种广泛的、受氧化还原调控的翻译后修饰,具有在氧化应激条件(如暴露于H₂O₂)下保护关键反应性半胱氨酸(例如SaGAPDH中的半胱氨酸)免于不可逆过度氧化的潜力 [1]。 - 分子动力学模拟模型: 分子动力学模拟提出了GAPDH发生CoAlation的“双锚定模型”。在缺乏NAD⁺的情况下,CoA的ADP部分占据了氧化型GAPDH中空的核苷酸结合口袋,将CoA硫醇基团所在的柔性泛酰巯基乙胺尾部定位在附近,以便与催化位点Cys151形成共价二硫键 [1]。 辅酶A是一种硫醇,由泛酸单元通过磷酸酐键与3',5'-二磷酸腺苷单元连接而成,并包含一个氨基乙硫醇单元。它既是大肠杆菌的代谢产物,也是小鼠的代谢产物,同时也是一种辅酶。它在功能上与ADP相关。它是辅酶A(4-)的共轭酸。 辅酶A(CoA、CoASH或HSCoA)是一种辅酶,因其在脂肪酸的合成和氧化以及柠檬酸循环中丙酮酸的氧化中的作用而闻名。迄今为止测序的所有基因组都编码以辅酶A为底物的酶,约4%的细胞酶以辅酶A或其硫酯形式为底物。它被用作痤疮治疗的辅助手段。 辅酶A是存在于大肠杆菌(K12菌株、MG1655菌株)中或由其产生的代谢产物。 据报道,果蝇、人类和其他有相关数据的生物体中也存在辅酶A。 辅酶A是一种含有泛酸、3-磷酸腺苷、5-焦磷酸腺苷和半胱胺的辅酶;参与酰基转移,尤其是在转乙酰化反应中。 另见:……查看更多…… |
| 分子式 |
C21H36N7O16P3S
|
|---|---|
| 分子量 |
767.53
|
| 精确质量 |
767.115
|
| 元素分析 |
C, 32.86; H, 4.73; N, 12.77; O, 33.35; P, 12.11; S, 4.18
|
| CAS号 |
85-61-0
|
| 相关CAS号 |
Coenzyme A trilithium;18439-24-2;Coenzyme A sodium;55672-92-9
|
| PubChem CID |
87642
|
| 外观&性状 |
White to light yellow solid powder
|
| 密度 |
2.0±0.1 g/cm3
|
| 沸点 |
146 - 147
|
| 熔点 |
-5ºC
|
| 折射率 |
1.737
|
| LogP |
-4.02
|
| tPSA |
414.79
|
| 氢键供体(HBD)数目 |
10
|
| 氢键受体(HBA)数目 |
21
|
| 可旋转键数目(RBC) |
18
|
| 重原子数目 |
48
|
| 分子复杂度/Complexity |
1270
|
| 定义原子立体中心数目 |
5
|
| SMILES |
CC(COP(O)(OP(O)(OC[C@](O1)([H])[C@](OP(O)(O)=O)([H])[C@](O)([H])[C@]1([H])N2C=NC(C2=NC=N3)=C3N)=O)=O)(C(O)([H])/C(O)=N/CC/C(O)=N/CCS)C
|
| InChi Key |
RGJOEKWQDUBAIZ-IBOSZNHHSA-N
|
| InChi Code |
InChI=1S/C21H36N7O16P3S/c1-21(2,16(31)19(32)24-4-3-12(29)23-5-6-48)8-41-47(38,39)44-46(36,37)40-7-11-15(43-45(33,34)35)14(30)20(42-11)28-10-27-13-17(22)25-9-26-18(13)28/h9-11,14-16,20,30-31,48H,3-8H2,1-2H3,(H,23,29)(H,24,32)(H,36,37)(H,38,39)(H2,22,25,26)(H2,33,34,35)/t11-,14-,15-,16+,20-/m1/s1
|
| 化学名 |
[[(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-4-hydroxy-3-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [(3R)-3-hydroxy-2,2-dimethyl-4-oxo-4-[[3-oxo-3-(2-sulfanylethylamino)propyl]amino]butyl] hydrogen phosphate
|
| 别名 |
coenzyme A; Coenzyme A (free acid); CoA; CoASH; CoA-SH; Zeel;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 本产品在运输和储存过程中需避光。 (2). 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~125 mg/mL (~162.86 mM)
DMSO : ~100 mg/mL (~130.29 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1.63 mg/mL (2.12 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 16.3 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.63 mg/mL (2.12 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 16.3mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1.63 mg/mL (2.12 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 25 mg/mL (32.57 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.3029 mL | 6.5144 mL | 13.0288 mL | |
| 5 mM | 0.2606 mL | 1.3029 mL | 2.6058 mL | |
| 10 mM | 0.1303 mL | 0.6514 mL | 1.3029 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。