| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 5g |
|
||
| Other Sizes |
|

| 靶点 |
EGFRL858R/T790M (IC50 = 1 nM); EGFRL858R (IC50 = 12 nM)
METTL7B is expressed at a higher level in lung adenocarcinoma (LUAD) cells that are resistant to osimertinib than in cells that are sensitive to the drug. LUAD cells were re-sensitized to osimertinib after METTL7B was knocked down using GNC-siRNA.[1] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:与野生型体外相比,AZD9291 对突变型 EGFR 细胞系的增殖具有明显更有效的抑制作用。激酶测定:Osimertinib(以前称为 AZD-9291 和 mereletinib)是一种口服的、不可逆的、突变选择性的第三代 EGFR 抑制剂,对于外显子 19 缺失 EGFR、L858R/T790M EGFR、IC50 分别为 12.92、11.44 和 493.8 nM。和 WT EGFR 分别在 LoVo 细胞中。它抑制激活性和耐药性 EGFR 突变,同时保留正常皮肤和肠道细胞中存在的正常形式 EGFR,从而减少当前可用药物遇到的副作用。细胞测定:AZD9291 在体外有效抑制 EGFRm+(例如 PC9;< 25 nM)和 EGFR m+/T790M(例如 H1975;< 25 nM)细胞系中的 EGFR 磷酸化,同时对野生型 EGFR 系(例如 LoVo)的活性要低得多;> 500 nM)。一致地,与野生型体外相比,AZD9291 在突变型 EGFR 细胞系中显示出更有效的增殖抑制作用。
在LUAD细胞系(PC9和HCC827)中过表达METTL7B会诱导对奥希替尼的耐药性,使IC50值相较于载体对照细胞提高2-3倍。相反,在奥希替尼耐药细胞系(PC9-OR、PC9-GR、H1975)中敲低METTL7B可使细胞重新对奥希替尼敏感,将IC50降至对照水平的40%-80%。METTL7B诱导的奥希替尼耐药与增强的谷胱甘肽代谢、抗氧化酶(GPX4、SOD1、HMOX1)表达及酶活性增加以及m6A RNA修饰水平升高相关。使用ROS清除抑制剂BSO (200 μM) 或m6A修饰抑制剂3-脱氮腺苷 (3-DA, 10 μM) 处理,可在体外逆转METTL7B介导的对奥希替尼的耐药性。[1] 金纳米簇辅助递送靶向METTL7B的siRNA (GNC-siMETTL7B) 与奥希替尼联用,能显著使奥希替尼耐药的PC9-OR细胞重新敏感,其IC50值低于siRNA对照组的治疗。[1] |
| 体内研究 (In Vivo) |
AZD9291(5mg/kg po)可引起 EGFRm+ (PC9) 和 EGFRm+/T790M (H1975) 肿瘤模型的肿瘤深度消退,并在体内深度抑制 EGFR 磷酸化和关键下游信号通路(如 AKT 和 ERK)。
在细胞来源的异种移植 (CDX) 小鼠模型中,由过表达METTL7B的PC9细胞形成的肿瘤对奥希替尼治疗(30 mg/kg,口服,每日一次)表现出显著耐药性,表现为肿瘤持续生长,而载体对照肿瘤则缩小。[1] 在多西环素诱导的METTL7B表达CDX模型中,诱导METTL7B表达会赋予肿瘤对奥希替尼治疗的耐药性。[1] 在奥希替尼耐药的PC9-OR CDX模型中,使用GNC-siMETTL7B敲低METTL7B并与奥希替尼(30 mg/kg,口服,每日一次)联合治疗,相较于单独使用奥希替尼,能显著抑制肿瘤生长。[1] 联合使用谷胱甘肽生物合成抑制剂BSO(450 mg/kg,腹腔注射,隔日一次)可消除CDX小鼠模型中METTL7B诱导的对奥希替尼的耐药性。[1] |
| 酶活实验 |
奥希替尼(Osimertinib),原名mereletinib和AZD-9291,是第三代EGFR抑制剂,可口服且不可逆。它选择性地靶向 EGFR 的特定突变体,在 LoVo 细胞中对野生型 EGFR、L858R/T790M EGFR 和外显子 19 缺失 EGFR 的 IC50 值分别为 493.8 nM。它通过抑制激活性和耐药性 EGFR 突变,同时保护正常皮肤和肠道细胞中的正常形式 EGFR,减少与当前可用药物相关的副作用。
|
| 细胞实验 |
在 96 孔板中,细胞以每孔 3,000 个细胞的密度铺板。在培养基中添加奥西替尼可产生 72 小时的治疗效果。 Cell Counting Kit-8 用于进行细胞活力测定。
进行细胞活力实验时,将LUAD细胞以每孔3000个细胞的密度接种于96孔板中。奥希替尼溶于DMSO并用培养基稀释。细胞用一系列浓度的奥希替尼或载体对照处理72小时。根据说明书使用Cell Counting Kit-8 (CCK-8) 评估细胞活力。测量吸光度,并使用GraphPad Prism软件计算和比较IC50值。[1] 为评估氧化应激,使用荧光探针 (DCFH-DA) 测量细胞内ROS水平。细胞与探针在37°C孵育30分钟,在488 nm激发光和525 nm发射光下测量荧光强度。使用特异性荧光探针测量RNS水平,在37°C孵育30分钟,在490 nm激发光和516 nm发射光下测量。[1] 为检测SOD酶活性,将细胞蛋白提取物与WST-8/酶工作液在37°C孵育30分钟,在450 nm波长测量吸光度。为检测GPX酶活性,将细胞蛋白提取物与含有NADPH的GPX检测工作液在25°C孵育15分钟。加入过氧化物后,在340 nm波长连续监测吸光度5分钟。[1] 金纳米簇辅助递送siRNA (GNC-siRNA) 复合物的制备方法是将带正电荷的金纳米簇与siRNA溶液在超纯水中混合并震荡,通过静电作用结合。形成的GNC-siMETTL7B复合物随后用于转染细胞。[1] |
| 动物实验 |
本研究采用 5 mg/kg 剂量的 p.oEGFRm+ 和 EGFRm+/T790M 转基因小鼠、METTL7B 过表达的肺腺癌 (LUAD) 细胞系、吉非替尼和奥希替尼耐药的细胞来源肿瘤异种移植 (CDX) 和患者来源肿瘤异种移植 (PDX) 小鼠模型,评估 METTL7B 在酪氨酸激酶抑制剂 (TKI) 耐药中的作用。采用超高效液相色谱-串联质谱 (UPLC-MS/MS) 鉴定 METTL7B 调控的代谢物。通过甲基化 RNA 免疫沉淀 (MeRIP)-qPCR 分析检测 METTL7B 靶基因 mRNA 的 N6-甲基腺苷 (m6A) 修饰状态。采用金纳米簇辅助递送靶向METTL7B的siRNA(GNC-siMETTL7B)来评估METTL7B在酪氨酸激酶抑制剂(TKI)耐药中的作用。[1]
对于细胞来源的异种移植(CDX)模型,将肺腺癌(LUAD)细胞(例如PC9、PC9-OR、PC9-GR;每只小鼠1×107个细胞)皮下接种到4-5周龄雌性BALB/c裸鼠(nu/nu)的侧腹部。[1] 对于强力霉素诱导的METTL7B表达模型,接种携带诱导构建体的PC9细胞。[1] 肿瘤达到稳定大小后,将小鼠随机分组进行治疗。奥希替尼以30 mg/kg体重的剂量,每日一次(qd)口服给药。 [1]在联合治疗研究中,奥希替尼(30 mg/kg,口服,每日一次)与BSO(450 mg/kg,腹腔注射,隔日一次)或GNC-siMETTL7B复合物(每只小鼠含6 mg siRNA当量,给药途径推测为静脉注射或瘤内注射,但原文未明确说明)联合给药。[1]对于诱导型模型,给予强力霉素(饮用水中浓度为1.5 mg/mL或等效浓度)以诱导METTL7B表达。[1]定期使用游标卡尺测量肿瘤尺寸,并使用公式V = L × W2 / 2计算肿瘤体积。同时监测体重。[1] |
| 药代性质 (ADME/PK) |
奥希替尼为口服药物。推荐临床剂量为每日一次,每次 80 mg。[2]
该综述指出,基于临床前和临床证据,奥希替尼具有优异的中枢神经系统穿透性。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
在 AURA3 试验中,奥希替尼的耐受性优于铂类-培美曲塞化疗,≥3 级不良反应的发生率更低(23% vs. 47%)。[2] 在一线 FLAURA 试验中,奥希替尼 ≥3 级不良反应的发生率低于第一代 EGFR-TKI(34% vs. 45%)。[2] 奥希替尼联合免疫检查点抑制剂度伐利尤单抗的试验因肺毒性发生率增加而终止。[2]
|
| 参考文献 | |
| 其他信息 |
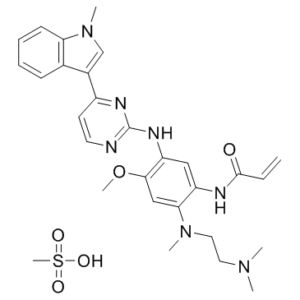
甲磺酸奥希替尼是由等摩尔量的奥希替尼和甲磺酸制备的甲磺酸盐。它用于治疗EGFR T790M突变阳性的非小细胞肺癌。它是一种抗肿瘤药物和表皮生长因子受体拮抗剂。它含有奥希替尼(1+)。
甲磺酸奥希替尼是奥希替尼的甲磺酸盐形式,奥希替尼是一种第三代口服、不可逆、突变选择性的表皮生长因子受体(EGFR)抑制剂,具有潜在的抗肿瘤活性。口服后,奥希替尼与多种EGFR突变体共价结合并抑制其活性,包括继发性耐药突变T790M、L858R和19号外显子缺失,从而阻断EGFR介导的信号传导。这既可以诱导EGFR过表达肿瘤细胞死亡,也可以抑制肿瘤生长。EGFR是一种受体酪氨酸激酶,在多种肿瘤细胞类型中发生突变,在肿瘤细胞增殖和肿瘤血管生成中起着关键作用。由于该药物对EGFR突变体具有选择性,因此与也会抑制野生型EGFR的非选择性EGFR抑制剂相比,其毒性可能降低。 另见:奥希替尼(具有活性部分)。 奥希替尼是一种第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),用于治疗EGFR突变型非小细胞肺癌(NSCLC),特别是肺腺癌(LUAD)。[1] 本研究旨在探讨EGFR-TKI(包括奥希替尼)的耐药机制。该研究发现甲基转移酶样蛋白7B (METTL7B) 是肺腺癌(LUAD)中奥希替尼耐药的关键因素,且与继发性EGFR突变无关。METTL7B通过m6A RNA修饰上调GPX4、SOD1和HMOX1,从而增强细胞抗氧化防御能力,进而促进耐药性,清除活性氧(ROS),而ROS的积累可能影响酪氨酸激酶抑制剂(TKI)的疗效。[1] 靶向METTL7B(例如,通过siRNA敲低)被认为是一种逆转奥希替尼耐药性的潜在策略。[1] |
| 分子式 |
C29H37N7O5S
|
|---|---|
| 分子量 |
595.72
|
| 精确质量 |
595.257
|
| 元素分析 |
C, 58.47; H, 6.26; N, 16.46; O, 13.43; S, 5.38
|
| CAS号 |
1421373-66-1
|
| 相关CAS号 |
Osimertinib;1421373-65-0;Osimertinib-d6;1638281-44-3;Osimertinib dimesylate;2070014-82-1
|
| PubChem CID |
78357807
|
| 外观&性状 |
Light yellow solid powder
|
| LogP |
5.817
|
| tPSA |
153.79
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
42
|
| 分子复杂度/Complexity |
845
|
| 定义原子立体中心数目 |
0
|
| SMILES |
S(C([H])([H])[H])(=O)(=O)O[H].O(C([H])([H])[H])C1=C(C([H])=C(C(=C1[H])N(C([H])([H])[H])C([H])([H])C([H])([H])N(C([H])([H])[H])C([H])([H])[H])N([H])C(C([H])=C([H])[H])=O)N([H])C1=NC([H])=C([H])C(C2=C([H])N(C([H])([H])[H])C3=C([H])C([H])=C([H])C([H])=C32)=N1
|
| InChi Key |
FUKSNUHSJBTCFJ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C28H33N7O2.CH4O3S/c1-7-27(36)30-22-16-23(26(37-6)17-25(22)34(4)15-14-33(2)3)32-28-29-13-12-21(31-28)20-18-35(5)24-11-9-8-10-19(20)24;1-5(2,3)4/h7-13,16-18H,1,14-15H2,2-6H3,(H,30,36)(H,29,31,32);1H3,(H,2,3,4)
|
| 化学名 |
N-[2-[2-(dimethylamino)ethyl-methylamino]-4-methoxy-5-[[4-(1-methylindol-3-yl)pyrimidin-2-yl]amino]phenyl]prop-2-enamide;methanesulfonic acid
|
| 别名 |
AZD-9291 mesylate; Mereletinib mesylate; AZD9291; AZD 9291; Trade name: Tagrisso
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1.39 mg/mL (2.33 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 13.9 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.39 mg/mL (2.33 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 13.9mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 1.39 mg/mL (2.33 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 1% DMSO+30% PEG 300+dd H2O: 30mg/mL 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6786 mL | 8.3932 mL | 16.7864 mL | |
| 5 mM | 0.3357 mL | 1.6786 mL | 3.3573 mL | |
| 10 mM | 0.1679 mL | 0.8393 mL | 1.6786 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05880706 | Recruiting | Drug: Osimertinib Mesylate Tablets Drug: BL-B01D1 |
Non-small Cell Lung Cancer | Sichuan Baili Pharmaceutical Co., Ltd. |
July 19, 2023 | Phase 2 |
| NCT05020769 | Recruiting | Drug: SI-B001 Drug: Osimertinib |
Non-small Cell Lung Cancer | Sichuan Baili Pharmaceutical Co., Ltd. |
January 6, 2022 | Phase 2 Phase 3 |
| NCT05085054 | Not yet recruiting | Drug: Osimertinib Mesylate | Non Small Cell Lung Cancer | Wuhan Union Hospital, China | June 1, 2022 | Phase 2 |
| NCT05816252 | Recruiting | Drug: Osimertinib Drug: Carboplatin |
Non-small Cell Lung Cancer | Klus Pharma Inc. | April 19, 2023 | Phase 2 |
| NCT05085054 | Not yet recruiting | Drug: Osimertinib Mesylate | Non Small Cell Lung Cancer | Wuhan Union Hospital, China | June 1, 2022 | Phase 2 |
AZD9291 binding mode and structure.Cancer Discov.2014 Sep;4(9):1046-61. |
|---|
Effect of AZD9291 on EGFR phosphorylationin vitro.Cancer Discov.2014 Sep;4(9):1046-61. |
In vivoanti-tumor efficacy of AZD9291 in subcutaneous xenograft models of EGFR-TKI sensitising and T790M resistant lung cancer.Cancer Discov.2014 Sep;4(9):1046-61. |
AZD9291 induces significant and sustained tumor regression in transgenic models of EGFR-TKI sensitising (C/L858R) and T790M resistant (C/L+T) lung cancer.Cancer Discov.2014 Sep;4(9):1046-61. |
|---|
AZD9291 inhibits EGFR phosphorylation and downstream signallng in murine models of EGFR T790M resistant lung cancer.Cancer Discov.2014 Sep;4(9):1046-61. |
Proof of concept clinical studies validating AZD9291 as a mutant-selective EGFR kinase T790M inhibitor.Cancer Discov.2014 Sep;4(9):1046-61. |