| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| Other Sizes |
|
| 靶点 |
Mitochondrial toxin; mitochondrial adenine nucleotide translocase (ANT)
|
|---|---|
| 体外研究 (In Vitro) |
Bongkrekic acid(0-50 μM;48 小时)的 EC50 分别为 34.14 μM、>50 μM 和 2.58 μM,可诱导 MDA-MB-231、MCF-7 和 LTED 细胞产生甲臜。在 LTED 细胞和亲代 MCF-7 细胞中,bongkrekic Acid(0.1–25 μM;48 小时)以剂量依赖性方式减少活细胞数量 [1]。
米酵菌酸/BKA/Bongkrekic acid对ERα阳性(MCF-7和LTED细胞)及ERα阴性MDA-MB-231细胞中甲臜生成的影响。[3] 我们首先使用MTS试剂[3-(4,5-二甲基噻唑-2-基)-5-(3-羧甲氧基苯基)-2-(4-磺苯基)-2H-四唑;Owen试剂]进行MTS实验,分析米酵菌酸/BKA(图1)和脂肪酸(FAs)是否影响乳腺癌细胞中甲臜的形成。MTS实验利用还原当量(如辅酶还原型烟酰胺腺嘌呤二核苷酸磷酸NADH)将MTS转化为有色甲臜产物;MTS可能被线粒体琥珀酸脱氢酶(复合体II组分)选择性裂解(图2)。该实验通常作为[3H]胸苷掺入法的替代方法。如图3所示,我们研究了BKA对三种乳腺癌细胞系(MDA-MB-231、MCF-7和LTED)甲臜生成的影响。虽然BKA在MCF-7细胞中显著促进甲臜形成(EC50=34.14 μM),但在MDA-MB-231细胞中仅微弱刺激(EC50>50 μM)(图3A)。当比较MCF-7与LTED细胞时,即使接种细胞数相同(5×103细胞/孔),LTED细胞的基线甲臜生成量仍比亲代MCF-7细胞高约1.5倍(图3B左图)。在LTED细胞实验中,BKA以EC50=2.58 μM有效刺激甲臜生成(图3B右图)。因此,BKA似乎优先加速乳腺癌细胞(尤其是ERα阳性的LTED细胞)的甲臜形成。 BKA/米酵菌酸介导的活细胞数量减少:LTED细胞与亲代MCF-7细胞的比较。[3] 甲臜生成的增强通常反映活细胞数量(即细胞活力)。若BKA处理的LTED细胞符合此规律,其他活细胞检测方法的结果应与MTS实验一致。我们使用钙黄绿素(calcein AM)探针和台盼蓝染色检测活细胞。该探针可穿透"活细胞"膜,被胞内酯酶水解为绿色荧光钙黄绿素。由于死细胞缺乏酯酶,活细胞被选择性标记。尽管25 μM BKA对MDA-MB-231细胞活力无影响(数据未显示),但在≤25 μM浓度下轻微减少MCF-7活细胞数量(图4A),并以浓度依赖性方式显著减少LTED活细胞(图4B)。台盼蓝排斥实验也检测到BKA介导的细胞生长抑制(数据未显示)。此外,与溶剂对照组相比,BKA更显著影响LTED细胞形态(暗示细胞死亡响应)(图4C)。EthD-III探针分析表明,BKA介导的细胞死亡不依赖坏死性凋亡(图4D)。 乳腺癌细胞中LDH-A的表达状态及米酵菌酸/BKA对其表达的影响。[3] LDH-A是乳腺组织中调节糖酵解过程丙酮酸转化为乳酸的主要亚型。侵袭性强的MDA-MB-231细胞即便在氧气存在下也通过糖酵解途径获取ATP(即"糖酵解"表型),将葡萄糖转化为乳酸并降低OXPHOS活性(图5A)。相比之下,非侵袭性/低致瘤性MCF-7细胞利用OXPHOS途径产ATP且糖酵解活性较低(即"氧化"表型)(图5B)。半定量和实时RT-PCR分析显示,LDH-A表达水平依次为:MDA-MB-231细胞(5.79/2.3倍)>> MCF-7细胞(1.0倍)=LTED细胞(0.76/1.3倍)(图6A)。因此LTED细胞与亲代MCF-7同属"氧化表型"。BKA和FAs(PA和AA)处理显示:AA对所有乳腺癌细胞无调节作用;PA普遍上调LDH-A表达;而BKA在LTED细胞中显著下调其表达(0.66倍 vs 对照1.0倍)(图6B-D)。 乳腺癌细胞中PDK4的表达状态及米酵菌酸/BKA对其表达的影响。[3] PDK4通过抑制线粒体丙酮酸脱氢酶复合体(PDH)调控葡萄糖氧化。实时RT-PCR显示三种乳腺癌细胞的基础PDK4表达差异显著:MDA-MB-231细胞(2.18倍)> MCF-7细胞(1.0倍)> LTED细胞(0.08倍)(图7A),表明LTED细胞生长高度依赖葡萄糖氧化供能。FAs处理中,两种FA均显著刺激MDA-MB-231细胞的PDK4表达;AA上调而PA下调MCF-7/LTED细胞的PDK4(图7B-D)。值得注意的是,BKA"选择性"下调LTED细胞的PDK4表达(图7D),与图6D中LDH-A的结果共同提示:BKA通过降低PDK4/LDH-A水平解除对PDH的抑制,从而促进葡萄糖利用。 乳腺癌细胞中Topo IIα的表达状态及米酵菌酸/BKA对其表达的影响。[3] 增殖标志物Topo IIα的表达强度依次为:MDA-MB-231细胞(1.3倍)> MCF-7细胞(1.0倍)> LTED细胞(0.54倍)(图8A)。25 μM PA降低MDA-MB-231细胞活力(图8B)。BKA仅下调LTED细胞的Topo IIα表达(图8D),此选择性调节与PDK4结果一致(见图6-7)。Ki-67检测进一步证实BKA对LTED细胞增殖的选择性抑制(0.41±0.014 vs 对照1.0, p<0.05)。与BKA促进甲臜形成相反(图2B),其降低了LTED细胞中增殖标志物(Topo IIα和Ki-67)水平和活细胞数量(图3B和8D)。 简化米酵菌酸/BKA类似物对甲臜生成及PPARγ介导转录活性的影响。[3] 我们合成两种简化BKA类似物BKA-1'和BKA-4,与BKA、BKA-2、BKA-3共同进行实验。其中仅BKA-3在50 μM时表现出弱于母体BKA的刺激活性(图3B和9B)。PPARγ转录实验显示BKA-3(4.86倍)、BKA-4(4.18倍)和BKA(2.07倍)激活PPARγ(图9C)。尽管BKA-3/BKA-4的PPARγ激活潜力约为BKA的2倍,但它们对甲臜形成的影响极弱或呈阴性,提示BKA对PPARγ的激活作用不直接参与LTED细胞死亡。 BKA/米酵菌酸对Cu2+介导氧化的不敏感性。[3] BKA结构中的二烯亚甲基(-CH=CH-CH=CH-CH2-)可能是可氧化位点(图1)。但如图10B所示,BKA对Cu2+氧化不敏感(而亚油酸LA可被氧化),且对15-LOX也具有抗性。200-800 nm波长范围内未检测到吸收峰(数据未显示),表明BKA比LA更耐受Cu2+介导的氧化。 ADP/ATP载体还能被米酵菌酸(BA)高效特异性抑制,这种由Pseudomonas cocovenenans细菌分泌的天然毒素是一种多不饱和长链脂肪酸衍生物(图2B)。BA以纳摩尔级亲和力(Kd)与线粒体基质侧载体位点结合,因此不同于ATRs,BA需穿过线粒体内膜才能抑制ADP/ATP转运。 研究表明ATRs与米酵菌酸/BA对ADP/ATP载体的结合互斥。此现象证明载体存在两种构象状态:能结合CATR的"CATR构象"和能结合BA的"BA构象"。这两种构象在线粒体膜中动态平衡,但CATR或BA会使平衡偏向形成稳定的CATR-载体或BA-载体复合物。这些复合物可通过化学/免疫化学反应性及蛋白酶敏感性区分。无抑制剂时,仅ADP/ATP能触发两种构象快速转换,表明该转变参与转运过程。此特性为在分子水平研究转运机制提供了独特优势。[2] |
| 体内研究 (In Vivo) |
Tempe bongkrek是印度尼西亚爪哇当地生产的廉价蛋白质来源。它是通过将椰奶或椰油生产的椰子肉副产品压成蛋糕,然后接种寡孢霉进行发酵制成的。最终产品被切成片或切成块用于煎炸或煮汤。如果发酵不完全,B. cocovenenans和Bongkrekic acid/BA可以增殖。1895年首次报道了与食用坦佩邦克有关的BA中毒死亡。自1975年以来,食用受污染的tempe bongkrek已导致近3000例BA中毒,其中至少150例死亡。在印度尼西亚,报告的BA中毒患者死亡率平均为60%。在1988年爆发后,禁止生产tempe bongkrek,但生产和偶尔爆发继续发生。
在中国东北,用于制作面包、面条和饺子的发酵玉米制品似乎是Bongkrekic acid/BA中毒的主要来源。在中国南方,吊姜糕与BA中毒事件有关。此外,在中国和其他亚洲国家消费的银耳蘑菇中,有一半可能被土壤中的cocovenenans污染。BA暴发通常发生在印度尼西亚和中国温暖的夏季。 2015年,亚洲以外首次报道了Bongkrekic acid/BA毒性的暴发。2015年在莫桑比克西北部爆发的疫情导致75人死亡,许多饮用pombe的人患病,pombe是一种自制的发酵玉米粉饮料(表1)。 在早期研究Bongkrekic acid/BA的细胞病理生理学中,Welling等人发现羊心脏组织中葡萄糖含量和细胞摄氧量呈剂量依赖性降低,并伴有乳酸积累和酸中毒。这些发现使他们假设BA抑制线粒体酶。后来的研究表明,BA是ANT的特异性配体,通过将ANT冻结在其“m”(基质取向)构象中来抑制转位酶。每1 mg线粒体蛋白中仅1 μmol BA就足以完全阻断ADP的磷酸化。在6 mmol ATP条件下,每1 mg线粒体蛋白约需要10 μmol BA才能完全阻断ATP的水解。其他也能抑制ANT的天然毒素包括白术苷、离白术苷、伪羧基白术苷、表白术苷、羧基白术苷、芳基叠氮白术苷、n-乙基马来酰亚胺、木耳酸和异戊二酸。 诊断测试: 检测B. cocovenenans和Bongkrekic acid/BA困难且不可靠。已从受污染的食物和呕吐物中分离出cocovenenans。可以使用Biologic GN2系统等商业检测试剂盒进行识别。cocovenenans最常用的鉴定方法是16S rDNA测序,但有时会错误地鉴定出cocovenenans的其他伯克氏菌病原体。B. cocovenenans可以通过毛细管电泳-单链构象多态性(CE-SSCP),微阵列分析或基于探针的细胞捕捞来鉴定。最可靠的方法可能是多重PCR协议。从泰国一名男子的淋巴腺样体和肺组织中分离到cocovenenans,并通过16s rDNA测序进行鉴定。我们未见其他从生物培养基中分离检测出cocovenenans的报道。 我们找不到任何已发表的检测生物培养基Bongkrekic acid/BA的报道,但环境样品中BA的存在和定量可以使用液体薄层色谱法、色谱-质谱法和高压液相色谱法[1]进行检测。 |
| 细胞实验 |
甲醛形成分析(MTS)。[3]
在MTS实验中,细胞以5×103细胞/孔的密度接种在96孔板上,并在4小时后引入FAs和Bongkrekic acid/BKA(单个浓度如图所示)。48小时孵育后,根据制造商的说明,使用CellTiter 96®水溶液细胞增殖试验分析细胞活力。试验化学品在适当的有机溶剂中制备,包括二甲基亚砜(DMSO)或乙醇。对照培养皿中添加了等量的溶剂,在使用的最终浓度下,载体对甲醛的形成没有可测量的影响。 活/死细胞分析。[3] 将MCF-7和LTED细胞以5×103细胞密度接种于200 μl细胞培养基的96孔板上,接种4 h后分别加入Bongkrekic acid/BKA(0.01、1和25 μM)。48小时孵育后,根据制造商的说明,使用活/死细胞染色试剂盒II分析活细胞和坏死细胞。采用glmax - multi检测系统检测钙黄素- am和乙啶同二聚体III (EthD-III)的荧光。在ltd细胞形态学检查中,使用徕卡dil倒置显微镜获得图像,使用Pixera®Penguin 600CL冷却CCD数码相机拍摄。数据处理采用Pixera Viewfinder 3.0软件。将乳腺癌细胞镀于6孔板上。在每口井中识别出三个细胞密度近似相等的区域,并捕获每个区域的图像。 转染和荧光素酶报告试验(双荧光素酶试验)。[3] 转染前一天,将MCF-7细胞(5×104 cells/well)接种于含有MEMα培养基的24孔板上。根据制造商的说明,使用Lipofectamine®LTX和PLUS™试剂转染每个表达质粒。人PPARγ表达质粒与人类视黄醇X受体α (RXRα)质粒结合的最大转录效率分别为100 ng和100 ng。将含有大鼠酰基辅酶a氧化酶PPRE的300 ng PPRE- luc质粒与20 ng Renilla荧光素酶报告质粒(pRL-CMV)的DNA混合物在24孔板上共转染。所有质粒浓度均与pcDNA3.1载体相等。人PPARγ、RXRα和PPRE报告基因表达质粒由Curtis J. Omiecinski博士赠送。转染24 h后,用磷酸盐缓冲盐水洗涤细胞,将细胞转化为不含酚红的MEMα,并添加5%血清,然后用Bongkrekic acid/BKA及其衍生物(BKA-1 ', BKA-2, BKA-3和BKA-4)处理24 h。用100 μl的被动裂解缓冲液制备细胞提取物,20 μl用于glmax - multi检测系统检测萤火虫荧光素酶和Renilla荧光素酶。每个样品中萤火虫荧光素酶活性(从报告质粒表达)与Renilla荧光素酶活性(从pRL-CMV表达)的比值作为标准化荧光素酶活性的测量。 共轭二烯形成的测定。[3] 实验是根据先前描述的程序进行的。Bongkrekic acid/BKA或LA在铜(Cu2+, CuSO4)存在下,在分光光度管(1.0 cm光程)中,在100mm硼酸缓冲液中,pH为9.0,室温下孵育不同时间。加入铜后,定期记录234 nm处的吸光度。结果表示为反应混合物在时间为零时吸光度的增加。 |
| 药代性质 (ADME/PK) |
暴露[1]
邦克列酸的产生取决于两个截然不同且先后发生的环境条件:首先是支持细菌生长和增殖的环境,其次是有利于邦克列酸/BA产生的环境(表2)。邦克列酸在温暖(22–30 °C)且pH值呈中性的环境中产生,这与天贝的制作条件相同。其产生还取决于脂肪酸的存在,特别是椰子和玉米中存在的脂肪酸。含有油酸的细菌培养基产生的BA浓度最高。当椰子毒素杆菌在理想条件下于椰子培养基上培养时,毒素产量在培养第二天即可达到2–4 mg/g。月桂酸、肉豆蔻酸和棕榈酸占椰子油中脂肪酸的71.5–74.5%(重量比),而玉米中也含有不同浓度的油酸。有趣的是,R. oligosporum 对 BA 的产生有抑制作用,当允许其形成足够数量的真菌菌落时,可以降低 BA 浓度。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒物动力学[1]
关于Bongkrekic acid/BA在人体内的毒物动力学和致死剂量信息有限。有资料显示,1-1.5 mg 的剂量即可致人死亡,另有资料显示,口服 LD50 为 3.16 mg/kg。小鼠研究表明,口服 LD50 为 0.68-6.84 mg/kg,静脉注射 LD50 为 1.41 mg/kg。另一项大鼠研究表明,口服 2 mg/100 g 的剂量可在 2-5 小时内导致死亡。在同一项研究中,大鼠在首次服用 1 mg/100 g 剂量后存活,但 48 小时后再次服用该剂量导致死亡。 尽管 BA 可能具有较大的分布容积,因为它是一种高度不饱和脂肪且脂溶性很高,但Bongkrekic acid/BA的吸收曲线和分布容积尚不清楚。我们尚不清楚邦克列酸 (BA) 的代谢途径。早期研究报告称,根据核磁共振波谱、紫外光谱、摩尔消光系数和质谱分析,黄毒素 A(一种也被认为存在于椰子毒伯克霍尔德氏菌中的毒素)和 BA 是同一种有机化合物。但最近的研究推测,黄毒素 A 可能是 BA 的代谢产物。BA 的消除途径尚不清楚。 毒性概述 鉴定和用途:邦克列酸 (BA) 是一种白色无定形固体。已知 BA 由椰子毒伯克霍尔德氏菌产生。它被用作生物化学研究的工具。人体研究:在莫桑比克的一个乡村小镇,超过 230 人患病,其中 75 人死于与饮用 pombe(一种传统酒精饮料)相关的疾病。在疑似污染的裂果中检测到了毒性水平的BA,但在对照裂果中未检测到。在用于制作裂果的面粉中检测到了产生BA的细菌——椰子毒伯克霍尔德氏菌(Burkholderia gladioli pathovar cocovenenans)。BA是腺嘌呤核苷酸转位酶(ANT)的抑制剂。由于ANT的抑制与线粒体释放细胞色素c的抑制有关,进而导致细胞凋亡的抑制,因此它被用作研究细胞凋亡机制的工具。BA与印度尼西亚和中国发生的涉及椰子和玉米制品的食源性疾病暴发有关。动物研究:BA 是一种强效的线粒体 ATP/ADP 转位酶抑制剂,它通过刺激 ATP 敏感性钾通道 (K-ATP 通道) 的活性来抑制胰岛 β 细胞中葡萄糖诱导的电活动。 小鼠静脉注射 LD50 为 1410 ug/kg,《四面体》,26(5993),1970 小鼠静脉注射 LDLotoralt 为 6840 ug/kg。行为:嗜睡(总体活动抑制);行为:僵硬;肺、胸腔或呼吸:呼吸困难,《应用与环境微生物学》,48(690),1984 [PMID:6391376] 相互作用 研究了邦克列酸对茎菠萝蛋白酶、木瓜蛋白酶和无花果蛋白酶的体外作用。邦克列酸抑制了这些酶对酪蛋白的水解,但即使使用大量过量的效应物,抑制作用也始终不完全。使用经有机汞琼脂糖亲和柱纯化的完全活化的茎菠萝蛋白酶样品,邦克列酸的抑制作用并非化学计量关系。在24℃下与过量的邦克列酸孵育20分钟后,半胱氨酸的巯基(-SH)仍然保持完整。然而,用 5 mM 半胱氨酸或 2-巯基乙醇在 37°C 孵育 5 分钟可逆转凤梨茎蛋白酶被邦克列酸部分抑制的现象。乙二醇和甘油则没有这种恢复作用。这些结果表明,邦克列酸分子与硫醇蛋白酶非共价结合,仅部分且可逆地屏蔽其必需的巯基 (-SH)。Murachi T 等;Toxicon 20 (6): 1011-7 (1982) 解毒剂和急救处理 /SRP:/ 立即采取急救措施:确保已进行充分的去污处理。如果患者停止呼吸,应立即开始人工呼吸,最好使用按需呼吸机、球囊面罩或简易呼吸面罩,并按照培训内容进行操作。必要时进行心肺复苏。立即用流动清水冲洗受污染的眼睛。切勿催吐。如果发生呕吐,应将患者身体前倾或置于左侧卧位(如有可能,头部向下),以保持呼吸道通畅并防止误吸。保持患者安静并维持正常体温。立即就医。/A类和B类中毒/ /SRP:/ 基本治疗:建立通畅的呼吸道(必要时使用口咽或鼻咽通气道)。必要时进行吸痰。观察呼吸功能不全的迹象,必要时辅助通气。使用无创呼吸面罩以10至15升/分钟的流量给予氧气。监测肺水肿,必要时进行治疗……。监测休克,必要时进行治疗……。预判癫痫发作,必要时进行治疗……。如果眼睛受到污染,立即用水冲洗眼睛。在转运过程中,持续用0.9%生理盐水冲洗每只眼睛……。不要使用催吐剂。误服时,漱口并给予5 mL/kg至200 mL的水稀释,前提是患者能够吞咽、有强烈的咽反射且不流涎……。皮肤烧伤经去污后,用干燥的无菌敷料覆盖……。/A类和B类毒物/ /SRP:/ 高级治疗:对于意识不清、严重肺水肿或严重呼吸窘迫的患者,考虑进行口咽或鼻咽气管插管以控制气道。使用球囊面罩进行正压通气可能有效。考虑药物治疗肺水肿……。考虑使用β受体激动剂(如沙丁胺醇)治疗严重支气管痉挛……。监测心律,必要时治疗心律失常……。开始静脉输注5%葡萄糖溶液(D5W TKO)/SRP:“保持通畅”,最小流速/。如果出现低血容量的迹象,请使用0.9%生理盐水(NS)或乳酸林格氏液(LR)。对于伴有低血容量迹象的低血压,应谨慎输液。注意液体过量的迹象……。使用地西泮(安定)或劳拉西泮(阿提凡)治疗癫痫发作……。使用盐酸丙美卡因辅助眼部冲洗……。/毒物A和B/ 人类毒性摘录/病例报告/ 2015年1月,莫桑比克奇蒂马村75人在参加葬礼后死亡,177人住院。死亡与饮用一种名为pombe的传统非洲饮料有关。对疑似致病的pombe样本进行了多项分析,并与对照样本进行了比较。最终,非靶向液相色谱-质谱联用筛选检测到了强效毒素邦克列酸及其结构异构体异邦克列酸的存在。定量分析发现,疑似裂殖酵母样品中这些毒素的含量可能达到致命水平。已知邦克列酸由椰子毒伯克霍尔德氏菌(Burkholderia gladioli pv. cocovenenans)产生。虽然未能从疑似裂殖酵母中分离出该菌,但从酿酒者家中获得的玉米粉(裂殖酵母的起始原料)中分离出了鉴定为椰子毒伯克霍尔德氏菌的细菌。当将这些细菌与同样从玉米粉中分离出的米根霉(Rhizopus oryzae)共培养时,观察到了邦克列酸的协同产生。研究结果提示了一种邦克列酸中毒的机制,这种现象此前被认为仅限于印度尼西亚和中国的特定地区。PMID:27823840 /病例报告/ 背景:2015年1月9日,在莫桑比克的一个乡村小镇,超过230人因饮用一种名为“pombe”的传统酒精饮料而患病,其中75人死亡。方法:我们开展了一项调查,以确定病例患者并找出疫情爆发的原因。病例患者的定义为:奇蒂马镇居民,在1月9日上午6:00至1月12日晚上11:59期间出现任何新的或无法解释的神经系统、胃肠道或心血管症状。我们进行了病历审查、医护人员和社区调查、对当地药用植物和商业杀虫剂进行人类学和毒理学调查,并对疑似病例和对照的“pombe”进行了实验室检测。结果:我们共识别出234例病例患者;其中75例(32%)死亡,159例康复。总体而言,61%的病例患者为女性(n = 142),年龄范围为1至87岁(中位年龄30岁)。体征和症状包括腹痛、腹泻、呕吐和全身不适。死亡前出现精神运动性躁动和异常姿势。从食用pombe到出现症状的中位时间间隔为16小时。在疑似病例的pombe中检测到了毒性水平的邦克列酸(BA),但在对照pombe中未检测到。在用于制作pombe的面粉中检测到了产生BA的细菌——椰子毒伯克霍尔德氏菌(Burkholderia gladioli pathovar cocovenenans)。结论:我们首次报道了非洲与致命食源性毒素BA相关的高致死性疾病暴发。鉴于此前亚洲以外地区未曾发现过此类疫情,我们的调查表明,BA 可能是全球范围内尚未被充分认识的毒性疫情的病因。PMID:29155976 /替代和体外试验/ 背景/目的:本研究利用长期雌激素剥夺的 MCF-7 (LTED) 细胞体外模型,分析了使用雌激素受体α (ERα) 信号阻断剂治疗的乳腺癌的再生长机制。邦克列酸 (BKA) 是一种从被椰子伯克霍尔德氏菌污染的椰子豆豉中分离得到的天然毒素。材料与方法:本研究采用了 LTED 细胞、MCF-7 细胞和 MDA-MB-231 细胞。用 BKA(化学合成;纯度:>98%)处理后,进行了多项生化分析。结果:LTED细胞被归类为氧化表型。当LTED细胞用BKA处理时,乳酸脱氢酶A(LDH-A)/丙酮酸脱氢酶激酶4(PDK4)表达下调,从而促进线粒体氧化磷酸化对葡萄糖的过度利用,并诱导细胞死亡反应。在所分析的其他乳腺癌细胞中未观察到BKA的这些作用。结论:我们认为BKA可作为LTED细胞癌症生物学分析的实验工具。PMID:27798877 /替代和体外试验/ 邦克列酸(BKA)是腺嘌呤核苷酸转位酶(ANT)的抑制剂。由于ANT抑制剂与线粒体释放细胞色素c的抑制相关,进而导致细胞凋亡的抑制,因此它被用作研究细胞凋亡机制的工具。BKA由一条长碳链组成,该碳链包含两个不对称中心、一个非共轭烯烃、两个共轭二烯、三个甲基、一个甲氧基和三个羧酸基团。这种复杂的化学结构给其合成、供应和生化机制研究带来了困难。在本研究中,我们受BKA分子结构的启发,设计并合成了一系列结构更为简单的三羧酸衍生物。随后,我们评估了这些衍生物在HeLa细胞中的细胞毒性和抗凋亡活性,以及它们对HL-60细胞线粒体内膜电位的影响。所有测试的三羧酸衍生物(包括BKA)对HeLa细胞的毒性均较低。 BKA及其两种合成衍生物显著抑制了星形孢菌素(STS)诱导的细胞活力下降。此外,BKA及其三羧酸衍生物的预处理显著恢复了STS诱导的线粒体膜电位崩溃。其他衍生物(其中三个羧酸中的一个被酯化)表现出强毒性,尤其是一种碳链长度与BKA相同的衍生物。总之,我们开发了一种新型化合物,该化合物作为一种凋亡抑制剂,其含有三个羧酸,并通过合适长度的长碳链连接。PMID:22998163 非人体毒性摘录 /替代和体外试验/ 邦克列酸可引起致命的食物中毒,并伴有高血糖。本文证明,线粒体ATP/ADP转位酶的强效抑制剂——邦克列酸,可通过刺激ATP敏感性钾通道(K-ATP通道)的活性来抑制胰岛β细胞中葡萄糖诱导的电活动。通过将其作用与寡霉素的作用进行比较,我们认为邦克列酸的作用机制是通过抑制葡萄糖代谢,并可能通过损害β细胞功能而诱发高血糖。PMID:2037079 /替代和体外试验/ 本研究旨在表征邦克列酸(BKA)、阿特拉西苷(ATR)和羧基阿特拉西苷(CAT)对线粒体氯离子通道单通道特性的影响。从大鼠心肌中分离出的线粒体膜被整合到双层脂质膜(BLM)中,并在250/50 mM KCl顺反溶液中测量单个氯离子通道电流。BKA(1-100 μM)、ATR和CAT(5-100 μM)以剂量依赖的方式抑制氯离子通道。BKA、ATR和CAT的抑制作用在BLM的反侧最为显著,并且随时间和负电压(反式-顺式)的增加而增强。这些化合物不影响单个通道的电流幅度,但会缩短通道的开放时间。 BKA、ATR 和 CAT 对线粒体氯离子通道的抑制作用可能有助于解释它们的一些细胞和/或亚细胞效应。PMID:17123460 /其他毒性信息/ 参与腺嘌呤核苷酸转运的线粒体 ADP/ATP 载体存在两种不同的构象,分别称为 BA 构象和 CATR 构象,因为它们分别通过特异性抑制剂邦克列酸 (BA) 和羧基阿曲苷 (CATR) 的结合来区分。为了确定哪些氨基酸参与了转运过程中发生的这两种构象之间的转换,我们鉴定并表征了酿酒酵母 ADP/ATP 载体 Anc2p 的突变体,该载体负责酵母细胞对 BA 的抗性,并通过体内化学或紫外线诱变进行分析。尽管分析了大量的突变体,但仅鉴定出四种不同的突变。它们位于Anc2p跨膜区段I (G30S)、II (Y97C)、III (L142S)和VI (G298S)中,并独立地使细胞在BA存在下生长。免疫化学分析和阿特拉西苷结合实验表明,突变体和野生型Anc2p在细胞线粒体中的表达水平几乎相同。在BA存在下,分离的线粒体中Anc2p突变体介导的ADP/ATP交换效率高于野生型Anc2p,证实突变细胞的BA抗性与修饰的ADP/ATP载体的功能特性相关。这些结果表明,BA抗性是由特定位置出现丝氨酸或半胱氨酸导致的Anc2p构象改变引起的。这些残基与其他氨基酸和/或BA的不同相互作用可能阻止稳定的非活性Anc2p BA复合物的形成。PMID:13678275 /其他毒性信息/ 产黄曲霉毒素真菌与细菌之间的相互作用为鉴定适用于控制黄曲霉毒素污染的生物制剂开辟了新途径。本研究分析了黄曲霉与共生于天然受黄曲霉污染大米中的伯克霍尔德氏菌M3之间的相互作用。结果表明,M3菌株的无细胞培养滤液(CCF)及其代谢产物邦克列酸能有效抑制菌丝生长和孢子产生,进而影响黄曲霉毒素的产生。M3菌株分泌的邦克列酸比其他类似物具有更高的抗真菌活性。 M3菌株的CCF及其代谢产物邦克列酸能够抑制黄曲霉的生长,但黄曲霉的代谢产物黄曲霉毒素对M3菌株的生长没有抑制作用。此外,我们发现M3细胞可以利用黄曲霉的死亡菌丝体作为能量来源进行繁殖,而黄曲霉则无法在含有死亡M3细胞的溶液中生长。总之,这些结果表明,当唐菖蒲与其真菌伙伴黄曲霉共存时,唐菖蒲具有生存竞争优势。PMID:26058536 非人类毒性值 小鼠静脉注射LD50:1.4 mg/kg PMID:10435074 小鼠口服LD50:3.16 mg/kg /纯化黄素毒素A/ |
| 参考文献 |
|
| 其他信息 |
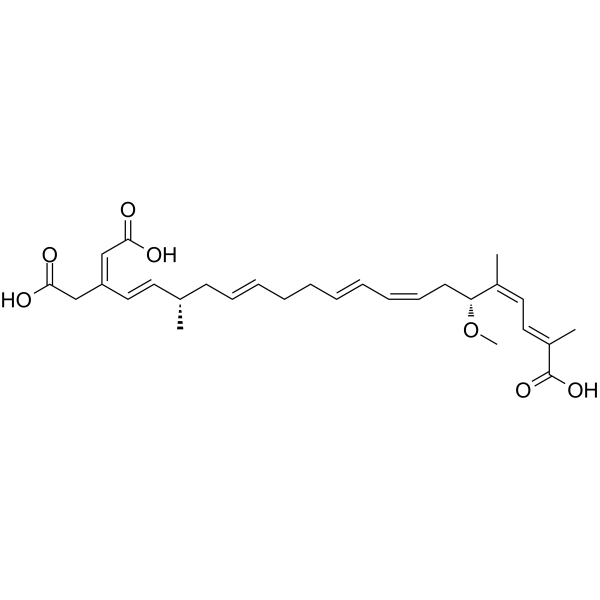
邦克列酸是一种三羧酸,其结构为二十二碳-2,4,8,10,14,18,20-庚烯二酸,其2、5和17位被甲基取代,6位被甲氧基取代,20位被羧甲基取代。它由伯克霍尔德氏菌(Burkholderia gladioli)产生,并与印度尼西亚和中国发生的涉及椰子和玉米制品的食源性疾病暴发有关。邦克列酸具有多种功能,包括抑制细胞凋亡、抑制EC 2.5.1.18(谷胱甘肽转移酶)、毒素、抑制ATP/ADP转位酶以及作为细菌代谢产物。它是一种三羧酸、醚类化合物和烯烃类化合物。它是邦克列酸(3-)的共轭酸。
据报道,邦克列酸存在于唐菖蒲伯克霍尔德氏菌(Burkholderia gladioli)中,并有相关数据。 它是一种由椰子毒假单胞菌(Pseudomonas cocovenenans)产生的抗生素。它是线粒体ADP、ATP转位酶的抑制剂。具体而言,它通过增强膜结合来阻断腺嘌呤核苷酸从线粒体流出。 作用机制 邦克列酸 (BKA) 是腺嘌呤核苷酸转位酶(ANT)的抑制剂。由于ANT的抑制与线粒体细胞色素c释放的抑制相关,进而导致细胞凋亡的抑制,因此它已被用作研究细胞凋亡机制的工具。 BKA由一条具有两个不对称中心的长碳链、一个非共轭烯烃、两个共轭二烯、三个甲基、一个甲氧基和三个羧酸组成。这种复杂的化学结构给其合成、供应和生化机制研究带来了困难。 在众多线粒体毒素中,邦克列酸(BA)具有独特的毒性机制:它抑制的是腺嘌呤核苷酸转位酶(ANT),而不是电子传递链。邦克列酸是由椰子毒伯克霍尔德氏菌(Burkholderia gladioli pathovar cocovenenans,简称B. cocovenenans)产生的,该菌与印度尼西亚和中国发生的涉及椰子和玉米制品的食源性疾病暴发有关。 引言:邦克列酸 (BA) 是一种独特的线粒体毒素,其毒性机制与其他线粒体毒素不同:它抑制腺嘌呤核苷酸转位酶 (ANT),而非电子传递链。邦克列酸是由椰子毒伯克霍尔德氏菌(Burkholderia gladioli pathovar cocovenenans,简称B. cocovenenans)产生的,该菌与印度尼西亚和中国发生的涉及椰子和玉米制品的食源性疾病暴发有关。我们的目标是总结目前关于人类邦克列酸中毒的流行病学、暴露来源、毒物动力学、病理生理学、临床表现、诊断和治疗方面的已知信息。 方法:我们检索了MEDLINE(1946年至今)、EMBASE(1947年至今)、SCOPUS、印尼出版物索引(http://id.portalgaruda.org/)、ToxNet、书籍章节、谷歌搜索、Pro-MED警报以及既往发表期刊文章的参考文献。我们共检索到109篇参考文献,并对其进行了审查。其中29篇(26%)包含相关信息,因此被纳入研究。邦克列酸是一种热稳定的高度不饱和三羧酸脂肪酸,分子量为486 kDa。印尼、中国以及最近的莫桑比克均有邦克列酸中毒暴发的报道。目前对邦克列酸的毒物动力学知之甚少。邦克列酸通过抑制线粒体(ANT)发挥毒性作用。ANT 还可以改变细胞凋亡。人类的体征和症状与其他线粒体毒素的临床表现相似,但严重程度和病程有所不同。患者的治疗以对症支持为主。 结论:邦克列酸是一种线粒体 ANT 毒素,主要见于涉及椰子和玉米的食源性中毒暴发。当出现累及肝脏、大脑和肾脏的体征和症状,且涉及椰子或玉米类食品时,应考虑邦克列酸的可能性。[1] ADP/ATP 载体在细胞代谢中起着关键作用。由于其独特的性质,它在生物化学和遗传学研究中为代谢物跨生物膜转运的分子基础提供了深入的见解。近期高分辨率解析了CATR-载体复合物的结构,极大地促进了我们对该载体的认识。解析该载体在其他构象状态下的结构,将为阐明腺嘌呤核苷酸跨线粒体内膜交换的分子机制提供重要信息,并有助于揭示相关遗传疾病中突变的后果。 线粒体ADP/ATP载体在为细胞提供氧化磷酸化产生的ATP方面,在有氧真核细胞中发挥着核心作用。结合生物化学、遗传学和结构生物学方法,有助于理解这一重要转运系统的分子机制,其功能障碍与神经肌肉疾病密切相关。[2] 在本研究中,我们并未获得Bongkrekic acid/BKA诱导的LDH-A/PDK4 (Topo IIα/Ki-67)下调与LTED细胞死亡之间存在相互作用的直接证据;然而,这是首个将BKA鉴定为LTED细胞代谢途径高选择性调节剂的研究(图5B)。BKA有望成为治疗已接受17β-雌二醇/ERα信号通路阻断剂治疗的乳腺癌复发的有效方法;然而,仍需进一步研究BKA介导LTED细胞死亡的机制。[3] |
| 分子式 |
C28H38O7
|
|---|---|
| 分子量 |
486.59712
|
| 精确质量 |
486.262
|
| CAS号 |
11076-19-0
|
| PubChem CID |
6433556
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
1.114g/cm3
|
| 沸点 |
715.1ºC at 760mmHg
|
| 熔点 |
50-60°
|
| 闪点 |
231ºC
|
| 折射率 |
1.545
|
| LogP |
5.885
|
| tPSA |
121.13
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
17
|
| 重原子数目 |
35
|
| 分子复杂度/Complexity |
898
|
| 定义原子立体中心数目 |
2
|
| SMILES |
OC(C/C(/C=C/[C@H](C/C=C/CC/C=C/C=C/C[C@H](/C(=C/C=C(/C(=O)O)\C)/C)OC)C)=C\C(=O)O)=O
|
| InChi Key |
SHCXABJSXUACKU-WUTQZGRKSA-N
|
| InChi Code |
InChI=1S/C28H38O7/c1-21(15-18-24(19-26(29)30)20-27(31)32)13-11-9-7-5-6-8-10-12-14-25(35-4)22(2)16-17-23(3)28(33)34/h6,8-12,15-19,21,25H,5,7,13-14,20H2,1-4H3,(H,29,30)(H,31,32)(H,33,34)/b8-6+,11-9+,12-10-,18-15+,22-16-,23-17+,24-19+/t21-,25+/m0/s1
|
| 化学名 |
(2E,4Z,6R,8Z,10E,14E,17S,18E,20Z)-20-(carboxymethyl)-6-methoxy-2,5,17-trimethyldocosa-2,4,8,10,14,18,20-heptaenedioic acid
|
| 别名 |
BONGKREKIC ACID; 11076-19-0; Flavotoxin A; Bongkrek acid; L7V4I673D2; (2E,4Z,6R,8Z,10E,14E,17S,18E,20Z)-20-(carboxymethyl)-6-methoxy-2,5,17-trimethyldocosa-2,4,8,10,14,18,20-heptaenedioic acid; (-)-BONGKREKIC ACID; BONGKREKIC ACID [MI];
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month Note: 1. 请将本产品存放在密封且受保护的环境中(例如氮气下),避免暴露在潮湿和光照下。 2. 本产品在运输和储存过程中需避光(避免光照)。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0551 mL | 10.2754 mL | 20.5508 mL | |
| 5 mM | 0.4110 mL | 2.0551 mL | 4.1102 mL | |
| 10 mM | 0.2055 mL | 1.0275 mL | 2.0551 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。