| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
B-Raf
|
|---|---|
| 体外研究 (In Vitro) |
PF-07799933是一种脑渗透、选择性、泛突变的BRAF抑制剂。PF-07799933在体外抑制brafv600e突变单体、BRAF II/ iii类突变二聚体以及诱导突变brafv600e二聚体的治疗获得性遗传改变驱动的细胞中的pERK。此外,PF-07799933在含有BRAFV600E + p61剪接变体或BRAFV600E + NRASQ61K的细胞中破坏内源性突变BRAF:野生型craf二聚体,诱导突变BRAF二聚体。然而,PF-07799933在体外BRAF野生型细胞中不破坏pERK,也不破坏BRAF野生型:craft野生型二聚体。[1]
PF-07799933破坏突变BRAF二聚体,在临床前克服多种BRAF突变在BRAF野生型细胞中,与泛raf二聚体抑制剂相比,PF-07799933没有表现出pERK抑制作用,并且比encorafenib更少地激活pERK。等温稳定性位移剂量反应试验(ITDR)显示,在A375 BRAFV600E突变黑色素瘤细胞裂解物中,PF-07799933结合BRAFV600E的亲和力比野生型CRAF蛋白高10倍。 |
| 体内研究 (In Vivo) |
PF-07799933在体内和脑内具有广泛的抗肿瘤活性,可作为单药治疗BRAFV600E和非v600突变蛋白,以及治疗获得性BRAF p61剪接变体联合binimetinib治疗BRAFV600E。[1]
在含有BRAFV600E (I类)突变的小鼠异种移植物皮下或颅内植入中,PF-07799933单药治疗比encorafenib + binimetinib带来更深的退化。PF-07799933治疗也导致皮下植入BRAFG469A (II类)突变型NSCLC、BRAFK601E (II类)突变型黑色素瘤和BRAF indel突变型胰腺癌肿瘤的消退。相比之下,plixorafenib对BRAFV600E-和brafg469a突变模型的疗效较差,这与较少的体外pERK抑制和已知的体内代谢脆弱性相一致。同样,与较少的体外pERK抑制一致,exarafenib对brafv600e突变模型的活性较低。对于plixorafenib和exarafenib,我们确认动物暴露量与人类接近。因此,观察到的相对于PF-07799933±比尼美替尼的疗效下降不是由于相对于临床可达到的人体剂量的暴露减少。在含有获得性BRAF p61剪接变体的brafv600突变黑色素瘤患者衍生异种移植瘤(PDX)模型中,恩可非尼+比尼美替尼联合治疗并没有提高比尼美替尼单药治疗的最低抗肿瘤活性。然而,单药PF-07799933表现出更强的活性,与binimetinib联用进一步增强了疗效,导致肿瘤消退,同时保持良好的耐受性,没有体重减轻。[1] |
| 酶活实验 |
将Braf KDS: encorafenib复合物与储层溶液(含18% PEG3350、0.2 mol/L Na2SO4、0.1 mol/L磷酸钠钾、pH 6.6)等量混合,采用悬垂气相扩散法进行共结晶。对于Braf-KDL: PF-07799933络合结晶,储层溶液中含有17% PEG5000MME、1% PEG6000、醋酸钠、0.2 mol/L NaCl和5% Tacsimate。收集两种晶体并在含有20% (v/v)甘油作为冷冻保护剂的储层溶液中快速冷冻在液氮中。[1]
|
| 细胞实验 |
等温稳定性偏移剂量反应试验[1]
胰蛋白酶化的A375细胞微球在PBS中重悬,用DMSO或PF-07799933(浓度范围为0.122至2,000 nmol/L)在37℃下处理30分钟。使用PTC-200热循环仪将细胞在PCR板中加热至50°C 3分钟,然后在4°C的摆动桶离心机中快速旋转4700 rpm 30秒。在加入非变性缓冲液[10-mmol/L Na2PO4、1.8-mmol/L KH2PO4 (pH 7.4)、137-mmol/L NaCl、2.7-mmol/L KCl、1-mmol/L CaCl2、10-mmol/L MgCl2、0.02% n-十二烷基β- d -麦糖苷、2×完全蛋白酶抑制剂和2%磷酸酶抑制剂混合物2和3]之前,在液氮中冷冻解冻3次细胞。 免疫共沉淀和免疫印迹[1] 对于内源性RAF蛋白的共免疫沉淀,将MEL21514或A375-NRASQ61K细胞以1.5 × 107个细胞/ 150-mm培养皿的方式进行免疫沉淀。细胞在37℃,5% CO2, DMSO对照或指定浓度的encorafenib或PF-07799933条件下孵育1小时。细胞裂解液以每盘1 mL的镁裂解缓冲液[25 mmol/L 4-(2-羟乙基)-1-哌嗪乙磺酸pH 7.5, 75 mmol/L NaCl, 5 mmol/L MgCl2, 5%甘油和0.1% NP-40]中添加HALT蛋白酶/磷酸酶抑制剂混合物。 |
| 动物实验 |
CTG-1441 和 CTG-0362 PDX 模型的疗效研究由一家合同研究组织 (CRO) 公司完成。MEL21514 PDX 模型取自一位 51 岁西班牙裔女性黑色素瘤患者(曾接受 Braftovi 和 Mektovi 治疗,MT 集团)的活检样本。通过全外显子组测序和 RNA 测序分别证实了 MEL21514 PDX 肿瘤中存在 BRAFV600E 突变和 p61 剪接变体表达。为了构建细胞系,根据推荐的硬肿瘤方案,使用 Miltenyi Biotec 人类肿瘤解离试剂盒结合 gentleMACS Octo 解离器对 MEL21514 PDX 肿瘤样本进行解离。然后使用 Miltenyi 小鼠细胞去除试剂盒对解离的细胞悬液进行磁性标记,并使用 MACS 磁分离器进行分离,以富集人肿瘤细胞。分离得到的MEL21514肿瘤细胞混合后,使用添加了10%胎牛血清(FBS)、青霉素/链霉素和霍乱毒素的Renaissance Essential Tumor Medium(RETM)进行培养。在RETM中传代10次后,将MEL21514细胞转移至添加了10% FBS和1 mmol/L丙酮酸钠的RPMI培养基中培养。细胞系和PDX模型均通过短串联重复序列分析进行鉴定,并定期检测支原体和鼠病毒。所有小鼠均在6至8周龄时获得,每组5只,并在接种癌细胞前进行1周的适应期。食物、水、温度和湿度均按照药理学测试设施的性能标准,并符合2011年《实验动物饲养和使用指南》(NRC)和AAALAC-International的要求进行维持。对于皮下异种移植,将每种细胞系(5 × 10⁶ 个细胞)或 PDX(使用 Miltenyi gentleMACS 制备的细胞悬液)皮下注射到雌性 Foxn1nu 小鼠的右侧腹部,待肿瘤生长至约 200 mm³ 后,根据肿瘤大小随机分组,每组 8 只动物。每周记录两次小鼠的体重和皮下肿瘤体积[计算公式为 (长 × 宽²)/2]。对于颅内异种移植,将 A375-荧光素酶细胞系(10,000 个细胞)注射到雌性 Foxn1nu 小鼠颅缝处,距前囟外侧 2 mm 处。7 天后,根据 IVIS Spectrum 体内成像系统测量的总发光通量(光子/秒)所反映的肿瘤负荷,将小鼠随机分组,每组 10 只动物。每周记录两次体重和总通量,并将平均总通量与肿瘤植入后天数作图。
|
| 毒性/毒理 (Toxicokinetics/TK) |
PF-07799933 单药治疗或联合治疗耐受性良好。未发生剂量限制性毒性(DLT),也未达到最大耐受剂量(MTD);单药治疗和联合治疗分别有 94% 和 100% 的患者出现 ≥1 例治疗期间出现的不良事件(TEAE),其中 28% 和 44% 的患者出现 ≥3 级不良事件。补充表 S4 列出了 ≥3 例患者报告的 TEAE,无论其归因如何。单药治疗中最常见的 TEAE 为疲乏(任何级别 44%/≥3 级 0%)、头痛(28%/0%)、视力模糊 [22%/6%(1 例 3 级)] 和脂肪酶升高(16%/0%)。联合治疗中最常见的 TEAE 为外周水肿(33%/0%)、痤疮样皮疹、腹泻和疲乏(均为 28%/0%)。一名接受 PF-07799933 单药治疗(450 mg,每日两次)的患者因出现视力模糊、周围感觉神经病变、肌痛、疲劳和食欲下降等不良反应而降低了剂量。8 例视力模糊不良反应中有 6 例无需调整剂量即可缓解,复查眼科未发现异常。没有患者因研究药物相关的不良反应而停止治疗。[1]
|
| 参考文献 |
[1]. A Next-Generation BRAF Inhibitor Overcomes Resistance to BRAF Inhibition in Patients with BRAF-Mutant Cancers Using Pharmacokinetics-Informed Dose Escalation. Cancer Discov . 2024 Sep 4;14(9):1599-1611.
|
| 其他信息 |
RAF抑制剂已彻底改变了BRAFV600突变型癌症患者的治疗,但其临床获益受限于ERK信号通路的适应性激活、诱导BRAFV600二聚化的基因改变以及脑穿透性差等因素。新一代泛RAF二聚体抑制剂的治疗指数较窄。PF-07799933(ARRY-440)是一种脑穿透性强、选择性高的泛突变型BRAF抑制剂。PF-07799933在体外抑制信号通路,破坏内源性突变型BRAF与野生型CRAF的二聚体,且不影响野生型ERK信号通路。PF-07799933联合或不联合比美替尼可抑制由以二聚体形式发挥作用的突变型BRAF以及对现有RAF抑制剂产生耐药性的BRAFV600E驱动的小鼠异种移植瘤的生长。我们在一项首次人体临床试验 (NCT05355701) 中,采用一种新型、灵活的、基于药代动力学的剂量递增设计,快速达到 PF-07799933 的有效浓度,治疗了难治性 BRAF 突变实体瘤患者。PF-07799933 ± 比美替尼耐受性良好,在对已批准的 RAF 抑制剂耐药的 BRAF 突变癌症患者中,全身和脑部均观察到多处确认的缓解。意义:PF-07799933 治疗在临床前研究和难治性患者中均显示出对 BRAFV600 突变和非 V600 突变癌症的抗肿瘤活性,并且 PF-07799933 可以安全地与 MEK 抑制剂联合使用。这种新型的、基于快速药代动力学 (PK) 数据的剂量递增设计,为加速下一代靶向疗法在临床早期阶段的测试提供了一种新的范式。[1] PF-07799933 (ARRY-440) 是一种新一代选择性泛突变 BRAF 抑制剂,它并非泛 RAF 抑制剂,不具有普利索拉非尼的代谢风险,可以与 MEK 抑制剂联合使用,并且能够穿透血脑屏障。鉴于 BRAF 突变型癌症患者在现有治疗失败后面临着巨大的未满足医疗需求,我们旨在首次人体 I 期试验中实施基于数据的剂量递增策略,以在更短的时间内、更少的患者中达到治疗所需的药物暴露量。[1]
|
| 分子式 |
C18H15CL2F2N5O3S
|
|---|---|
| 分子量 |
490.31
|
| 精确质量 |
489.0240722
|
| CAS号 |
2754408-94-9
|
| PubChem CID |
165150001
|
| 外观&性状 |
White to light yellow solid powder
|
| 沸点 |
585.0±60.0 °C(Predicted)
|
| 熔点 |
1.72±0.1 g/cm3(Temp: 20 °C; Press: 760 Torr)(Predicted)
|
| LogP |
2.8
|
| tPSA |
103Ų
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
31
|
| 分子复杂度/Complexity |
826
|
| 定义原子立体中心数目 |
0
|
| SMILES |
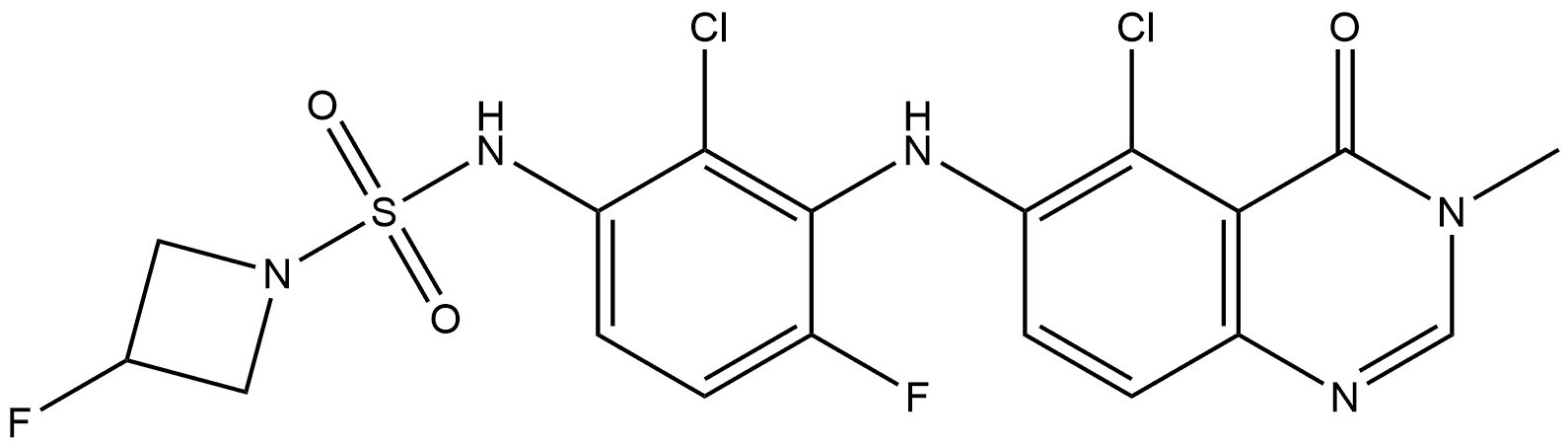
CN1C=NC2=C(C1=O)C(=C(C=C2)NC3=C(C=CC(=C3Cl)NS(=O)(=O)N4CC(C4)F)F)Cl
|
| InChi Key |
SHENFUUACGRLOZ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C18H15Cl2F2N5O3S/c1-26-8-23-11-4-5-12(15(19)14(11)18(26)28)24-17-10(22)2-3-13(16(17)20)25-31(29,30)27-6-9(21)7-27/h2-5,8-9,24-25H,6-7H2,1H3
|
| 化学名 |
N-[2-chloro-3-[(5-chloro-3-methyl-4-oxoquinazolin-6-yl)amino]-4-fluorophenyl]-3-fluoroazetidine-1-sulfonamide
|
| 别名 |
2754408-94-9; PF07799933; Claturafenib (USAN); PF-07799933; SCHEMBL25280690; N-(2-chloro-3-((5-chloro-3-methyl-4-oxo-3,4-dihydroquinazolin-6-yl)amino)-4-fluorophenyl)-3-fluoroazetidine-1-sulfonamide
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0395 mL | 10.1976 mL | 20.3953 mL | |
| 5 mM | 0.4079 mL | 2.0395 mL | 4.0791 mL | |
| 10 mM | 0.2040 mL | 1.0198 mL | 2.0395 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。