| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
β-1,3-glucan synthesis
|
|---|---|
| 体外研究 (In Vitro) |
Ibrexafungerp正在开发中,作为第一种口服和静脉注射GSI(静脉注射葡聚糖合酶抑制剂),用于治疗和预防真菌感染,包括由念珠菌属、曲霉属和支氏肺孢子虫引起的严重和危及生命的感染,有可能提供静脉注射和口服制剂的治疗优势。Ibrexafungerp导致(1→3)-β-D-葡聚糖聚合物减少,真菌细胞壁减弱。Ibrexafungerp在结构上与棘白菌素不同,与靶酶的相互作用也不同(图2)。尽管ibrexafungerp的(1→3)-β-D-葡聚糖合酶上的结合位点与棘白菌素的结合位点部分重叠,但似乎是不相同的,导致对ibrexafungarp的耐药率较低。在体外研究中,在fks突变存在的情况下,ibrexafungerp对野生型和棘白菌素耐药念珠菌菌株的活性受到的影响最小。因此,ibrexafungerp与棘白菌素的交叉抗性潜力有限。
[1]
Ibrexafungerp对一系列曲霉属分离物和念珠菌分离物具有广泛的体外活性,包括光滑念珠菌和耳念珠菌,它们表现出与棘白菌素抗真菌药耐药性相关的fks1和fks2点突变。在对氟康唑敏感性降低的念珠菌属中,包括光滑念珠菌、克鲁塞念珠菌、热带念珠菌和副丝酵母菌,使用ibrexafungerp的MIC50范围分别为0.125-1μg/mL、0.5-1μg/mL、<0.03-1μg/mL和0.25-1μ/mL。此外,正如朱[32]使用从纽约患者获得的分离物所报道的那样,ibrexafungerp(范围为0.05至0.5μg/mL)对金黄色葡萄球菌的体外活性优于氟康唑(范围为2至>256μg/mL),与棘白菌素(范围为0.015至16μg/mL)相当或更优。这一观察结果得到了其他使用全球菌株的研究的证实。Ibrexafungerp对80%的棘白菌素耐药念珠菌菌株显示出野生型MIC分布,表明fks突变对Ibrexafungerp的体外活性影响较小。[1] Ibrexafungerp(SCY-078)是一种针对葡聚糖合酶的新型一流抗真菌药物。耳念珠菌是一种新兴的多重耐药物种,已在五大洲爆发。我们采用EUCAST E.Def 7.3.1方法研究了ibrexafungerp对金黄色葡萄球菌的体外活性。白色念珠菌和光滑念珠菌,以及阿尼丁菌素、米卡芬净、两性霉素B、氟康唑、伏立康唑和伊沙唑被列为对照。对3株耳念珠菌参考菌株(CBS12372、CBS12373和CBS10913)和122株耳念珠菌、16株白色念珠菌和16株光滑念珠菌分离株进行了评估。白色念珠菌ATCC 64548、副丝酵母菌ATCC 22019和克鲁氏念珠菌ATCC 6258作为质量控制菌株。对棘球蛋白抗性分离株进行fks测序。测定MIC范围和模式MIC和MIC50值。野生型上限(野生型分布结束时的MIC上限)根据EUCAST原则确定,用于设置ECOFF。白色念珠菌和光滑念珠菌的三种QC菌株和MIC的九次重复产生了窄的MIC范围,模式MIC与已建立的EUCAST模式MIC一致,证实了稳健的测试性能。针对金黄色葡萄球菌分离物的ibrexafungerp MIC呈高斯分布,模式MIC(范围)为0.5 mg/l(0.06至2 mg/l),表明敏感性一致。在122株分离物中,8株对棘白菌素耐药,并携带S639F Fks1变异。除一例外,其余均对氟康唑耐药,伏立康唑和伊沙唑的MIC分布呈多峰分布,证实了可变敏感性。Ibrexafungerp对金黄色葡萄球菌表现出有前景的活性,包括对棘白菌素和/或其他药物具有抗性的分离株。MIC与临床和实验室标准研究所方法报告的MIC相似,表明一个共同的临床断点可能是合适的[4]。 |
| 体内研究 (In Vivo) |
SCY-078(MK-3118)是安氟霉素的一种新型半合成衍生物,是三萜类抗真菌药物中的第一种化合物。SCY-078表现出对β-(1,3)-d-葡聚糖合成的强烈抑制作用,β-(1,3,)-d-葡聚糖是许多致病真菌(包括念珠菌属和曲霉属)的重要细胞壁成分。SCY-077目前正处于治疗侵袭性真菌疾病的2期临床开发阶段。评估溶解度、肠道通透性和代谢稳定性的体外处置研究预测了良好的口服生物利用度。临床前药代动力学研究与人体每日一次给药一致。静脉注射后,啮齿动物和狗的血浆清除率较低,分别占肝血流量的<15%和<25%。啮齿动物的终末消除期半衰期为5.5至8.7小时,狗的半衰期为9.3小时。稳态下的分布体积很高(4.7至5.3升/千克),这一发现表明组织分布广泛。SCY-078在肾脏组织中的暴露量是侵袭性真菌疾病(如念珠菌病)的靶器官,在0小时至无穷大(AUC0-∞)的浓度-时间曲线下面积超过血浆20至25倍,Cmax SCY-077在多个播散性念珠菌炎小鼠模型中口服给药后达到疗效终点。药代动力学/药效学指标Cmax/MIC和AUC/MIC与结果相关。以血浆AUC0-24表示的目标治疗暴露量在各模型之间具有可比性,上限值为11.2μg·h/ml(15.4μM·h);游离药物AUC/MIC的相应平均值为∼0.75。总体而言,这些结果表明,SCY-078在播散性念珠菌病的小鼠感染模型中具有口服和静脉注射(i.v.)药代动力学特性和效力,以支持进一步研究作为侵袭性真菌疾病的新型静脉注射和口服治疗方法。[2]
耳念珠菌已被证明在住院患者中具有很高的皮肤定植风险,可能会导致医院传播。在豚鼠皮肤模型中,对动物的临床外观、组织真菌负荷、组织学和药代动力学进行了评估。与未经治疗的对照组相比,口服10mg/kg ibrexafungerp(IBX)可减轻病变的严重程度,并显著降低感染动物的耳道念珠菌真菌负担。这表明IBX有望用于控制住院患者的皮肤感染和定植[3]。 |
| 酶活实验 |
溶解性。[2]
Crystal Pharmatech测量了Ibrexafungerp/SCY-078在模拟胃液(SGF)、禁食状态模拟肠液(FaSSIF)和进食状态肠液(FeSSIF)中的溶解度。通常,将约15mg固体称重到4ml小瓶中,加入3.0ml培养基,在室温下在滚动培养箱(25rpm)上搅拌悬浮液24小时。培养后,离心0.5ml悬浮液并过滤(0.45-μm孔径),通过高压液相色谱法(HPLC)和紫外检测法测定上清液中SCY-078的浓度。根据需要调节SCY-078的量和培养基的体积,以确定其在每种培养基中的溶解度。 肝微粒体中的体外代谢稳定性。[2] 用雄性和雌性小鼠、雄性大鼠、雄性和雌性犬以及混合性别的人肝微粒体评估Ibrexafungerp/SCY-078的代谢稳定性。在NADPH存在下,将SCY-078(1μM)与混合的肝微粒体(0.5 mg蛋白质/ml)在37°C下孵育0、5、10、20和30分钟。在每个取样时间点取等分试样,用5倍体积的含有内标(d9-SCY-078125 ng/ml)的冰冷乙腈提取。根据下述条件,通过LC-MS/MS分析培养混合物中的上清液中的母体化合物。使用对照化合物7-乙氧基香豆素、普萘洛尔和维拉帕米建立微粒体制剂的代谢能力。测定了与每种物种的微粒体一起孵育的SCY-078的体外固有清除率(CLint)、CLint与体内固有清除率的比值(CL′int)和半衰期。 体外血浆蛋白结合和血液分布。[2] 通过平衡透析和液体闪烁计数法测定小鼠、大鼠、狗和人血浆中[3H]SCY-078的蛋白结合。将氚标记的Ibrexafungerp/SCY-078乙醇溶液加入到未标记的SCY-078甲醇溶液中,以制备10、100和1000μM SCY-077的恒定活性储备溶液。 在37°C下用等渗磷酸盐缓冲盐水(pH 7.4)测定蛋白质结合24小时。将每种储备溶液的等分试样(10μl)加入到混合的DBA小鼠(n=>10只动物)、Sprague-Dawley大鼠、比格犬或人血浆(1ml)中,以达到0.1、1和10μM SCY-078的最终总浓度。有机溶剂的最终浓度为0.9%(体积/体积)。在1ml丙烯酸透析细胞中进行透析,其中血浆和缓冲液由12.4-kDa截止膜分离。孵育后,对血浆和磷酸盐缓冲液的等分试样(100μl)进行放射性计数,并根据以下计算估算SCY-078的未结合分数:未结合分数=缓冲液中的放射性(dpm/0.1ml)/血浆中的总放射性(dpm/0.1ml)。 |
| 细胞实验 |
Caco2细胞单层的体外渗透性。[2]
Caco2细胞(ATCC CRL-2102)在Dulbecco改良的Eagle培养基中培养,该培养基含有二肽形式的l-谷氨酰胺(GlutaMAX)、10%(体积/体积)胎牛血清和1%(体积/容量)青霉素-链霉素,在37°C的75 ml烧瓶中,在5%CO2的加湿气氛中以10000 U/ml的浓度培养。通过在37°C下用0.25%胰蛋白酶胰蛋白酶消化5分钟来收获接近融合的Caco-2细胞培养物,并将其重新悬浮在培养基中。将细胞以约200000个细胞/cm2的密度接种到半透膜过滤器插件 上。在总共21天的培养过程中,每2至3天更换一次细胞培养基。在试验当天,用运输介质(Hanks平衡盐溶液,含25 mM葡萄糖和25 mM HEPES 冲洗细胞单层,并通过测量从顶端到基底外侧隔室的通量来评估Ibrexafungerp/SCY-078的吸收渗透。将细胞单层与SCY-078(5μM)在37°C下孵育2小时,一式三份。孵育后,从顶端和基底外侧隔室取出样品,通过LC-MS/MS测定试验化合物浓度。表观渗透系数(Papp;cm/s)计算如下:Papp=1/A·C0(dQ/dt),其中dQ/dt是基底外侧隔室内药物出现的速率(μmol/s),C0是供体隔室中的初始药物浓度(μM),A是单层的表面积(cm2)。结果表示为三份样本(n=3)的平均值±标准差。 敏感性测试。[4] EUCAST MIC是按照E.Def 7.3.1方法确定的。将Ibrexafungerp(SCY-078)纯物质在-80°C下等分储存,并在二甲亚砜(5000 mg/l)中制备储备溶液。研究的最终药物浓度范围为0.008至4mg/l。还研究了以下对照化合物(化合物来源,括号内为最终浓度范围):阿尼丁菌素(白色念珠菌和光滑念珠菌分离物为0.004至4毫克/升,金黄色念珠菌分离物的浓度为0.03至32毫克/升)、米卡芬金(白色念珠菌、光滑念珠菌分离株为0.004到4毫克/升至,金黄色梭菌分离物为0.03至32mg/升)、两性霉素B(0.004到4mg/升)、氟康唑(血液分离物为0.03-32毫克/升、金黄色念珠菌为0.5至256mg/升4毫克/升)。全程使用细胞培养处理的样品。制备2倍稀释的微量滴定板,并在使用前在-80°C下冷冻。 |
| 动物实验 |
播散性念珠菌病小鼠模型。[2]
\n使用两种播散性念珠菌病小鼠模型评估了SCY-078的体内活性,以确定药代动力学暴露目标和与疗效相关的PK/PD指标。\n\n在第一个模型中,通过四次独立实验确定了目标治疗暴露量,每次实验均采用每日两次(BID)口服治疗,持续7天,并在感染后不久开始。为了确定与结果相关的PK/PD参数,比较了在感染后16小时开始单次给药或分次给药后SCY-078的疗效。\n[2] \n通过静脉注射白色念珠菌MY1055,在平均体重20克的C′5缺陷型DBA/2N小鼠中诱导播散性念珠菌感染。将白色念珠菌MY1055接种于沙氏葡萄糖琼脂平板上,于35℃培养24小时。用无菌生理盐水洗涤琼脂平板表面的酵母细胞,并使用血细胞计数器定量细胞浓度。通过将细胞悬液进行10倍系列稀释并涂布于沙氏葡萄糖琼脂平板上,确认活细胞计数。平板于35℃培养24至48小时后,测定菌落形成单位(CFU)。采用肉汤微量稀释法(如CLSI M27-A3所述)评估SCY-078对MY1055分离株的体外活性。 MIC终点基于24小时内真菌生长抑制率达50%。\n[2] \n感染时,将0.2 ml含有2.44 × 10⁴至3.56 × 10⁴ CFU白色念珠菌MY1055的芽孢悬液接种到小鼠尾侧静脉。小鼠以最多10只为一组饲养在铺有无菌垫料的无菌微隔离笼中。小鼠可自由摄取水和食物。感染组和未用药组(假治疗对照组)(n = 20)仅接受赋形剂。治疗组每组5只小鼠,另有3只小鼠用于SCY-078的药代动力学分析。通常情况下,在第7天第13剂给药后0、0.25、0.5、1、2、4、6和24小时,从感染的卫星PK小鼠中采集血样。除非另有说明,否则在感染攻击后第7天,从每个治疗组中无菌取出5只小鼠的肾脏。\n[2] \n在攻击后15至30分钟内开始使用SCY-078、卡泊芬净或氟康唑进行治疗。小鼠接受SCY-078治疗,每日两次口服给药,剂量分别为6.25、12.5或25 mg/kg,采用“适用”制剂。卡泊芬净每日两次腹腔注射给药,剂量分别为0.0078、0.03、0.125和0.5 mg/kg。氟康唑以0.078、0.31、1.25和5.0 mg/kg的剂量,每日两次口服给药。攻毒后第7天,处死小鼠(每组n=5),无菌取出双肾,置于无菌Whirl-Pak袋中称重,并在5 ml无菌生理盐水中匀浆。将肾脏匀浆液用无菌生理盐水进行10倍系列稀释,并接种于SDA培养基上。培养板于35℃培养,30至48小时后计数。测定每克肾脏的菌落形成单位(CFU/g),并使用配对双尾t检验(Microsoft Excel)比较各治疗组与假手术对照组的菌落计数。由于稀释方案的限制,每对肾脏中酵母菌的检测限为50个,因此清除率定义为未检测到酵母菌的小鼠数量。对于从成对肾脏中未检测到酵母菌的小鼠数据,将9.8代入Microsoft Excel电子表格公式[log10(5 × 原始计数)/成对肾脏重量)],使计数结果比检测限低1,即每对肾脏49个细胞。\n[2] \n在治疗第7天,对感染卫星病毒的小鼠(每组n = 3)进行药代动力学分析,这些小鼠在接受第13剂SCY-078治疗后采集样本。在15分钟至6小时的时间点采集尾部血液(收集20 μl血液至60 μl 0.1 M柠檬酸钠溶液中),并在24小时进行终末采血。蛋白质沉淀后,采用液相色谱-串联质谱法(LC-MS/MS)分析样本。 SCY-078 的血浆暴露量根据体外血浆/全血分布比值计算(见下文)。[2] 疗效评估采用基于上述方案的延迟治疗模型,通常每个治疗组使用 5 只小鼠。在单次延迟给药模型中,感染后 16 小时给予单剂量 SCY-078。该模型的疗效终点为治疗后 96 小时测得的组织负荷的稳定变化。卡泊芬净和氟康唑未在该模型中进行评估。在分次延迟给药模型中,SCY-078 以两次半剂量或四次四分之一剂量(相对于单次剂量)分次给药。总剂量分别为 12.5、25 和 50 mg/kg,以“适用”制剂的混悬液形式给药。分次给药分别在0或48小时,或相对于单次给药0、24、48和72小时给药(半剂量和四分之一剂量)。本模型未评估卡泊芬净和氟康唑。\n \n\nSCY-078在血浆和肾组织中的药代动力学。[2] \n在未感染的小鼠、大鼠和犬中,经口服和静脉注射给药后,评估了SCY-078的药代动力学和生物利用度。Avastis和MPI Research是经国际实验动物评估和认证协会(AAALAC)认证的机构。制备了用于口服或静脉给药的SCY-078水溶液制剂,静脉给药的制剂为0.45%(质量/体积)生理盐水或含2%(质量/体积)PEG400的0.45%(质量/体积)生理盐水,分别以4、5或5 ml/kg的剂量给药于小鼠、大鼠或犬。用于药代动力学研究的制剂由优化的SCY-078盐型制备,与用于小鼠疗效研究的适用SCY-078制剂相比,该盐型提高了吸收分数。药代动力学研究的血液样本收集于含K2EDTA抗凝剂的试管中,并置于冰上保存,直至离心分离血浆(血浆储存于约-80°C)。啮齿动物的血浆浓度-时间综合平均数据和犬的血浆浓度-时间个体数据分别确定了峰浓度 (Cmax)、达峰时间 (Tmax)、半衰期和 AUC。所有 SCY-078 的剂量和血浆浓度均以游离碱形式表示。\n \n小鼠。[2] \n体重约 25 g 的雌性 CD-1 小鼠(每组每性别每时间点 n = 5)通过灌胃法给予 SCY-078,每日一次或每日两次(每 12 小时一次)给药,单次剂量范围为 3 至 100 mg/kg(6 至 150 mg/kg/天)。小鼠还接受了单次 1 mg/ml 的 SCY-078 静脉注射。在单次静脉给药前以及给药后0.25、0.5、1、2、4、6、9、12、18、24、36、48和60小时采集血浆样本;在治疗第7天口服第13剂后,从给药后1小时开始,在相同时间点采集血浆样本。在口服治疗的第一天,分别在两次给药前以及给药后1、2、4、6、9和12小时采集血浆样本。在治疗第4天首次给药后,额外采集两个样本(给药前和大约在达峰时间点),以确定药物暴露是否达到稳态水平。在治疗第 7 天口服第 13 剂后 2、4、12、24、36、48 和 60 小时收集肾脏组织,吸干水分,并储存在约 -80°C 直至分析。\n \n大鼠。[2] \n体重 0.329 至 0.398 kg(雄性)或 0.187 至 0.244 kg(雌性)的雄性和雌性 Wistar Han 大鼠(每性别/组/时间点 n = 3)接受单次 5 mg/kg 剂量的 SCY-078,通过尾侧静脉注射,注射时间为 5 分钟,或如上所述口服 20 mg/kg 剂量。采用稀疏采样策略,通过舌下静脉从每组每时间点的 4 只动物采集血液样本,时间间隔至给药后 72 小时,并按上述方法进行处理。\n \n犬。 [2] \n体重8至12公斤(雄性)或6至10公斤(雌性)的未经治疗的雄性和雌性比格犬(每性别/组/时间点n=3)接受单次5毫克/公斤剂量的SCY-078静脉注射(5分钟内完成)或口服20毫克/公斤剂量,如上所述。在给药后72小时内的不同时间间隔从颈静脉采集血样,并按上述方法进行处理。\n \n生物样本中SCY-078的分析:小鼠肾组织匀浆。[2] \n在分析当天,称量未经治疗(无药物)的肾组织或来自药代动力学研究的新鲜解冻的组织样本,并在3倍体积的磷酸盐缓冲液中进行匀浆。用于确定体积的肾组织密度假定为1.0克/毫升。 [2] \n\n使用 Precellys 24 珠磨匀浆器,以 2 ml Precellys 管(内含直径 1.4 mm 的陶瓷珠 (CK14))平行匀浆全肾组织样本,并以 5,500 rpm 的转速进行 15 秒的单次匀浆循环。平行珠磨匀浆提高了处理效率,并避免了样本间的潜在交叉污染,因为每个样本都完全包含在其各自的密封小瓶中进行匀浆,匀浆器与其他样本之间没有直接接触。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
每日两次服用300毫克伊布沙芬普,血药浓度峰值(Cmax)为435纳克/毫升,达峰时间(Tmax)为4-6小时,AUC0-24为6832小时纳克/毫升。 90%的放射性标记口服伊布沙芬普可从粪便中回收,其中51%为未改变的母体药物。口服放射性标记剂量的1%会从尿液中回收。 稳态分布容积约为600升。 已报道的清除率分别为53.6升/小时和56.1升/小时。 代谢/代谢物 伊布沙芬格在消除前,先经CYP3A4羟基化,然后羟基与葡萄糖醛酸或硫酸盐结合。 生物半衰期 伊布沙芬格的消除半衰期约为20小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期用药概述 目前尚无关于哺乳期使用伊布沙芬普的信息。该药物的蛋白结合率超过99%,因此乳汁中的含量可能非常低。如果较大婴儿的母亲需要使用伊布沙芬普,这并非停止母乳喂养的理由,但在获得更多数据之前,可能更倾向于选择其他药物,尤其是在哺乳新生儿或早产儿时。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 伊布沙芬普在血浆中的蛋白结合率为99.5-99.8%,主要与白蛋白结合。 |
| 参考文献 |
[1]. Ibrexafungerp: A Novel Oral Triterpenoid Antifungal in Development for the Treatment of Candida auris Infections. Antibiotics (Basel). 2020 Aug 25;9(9):539.
[2]. Preclinical Pharmacokinetics and Pharmacodynamic Target of SCY-078, a First-in-Class Orally Active Antifungal Glucan Synthesis Inhibitor, in Murine Models of Disseminated Candidiasis. Antimicrob Agents Chemother. 2017 Mar 24;61(4):e02068-16. [3]. Efficacy of Ibrexafungerp (SCY-078) against Candida auris in an In Vivo Guinea Pig Cutaneous Infection Model. Antimicrob Agents Chemother. 2020 Sep 21;64(10):e00854-20. [4]. In Vitro Activity of Ibrexafungerp (SCY-078) against Candida auris Isolates as Determined by EUCAST Methodology and Comparison with Activity against C. albicans and C. glabrata and with the Activities of Six Comparator Agents. Antimicrob Agents Chemother. 2020 Feb 21;64(3):e02136-19. |
| 其他信息 |
伊布沙芬格(Ibrexafungerp),又名SCY-078或MK-3118,是一种新型恩氟芬净衍生物口服三萜类抗真菌药物,获批用于治疗外阴阴道念珠菌病(VVC),也称为阴道酵母菌感染。它的研发源于治疗可能对棘白菌素类或唑类抗真菌药物产生耐药性的真菌感染的需求。与只能肠外给药的棘白菌素类药物(如卡泊芬净、米卡芬净和阿尼芬净)相比,伊布沙芬格具有口服生物利用度。与棘白菌素类药物类似,伊布沙芬格靶向真菌β-1,3-葡聚糖合酶,而该酶在人体内并不存在,因此降低了肾脏或肝脏毒性的风险。伊布沙芬普于2021年6月1日获得FDA批准。
伊布沙芬普是一种三萜类抗真菌药物。其作用机制是作为葡聚糖合成酶抑制剂。 伊布沙芬普是恩氟芬净的半合成衍生物,具有潜在的抗真菌活性,可静脉注射或口服给药,具有良好的生物利用度。给药后,伊布沙芬普抑制β-1,3-D-葡聚糖合成酶,该酶是真菌细胞壁合成所必需的。这会导致真菌细胞壁减弱,从而导致渗透性溶解,最终导致真菌细胞死亡。 另见:伊布沙芬普柠檬酸盐(其活性成分)。 适应症 伊布沙芬普适用于治疗初潮后患者的外阴阴道念珠菌病。它还适用于降低复发性外阴阴道念珠菌病的发生率。 预防复发性外阴阴道念珠菌病,治疗外阴阴道念珠菌病 作用机制 β-1,3-葡聚糖合酶由催化亚基FKS1或FKS2和GTP结合调节亚基Rho1组成。该合酶参与β-1,3-葡聚糖(真菌细胞壁成分)的合成。伊布沙芬普的作用机制与棘白菌素类抗真菌药物类似,均通过抑制β-1,3-葡聚糖合酶的合成发挥作用。棘白菌素类药物与β-1,3-葡聚糖合酶的FKS1结构域结合,而恩氟芬净及其衍生物则与另一个位点结合,这使得它们能够对棘白菌素耐药的真菌感染保持活性。动物研究表明,伊布沙芬普能很好地分布于阴道组织,因此是治疗外阴阴道念珠菌病的理想药物。 药效学 伊布沙芬普是一种恩氟芬净衍生物,属于口服三萜类抗真菌药物,已获准用于治疗外阴阴道念珠菌病。由于需每日服用两次,其作用持续时间适中;临床试验中,患者服用超过推荐剂量后未出现严重不良反应,因此其治疗指数较宽。应告知患者该药存在胎儿毒性风险。 |
| 分子式 |
C44H70N5O8P
|
|---|---|
| 分子量 |
828.029073238373
|
| 精确质量 |
921.546308
|
| 元素分析 |
C, 63.82; H, 8.52; N, 8.46; O, 15.46; P, 3.74
|
| CAS号 |
1965291-14-8
|
| 相关CAS号 |
1965291-08-0 (citrate) ; 1207753-03-4; 1965291-14-8 (phosphate);
|
| PubChem CID |
131801103
|
| 外观&性状 |
Typically exists as solids at room temperature
|
| tPSA |
258 Ų
|
| 氢键供体(HBD)数目 |
6
|
| 氢键受体(HBA)数目 |
15
|
| 可旋转键数目(RBC) |
14
|
| 重原子数目 |
66
|
| 分子复杂度/Complexity |
1650
|
| 定义原子立体中心数目 |
12
|
| SMILES |
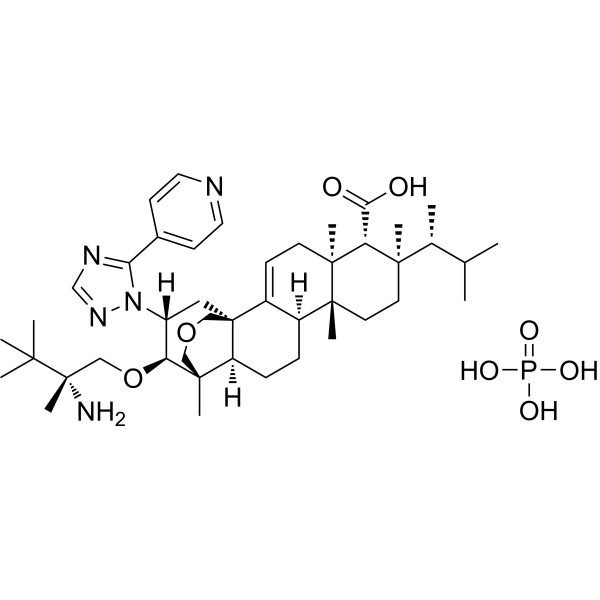
P(=O)(O)(O)O.O1CC2(C)[C@H]([C@@H](C[C@]3(C1)C1=CC[C@@]4(C)[C@H](C(=O)O)[C@@](C)([C@H](C)C(C)C)CC[C@]4(C)[C@H]1CC[C@H]32)N1C(C2C=CN=CC=2)=NC=N1)OC[C@@](C)(C(C)(C)C)N
|
| InChi Key |
OAKUEXTYOMFKTF-GSTQBDTKSA-N
|
| InChi Code |
InChI=1S/C44H67N5O4.H3O4P/c1-27(2)28(3)39(7)18-19-41(9)30-12-13-33-40(8)23-52-25-44(33,31(30)14-17-42(41,10)34(39)37(50)51)22-32(35(40)53-24-43(11,45)38(4,5)6)49-36(47-26-48-49)29-15-20-46-21-16-29;1-5(2,3)4/h14-16,20-21,26-28,30,32-35H,12-13,17-19,22-25,45H2,1-11H3,(H,50,51);(H3,1,2,3,4)/t28-,30+,32-,33+,34-,35+,39-,40?,41-,42+,43+,44+;/m1./s1
|
| 化学名 |
(1R,5S,6R,7R,10R,11R,14R,20R,21R)-21-[(2R)-2-amino-2,3,3-trimethylbutoxy]-5,7,10,15-tetramethyl-7-[(2R)-3-methylbutan-2-yl]-20-(5-pyridin-4-yl-1,2,4-triazol-1-yl)-17-oxapentacyclo[13.3.3.01,14.02,11.05,10]henicos-2-ene-6-carboxylic acid;phosphoric acid
|
| 别名 |
MK 3118 phosphate; SCY-078 phosphate; MK-3118 phosphate; 76HJ8T68WO; UNII-76HJ8T68WO; ...; IBREXAFUNGERP PHOSPHATE; SCY-078 phosphate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.2077 mL | 6.0384 mL | 12.0769 mL | |
| 5 mM | 0.2415 mL | 1.2077 mL | 2.4154 mL | |
| 10 mM | 0.1208 mL | 0.6038 mL | 1.2077 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。