| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
sPLA2 ( Ki = 15 nM ); 5-HT3A Receptor ( Ki = 3.7 nM ); 5-HT7 Receptor ( Ki = 19 nM ); SERT ( Ki = 1.6 nM )
Serotonin transporter (SERT) (IC50 = 1.6 nM for human SERT; Ki = 0.54 nM for human SERT) [1][5] 5-HT1A receptor (Ki = 15 nM for human 5-HT1A; partial agonist, EC50 = 3.7 nM) [1][5] 5-HT1B receptor (Ki = 33 nM for human 5-HT1B; antagonist) [1][5] 5-HT3A receptor (Ki = 3.7 nM for human 5-HT3A; antagonist, IC50 = 2.3 nM) [1][5] 5-HT7 receptor (Ki = 19 nM for human 5-HT7; antagonist, IC50 = 4.9 nM) [1][5] Dopamine transporter (DAT) (Ki = 1100 nM for human DAT; weak inhibition) [1] Norepinephrine transporter (NET) (Ki = 330 nM for human NET; weak inhibition) [1] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Lu-AA21004 抑制重组人 CYP1A2、CYP2C9、CYP2D6 和 CYP3A4,IC50 分别为 40 μM、39 μM、9.8 μM 和 10 μM。 Lu AA21004 是一种 h5-HT1B 受体部分激动剂,基于全细胞 cAMP 的检测,EC50 为 460 nM,内在活性为 22%。 Lu AA21004 与 r5-HT7 受体结合,Ki 值为 200 nM,是 r5-HT7 受体的功能性拮抗剂,在体外全细胞 cAMP 测定中,IC50 为 2 μM。激酶测定:Vortioxetine(化合物 5m)是一种多模式血清素能药物,抑制 5-HT1A、5-HT1B、5-HT3A、5-HT7 受体和 SERT,Ki 值为 15 nM、33 nM、3.7 nM、19 nM 和 1.6分别为nM。沃替西汀对 5-HT3A 和 5-HT7 受体表现出拮抗特性,对 5-HT1B 受体表现出部分激动剂特性,对 5-HT1A 受体表现出激动特性,并对 SERT 具有有效抑制作用。细胞测定:Vortioxetine 是一种 h5-HT1B 受体部分激动剂,基于全细胞 cAMP 测定,EC50 为 460 nM,内在活性为 22%。 Vortioxetine 与 r5-HT7 受体结合的 Ki 值为 200 nM,是 r5-HT7 受体的功能性拮抗剂,在体外全细胞 cAMP 测定中 IC50 为 2 μM。
在人SERT抑制实验中,Vortioxetine lactate强效抑制血清素再摄取,IC50为1.6 nM,对NET和DAT的选择性分别为206倍和688倍[1][5] 在人5-HT1A受体上,Vortioxetine lactate表现为部分激动剂,刺激[35S]GTPγS结合的EC50为3.7 nM,最大反应为血清素的65%[5] 它拮抗人5-HT1B受体,抑制血清素诱导的[35S]GTPγS结合,IC50为25 nM[5] 在人5-HT3A受体上,Vortioxetine lactate阻断血清素诱导的钙内流,IC50为2.3 nM,100 nM时可完全抑制受体激活[1][5] 它拮抗人5-HT7受体,抑制血清素诱导的cAMP积累,IC50为4.9 nM[5] 在大鼠皮质切片中,Vortioxetine lactate(0.1-10 μM)以剂量依赖性方式增加细胞外血清素、去甲肾上腺素和多巴胺水平,10 μM时最大增幅分别为320%、150%和130%[5] 在人SH-SY5Y神经母细胞瘤细胞中,Vortioxetine lactate(1-10 μM)使BDNF mRNA表达上调2.1-3.5倍,并增加磷酸化ERK1/2水平,表明其促进神经营养信号传导[2] |
| 体内研究 (In Vivo) |
对于 Lu-AA21004,大鼠的肝脏清除率和口服生物利用度为 7.1 (L/h)/kg 和 16%。 Lu-AA21004(2.5 mg/kg、5 mg/kg 或 10 mg/kg sc)可增加清醒大鼠腹侧海马的细胞外 5-HT 水平。治疗 3 天后,Lu-AA21004(5 mg/kg 或 10 mg/kg sc)还会导致内侧前额皮质 (mPFC) 中 5-HT 基础水平显着升高。 Lu-AA21004在大鼠内侧前额叶皮层中用5mg/kg或10mg/kg治疗3天后,占据SERT的43%和57%。 Lu AA21004 剂量依赖性地占据 5-HT1B 受体,大鼠皮下给药 1 小时后 SERT 的 ED50 分别为 3.2 mg/kg 和 0.4 mg/kg。 Lu AA21004 剂量依赖性地影响大鼠的 Bezold-Jarisch 反射,抑制短暂性心动过缓,ED50 为 0.11 mg/kg。 Lu AA21004 (2.5-10.0 mg/kg sc) 增加大鼠内侧前额皮质和腹侧海马中 5-HT、DA 和 NA 的细胞外水平。 Lu AA21004(5 mg/kg sc)可增加大鼠腹侧海马中 5-HT 的细胞外水平(200%),SERT 占用率为 41%。 Lu AA21004 (7.8 mg/kg sc) 显着减少 FSL 大鼠的不动时间,但不减少 FRL 大鼠的不动时间。 Lu AA21004(8.0 mg/kg po)可增加大鼠的社交互动,并小幅但显着地增加大鼠的运动活动。 Lu AA21004 (7.9 mg/kg sc) 在大鼠条件性恐惧测定中显示出剂量依赖性抗焦虑样作用。沃替西汀 (10 mg/kg) 显着增加雄性 Sprague-Dawley 大鼠采集前 60 分钟的冻结,表明在采集和/或巩固过程中情境记忆形成增强。沃替西汀(5 mg/kg)还会导致保留期间的冻结率增加,这种效应通过事后测试达到了统计显着性。采集前的沃替西汀(2.5 mg/kg 或 5 mg/kg)显示新物体的平均探索时间分别为 29 秒和 33 秒。沃替西汀 (10 mg/kg) 显着降低大鼠的伤害感受,评估为缩爪潜伏期延长。注射后 20 分钟,5 和 10 mg/kg 的沃替西汀使乙酰胆碱水平增加至基线的 224% 和 204%。
在小鼠强迫游泳实验(抗抑郁模型)中,口服Vortioxetine lactate(1-10 mg/kg)以剂量依赖性方式减少不动时间28-52%,最低有效剂量为3 mg/kg[2][5] 在小鼠悬尾实验中,Vortioxetine lactate(3-30 mg/kg口服)减少不动时间31-48%,符合抗抑郁活性[5] 在小鼠高架十字迷宫实验(焦虑模型)中,Vortioxetine lactate(3-10 mg/kg口服)增加开放臂探索时间35-60%,显示抗焦虑作用[2][4] 在小鼠慢性温和应激抑郁模型中,Vortioxetine lactate(1-10 mg/kg/天口服,持续21天)逆转快感缺失(通过蔗糖偏好度测量),从45%提升至68-82%,并使海马神经发生(BrdU阳性细胞)增加1.8-3.2倍[2] 在一项针对广泛性焦虑障碍患者的随机、双盲、安慰剂对照临床试验中,Vortioxetine lactate 5 mg/天口服,持续8周,使汉密尔顿焦虑量表(HAM-A)评分显著降低7.2分(安慰剂组为4.5分),应答率为42%(安慰剂组为28%)[4] 在人体驾驶研究中,Vortioxetine lactate(5-20 mg/天口服,持续14天)与安慰剂相比,未损害实际驾驶表现(横向位置标准差、速度变异)或认知功能(注意力、工作记忆)[3] 在大鼠中,口服Vortioxetine lactate(1-10 mg/kg)以剂量依赖性方式增加脑内血清素、去甲肾上腺素和多巴胺水平,给药后2-4小时达到峰值效应[5] |
| 酶活实验 |
Vortioxetine (Compound 5m) 是一种多模式血清素能药物,可抑制 SERT,抑制值分别为 1.6 nM、33 nM、3.7 nM、19 nM 以及 5-HT1A、5-HT1B 和 5-HT7 受体。 Vortioxetine 表现出强烈的 SERT 抑制作用以及对 5-HT3A 和 5-HT7 受体的拮抗作用、对 5-HT1B 受体的部分激动作用以及对 5-HT1A 受体的激动作用。
Vortioxetine/化合物5m (Lu AA21004)是先导化合物,对重组人5-HT(1A) (K(i) = 15 nM)、5-HT(1B) (K(i) = 33 nM)、5-HT(3A) (K(i) = 3.7 nM)、5-HT(7) (K(i) = 19 nM)、去甲肾上腺素能β(1) (K(i) = 46 nM)受体和SERT (K(i) = 1.6 nM)具有高亲和力。化合物5m对5-HT(3A)和5-HT(7)受体具有拮抗作用,对5-HT(1B)受体具有部分激动作用,对5-HT(1A)受体具有激动作用,对SERT具有有效抑制作用[1]。 体外SERT和5-HT3受体占用率测定[2] 用载体、氟西汀或沃替西汀(急性给药后1小时或第14次或第21次注射后24小时)处理小鼠的大脑,快速冷冻,用低温恒温器冠状切片,然后装在载玻片上冷冻待用。切片厚度为20 μm,从距bregma正前方约1.2 mm处开始测定SERT受体占用,从距bregma正前方约2.7 mm处开始测定5-HT3受体占用(Franklin and Paxinos, 2008)。在用于放射自显影实验之前,载玻片在- 20°C下保存至少24小时。[2] 将表达人SERT的细胞与[3H]血清素和系列稀释的Vortioxetine lactate(0.01-100 nM)在37°C孵育10分钟,在高亲和力SERT抑制剂存在下测定非特异性摄取。洗涤细胞并裂解,使用闪烁计数器测量放射性,根据浓度-反应曲线计算SERT抑制的IC50值[1][5] 5-HT受体结合实验:将人重组5-HT1A/1B/3A/7受体固定在微量滴定板上,将Vortioxetine lactate(0.001-1000 nM)与受体在放射性标记配体(如5-HT1A用[3H]8-OH-DPAT,5-HT1B用[3H]GR125743)存在下于25°C孵育60分钟。洗涤去除未结合配体,定量结合放射性,通过Cheng-Prusoff方程推导Ki值[1][5] 5-HT3A受体功能实验:将表达人5-HT3A受体的CHO细胞加载钙敏感荧光染料,用Vortioxetine lactate(0.1-100 nM)预孵育细胞15分钟,随后用血清素(1 μM)刺激。实时测量荧光强度评估钙内流,计算拮抗作用的IC50值[5] 5-HT7受体cAMP实验:将表达人5-HT7受体的细胞用Vortioxetine lactate(0.1-100 nM)预孵育30分钟,然后用血清素(100 nM)刺激1小时。使用竞争性ELISA试剂盒定量cAMP水平,确定抑制cAMP积累的IC50值[5] |
| 细胞实验 |
Vortioxetine 是一种 h5-HT1B 受体部分激动剂,在基于 cAMP 的全细胞测定中,EC50 为 460 nM,内在活性为 22%。在体外全细胞 cAMP 测定中,vortioxetine 与 r5-HT7 受体结合,Ki 值为 200 nM,并且是 r5-HT7 受体的功能性拮抗剂,IC50 为 2 μM。
SERT占用率评估[2] 载玻片在含有4.5 nM [3H]-escitalopram的缓冲液(50 mM Tris-HCl, 150 mM NaCl, 5 mM KCl, pH = 7.4)中室温孵育60 min。用1 μM艾司西酞普兰检测非特异性结合。载玻片在冷缓冲液中短暂洗涤,干燥,并在Beta成像仪中暴露16小时。SERT检测的感兴趣区域(ROI)包括外侧和内侧隔膜、伏隔核和嗅结节。SERT检测的ROI示例图像可以在补充图2A中找到。 5-HT3受体占用率的评价[2] 载玻片在由50 mM Tris和150 mM NaCl组成的缓冲液中预孵育5分钟。载玻片在空气流下干燥30-45分钟。随后,载玻片在含有1 nM [3H]LY278584的缓冲液(50 mM Tris-HCl, 150 mM NaCl, 5 mM KCl, pH = 7.4)中室温孵育60分钟。用1 μM昂丹司琼测定非特异性结合。载玻片在冷缓冲液中短暂洗涤,干燥,并在Beta成像仪中暴露24小时。5-HT3受体占用试验的ROI由海马组成。5-HT3受体占用测定的示例图像可以在补充图2B中找到。 制备大鼠皮质切片(400 μm),在含氧人工脑脊液(aCSF)中37°C孵育1小时。向aCSF中加入Vortioxetine lactate(0.1-10 μM),切片再孵育2小时。收集细胞外液,通过高效液相色谱(HPLC)结合电化学检测测量神经递质(血清素、去甲肾上腺素、多巴胺)水平[5] SH-SY5Y细胞在添加胎牛血清和抗生素的DMEM/F12培养基中培养,接种到6孔板后用Vortioxetine lactate(1-10 μM)处理24-48小时。提取总RNA并逆转录为cDNA,以GAPDH为管家基因,通过qPCR定量BDNF mRNA表达[2] ERK1/2磷酸化分析:SH-SY5Y细胞经Vortioxetine lactate(1-10 μM)处理15-60分钟后,用含蛋白酶和磷酸酶抑制剂的RIPA缓冲液裂解,测定蛋白浓度。将等量蛋白通过SDS-PAGE分离,转移到PVDF膜上,用针对p-ERK1/2、ERK1/2和β-肌动蛋白的抗体孵育,化学发光显影条带并进行密度分析[2] |
| 动物实验 |
溶于 10% 羟丙基-β-环糊精;10 mg/kg;皮下注射
大鼠急性研究[2] 在旷场试验 (OF)、神经纤维瘤病试验 (NSF) 和强迫游泳试验 (FST) 中使用了三种剂量的沃替西汀(2.5、5 和 10 mg/kg,游离碱溶于 10% β-环糊精,灌胃给药)。将沃替西汀的作用与溶剂对照组(10% β-环糊精)以及氟西汀组(18 mg/kg,灌胃给药 (David 等,2007))和地西泮组(1.5 mg/kg,皮下注射 (David 等,2007))进行比较。所有剂量均根据盐的重量进行了校正。所有治疗均在测试前 1 小时进行。 慢性研究[2] 在小鼠中测试了两种剂量的沃替西汀(5 和 20 mg/kg/天,游离碱溶于 10% β-环糊精,灌胃给药,po)。在 NSF 测试中,分别于给药 14 天后进行测试;在 OF 测试、NSF 测试和 FST 测试中,分别于给药 21 天后进行测试。小鼠在末次给药后 24 小时进行测试。将沃替西汀的作用与溶剂对照组(10% β-环糊精)以及氟西汀治疗组(18 mg/kg/天,灌胃给药)进行比较。 强迫游泳和悬尾测试使用雄性 C57BL/6 小鼠(20-25 g)。小鼠被随机分组(每组 n=8-10),并在测试前 60 分钟通过灌胃给予乳酸沃替西汀(1-30 mg/kg)或赋形剂(0.5% 甲基纤维素)。记录小鼠的不动时间,分别进行 6 分钟(强迫游泳试验)或 5 分钟(悬尾试验)[2][5]。 对于慢性轻度应激模型,C57BL/6 小鼠接受为期 4 周的不可预测应激(食物/水剥夺、笼子倾斜、光暗周期紊乱)。在最后 3 周,小鼠通过灌胃给予乳酸沃替西汀(1-10 mg/kg/天)或赋形剂。每周测量蔗糖偏好,并在研究结束时,小鼠每天两次腹腔注射BrdU(50 mg/kg),连续3天,然后处死,并对海马切片进行BrdU免疫染色以量化神经发生[2]。 雄性Sprague-Dawley大鼠(250-300 g)用于神经化学研究。大鼠经口灌胃给予乳酸沃替西汀(1-10 mg/kg)或溶剂,并在给药后0.5、2、4、8和24小时处死大鼠,解剖脑组织,并对脑区(皮层、海马)进行匀浆处理。采用高效液相色谱法 (HPLC) 测定神经递质水平 [5] 在一项针对广泛性焦虑症的人体临床试验中,481 名患者(18-65 岁)被随机分配接受每日口服 5 mg、10 mg 或安慰剂,疗程为 8 周。在基线和每周记录汉密尔顿焦虑量表 (HAM-A) 评分、临床总体印象 (CGI) 量表评分和不良事件 [4] 在一项人体驾驶研究中,180 名健康志愿者(18-65 岁)被随机分配接受每日口服 5 mg、10 mg、20 mg 或安慰剂,疗程为 14 天。在第 14 天,在高速公路环路(100 公里驾驶)上评估实际驾驶表现,并进行认知测试(数字符号替换、选择性注意)[3] |
| 药代性质 (ADME/PK) |
沃替西汀乳酸盐的口服生物利用度在大鼠中为 75%,在人体中为 93% [1][5]。
血浆消除半衰期 (t1/2) 在大鼠中为 6.8 小时,在犬中为 17 小时,在人体中为 66 小时 [1][5]。 在人体中,口服给药后 6-8 小时达到血浆峰浓度 (Cmax),在 2.5-40 mg/天的剂量范围内,其药代动力学呈剂量比例关系 [1][3]。 该药物广泛分布于组织中,在人体中的分布容积 (Vd) 为 2600 L [5]。 人肝微粒体代谢研究表明,沃替西汀乳酸盐主要由 CYP2D6 代谢,CYP3A4、CYP2C19 和 CYP2C9 的贡献较小。 [1][5] 在人体中,约 59% 的给药剂量在 7 天内经尿液排出,约 26% 经粪便排出,不足 2% 的药物以原形排出。[5] 在大鼠中,口服给药后 2 小时,脑组织与血浆的浓度比为 2.8。[5] |
| 毒性/毒理 (Toxicokinetics/TK) |
在一项为期 13 周的大鼠重复给药毒性研究中,口服高达 150 mg/kg/天的乳酸沃替西汀未引起体重、食物消耗量或临床化学参数(ALT、AST、肌酐、BUN)的显著变化[1][5]。乳酸沃替西汀在人血浆中的血浆蛋白结合率为 98%[1][5]。在人体临床试验中,最常见的不良事件是恶心(10-15%)、头痛(8-12%)和腹泻(5-7%),这些不良事件均为轻度至中度且短暂[3][4]。在人肝微粒体中,浓度高达 10 μM 时,未观察到对 CYP 酶(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4)的显著抑制。 [1][5]
在人体驾驶研究中,与安慰剂相比,乳酸沃替西汀未引起明显的镇静、头晕或精神运动功能障碍[3] 临床前研究未观察到遗传毒性或致癌性[1] |
| 参考文献 |
|
| 其他信息 |
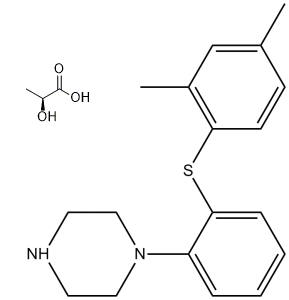
沃替西汀是一种N-芳基哌嗪类化合物,其中芳基为2-[(2,4-二甲基苯基)硫基]苯基。它(以氢溴酸盐的形式)用于治疗重度抑郁症。沃替西汀具有抗抑郁、抗焦虑、5-羟色胺能激动剂和5-羟色胺能拮抗剂的双重作用。它是一种N-芳基哌嗪类化合物,也是一种芳基硫醚类化合物。它是沃替西汀(1+)的共轭碱。 沃替西汀是一种抗抑郁药物,适用于治疗重度抑郁症(MDD)。它被归类为5-羟色胺调节剂和兴奋剂(SMS),因为它对5-羟色胺神经递质系统具有多模式作用机制,能够同时调节一种或多种5-羟色胺受体并抑制5-羟色胺的再摄取。更具体地说,沃替西汀通过以下生物学机制发挥作用:作为血清素再摄取抑制剂(SRI),通过抑制血清素转运体发挥作用;作为5-HT1B受体的部分激动剂;作为5-HT1A受体的激动剂;以及作为5-HT3、5-HT1D和5-HT7受体的拮抗剂。由于血清素受体存在多种亚型,因此开发了血清素再摄取抑制剂(SRI)。然而,并非所有这些受体都参与了SRI的抗抑郁作用。一些血清素受体在情绪调节中似乎起着相对中性或微不足道的作用,但另一些受体,例如5-HT1A自身受体和5-HT7受体,似乎在SRI治疗抑郁症的疗效中起着拮抗作用。沃替西汀是一种用于治疗重度抑郁症的血清素能抗抑郁药。沃替西汀治疗期间血清转氨酶轻微升高的发生率较低,但尚未发现与临床上明显的急性肝损伤病例相关。 沃替西汀是一种哌嗪衍生物,可作为5-羟色胺再摄取抑制剂、5-HT3受体拮抗剂和5-HT1A受体激动剂发挥作用。它用于治疗焦虑和抑郁症。 沃替西汀(Lu AA21004)是一种在研的新型抗抑郁药,具有多模式活性,在体外可作为5-HT3、5-HT7和5-HT(1D)受体拮抗剂、5-HT(1B)受体部分激动剂、5-HT(1A)受体激动剂和5-HT转运体抑制剂发挥作用。本文探讨了其在成年小鼠中的抗焦虑和抗抑郁潜力。本研究采用旷场实验和强迫游泳实验评估了沃替西汀在BalB/cJ@RJ小鼠中的作用(急性给药:口服1小时;重复给药:每日口服,持续21天);并采用新奇抑制进食范式评估了沃替西汀在129S6/SvEvTac小鼠中的作用(急性给药:口服1小时;持续给药:每日口服,持续14或21天)。氟西汀和地西泮作为对照。沃替西汀的急性给药和重复给药均比氟西汀表现出更显著的抗焦虑和抗抑郁样活性。沃替西汀治疗21天后,显著促进了海马齿状回颗粒下区未成熟颗粒细胞的增殖和存活,并刺激了其成熟。 14天后,高剂量沃替西汀可增加树突长度和树突交叉点数量,表明沃替西汀能加速未成熟神经元的成熟。重复给药后,沃替西汀表现出抗抑郁和抗焦虑作用,并伴有多个阶段神经发生的增加。在 5-HT 转运体占有率较低的情况下观察到了沃替西汀的作用,这提示其作用机制可能并非抑制 5-HT 再摄取。[2] 查看更多本研究旨在评估一种新型抗抑郁药沃替西汀 10 mg 对 24 名健康受试者驾驶、认知和精神运动能力的影响。研究采用双盲、安慰剂对照、三期交叉设计。米氮平 30 mg 作为活性对照药。药物于连续 15 天的晚上服用。在第2天和第16天的上午,使用标准化测试评估受试者的驾驶能力、记忆力、追踪能力、注意力分配能力和警觉性。对主要驾驶指标(即侧向位置的标准差)的统计分析显示,沃替西汀在第2天和第16天均不劣于米氮平,而米氮平在第2天劣于沃替西汀。沃替西汀不会引起认知或精神运动功能障碍。然而,米氮平在第2天会损害认知和精神运动功能。多次服用米氮平后,这些影响大多消失。总之,单次或多次服用沃替西汀后,并未损害驾驶、认知或精神运动能力。[3] 药效学 沃替西汀与人血清素转运体具有高亲和力(Ki=1.6 nM),但与去甲肾上腺素(Ki=113 nM)或多巴胺(Ki>1000 nM)转运体无亲和力。沃替西汀通过抑制血清素转运体,强效且选择性地抑制血清素的再摄取(IC50=5.4 nM)。具体而言,沃替西汀可与 5-HT3 (Ki=3.7 nM)、5-HT1A (Ki=15 nM)、5-HT7 (Ki=19 nM)、5-HT1D (Ki=54 nM) 和 5-HT1B (Ki=33 nM) 受体结合,是 5-HT3、5-HT1D 和 5-HT7 受体拮抗剂,5-HT1B 受体部分激动剂,以及 5-HT1A 受体激动剂。 吸收 给药后,沃替西汀血浆浓度峰值 (Cmax) 在给药后 7 至 11 小时内达到。绝对生物利用度为 75%。未观察到食物对药代动力学的影响。 消除途径 单次口服[14C]标记的沃替西汀后,约59%和26%的给药放射性分别以代谢物的形式从尿液和粪便中回收。48小时内,尿液中排出的未代谢沃替西汀量可忽略不计。 分布容积 沃替西汀的表观分布容积约为2600升,表明其广泛分布于血管外。 代谢/代谢物 沃替西汀主要通过细胞色素P450同工酶CYP2D6、CYP3A4/5、CYP2C19、CYP2C9、CYP2A6、CYP2C8和CYP2B6进行氧化代谢,随后与葡萄糖醛酸结合。 CYP2D6 是催化伏硫西汀代谢为主要、无药理活性的羧酸代谢物的主要酶,CYP2D6 代谢能力弱者的伏硫西汀血浆浓度约为代谢能力强者的两倍。NIH;DailyMed。Brintellix(氢溴酸伏硫西汀)薄膜衣片(2014 年 7 月更新)的最新用药信息。截至 2015 年 6 月 30 日,可从以下网址获取:https://dailymed.nlm.nih.gov/dailymed/drugInfo.cfm?setid=4b0700c9-b417-4c3a-b36f-de461e125bd3 除单羟基伏硫西汀的葡萄糖醛酸苷结合物外,在人肝细胞中检测到的所有代谢物也存在于犬、小鼠和大鼠(血浆和/或尿液)体内,而单羟基伏硫西汀的葡萄糖醛酸苷结合物在小鼠或大鼠中未发现。在所有测试物种中,兔肝细胞的代谢物谱似乎与人肝细胞的代谢物谱最为接近。 生物半衰期 平均末端半衰期约为66小时 大鼠、犬和患者的口服绝对生物利用度分别约为10%、48%和75%,相应的末端消除半衰期分别为3.0小时、7.9小时和66小时。 作用机制 沃替西汀被归类为5-羟色胺调节剂和激动剂(SMS),因为它对5-羟色胺神经递质系统具有多模式作用机制,可同时调节一种或多种5-羟色胺受体并抑制5-羟色胺的再摄取。更具体地说,沃替西汀通过以下生物学机制发挥作用:作为血清素再摄取抑制剂 (SRI),通过抑制血清素转运体发挥作用;同时,它也是 5-HT1B 受体的部分激动剂、5-HT1A 受体的激动剂以及 5-HT3、5-HT1D 和 5-HT7 受体的拮抗剂。 1-(2-(2,4-二甲基苯硫基)-苯基)-哌嗪 (Lu AA21004) 是一种人血清素 (5-HT)3A 受体拮抗剂 (Ki = 3.7 nM)、5-HT7 受体拮抗剂 (Ki = 19 nM)、5-HT1B 受体部分激动剂 (Ki = 33 nM) 和 5-HT1A 受体激动剂。 (K(i) = 15 nM),以及人 5-HT 转运蛋白 (SERT) 抑制剂 (K(i) = 1.6 nM) (J Med Chem 54:3206-3221, 2011)。在此,我们使用基于全细胞 cAMP 的检测方法证实 Lu AA21004 是 h5-HT(1B) 受体的部分激动剂 [EC(50) = 460 nM,内在活性 = 22%],并证明 Lu AA21004 是大鼠 (r) 5-HT(7) 受体拮抗剂 (K(i) = 200 nM 和 IC(50) = 2080 nM)。体内实验表明,皮下注射 Lu AA21004 后可占据 r5-HT(1B) 受体和 rSERT 受体(ED(50) 分别为 3.2 和 0.4 mg/kg),并且在 Bezold-Jarisch 反射试验中表现出 5-HT(3) 受体拮抗作用(ED(50) = 0.11 mg/kg,皮下注射)。在大鼠微透析实验中,皮下注射 Lu AA21004(2.5-10.0 mg/kg)可增加内侧前额叶皮层和腹侧海马中细胞外 5-HT、多巴胺和去甲肾上腺素的水平。皮下注射 Lu AA21004(5 mg/kg/天,连续 3 天),相当于 41% 的 rSERT 受体占有率,可显著增加腹侧海马中细胞外 5-HT 的水平。此外,5-HT(3)受体拮抗剂昂丹司琼增强了西酞普兰诱导的细胞外5-HT水平升高。Lu AA21004在大鼠强迫游泳(弗林德斯敏感系)以及社交互动和条件性恐惧测试中均表现出抗抑郁和抗焦虑样作用(最小有效剂量分别为7.8、2.0和3.9 mg/kg)。总之,Lu AA21004通过两种药理机制发挥其药理作用:SERT抑制和5-HT受体调节。在体内,这导致多种神经递质释放增加,并在除SERT以外的其他靶点被占据的剂量下表现出抗抑郁和抗焦虑样作用。 Lu AA21004 的多模式活性谱与现有抗抑郁药截然不同。 单胺能网络,包括血清素 (5-HT)、去甲肾上腺素 (NE) 和多巴胺 (DA) 通路,高度相互关联,并在情绪障碍中发挥着重要作用。临床前研究表明,5-HT 受体亚型,包括 5-HT1A、5-HT1B、5-HT3 和 5-HT7 受体以及 5-HT 转运蛋白 (SERT),可能在抑郁症的治疗中发挥重要作用。本研究在重组细胞系中评估了新型多模式抗抑郁药 Lu AA21004 的神经药理学特征。Lu AA21004 结合了 5-HT3 和 5-HT7 受体拮抗作用、5-HT1B 受体部分激动作用、5-HT1A 受体激动作用以及 SERT 抑制作用。本研究评估了在急性及亚慢性使用 Lu AA21004 或艾司西酞普兰治疗后,腹侧海马 (vHC)、内侧前额叶皮层 (mPFC) 和伏隔核 (NAc) 中细胞外 5-羟色胺 (5-HT)、去甲肾上腺素 (NE) 和多巴胺 (DA) 的水平。此外,还分别评估了 LuAA21004 对蓝斑 (LC) 和腹侧被盖区 (VTA) 中 NE 和 DA 神经元放电的急性影响。急性 Lu AA21004 剂量依赖性地增加 vHC、mPFC 和 NAc 中的 5-HT 水平。vHC 中的 5-HT 峰值高于 mPFC。此外,mPFC 中的 5-HT 水平在低 SERT 受体占有率下升高。在 vHC 和 mPFC 中,而非 NAc 中,高剂量 Lu AA21004 可增加 NE 和 DA 水平。 Lu AA21004 轻微降低了蓝斑核 (LC) 去甲肾上腺素 (NE) 神经元的放电频率,但对腹侧被盖区 (VTA) 多巴胺 (DA) 神经元的放电频率没有影响。本文讨论了 5-HT3、5-HT1B 和 5-HT1A 受体以及 SERT 的占位情况。总之,Lu AA21004 通过两种药理学机制——5-HT 受体调节和 SERT 抑制——导致多种神经递质浓度出现脑区依赖性增加。和 ECNP。版权所有。PMID:22612991。Pehrson AL 等; 《欧洲神经精神药理学杂志》23 (2): 133-45 (2013) 沃替西汀是一种新型多模式抗抑郁药,它是一种5-羟色胺(5-HT)3、5-HT7和5-HT1D受体拮抗剂,5-HT1B受体部分激动剂,5-HT1A受体激动剂以及5-HT转运体(SERT)抑制剂。沃替西汀已被证明可以改善多种临床前大鼠模型和重度抑郁症患者的认知功能。本研究通过探讨沃替西汀对大鼠海马和额叶皮层突触传递、长时程增强(LTP,一种与学习和记忆相关的细胞机制)以及θ振荡的影响,来探究其作用机制。研究发现,沃替西汀能够抑制5-羟色胺(5-HT)诱导的CA1锥体细胞抑制性突触后电位(IPP)的增加,这很可能是通过拮抗5-HT3受体实现的。沃替西汀还能增强海马CA1区的长时程增强(LTP)。此外,在动物整体脑电图记录中,沃替西汀还能增加清醒状态下额叶皮层的θ波功率。相比之下,选择性5-羟色胺转运体(SERT)抑制剂艾司西酞普兰对上述任何指标均无影响。综上所述,我们的研究结果表明,沃替西汀能够增加锥体细胞的输出,从而增强海马的突触可塑性。鉴于海马体在认知功能中的核心作用,这些发现可能为观察到的沃替西汀的临床前和临床认知增强作用提供细胞层面的解释。 临床实验室方法 本研究建立并验证了一种简便、灵敏、快速的超高效液相色谱-串联质谱(UPLC-MS/MS)方法,用于定量测定大鼠血浆中的沃替西汀。血浆样品经蛋白质沉淀处理。分离采用Acquity UPLC BEH C18色谱柱(2.1mm×50mm,1.7μm),流动相为0.1%甲酸水溶液和乙腈的梯度洗脱液。检测采用正离子电喷雾串联质谱,并进行多反应监测(MRM)。经验证的方法在0.05-20 ng/mL范围内具有良好的线性(R²>0.997),定量下限为0.05 ng/mL。伏硫西汀的提取回收率为78.3-88.4%,卡马西平(内标,IS)的提取回收率为80.3%。日内和日间精密度均低于8.5%,准确度为-11.2%至9.5%。伏硫西汀未观察到明显的基质效应和失活效应。该方法首次成功应用于伏硫西汀在大鼠体内的药代动力学研究,为伏硫西汀的进一步开发和应用奠定了基础。PMID:26094207 Gu EM et al; J Chromatogr B Analyt Technol Biomed Life Sci 997: 70-74 (2015) 毒性概述 识别和用途:沃替西汀是一种白色至微米色粉末,制成薄膜衣片。它用于治疗成人重度抑郁症。人体暴露和毒性:关于沃替西汀人体过量服用的临床试验经验有限。在上市前临床研究中,过量服用病例仅限于意外或故意服用不超过40毫克沃替西汀的患者。男性受试者测试的最大单次剂量为75毫克。服用40至75毫克剂量范围内的沃替西汀与恶心、头晕、腹泻、腹部不适、全身瘙痒、嗜睡和潮红的发生率增加有关。沃替西汀在治疗剂量水平下也可能出现毒性。据报道,单独使用血清素能抗抑郁药(包括伏硫西汀)可能会引起危及生命的血清素综合征,尤其是在同时使用其他血清素能药物(包括血清素(5-羟色胺;5-HT)1 型受体激动剂(“曲坦类”)、三环类抗抑郁药、丁螺环酮、芬太尼、锂、曲马多、色氨酸和圣约翰草(贯叶连翘))以及损害血清素代谢的药物(特别是单胺氧化酶(MAO)抑制剂,包括用于治疗精神疾病的药物和其他药物,如利奈唑胺和亚甲蓝)时。血清素综合征的临床表现可能包括精神状态改变(例如,躁动、幻觉、谵妄和昏迷)、自主神经功能紊乱(例如,心动过速、血压波动、头晕、多汗、潮红和高热)、神经肌肉症状(例如,震颤、肌强直、肌阵挛、反射亢进和运动不协调)、癫痫发作和/或胃肠道症状(例如,恶心、呕吐和腹泻)。禁止同时或近期(即2周内)使用单胺氧化酶抑制剂(MAO抑制剂)治疗精神疾病。停用沃替西汀后3周内使用MAO抑制剂治疗精神疾病也是禁忌的。此外,正在接受其他MAO抑制剂(例如利奈唑胺或静脉注射亚甲蓝)治疗的患者也不应开始服用沃替西汀。如果临床上确有必要同时使用沃替西汀和其他血清素能药物,应告知患者血清素综合征风险可能增加,尤其是在治疗初期或剂量增加时。短期研究表明,抗抑郁药会增加儿童、青少年和年轻成人的自杀意念和行为风险。这些研究并未显示24岁以上患者使用抗抑郁药会增加自杀意念和行为风险;65岁及以上患者使用抗抑郁药则有降低风险的趋势。在体外培养的人类淋巴细胞染色体畸变试验中,沃替西汀未显示出遗传毒性。动物研究:沃替西汀的急性单次口服毒性相对较低,小鼠和大鼠的最大耐受剂量(MTD)分别为300 mg/kg和500 mg/kg。大鼠服用 500 mg/kg 剂量后出现临床症状,表现为对触觉和干扰的明显敏感、呼吸急促以及鼻周褐色染色。小鼠服用 200 和 300 mg/kg 剂量后出现震颤、触觉敏感、双眼半闭和活动减少;服用 400 和 500 mg/kg 剂量后出现呼吸急促、呼吸音粗重和/或呼吸困难、运动不协调、步态不稳、身体倾斜、流涎和活动过度。若以间隔一小时两次服用沃替西汀(200 mg/kg),则出现临床症状,包括抽搐,最终导致死亡。致癌性研究中,小鼠和大鼠分别口服沃替西汀,雄性小鼠和雌性小鼠的剂量分别高达 50 和 100 mg/kg/天,雄性大鼠和雌性大鼠的剂量分别高达 40 和 80 mg/kg/天,持续两年。在雌性大鼠中,直肠良性息肉样腺瘤的发生率显著高于雄性大鼠。这些息肉样腺瘤被认为与炎症和增生有关,并可能由研究中所用制剂的赋形剂成分相互作用引起。雄性大鼠未观察到此现象。在小鼠中,沃替西汀对雄性和雌性小鼠均无致癌性。妊娠期给予大鼠和兔沃替西汀会导致发育迟缓。妊娠期和哺乳期给予沃替西汀的大鼠,出生后也出现发育迟缓。在器官形成期给予大鼠或兔沃替西汀未观察到致畸作用。以高达120 mg/kg/天的剂量给予大鼠沃替西汀,对雄性和雌性大鼠的生育能力均无影响。沃替西汀在体外细菌回复突变试验(Ames试验)和体内大鼠骨髓微核试验中均未显示出遗传毒性。 肝毒性 少数患者会出现肝功能异常(可能性评分:E(未经证实但怀疑是临床上明显的肝损伤的罕见原因))。 蛋白结合 沃替西汀在人体内的血浆蛋白结合率为98%,与血浆浓度无关。健康受试者与肝功能(轻度、中度)或肾功能(轻度、中度、重度、终末期肾病)受损的受试者之间,血浆蛋白结合率未见明显差异。 乳酸沃替西汀(Lu AA21004)是一种新型多模式抗抑郁药,具有独特的作用机制:它抑制5-羟色胺再摄取(SERT)并调节多种5-HT受体亚型。 |