| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Glycopeptide; macrolides antibiotic/bactericidal; cell wall synthesis
Oritavancin (LY333328) targets bacterial cell wall synthesis by binding to the D-alanyl-D-alanine (D-Ala-D-Ala) terminus of peptidoglycan precursors, with minimum inhibitory concentrations (MIC) against susceptible bacteria ranging from 0.015 μg/mL to 2 μg/mL [2] |
|---|---|
| 体外研究 (In Vitro) |
Oritavancin是一种半合成的脂糖肽,具有抗革兰氏阳性细菌的活性,具有多种作用机制,包括抑制细胞壁合成和扰动膜电位。[1]
Oritavancin和万古霉素均达到99.9%(3-log)的杀灭率,奥利万星在1小时内达到检测限值(10(2)CFU/ml),万古霉素在24小时内达到这一限值。在48小时的实验中,未观察到奥利万星或万古霉素的耐药性检测。奥利万星的关键药效学参数尚未明确。在我们的实验中,奥利万星、奥利万星加白蛋白和万古霉素在0至24小时的曲线下面积与MIC的比值均大于944.5,血清中药物的最大浓度与MIC的比率在73.7至7188.5之间。T> 奥利万星和万古霉素的MIC均为100%。奥替万新是一种独特而有效的抗菌药物,值得对多重耐药肺炎链球菌进行进一步研究[2]。 针对多重耐药肺炎链球菌(包括青霉素耐药和红霉素耐药菌株),Oritavancin (LY333328) 具有强效抗菌活性,MIC90值为0.125 μg/mL,比万古霉素(MIC90 = 0.5-1 μg/mL)强效4-8倍 [2] - 在模拟人血清药代动力学的体外药效学模型中,Oritavancin (LY333328) 浓度对应2 mg/kg静脉给药剂量时,24小时内可使多重耐药肺炎链球菌活菌数减少>99%,杀菌效果持续长达72小时 [2] - 聚山梨酯80(0.01-0.1%)在药敏试验中可显著减少Oritavancin (LY333328) 与塑料表面的结合,使MIC值较无聚山梨酯80的试验降低2-4倍(如金黄色葡萄球菌的MIC从0.5 μg/mL降至0.125 μg/mL)[1] - Oritavancin (LY333328) 对炭疽杆菌(亲本菌株和荚膜缺陷突变体)具有杀菌活性,MIC值分别为0.06 μg/mL和0.03 μg/mL [3] - 针对急性细菌皮肤和皮肤结构感染(ABSSSI)相关病原体(金黄色葡萄球菌、化脓性链球菌、粪肠球菌),Oritavancin (LY333328) 的MIC90值分别为0.125 μg/mL、0.03 μg/mL和0.25 μg/mL,且具有杀菌活性(最低杀菌浓度[MBC]/MIC比值≤4)[4] |
| 体内研究 (In Vivo) |
在暴露后预防剂量范围研究中,在用Ames菌株孢子中位致死剂量的50至75倍进行攻击后24小时,单次静脉注射(i.v.)剂量为5、15或50mg/kg的奥利万星,在攻击后30天分别提供了40%、70%和100%的存活率。未经治疗的动物在攻击后4天内死亡,而90%的对照组动物从攻击后24小时开始每天两次接受30mg/kg环丙沙星腹腔注射,持续14天。奥立他万古霉素在症状发展后表现出显著的活性;在攻击后42小时单次静脉注射50mg/kg的剂量,在30天内提供了56%的比例存活率。在一项暴露前预防研究中,在致死攻击前1、7、14或28天静脉注射50mg/kg的奥利万星,在30天内保护了90%、100、100和20%的小鼠;在攻击前24小时或24和12小时用环丙沙星治疗的小鼠均在5天内死亡。吸入性炭疽暴露前和暴露后模型的疗效,以及产生耐药性的低倾向,促进了奥利万星在非人灵长类动物模型中的药代动力学和疗效的进一步研究[3]。
在炭疽杆菌孢子吸入感染小鼠模型中,Oritavancin (LY333328) 于感染后24小时单次静脉注射10 mg/kg、25 mg/kg或50 mg/kg,生存率分别为60%、90%和100%;万古霉素(50 mg/kg,每日2次,连续5天)的生存率为80% [3] - Oritavancin (LY333328)(25 mg/kg,静脉注射)在感染后48小时,可使小鼠肺、脾和血液中的细菌载量较未治疗对照组减少>3 log10 CFU/器官 [3] - 在ABSSSI的临床研究中,Oritavancin (LY333328) 单次静脉注射1200 mg,在治疗后7-14天的临床治愈率为86-92%,不劣于万古霉素(1 g静脉注射,每日2次,连续7-10天)[4] - 该化合物可在3-7天内缓解ABSSSI患者的感染体征(红斑、水肿、疼痛),治疗后28天仍维持临床应答 [4] |
| 酶活实验 |
Susceptibility of B. anthracis strains to oritavancin/奥替万星 as measured by broth microdilution. [3]
根据临床和实验室标准研究所的指导方针,通过96孔平板中的肉汤微量稀释法测定奥立他万古霉素MIC。按照指南M100-S18的建议,在整个药物溶解过程和测定的所有步骤中,聚山梨酯80的终浓度为0.002%,以尽量减少奥利万星与表面的结合。为了确定聚山梨酯80对炭疽杆菌的奥利万星MIC的影响(如果有的话),进行了平行肉汤微量稀释试验,其中奥利万星溶解在水中,药物稀释液不含聚山梨酸酯80。通过使用金黄色葡萄球菌ATCC 29213和0.002%的聚山梨酯80建立奥利万星稀释液的质量控制;针对该菌株的奥利万星MIC的可接受范围为0.015至0.12μg/ml。 奥替万星MIC试验中聚山梨酯80的滴定。[1] 为了确定奥利万星MIC对聚山梨酯80浓度的依赖性,根据CLSI M7-A7方法,以金黄色葡萄球菌ATCC 29213作为指示菌株进行了肉汤微量稀释敏感性试验,不同的是在药物溶解步骤中包括了不同试验浓度的聚山梨酸酯80,并将其保持在试验浓度。[1] 奥利万星MIC试验中聚山梨酯80的添加顺序。[1] 为了确定添加聚山梨酯80的顺序是否影响奥利万星MIC,以金黄色葡萄球菌ATCC 29213作为指示菌株进行了肉汤微量稀释敏感性试验,其中奥利万星溶解在0.002%的聚山梨酯80%中,并通过将聚山梨酯80维持在0.002%进行稀释和测定,或者溶解在水中并稀释,然后通过添加有或没有聚山梨酯八十的接种物进行测定。当存在聚山梨酯80时,按照CLSI达伐他汀指南中的描述,以0.002%的终浓度加入。 细菌肽聚糖结合实验:将含D-Ala-D-Ala末端的纯化细菌细胞壁肽聚糖片段固定在固相载体上,系列稀释的Oritavancin (LY333328) 与固定化肽聚糖孵育后,洗去未结合的化合物,使用特异性抗体检测结合的Oritavancin (LY333328),通过吸光度测量定量结合亲和力 [2] |
| 细胞实验 |
体外药效学模型。[2]
体外药效学模型由一个250毫升的单室玻璃室组成,该玻璃室带有端口,用于添加和去除含有0.5%酵母提取物(含或不含白蛋白)的THB、注射抗生素和去除样品。在每次实验之前,将含有5%SB的TSA板上过夜生长的细菌菌落加入含有0.5%酵母提取物的THB中,使浓度达到106 CFU/ml。每天制备奥利万星和万古霉素的新鲜储备溶液,并在两次给药之间在2至8°C下储存。实验方案模拟了人血浆中达到的抗生素浓度。万古霉素以每12小时1克的剂量给药(给予四剂),使血清峰值浓度(Cmax)达到30μg/ml,谷值浓度达到7.5μg/ml。为了在人类给药的前48小时内达到奥利万星在血浆中的目标浓度,奥利万星以5mg/kg体重的负荷剂量在0小时给药,然后在24小时给药4mg/kg,以达到100μg/ml的峰值浓度和15μg/ml的24小时谷值浓度。每种抗生素都使用皮下注射器在30秒内以丸剂形式给药到模型中。通过蠕动泵组连续供应新鲜培养基(SMHB)并将其与药物一起从模型中取出,以模拟万古霉素(6.5小时)和奥利万星(α期[t1/2α]=2小时的t1/2)的半衰期(t1/2s);泵在给药后以这种方式运行8小时,然后在24小时给药期的剩余16小时内改变为模拟12.3小时的t1/2。将每个模型装置置于水浴中,并在整个48小时的研究期间保持在37°C。药效学模型实验同时进行两次,以确保可重复性。
最低抑菌浓度(MIC)实验:将细菌菌株(肺炎链球菌、金黄色葡萄球菌、炭疽杆菌等)接种到含系列浓度Oritavancin (LY333328)(含或不含0.05%聚山梨酯80)的阳离子调节Mueller-Hinton肉汤(CAMHB)中,35°C孵育18-24小时,MIC定义为抑制细菌可见生长的最低浓度 [1] - 体外药效学模型:采用双室模型模拟Oritavancin (LY333328)(2 mg/kg静脉给药)的人血清浓度,模型中接种细菌,在0、2、4、8、24、48和72小时通过琼脂平板接种计数菌落,测定活菌数 [2] - 杀菌活性实验:将MIC实验中无可见生长的孔中100 μL肉汤接种到琼脂平板上,MBC定义为与初始接种量相比,活菌数减少≥99.9%的最低浓度 [4] |
| 动物实验 |
小鼠炭疽芽孢吸入模型:将6-8周龄的雌性BALB/c小鼠置于吸入室中,暴露于气溶胶化的炭疽芽孢(100×LD50)。感染后24小时,将奥利万星(LY333328)溶于生理盐水中,分别以10 mg/kg、25 mg/kg或50 mg/kg的剂量单次静脉注射给药。对照组分别注射生理盐水或万古霉素(50 mg/kg,静脉注射,每日两次,连续5天)。对小鼠进行为期 14 天的存活率监测,并在感染后 48 小时定量分析器官中的细菌载量 [3]
- ABSSSI 临床研究方案:将患有 ABSSSI(红斑/水肿 ≥75 cm²,伴有脓液或培养阳性)的成年患者随机分为两组,分别接受单次静脉注射奥利万星 (LY333328) (1200 mg) 或万古霉素 (1 g,每日两次,静脉注射),疗程 7-10 天。临床治愈定义为治疗后 7-14 天内感染体征/症状完全消退或显著改善 [4] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
奥利万星的药代动力学分析显示,其Cmax为138 μg/mL,AUC0-∞为2800 μg•h/mL。一项健康志愿者服用800 mg剂量后,AUC0-t为1111 μg•h/mL。另一项药代动力学研究报告称,Cmax为4.7-7.6 μg/mL,通常在给药后24小时内达到。 奥利万星以原形药物经尿液和粪便排泄。尿液中回收的药物不足5%,粪便中回收的药物为1%。 奥利万星的分布容积估计为87.6 L,表明其组织分布广泛。 奥利万星的清除率约为0.445 L/h。一项研究显示,肾清除率为 0.457 mL/min。 代谢/代谢物 体外人肝细胞研究表明,奥利万星不发生代谢,以原形排出体外。 生物半衰期 奥利万星的平均终末半衰期约为 245 小时。药代动力学研究显示,奥利万星 (LY333328) 的终末半衰期为 135.8-273.8 小时。在人体中,单次静脉注射 1200 mg 奥利万星 (LY333328) 后,血浆峰浓度 (Cmax) 为 113.8 μg/mL,血浆浓度-时间曲线下面积 (AUC0-∞) 为 3582 μg·h/mL,终末半衰期 (t1/2) 为 393 小时 [4]。该化合物具有较大的表观分布容积 (Vdss = 10.2 L/kg),表明其组织渗透性广泛,在皮肤和软组织(ABSSSI 的靶部位)中达到较高浓度 [4]。奥利万星 (LY333328) 主要通过非肾脏途径清除(肾脏排泄占总清除率的 <10%)[4]。 - 奥利万星 (LY333328) 在人血浆中的血浆蛋白结合率为 85-90% [4] |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概要 由于奥利万星口服吸收不良,不太可能进入婴儿血液循环,也不会对母乳喂养的婴儿造成任何不良反应。应监测婴儿的胃肠道反应,例如腹泻、呕吐和念珠菌病(如鹅口疮、尿布疹)。然而,由于目前尚无关于哺乳期使用奥利万星的已发表经验,因此,尤其是在哺乳新生儿或早产儿时,可能更倾向于选择其他药物。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 奥利万星与血浆蛋白的结合率约为 85%。 在 ABSSSI 的临床试验中,奥利万星 (LY333328)(1200 mg 静脉单次给药)具有良好的安全性,最常见的不良事件为头痛 (12%)、恶心 (8%) 和输注相关反应 (6%) [4] - 在小鼠毒性研究中,高达 50 mg/kg 的剂量(静脉单次给药)未引起明显的体重减轻,死亡率或主要器官(肝脏、肾脏、心脏、肺脏)的组织病理学异常[3] - 该化合物不抑制细胞色素P450同工酶,且在临床研究中未观察到显著的药物相互作用[4] |
| 参考文献 |
[1]. Effect of polysorbate 80 on oritavancin binding to plastic surfaces: implications for susceptibility testing. Antimicrob Agents Chemother. 2008 May;52(5):1597-1603.
[2]. Activity of oritavancin (LY333328), an investigational glycopeptide, compared to that of vancomycin against multidrug-resistant Streptococcus pneumoniae in an in vitro pharmacodynamic model. Antimicrob Agents Chemother. 2001 Mar;45(3):706-9.
[3]. Efficacy of oritavancin in a murine model of Bacillus anthracis spore inhalation anthrax. Antimicrob Agents Chemother. 2008 Sep;52(9):3350-7.
[4]. Oritavancin for the treatment of acute bacterial skin and skin structure infections: an evidence-based review. Core Evid. 2015 Feb 11;10:39-47. |
| 其他信息 |
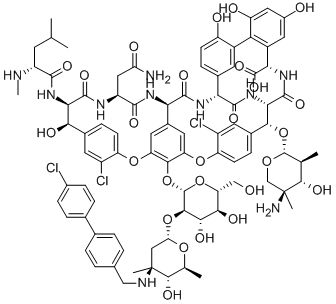
奥利万星是一种半合成糖肽类抗生素(以其磷酸二氢盐形式),用于治疗由特定革兰氏阳性菌(包括耐甲氧西林金黄色葡萄球菌[MRSA])的敏感菌株引起的或疑似引起的急性细菌性皮肤及皮肤软组织感染。它具有抗菌药物和抗微生物剂的作用。奥利万星是一种二糖衍生物、糖肽类抗生素和半合成衍生物,其功能与万古霉素苷元相关。
奥利万星是一种用于治疗皮肤感染的糖肽类抗生素,由医药公司(已被诺华收购)研发。奥利万星于2014年首次获得美国食品药品监督管理局(FDA)批准,其配方旨在对抗引起皮肤及皮肤软组织感染的敏感革兰氏阳性菌。奥利万星可单次给药,并已被证实其疗效不劣于完整的万古霉素疗程。 2021年3月12日,FDA批准了Kimyrsa上市,该药只需单次1小时静脉输注1200毫克即可完成一个疗程。另一种获得FDA批准的奥利万星产品Orbactiv,需3小时静脉输注,剂量较低,为400毫克。Kimyrsa由Melinta Therapeutics公司销售,可有效且快速地治疗皮肤及皮肤软组织感染。 奥利万星是一种脂肽类抗菌药物。奥利万星的作用机制是作为细胞色素P450 2C19抑制剂、细胞色素P450 2C9抑制剂、细胞色素P450 3A4诱导剂和细胞色素P450 2D6诱导剂。 另见:奥利万星二磷酸酯(活性成分)。 适应症 奥利万星适用于治疗成人急性细菌性皮肤及皮肤软组织(包括皮下组织)感染。它用于确诊/疑似由指定且对奥利万星敏感的革兰氏阳性菌引起的感染。奥利万星有两种制剂:400 mg剂量,3小时内给药;以及1200 mg剂量,1小时内给药。两种制剂均适用于治疗成人对奥利万星敏感的革兰氏阳性菌引起的皮肤及皮肤软组织感染。由于抗菌药物敏感性模式存在地域差异,使用前应参考当地的药敏试验结果,以确保对相关病原体具有充分的抗菌覆盖。 FDA标签 Tenkasi适用于治疗成人和3个月及以上儿童的急性细菌性皮肤及皮肤结构感染(ABSSSI)(参见4.2、4.4和5.1节)。应参考关于合理使用抗菌药物的官方指南。 作用机制 细胞壁对细菌的生存和复制至关重要,因此是抗生素治疗的主要靶点。奥利万星通过三种不同的机制对抗敏感的革兰氏阳性菌。首先,它与肽聚糖前体的肽链结合,抑制转糖基化(聚合)。该过程通常发生在细胞壁合成过程中。其次,奥利万星通过与细胞壁五甘氨酸肽桥接片段结合,抑制细菌细胞壁生物合成过程中的交联。最后,该药物还能通过破坏细菌细胞膜发挥作用,干扰其完整性,最终通过多种机制导致细胞死亡。 奥利万星 (LY333328) 是一种半合成糖肽类抗生素,具有双重作用机制:与 D-Ala-D-Ala 末端结合以抑制细胞壁合成,并破坏细菌细胞膜的完整性 [2] - 它对革兰氏阳性菌有效,包括多重耐药菌株(耐甲氧西林金黄色葡萄球菌 [MRSA]、万古霉素中介金黄色葡萄球菌 [VISA]、耐青霉素肺炎链球菌)[2] - 其较长的半衰期(约 16 天)使得 ABSSSI 可以单次给药治疗,无需每日多次给药或长时间静脉输注 [4] - 建议在药敏试验中使用聚山梨酯 80 以防止奥利万星 (LY333328) 与塑料表面结合,可能导致MIC值假性升高[1] |
| 分子式 |
C86H97N10O26CL3
|
|---|---|
| 分子量 |
1793.10078
|
| 精确质量 |
1790.56
|
| 元素分析 |
C, 57.61; H, 5.45; Cl, 5.93; N, 7.81; O, 23.20
|
| CAS号 |
171099-57-3
|
| 相关CAS号 |
Oritavancin diphosphate;192564-14-0
|
| PubChem CID |
16136912
|
| 外观&性状 |
Solid powder
|
| LogP |
8.57
|
| tPSA |
560.98
|
| 氢键供体(HBD)数目 |
20
|
| 氢键受体(HBA)数目 |
29
|
| 可旋转键数目(RBC) |
19
|
| 重原子数目 |
125
|
| 分子复杂度/Complexity |
3700
|
| 定义原子立体中心数目 |
22
|
| SMILES |
CC(C[C@H](C(N[C@H]1C(=O)N[C@@H](CC(=O)N)C(=O)N[C@H]2C(N[C@H]3C(=O)N[C@@H]([C@@H](C4C=CC(OC5C=C2C=C(C=5O[C@@H]2O[C@H](CO)[C@@H](O)[C@H](O)[C@H]2O[C@@H]2O[C@@H](C)[C@H](O)[C@@](C)(NCC5C=CC(C6C=CC(Cl)=CC=6)=CC=5)C2)OC2C=CC(=CC=2Cl)[C@H]1O)=C(Cl)C=4)O[C@@H]1O[C@@H](C)[C@H](O)[C@@](C)(N)C1)C(=O)N[C@H](C(=O)O)C1=CC(=CC(O)=C1C1=C(C=CC3=C1)O)O)=O)=O)NC)C
|
| InChi Key |
PWTROOMOPLCZHB-BHYQHFGMSA-N
|
| InChi Code |
InChI=1S/C86H97Cl3N10O26.2H3O4P/c1-35(2)22-51(92-7)77(110)98-67-69(105)42-15-20-55(49(88)24-42)120-57-26-44-27-58(73(57)125-84-74(71(107)70(106)59(34-100)122-84)124-62-32-86(6,76(109)37(4)119-62)93-33-38-8-10-39(11-9-38)40-12-17-45(87)18-13-40)121-56-21-16-43(25-50(56)89)72(123-61-31-85(5,91)75(108)36(3)118-61)68-82(115)97-66(83(116)117)48-28-46(101)29-54(103)63(48)47-23-41(14-19-53(47)102)64(79(112)99-68)96-80(113)65(44)95-78(111)52(30-60(90)104)94-81(67)1142*1-5(2,3)4/h8-21,23-29,35-37,51-52,59,61-62,64-72,74-76,84,92-93,100-103,105-109H,22,30-34,91H2,1-7H3,(H2,90,104)(H,94,114)(H,95,111)(H,96,113)(H,97,115)(H,98,110)(H,99,112)(H,116,117)2*(H3,1,2,3,4)/t36-,37-,51+,52-,59+,61-,62-,64+,65+,66-,67+,68-,69+,70+,71-,72+,74+,75-,76-,84-,85-,86-/m0../s1
|
| 化学名 |
(4R)-22-O-(3-Amino-2,3,6-trideoxy-3-C-methyl-α-L-arabinohexopyranosyl)-N3-(p-(p-chlorophenyl)benzyl)vancomycin diphosphate
|
| 别名 |
Oritavancin Free Base; LY333328; LY 333328; 171099-57-3; LY333328; Chlorobiphenyl-chloroeremomycin; Oritavancin [INN]; LY-333328; UNII-PUG62FRZ2E; PUG62FRZ2E; LY-333328
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.5577 mL | 2.7885 mL | 5.5769 mL | |
| 5 mM | 0.1115 mL | 0.5577 mL | 1.1154 mL | |
| 10 mM | 0.0558 mL | 0.2788 mL | 0.5577 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。