| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
5-HT2B Receptor (pKi = 7.5); 5-HT2C Receptor (pKi = 6.9); 5-HT2A Receptor (pKi = 5.2)
|
|---|---|
| 体外研究 (In Vitro) |
SB200646A (4 μM) 消除了乙醇引起的微型抑制性突触后电流 (mIPSC) 频率的上升,而基础 mIPSC 频率不受影响[1]。
|
| 体内研究 (In Vivo) |
用 SB-200646A(20 mg/kg;静脉注射;每天;持续 21 天)治疗雄性白化 Sprague-Dawley 大鼠可显着减少腹侧被盖区 (VTA) 中自发激活的多巴胺能神经元的数量[1]。在自发激活的 VTA 多巴胺能神经元中,静脉注射 4-16 mg/kg SB-200646A 极大地提高了放电率和爆发事件的百分比,而在黑质致密部 (SNC) 多巴胺能神经元中,它显着增加了放电率和爆发事件的百分比突发事件[1]。
1.SB 200646A,N-(1-甲基-5-吲哚基)-N'-(3-吡啶基)脲盐酸盐,首次报道的选择性5-HT2C/2B超过5-HT2A受体拮抗剂,(pK1大鼠5-HT2C受体6.9,pA2大鼠5-HT2B受体7.5,pK1大白鼠5-HT2A受体5.2)剂量依赖性阻断了5-HT2C受体激活的大鼠模型;1-(3-氯苯基)哌嗪(mCPP,5 mg kg-1,腹腔注射20分钟预测试)诱导的运动减少(估计ID50 19.2 mg kg-1)。2.SB 200646A还阻断了另一种推测的5-HT2C受体功能的体内模型;mCPP(5 mg kg-1,腹腔注射20分钟预试验)诱导23小时食物剥夺大鼠出现低吞咽(估计ID50 18.3 mg kg-1)。3.SB 200646A在口服剂量高达200mg kg-1时,不能拮抗1-(2,5-二甲氧基-4-碘苯基)-2-氨基丙烷(DOI)诱导的大鼠摇头,这种作用被认为是由5-HT2A受体介导的,SB 200646A对5-HT2A受体的亲和力仅次于5-HT2C和5-HT2B位点(低50倍)。4.SB 200646A(20,40 mg kg-1,口服,1小时预测试)也在低光熟悉条件下逆转了mCPP(0.5 mg kg-1)诱导的社交互动测试中的焦虑。5.在强光不熟悉的条件下单独给药时,SB 200646A(2-40mg kg-1,口服)在大鼠社交互动测试中增加了积极的社交互动,而不影响运动活动。这与SB 200646A的抗焦虑作用是一致的。6.这些结果表明,SB 200646A具有体内疗效,5-HT2C或5-HT2B受体确实可能介导mCPP诱导的低运动、低焦虑和焦虑。他们还表明,5-HT2C、2B受体阻断可诱导抗焦虑[2]。 |
| 细胞实验 |
VTA-DA神经元的电生理记录。将单个切片转移到记录室中,以约2 ml/min的流速用含氧aCSF(30-32°C)灌注。记录aCSF如上所述,但其中含有0.9 mM MgSO4和2 mM CaCl2。在Olympus BX-50WI显微镜上使用IR-DIC光学元件对细胞进行可视化。VTA被确定为副视束内侧终末核内侧和动眼神经及内侧悬韧带的头端。大多数记录是在副视束内侧终核内侧的外侧VTA进行的。所有实验均使用全电池电压钳记录;通过存在大的超极化激活的阳离子电流(>200 pA)来鉴定推定的DA神经元,该电流在闯入后立即通过施加-60至-110 mV的1.5秒超极化步长进行测量(Johnson和North,1992b)。记录电极由薄壁硼硅酸盐玻璃(TW 150F-4;WPI,Sarasota,FL;1.5-2.5 MΩ)制成,含有135 mM KCl、12 mM NaCl、0.5 mM EGTA、10 mM HEPES、2 mM Mg-ATP和0.3 mM Tris-GTP,pH 7.3,含KOH。数据由Axon Instruments 200B型放大器收集,该放大器在1 kHz下滤波,并使用pClamp 9.2和10.2版本的Digidata接口在10至20 kHz下数字化。
GABA能mIPSCs用犬尿酸(1 mM)进行药理学分离,以抑制α-氨基-3-羟基-5-甲基-4-异恶唑丙酸和N-甲基-d-天冬氨酸受体介导的电流。包括河豚毒素(TTX;0.5μM)和依替洛匹林(250 nM),分别阻断Na+电流和D2受体介导的电流。在这些条件下,mIPSCs在-60 mV的保持电位下向内生长,在最初的一组实验中,通过用苦味毒或荷包牡丹碱进行阻断测试,验证了它们作为GABAric事件的身份(数据未显示)。在中断和稳定的10分钟基线(对照)记录后,通过aCSF灌注线对药物进行浴敷,并使用连续10至15分钟的记录时间来检测mIPSC频率和振幅的变化。在每种治疗条件下,在开始数据收集之前进行4分钟的药物清洗,在药物应用后进行12分钟的清洗期。我们的数据分析中使用了洗脱期的后半段(6分钟)。每种治疗条件下使用的神经元数量表示为n,每个切片只使用一个神经元[3]。
|
| 动物实验 |
动物/疾病模型:雄性白化SD(Sprague-Dawley)大鼠(治疗开始时体重200-225克,实验时体重300-350克)[1]
剂量:20毫克/千克 给药途径:静脉注射(iv);每日一次;持续21天 实验结果:显著减少了腹侧被盖区(VTA)自发活动多巴胺能神经元的数量。 |
| 参考文献 |
[1]. Blackburn TP, et al. The acute and chronic administration of the 5-HT(2B/2C) receptor antagonist SB-200646A significantly alters the activity of spontaneously active midbrain dopamine neurons in the rat: An in vivo extracellular single cell study. Synapse
[2]. Kennett GA, et al. In vivo properties of SB 200646A, a 5-HT2C/2B receptor antagonist. Br J Pharmacol. 1994 Mar;111(3):797-802. [3]. Theile JW, et al. Role of 5-hydroxytryptamine2C receptors in Ca2+-dependent ethanol potentiation of GABA release onto ventral tegmental area dopamine neurons. J Pharmacol Exp Ther. 2009 May;329(2):625-33. |
| 其他信息 |
本研究探讨了5-HT(2B/2C)受体拮抗剂N-(1-甲基-5-吲哚基)-N'-(3-吡啶基)脲盐酸盐(SB-200646A)急性及慢性给药对麻醉雄性Sprague-Dawley大鼠黑质致密部(SNC)和腹侧被盖区(VTA)自发活动多巴胺能神经元活性的影响。采用体内细胞外单细胞记录技术进行研究。静脉注射4-16 mg/kg SB-200646A可显著增加VTA自发活动多巴胺能神经元的放电频率和爆发放电百分比,并显著增加SNC多巴胺能神经元的爆发放电百分比。与载体对照组相比,腹腔注射20和40 mg/kg的SB-200646A可显著增加VTA自发活动DA神经元的数量。与载体对照组相比,腹腔注射10 mg/kg的SB-200646A可显著增加SNC和DA神经元自发活动变异系数。然而,腹腔注射20 mg/kg的SB-200646A可显著降低VTA DA神经元的爆发性放电程度。同样,腹腔注射10 mg/kg的SB-200646A对神经元放电无显著影响,而腹腔注射20 mg/kg的SB-200646A或20 mg/kg的氯氮平则可显著降低VTA自发活动DA神经元的数量。 SB-200646A 诱导的自发性 VTA 多巴胺能神经元数量减少可通过静脉注射 (+)-阿扑吗啡或 (-)-巴氯芬逆转。长期腹腔注射 10 或 20 mg/kg SB-200646A 并未显著改变自发性 SNC 多巴胺能神经元的放电模式。然而,与溶媒组相比,长期注射 20 mg/kg SB-200646A 显著增加了 VTA 多巴胺能神经元的爆发性放电程度。总体而言,SB-200646A 的急性及慢性给药均可产生与非典型抗精神病药物类似的体内电生理效应。[1]
|
| 分子式 |
C15H15CLN4O
|
|---|---|
| 分子量 |
302.76
|
| 精确质量 |
302.093
|
| 元素分析 |
C, 59.51; H, 4.99; Cl, 11.71; N, 18.51; O, 5.28
|
| CAS号 |
143797-62-0
|
| 相关CAS号 |
SB-200646; 143797-63-1
|
| PubChem CID |
5311422
|
| 外观&性状 |
Typically exists as Off-white to light yellow solid at room temperature
|
| tPSA |
59Ų
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
349
|
| 定义原子立体中心数目 |
0
|
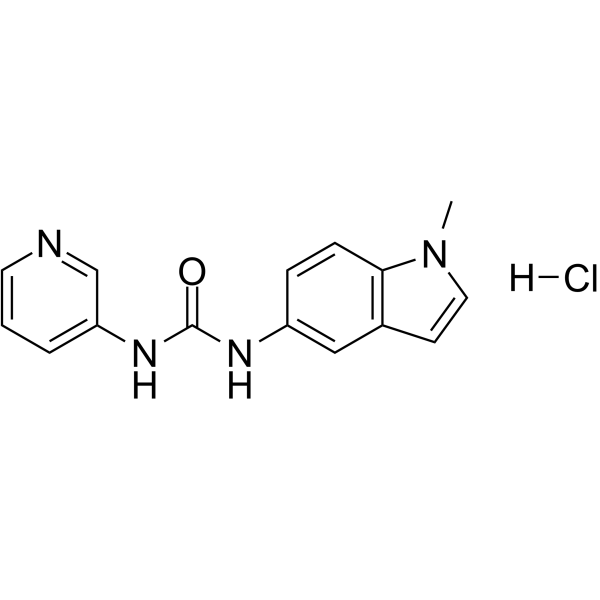
| SMILES |
Cl.C1C=CC(NC(NC2C=CC3N(C=CC=3C=2)C)=O)=CN=1
|
| InChi Key |
IGRYPUQJEDJLHC-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C15H14N4O.ClH/c1-19-8-6-11-9-12(4-5-14(11)19)17-15(20)18-13-3-2-7-16-10-13;/h2-10H,1H3,(H2,17,18,20);1H
|
| 化学名 |
1-(1-methylindol-5-yl)-3-pyridin-3-ylurea;hydrochloride
|
| 别名 |
SB 200646 hydrochloride; 143797-62-0; SB-200646A; SB 200646 HCl; 1-(1-methylindol-5-yl)-3-pyridin-3-ylurea;hydrochloride; SB-200646 hydrochloride; SB200646; 3-(1-METHYLINDOL-5-YL)-1-(PYRIDIN-3-YL)UREA HYDROCHLORIDE;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 250 mg/mL (825.74 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.3029 mL | 16.5147 mL | 33.0295 mL | |
| 5 mM | 0.6606 mL | 3.3029 mL | 6.6059 mL | |
| 10 mM | 0.3303 mL | 1.6515 mL | 3.3029 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。