| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
KRAS G12C
|
|---|---|
| 体外研究 (In Vitro) |
结束了一个被药物开发失败所破坏的时代,人们对直接靶向KRAS的兴趣减弱,并认为难以解决,新技术和策略正在帮助目标的复苏。如前所述,四氢吡啶并嘧啶被鉴定为KRASG12C的不可逆共价抑制剂,它们结合在KRAS的开关II口袋中,与半胱氨酸12形成共价键。使用基于结构的药物设计,结合集中的体外吸收、分布、代谢和排泄筛选方法,合成了类似物,以提高该系列的效力并降低代谢责任。描述了临床开发候选物MRTX849作为KRASG12C的强效选择性共价抑制剂的发现[1]。
|
| 酶活实验 |
KRASG12C目标参与度[1]
肿瘤片段在6 M胍-HCl、50 mM N-(2-羟乙基)哌嗪-N′-乙磺酸(HEPES)(pH 7.5)和5 mM TCEP中均化。离心后,使用Bradford测定法测定上清液的蛋白质浓度。将内标物(13C15N重组KRASG12C)和20 mM碘乙酰胺加入200μL裂解缓冲液中的200μg肿瘤蛋白中,并在37°C下在黑暗中孵育样品30分钟。烷基化后,使用96孔Zeba旋转板将100μL反应物交换为1 M胍-HCl、50 mM HEPES(pH 7.5)。在37°C下用1μg胰蛋白酶/Lys-C混合物消化蛋白质18小时。使用C18旋转板对肽进行脱盐,并通过蒸发去除溶剂。将肽溶解在0.1%甲酸、5%乙腈、95%水中,用于LCMS分析。使用Sciex TripleTOF仪器上的靶向方法监测含Cys-12的KRASG12C肽(一种内部参考肽)以及相应的同位素标记肽。KRASG12C的参与度是按照之前的报告计算的。 |
| 细胞实验 |
基于细胞的磷酸化ERK检测[1]
所有实验均在标准条件下(37°C和5%CO2)进行。采用四参数法通过剂量反应曲线拟合计算IC50值。将携带KRASG12C突变的NCI-H358细胞接种在补充有10%胎牛血清的RPMI中的96孔板中。将培养皿孵育过夜。用抑制剂孵育细胞3小时后,用磷酸缓冲盐水(PBS)洗涤细胞一次,用3.8%甲醛固定,用冰冷的甲醇渗透。然后将平板与Li-Cor阻断缓冲液一起孵育。随后,通过与针对GAPDH(小鼠)和磷酸化ERK(兔)的一抗孵育,通过细胞内蛋白质法评估ERK的磷酸化。然后将平板与小鼠或兔特异性的荧光二抗一起孵育。在Li-Cor荧光平板阅读器上以680和800nm波长对平板进行成像。将磷酸化ERK信号归一化为GAPDH信号,并生成POC值[1]。 |
| 动物实验 |
体内研究[1]
小鼠饲养于无病原体(SPF)条件下,并自由摄取食物和水。将6-8周龄的雌性无胸腺裸鼠(Foxn1nu)右后侧皮下注射NCI-H358或MIA PaCa-2细胞,细胞悬液为100 μL PBS和Matrigel基质混合液,细胞浓度为5.0 × 10⁶个,细胞与Matrigel的比例为50:50。每日监测小鼠健康状况,当肿瘤可触及时开始使用游标卡尺测量肿瘤体积。肿瘤体积的计算公式为0.5 × L × W²,其中L代表肿瘤长度,W代表肿瘤宽度。当肿瘤平均体积达到约350 mm³时,将小鼠随机分组。小鼠经口灌胃给予赋形剂(10% 研究级 Captisol,溶于 50 mM pH 5.0 的柠檬酸缓冲液)或赋形剂(研究化合物),剂量如所示。在疗效研究中,动物经口给予研究化合物或赋形剂,并每日监测,每周测量 3 次肿瘤大小,每周测量 2 次体重。疗效图中的研究日表示化合物给药后的第二天。在药代动力学/药效学研究中,于指定时间点和浓度范围内,单次给药后采集肿瘤和血浆样本。 |
| 参考文献 |
[1]. Jay B Fell, et al. Identification of the Clinical Development Candidate MRTX849, a Covalent KRAS G12C Inhibitor for the Treatment of Cancer. J Med Chem. 2020 Jul 9;63(13):6679-6693.
|
| 其他信息 |
稳定性——添加GSH的肝细胞溶胶[1]
将化合物(1 μM)在37 °C下于1 mg/mL肝细胞溶胶中孵育30分钟,该溶胶在KPB缓冲液中添加了5 mM GSH。在指定时间点结束时,用添加了40 mM NEM和0.2 μM拉贝洛尔(内标)的乙腈终止反应。离心后,用LC-MS/MS分析上清液。 全血稳定性[1] 将化合物(5 μM)在37 °C下于1:1 (v/v)血液和PBS(pH 7.4)混合液中孵育30、60和240分钟。稀释后的血液在 37 °C 和 100% 湿度下预孵育 15 分钟,然后加入化合物启动反应。在每个指定时间点结束时,将红细胞与水按 1:1 的比例裂解,以 600 rpm 的速度混合 1 分钟,然后用含有 0.625 μM 拉贝洛尔(内标)的乙腈终止反应。样品经离心后,取上清液进行LC-MS/MS分析。 kinact/KI[1]的测定 将重组KRASG12C“Lite”(C51S/C80L/C118S)与不同浓度的MRTX849在25 mM HEPES(pH 7.0)、150 mM NaCl、5 mM MgCl2、10 mM辛基β-吡喃葡萄糖苷和0.5 mM TCEP的反应体系中于室温下反应0-45秒。在每个时间点,用50 mM HCl终止反应,并加入0.25 μg胃蛋白酶。KRASG12C在37℃下消化4小时,所得含Cys-12的肽段用LCMS分析。在每个时间点,根据每种 MRTX849 浓度的 0 秒对照样品计算修饰的 KRASG12C 的百分比,然后根据 ln(POC) 与时间数据的斜率计算 kobs 值。速率与浓度数据符合米氏方程。 肝细胞代谢物鉴定[1] 将冷冻保存的小鼠、大鼠、犬和人肝细胞解冻,并使用 Dulbecco 改良 Eagle 培养基稀释至 1 × 10⁶ 个细胞/mL 的活细胞密度。向 1 mL 各肝细胞悬液中加入 MRTX849 (10 μM),并在 37 °C 下孵育 2 小时。加入 1% 甲酸终止代谢,离心后将上清液上样至 3 cc Oasis HLB 固相萃取柱。 MRTX849及其代谢物用5%甲醇水溶液洗涤,并用100%甲醇洗脱。溶剂在氮气流下蒸发,代谢物用150 μL 30:70 (v/v)乙腈/水溶液复溶。代谢物在Gemini NX-C18色谱柱上分离,并通过290 nm波长下的吸光度和质谱进行检测。代谢物的相对含量通过290 nm波长下的吸光度峰强度确定,生物转化通过相关的m/z和MS/MS碎片模式进行表征。 NCI-H358蛋白质组半胱氨酸选择性分析[1] 将NCI-H358细胞用3 μM MRTX849处理3小时,然后用含1% NP-40的裂解缓冲液裂解并进行超声处理。细胞提取物用 5 mM 碘乙酰胺脱硫生物素处理 1 小时(室温)。蛋白质用丙酮沉淀,并重悬于含有 6 M 盐酸胍、50 mM HEPES(pH 7.5)和 5 mM TCEP 的缓冲液中,于 65 °C 孵育 15 分钟。经碘乙酰胺处理后,将缓冲液置换为 1 M 盐酸胍、50 mM HEPES(pH 7.5),然后用胰蛋白酶/Lys-C 消化过夜。脱硫生物素化的肽段用链霉亲和素琼脂糖富集,并用 50% 乙腈和 0.1% TFA 洗脱。溶剂通过蒸发去除,肽段重悬于 0.1% 甲酸、5% 乙腈和水中。样品在 Sciex 6600 TripleTOF 质谱仪上进行分析。使用 Protein Pilot 5 软件,通过数据依赖型 MS/MS 扫描鉴定脱硫生物素标记的肽段,并使用 SWATH 分析进行相对定量(MTRX849 处理组与对照组)。 点击化学靶标鉴定[1] 将两瓶 NCI-H358 细胞(每瓶 6000 万个细胞)接种于 RPMI 1640 SILAC 轻培养基中,并用 DMSO 处理作为对照;另将两瓶接种于 RPMI 1640 SILAC 重培养基(含 13C6-赖氨酸和 13C6,15N4-精氨酸)中的细胞用 1 μM MRTX849 在 37 °C 下处理 3 小时。所有细胞随后均用 2 μM 化合物 24 在 37 °C 下处理 3 小时。随后,将细胞用 50 mM HEPES、150 mM NaCl、0.5% Triton-X 100、1 mM EDTA、1 mM EGTA 和 HALT 蛋白酶抑制剂混合物裂解 5 分钟,进行超声破碎,离心,并用 45 μm 针筒式过滤器过滤上清液。每个重复实验中,将 4 mg “轻”裂解液中的蛋白质与 4 mg “重”裂解液中的蛋白质混合进行样品处理。使用氯仿/甲醇沉淀法分离蛋白质,将其重悬于 0.18% 十二烷基硫酸钠 (SDS) 的 50 mM HEPES (pH 7.5) 缓冲液中,并在室温下与 5 mM 抗坏血酸、1 mM CuSO4 和 2 mM BTTAA 孵育 2.5 小时,进行叠氮琼脂糖“点击”反应。将树脂结合的蛋白质用 10 mM DTT 处理 40 分钟,再用 20 mM 碘乙酰胺处理 30 分钟,然后依次用以下溶液洗涤:(1) 100 mM Tris(pH 8.0)、250 mM NaCl、1% SDS、5 mM EDTA;(2) 8 M 尿素、100 mM Tris(pH 8.0);(3) 20% 乙腈水溶液。向蛋白结合的树脂中加入 1 μg 胰蛋白酶/Lys-C,悬浮于 20 mM Tris(pH 8.0)、2 mM CaCl₂、10% 乙腈溶液中,并在 37 °C 下孵育 18 小时。洗脱的肽段经C18旋转柱脱盐,蒸发除去溶剂,然后将肽段重悬于0.1%甲酸、5%乙腈和水中,用于LCMS分析。样品在Sciex 6600 TripleTOF质谱仪上进行分析。使用Protein Pilot 5软件从未标记样品的基于数据的MS/MS扫描中鉴定肽段,并使用SILAC样品的SWATH分析进行相对定量(MTRX849处理组与对照组)。 |
| 分子式 |
C36H39CLFN7O2
|
|---|---|
| 分子量 |
656.19
|
| 精确质量 |
655.283
|
| CAS号 |
2490716-96-4
|
| 相关CAS号 |
Adagrasib;2326521-71-3
|
| PubChem CID |
162642619
|
| 外观&性状 |
Typically exists as White to off-white solid at room temperature
|
| LogP |
6
|
| tPSA |
88.8Ų
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
47
|
| 分子复杂度/Complexity |
1200
|
| 定义原子立体中心数目 |
2
|
| SMILES |
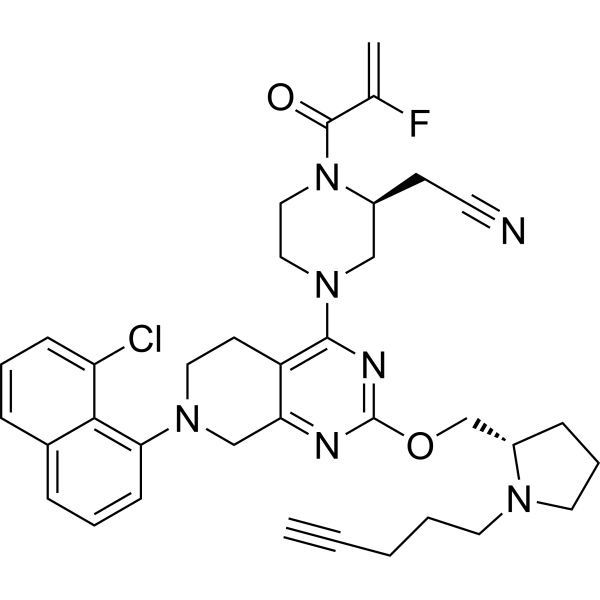
C=C(C(=O)N1CCN(C[C@@H]1CC#N)C2=NC(=NC3=C2CCN(C3)C4=CC=CC5=C4C(=CC=C5)Cl)OC[C@@H]6CCCN6CCCC#C)F
|
| InChi Key |
YUPCFANWZUHYAJ-NSOVKSMOSA-N
|
| InChi Code |
InChI=1S/C36H39ClFN7O2/c1-3-4-5-17-42-18-8-11-28(42)24-47-36-40-31-23-43(32-13-7-10-26-9-6-12-30(37)33(26)32)19-15-29(31)34(41-36)44-20-21-45(35(46)25(2)38)27(22-44)14-16-39/h1,6-7,9-10,12-13,27-28H,2,4-5,8,11,14-15,17-24H2/t27-,28-/m0/s1
|
| 化学名 |
2-[(2S)-4-[7-(8-chloronaphthalen-1-yl)-2-[[(2S)-1-pent-4-ynylpyrrolidin-2-yl]methoxy]-6,8-dihydro-5H-pyrido[3,4-d]pyrimidin-4-yl]-1-(2-fluoroprop-2-enoyl)piperazin-2-yl]acetonitrile
|
| 别名 |
MRTX-849 analog 24; MRTX849 analog 24
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~76.20 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5239 mL | 7.6197 mL | 15.2395 mL | |
| 5 mM | 0.3048 mL | 1.5239 mL | 3.0479 mL | |
| 10 mM | 0.1524 mL | 0.7620 mL | 1.5239 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。