| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
AT2/1 Receptor
|
|---|---|
| 体外研究 (In Vitro) |
Ang II 增加的增殖细胞核抗原(PCNA)蛋白在 Ang-(1-7) 被抑制时不表达,而 A-779 本身对引起 VSMC 迁移和增殖几乎没有作用。 A-779 阻断 Ang-(1-7) 对 VSMC 炎症反应的影响,该反应与 MCP-1、VCAM-1 和 IL-1β 产生的升高有关。 Ang-(1-7)预处理可以大大延缓这种炎症反应。但 A-779 本身无法引起 VSMC 发炎。在 Ang II 诱导的 Akt 和 ERK1/2 激活显着降低之前,用 Ang-(1-7) 处理 VSMC 5 分钟。 A-779 也有这种作用,尽管它本身不会引起 Akt 和 ERK1 磷酸化。 /2 在 VSMC[3] 中的功能。
结果:(1)Annexin V-FITC/PI双染流式细胞术结果显示,ox-LDL组凋亡细胞比例高于对照组((21.18±1.40)%对(1.59±0.26)%,P<0.01),ox-LLDL+Ang-(1-7)组((7.42±1.07)%)和ox-LLD+HTA125组(9.19±1.01)%低于ox-LDL(均P<0.01),ox-LLDL+(1-7)+A-779组(19.91±1.30)%和ox-LDL+A-779组((20.47±0.95)%)明显高于ox-LLDL+Ang-(1-7)组(均P<0.01)。(2)TUNEL结果显示,ox-LDL组凋亡细胞比例高于对照组((10.83±0.77)%对(2.83±0.82)%,P<0.01),ox-LLDL+Ang-(1-7)组((3.66±0.54)%)和ox-LLD+HTA125组(4.97±0.60)%低于ox-LDL对照组(均P<0.01),ox LDL+Ang+A-779组(10.69±0.62)%和ox-LDL+A-779组(11.43±0.42)%高于ox-LLD+Ang-(1-7)组(均P<0.01)。(3)ox-LDL组ROS水平高于对照组(0.093±0.014 vs.0.053±0.011,P<0.01),ox-LLDL+Ang-(1-7)组(0.063±0.0111,P<0.01)和ox-LLD+HTA125组(0.070±0.010,P<0.05)低于ox-LDL,ox-LDL+Ang-(1-7)+A-779(0.088±0.003)和oxLDL+A-779组(0.095±0.005)高于ox-LLD+Ang-(1-七)组(均P<0.01)。(4)ox-LDL组NOX4 mRNA表达水平高于对照组(11.74±0.65 vs.1.00±0.00,P<0.01),ox-LLDL+Ang-(1-7)组(2.85±0.75)和ox-LLD+HTA125组(5.57±0.52)低于ox-LDL(均P<0.01),ox-LLDL+Ang-(1-7)+A-779组(10.51±0.54)和oxLDL+A-779组(11.04±1.01±1.86 vs.1.00±0.00,P<0.01),ox-LLDL+Ang-(1-7)组(8.00±1.03)和ox-LLD+HTA125组(14.83±0.97)低于ox-LDL组(均P<0.01),ox-LLDL+Ang(1-7+A-779)组(24.81±2.19)和ox LDL+A-779组(26.64±0.65)高于ox-LLDN+Ang-(1-7)组,均P<0.01。(5)ox-LDL组NOX4蛋白表达水平高于对照组(0.61±0.09 vs.0.23±0.02,P<0.01),ox-LLDL+Ang-(1-7)组(0.27±0.03)和ox-LLD+HTA125组(0.22±0.02)低于ox-LDL(均P<0.01),ox-LLDL+Ang-(1-7)+A-779组(0.58±0.06)和oxLDL+A-779组。ox-LDL组TLR4的蛋白表达水平高于对照组(0.18±0.02 vs.0.08±0.01,P<0.01),ox-LLDL+Ang-(1-7)组(0.07±0.01)和ox-LLD+HTA125组(0.09±0.01。结论:TLR4介导了ox-LDL诱导的HUVEC损伤,Ang-(1-7)可以通过调节特异性Mas受体来减轻ox-LDL对HUVEC的损伤[3]。 |
| 体内研究 (In Vivo) |
六周内,单独或联合输注 Ang(1-7) 和 A-779(400ng/kg/min,皮下注射)的 OVX 大鼠并未阻止子宫萎缩或抑制体重增加。 A-779 显着升高 I 型胶原端肽 (CTX)、抗酒石酸酸性磷酸酶 (TRAcP 5b)、骨钙素 (OC)、尿脱氧吡啶苯啉 (DPD) 和骨特异性碱性磷酸酶 (BALP) 的血清水平。输注 Ang(1-7) 和/或 A-779 未显着改变 OVX 组或假手术组的血清矿物质浓度。与 OVX 组相反,OVX 动物中的 A-779 不会改变 AngII、Ang(1-7)、AT1R、AT2R、ACE、ACE-2、Mas 受体、RANKL 或 OPG 蛋白的表达。然而,A-779(400ng/kg/min)显着降低了卡托普利对骨代谢、矿化和微观结构的保护作用。 A-779 还恢复了 OVX 对 RANKL 表达 ACE-1/AngII/AT1R 级联的影响,并下调 OPG 表达和 ACE-2/Ang1-7/Mas 通路 [2]。
|
| 细胞实验 |
人脐静脉内皮细胞的培养和分组:[3]
用含10%胎牛血清和1%青、链霉素混合液的1640培养基,在37 ℃、5%CO 2培养箱中培养人脐静脉内皮细胞,以倒置相差显微镜观察细胞的生长情况。在细胞生长至融合度为80%以上时,以磷酸盐缓冲液(含8.0 g NaCl、0.2 g KCl、3.4 g Na 2HPO 4·H 2O和0.2 g KH 2PO 4,pH值7.4)清洗,0.25%胰酶和0.04%乙二胺四乙酸(EDTA)消化传代。6孔板接种细胞,每孔5×10 5个细胞/ml。细胞生长至80%时,无血清培养基同步化处理12 h,然后进行分组。 将细胞分为6组,分别为对照组(不干预)、ox-LDL组(以ox-LDL 75 mg/L干预)、ox-LDL+Ang-(1-7)组[Ang-(1-7) 1 μmol/L预处理30 min后,以ox-LDL 75 mg/L干预]、ox-LDL+Ang-(1-7)+A-779组[A-779(Mas受体阻断剂) 1 μmol/L预处理30 min,然后以Ang-(1-7)1 μmol/L预处理30 min,再以ox-LDL 75 mg/L干预]、ox-LDL+A-779组(A-779 1 μmol/L预处理30 min后,以ox-LDL 75 mg/L干预)、ox-LDL+HTA125组[HTA125(TLR4特异性阻断抗体)10 μg/L预处理30 min后,以ox-LDL 75 mg/L干预]。24 h后进行实验观察指标的检测。 |
| 动物实验 |
实验模型和研究方案[1]
\n采用双侧卵巢切除术(OVX)诱导雌性Wistar白化大鼠发生绝经后骨质疏松。动物采用腹腔注射氯胺酮+赛拉嗪(分别为80 mg/kg和5 mg/kg)进行全身麻醉。结扎后,通过背外侧纵向切口切除卵巢。假手术组大鼠接受相同的手术操作,但不进行结扎和切除。术后每周两次局部涂抹夫西地酸抗生素软膏,持续4周,以消除感染风险。在假手术和卵巢切除手术后,将动物分为八组(每组 n = 8),包括:假手术组、假手术 + Ang(1-7) 组、假手术 + A-779 组、假手术 + Ang(1-7) + A-779 组、卵巢切除组、卵巢切除 + Ang(1-7) 组、卵巢切除 + A-779 组和卵巢切除 + Ang(1-7) + A-779 组。在假手术和卵巢切除术(OVX)后八周,皮下植入渗透泵,连续六周输注Ang(1-7)(200 ng/kg/min)、A-779(400 ng/kg/min)或Ang(1-7)与A-779的混合物(分别为200 ng/kg/min和400 ng/kg/min)。在研究开始时以及整个研究期间每周监测并记录所有动物的体重。在治疗期间,维持动物的总体健康状况。治疗结束后,将动物置于代谢笼中禁食16小时,收集尿液样本并冷冻于-70℃。然后,在氯胺酮+赛拉嗪麻醉下通过心脏穿刺采集血液样本,并通过4000 rpm离心获得血清样本。随后将动物断头处死,取出并清洗子宫组织和股骨。去除子宫组织中的脂肪后,直接测定其湿重,并以每100克体重的克数表示。每只大鼠的双侧股骨均被取出并清洗软组织。左侧股骨样本冷冻于−70 °C直至分析,而右侧股骨则保存在10%福尔马林溶液中,用于微型CT和矿物质分析。\n \n\n研究设计和动物分组[2] \n卵巢切除术(OVX)或假手术后,动物被收集8周。然后,将动物分为六组(n = 10),具体如下:第 1 组:假手术组,第 2 组:假手术 + 帽组,第 3 组:假手术 + 帽组 + A-779 组,第 4 组:卵巢切除组,第 5 组:卵巢切除 + 帽组,第 6 组:卵巢切除 + 帽组 + A-779 组。同时,假手术 + 帽组 + A-779 组和卵巢切除 + 帽组 + A-779 组均皮下植入渗透泵(型号 2006,Alzet,Durect 公司,明尼阿波利斯,美国),以 400 ng/kg/min 的输注速率持续 6 周,输送特异性质量受体拮抗剂 (D-Ala7)-血管紧张素 I/II (1–7) 三氟乙酸盐 (A-779)。同时,Sham + Cap、Sham + Cap + A-779、OVX + Cap 和 OVX + Cap + A-779 组开始接受口服卡托普利治疗。卡托普利溶于蒸馏水,以 40 mg kg⁻¹ d⁻¹ 的剂量通过胃管灌注给药,持续 6 周。在治疗期间监测动物的一般健康状况和体重,并每周调整卡托普利的剂量。所有组均在受控的实验条件下饲养(温度 22 ± 1 °C,12/12 小时光照/黑暗循环,湿度 50–55%),并可自由摄取普瑞纳大鼠饲料和水。在第六周的最后一天,将所有组动物置于代谢笼中固定 16 小时,收集尿液样本并保存在 -70 °C 的冰箱中。在氯胺酮和赛拉嗪麻醉下,通过心脏穿刺采集血液,并在4000转/分钟的转速下分离血清样本。随后,取出股骨样本,去除软组织后称重,结果以克为单位表示。左侧股骨样本保存在-70℃直至分析,而右侧股骨样本则保存在10%福尔马林溶液中,用于微型CT和矿物质分析。此外,切除子宫组织,去除脂肪后称重,结果以克/100克最终体重表示。 |
| 参考文献 |
|
| 其他信息 |
局部和全身性肾素-血管紧张素系统(RAS)影响骨骼系统的微观结构和代谢。研究表明,血管紧张素1-7(Ang(1-7))可通过激活Mas受体发挥有益的RAS分子作用。本研究在去卵巢(OVX)骨质疏松症啮齿动物模型中探讨了Ang(1-7)在骨微结构和代谢中的作用。OVX大鼠表现出结构和骨代谢退化,同时血管紧张素转换酶2(ACE-2)/Ang(1-7)/Mas相关组分的表达受到抑制。输注Ang(1-7)显著改善了异常的骨代谢,并显著增强了骨小梁(干骺端)和皮质骨(干骺端-骨干)的形态计量学特征。Ang(1-7)还改善了OVX大鼠的尿液和骨矿物质含量。在卵巢切除(OVX)动物中,输注七肽可增强ACE-2/Mas受体的表达,同时下调血管紧张素II(AngII)、血管紧张素转换酶(ACE)和血管紧张素II 1型受体(AT1R)的表达。此外,Ang(1-7)显著提高了骨保护素(OPG)的水平,并降低了核因子κB受体激活因子配体(RANKL)的表达。用A-779阻断Mas受体后,Ang(1-7)对骨代谢、结构和矿物质的保护作用显著减弱。A-779可消除Ang(1-7)诱导的ACE-2/Ang(1-7)/Mas信号通路和OPG表达的上调,并诱导ACE/AngII/AT1R和RANKL的表达。这些发现首次揭示了Ang(1-7)通过ACE-2/Mas信号通路在骨骼健康和代谢中发挥的新型治疗作用。 [1]
除传统的全身功能外,肾素-血管紧张素系统 (RAS) 的局部作用近期也得到了证实。研究表明,效应分子血管紧张素 II (AngII) 可影响骨骼健康,而抑制血管紧张素转换酶 (ACE-1) 则可维持这些作用。新发现的 Ang1-7 具有多种与 AngII 拮抗的有益作用。因此,本研究利用卵巢切除 (OVX) 大鼠骨质疏松模型,探讨 Ang1-7 通过 G 蛋白偶联 Mas 受体介导 ACEI(卡托普利)的骨骼保护作用。术后 8 周,大鼠口服卡托普利(40 mg/kg/d),同时以 400 ng/kg/min 的速率持续静脉输注特异性 Mas 受体阻滞剂 (A-779) 6 周。检测血清和尿液中的骨代谢标志物。采用电感耦合等离子体质谱法(ICP-MS)定量分析血清、尿液和股骨中的矿物质浓度。利用微型计算机断层扫描(micro-CT)分析右侧远端股骨的骨小梁和皮质形态。最后,测定股骨头中肾素-血管紧张素系统(RAS)肽、酶和受体以及核因子κB受体激活因子配体(RANKL)和骨保护素(OPG)的表达。卵巢切除(OVX)动物表现出明显的骨代谢和矿化改变以及骨微结构紊乱。卡托普利显著恢复了雌激素缺乏大鼠的骨代谢生物标志物,并纠正了尿液和骨骼中的Ca2+和P值。此外,卡托普利还修复了OVX组的骨小梁和皮质形态特征。卡托普利还能改善ACE-2、Ang1-7、Mas和OPG的表达,同时消除卵巢切除术(OVX)诱导的ACE-1、AngII、血管紧张素II受体1型(AT1R)和RANKL的表达上调。A-779对Ang1-7信号通路的抑制显著消除了卡托普利对骨代谢、矿化和微结构的保护作用。A-779还能恢复卵巢切除术对RANKL表达和ACE-1/AngII/AT1R信号通路的影响,并下调OPG表达和ACE-2/Ang1-7/Mas信号通路。与ACE-1抑制剂的骨保护特性临床观察结果一致,局部激活ACE-2/Ang1-7/Mas信号通路和抑制破骨细胞生成似乎是卡托普利骨保护作用的原因,这可能为治疗致残性骨骼和骨骼肌疾病提供潜在的治疗价值。[2] 目的:探讨血管紧张素-(1-7)(Ang-(1-7))在Toll样受体4(TLR4)介导的氧化低密度脂蛋白(ox-LDL)诱导的人脐静脉内皮细胞(HUVECs)氧化应激中的作用及其相关机制。方法:将人脐静脉内皮细胞(HUVECs)进行体外培养,并分为六组:对照组(正常培养基)、ox-LDL组(75 mg/L ox-LDL处理)、ox-LDL+Ang-(1-7)组(1 μmol/L Ang-(1-7)预处理30分钟,再加入75 mg/L ox-LDL)、ox-LDL+Ang-(1-7)+A-779组(1 μmol/L A-779(Mas受体)预处理30分钟,1 μmol/L Ang-(1-7)预处理30分钟,再加入75 mg/L ox-LDL)、ox-LDL+A-779组(1 μmol/L A-779预处理30分钟,再加入75 mg/L ox-LDL)、ox-LDL+ HTA125组(预先用10 μg/L HTA125(TLR4阻断抗体)处理30分钟,然后用75 mg/L ox-LDL干预)。干预24小时后检测相应指标。采用Annexin V-FITC/PI双染流式细胞术和TUNEL法检测细胞凋亡。采用DCFH-DA染色检测氧化应激产物活性氧(ROS)的生成。采用实时逆转录-聚合酶链式反应(RT-PCR)和Western blotting分析分别检测NADPH氧化酶4(NOX4)和TLR4的mRNA和蛋白表达水平。[3] |
| 分子式 |
C39H60N12O11
|
|---|---|
| 分子量 |
872.96700
|
| 精确质量 |
872.45
|
| 元素分析 |
C, 53.66; H, 6.93; N, 19.25; O, 20.16
|
| CAS号 |
159432-28-7
|
| PubChem CID |
10169886
|
| 序列 |
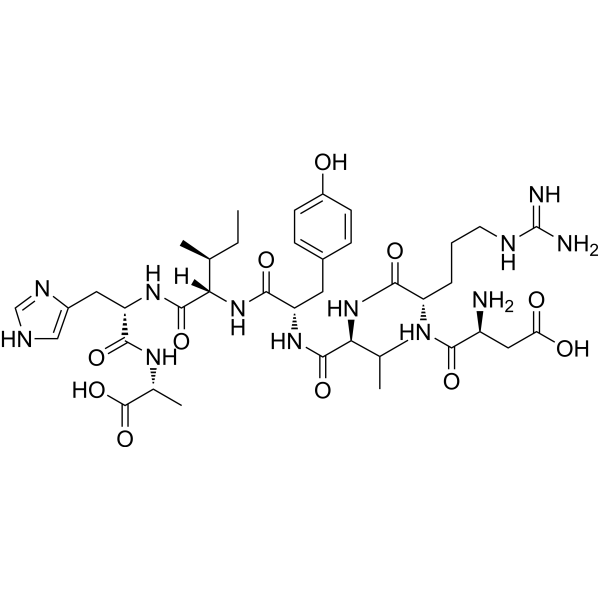
Asp-Arg-Val-Tyr-Ile-His-{d-Ala};
H-Asp-Arg-Val-Tyr-Ile-His-D-Ala-OH;
L-alpha-aspartyl-L-arginyl-L-valyl-L-tyrosyl-L-isoleucyl-L-histidyl-D-alanine
|
| 短序列 |
DRVYIHA; DRVYIH-{d-Ala}
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.5±0.1 g/cm3
|
| 折射率 |
1.651
|
| LogP |
0.3
|
| tPSA |
386.03
|
| 氢键供体(HBD)数目 |
13
|
| 氢键受体(HBA)数目 |
14
|
| 可旋转键数目(RBC) |
26
|
| 重原子数目 |
62
|
| 分子复杂度/Complexity |
1570
|
| 定义原子立体中心数目 |
8
|
| SMILES |
CC[C@H](C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N[C@H](C)C(=O)O)NC(=O)[C@H](CC2=CC=C(C=C2)O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(=O)O)N
|
| InChi Key |
GZSZZUXDAPDPOR-NGIFJXEWSA-N
|
| InChi Code |
InChI=1S/C39H60N12O11/c1-6-20(4)31(37(60)49-28(15-23-17-43-18-45-23)34(57)46-21(5)38(61)62)51-35(58)27(14-22-9-11-24(52)12-10-22)48-36(59)30(19(2)3)50-33(56)26(8-7-13-44-39(41)42)47-32(55)25(40)16-29(53)54/h9-12,17-21,25-28,30-31,52H,6-8,13-16,40H2,1-5H3,(H,43,45)(H,46,57)(H,47,55)(H,48,59)(H,49,60)(H,50,56)(H,51,58)(H,53,54)(H,61,62)(H4,41,42,44)/t20-,21+,25-,26-,27-,28-,30-,31-/m0/s1
|
| 化学名 |
(3S)-3-amino-4-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S,3S)-1-[[(2S)-1-[[(1R)-1-carboxyethyl]amino]-3-(1H-imidazol-5-yl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-oxobutanoic acid
|
| 别名 |
159432-28-7; A 779; (D-Ala7)-Angiotensin I/II (1-7); A-779; CHEMBL4578721; (2R,5S,8S,11S,14S,17S,20S)-5-((1H-imidazol-4-yl)methyl)-20-amino-8-((S)-sec-butyl)-17-(3-guanidinopropyl)-11-(4-hydroxybenzyl)-14-isopropyl-2-methyl-4,7,10,13,16,19-hexaoxo-3,6,9,12,15,18-hexaazadocosanedioic acid; (3S)-3-amino-4-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S,3S)-1-[[(2S)-1-[[(1R)-1-carboxyethyl]amino]-3-(1H-imidazol-5-yl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-oxobutanoic acid; Ang(1-7) D-Ala7;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
0.1 M HCL : 25 mg/mL (~28.64 mM)
H2O : ~5 mg/mL (~5.73 mM) |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.1455 mL | 5.7276 mL | 11.4551 mL | |
| 5 mM | 0.2291 mL | 1.1455 mL | 2.2910 mL | |
| 10 mM | 0.1146 mL | 0.5728 mL | 1.1455 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05786729 | Enrolling by invitation | Other: Aerobic Exercise (AER) Other: Rehabilitation |
Traumatic Brain Injury | Centre for Neuro Skills | January 18, 2022 | Phase 1 Phase 2 |
|
|
|