| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
P2X7 receptor (P2X7R) [1]
P2X7 receptor (P2X7R) [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性: 在表达人P2X7受体(修饰后的P2X7-2N3构建体)的非洲爪蟾卵母细胞中,AZ10606120 抑制ATP诱发电流的pIC50约为7.9(IC50 ~12.6 nM)。该化合物对P2X7R的选择性超过其他P2X受体亚型1000倍以上,在浓度高达10 μM时对P2X1受体无效 [1]。
在人U251胶质母细胞瘤细胞中,使用15 μM AZ10606120 处理72小时,与未处理组相比,肿瘤细胞数量(DAPI+细胞)显著减少(1309 ± 378.3个 vs. 4744 ± 302.4个)。此效果优于50 μM替莫唑胺治疗组(5921 ± 495.1个细胞)。AZ10606120 与替莫唑胺联合给药未观察到协同抗肿瘤效应 [2]。 在患者来源的原代胶质母细胞瘤培养物中,使用15 μM AZ10606120 处理72小时,与未处理组相比,GFAP+/DAPI+肿瘤细胞数量显著减少(114.3 ± 35.9个 vs. 569.1 ± 157个)。使用15 μM或更高浓度的 AZ10606120 处理,可观察到肿瘤细胞数量的显著减少。AZ治疗组与替莫唑胺治疗组之间的细胞数量无统计学显著差异 [2]。 使用15 μM及以上浓度的 AZ10606120 处理原代胶质母细胞瘤培养物72小时,可显著增加培养上清液中乳酸脱氢酶的释放,表明细胞膜受损和细胞毒性。替莫唑胺处理未诱导乳酸脱氢酶释放 [2]。 |
| 体内研究 (In Vivo) |
体内活性: 在链脲佐菌素诱导的1型糖尿病大鼠模型中,腹腔注射AZ10606120(100 μg/kg),每2天一次,持续15天(共7次注射),完全逆转了糖尿病引起的视网膜微血管通透性增加(通过伊文思蓝渗漏测定),并且完全逆转了糖尿病引起的视网膜VEGF积累和IL-6表达增加,但对血糖水平无影响 [3]。
在C57BL/6J小鼠中,通过腹腔注射AZ-10606120(2 mg/kg,在测试前30分钟急性给药)可显著减轻脂多糖诱导的快感缺乏(通过蔗糖偏好测试评估)。急性AZ-10606120的抗快感缺乏效应在P2rx7基因敲除小鼠中完全消失 [4]。 亚急性AZ-10606120治疗(2 mg/kg,腹腔注射,每日1次,连续4天)同样可减轻脂多糖诱导的快感缺乏,且该效应在P2rx7基因敲除小鼠中比野生型小鼠显著减弱 [4]。 |
| 酶活实验 |
酶学实验: 未进行传统的酶学实验。但进行了分子建模和配体对接研究。使用FTsite在人P2X7受体同源模型上无偏倚地搜索潜在结合位点,预测了一个正构位点和一个位于受体顶部亚基间界面的推定变构位点。使用RosettaLigand进行柔性配体对接,扫描整个胞外区,结果显示,对于 AZ10606120,在1000个能量最低的构象中,有60%位于此推定变构位点,表明这是其最可能的结合位点。第二轮针对变构位点的靶向对接确定了两个主要的结合构象簇。最受青睐的对接解决方案显示,P2X7R独特的F88残基以及保守的D92和M105残基排列了 AZ10606120 的芳香族部分,而金刚烷基团则深埋于靠近T94的袋中 [1]。
|
| 细胞实验 |
细胞实验: 对于U251人胶质母细胞瘤细胞系,细胞在添加了丙酮酸钠、青霉素-链霉素、胎牛血清和非必需氨基酸的DMEM培养基中培养。在细胞融合度达到80%时,用 AZ10606120(1, 5, 15, 25 μM)和/或替莫唑胺(50 μM)处理72小时(部分实验处理24和48小时)。处理后,细胞用1:1的丙酮-甲醇溶液固定,细胞核用DAPI在室温下染色1小时。使用荧光显微镜和ImageJ软件,对每个样品的16个随机视野中的DAPI+细胞总数进行量化 [2]。
对于患者来源的原代胶质母细胞瘤培养物,肿瘤样本来自接受常规切除手术的患者。组织用木瓜蛋白酶消化,将细胞接种到涂有多聚-D-赖氨酸的盖玻片上,培养基为添加了D-葡萄糖、L-谷氨酰胺、青霉素-链霉素、胎牛血清和血清添加物的MEM。在细胞融合度达到80%时,用 AZ10606120(1, 5, 15, 25, 50, 100 μM)和/或替莫唑胺(50 μM)处理72小时。随后固定细胞,并与兔抗GFAP一抗在4°C下孵育过夜,然后与Texas Red-X标记的山羊抗兔二抗在室温下孵育2小时。细胞核用DAPI在室温下复染1小时。使用荧光显微镜和ImageJ软件,对每个样品的16个随机视野中的GFAP+/DAPI+细胞总数进行量化 [2]。 对原代胶质母细胞瘤培养物进行了乳酸脱氢酶细胞毒性测定。细胞用 AZ10606120(1, 5, 15, 25, 50, 100 μM)或替莫唑胺(50 μM)处理72小时。然后收集无细胞培养上清液,与乳酸脱氢酶反应混合物在室温下孵育25分钟。使用酶标仪在492 nm处测量吸光度,该吸光度与乳酸脱氢酶水平成正比 [2]。 |
| 动物实验 |
动物实验方案: 对于1型糖尿病大鼠模型:雄性Wistar大鼠(150-180 g)通过单次腹腔注射链脲佐菌素(60 mg/kg)诱导糖尿病。注射链脲佐菌素15天后,大鼠每2天腹腔注射AZ10606120(剂量100 μg/kg)或溶媒,持续15天(共7次注射)。AZ10606120储备液用无菌PBS配制,然后用无菌PBS稀释后给药 [3]。
对于脂多糖诱导的快感缺乏小鼠模型:使用雄性野生型C57BL/6J小鼠(2-3月龄,约30g)。急性处理:在蔗糖偏好测试前30分钟腹腔注射AZ-10606120(2 mg/kg)。亚急性处理:连续4天每天腹腔注射AZ-10606120(2 mg/kg)。脂多糖(0.2 mg/kg或1 mg/kg)腹腔注射用于诱导抑郁样行为 [4]。 |
| 毒性/毒理 (Toxicokinetics/TK) |
在患者来源的原代胶质母细胞瘤培养物中,使用15、25、50和100 μM的 AZ10606120 处理72小时,与未处理组相比,乳酸脱氢酶释放显著增加,表明存在细胞毒性和细胞膜损伤(p值分别为0.01、0.03、0.02和0.015)。随着AZ浓度的增加,乳酸脱氢酶释放呈增加趋势。替莫唑胺处理未促进乳酸脱氢酶释放 [2]。
|
| 参考文献 |
[1]. Unique residues in the ATP gated human P2X7 receptor define a novel allosteric binding pocket for the selective antagonist AZ10606120. Sci Rep. 2017 Apr 7;7(1):725.
[2]. P2X7 receptor antagonism by AZ10606120 significantly reduced in vitro tumour growth in human glioblastoma. Sci Rep. 2023 May 24;13(1):8435. [3]. Pharmacological blockade of the P2X7 receptor reverses retinal damage in a rat model of type 1 diabetes. Acta Diabetol. 2019 Sep;56(9):1031-1036. [4]. Neurochemical Changes in the Mouse Hippocampus Underlying the Antidepressant Effect of Genetic Deletion of P2X7 Receptors. PLoS One. 2013 Jun 21;8(6):e66547. |
| 其他信息 |
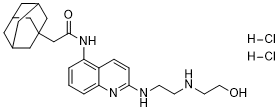
AZ10606120(N-[2-[[2-[(2-羟乙基)氨基]乙基]氨基]-5-喹啉基]-2-三环[3.3.1.13,7]癸-1-基乙酰胺二盐酸盐)是人及大鼠P2X7R的选择性高亲和力拮抗剂,对其他P2X受体亚型几乎没有影响 [1]。
分子动力学模拟表明,P2X7R的独特特征(73-79环插入和T90、T94苏氨酸残基)通过塑造变构口袋的动力学和体积,调控 AZ10606120 进入变构位点的途径。野生型P2X7R变构口袋的平均体积为410 ± 38 ų,而在缺失突变体(301 ± 30 ų)和T90V/T94V突变体(260 ± 33 ų)中,该体积显著减小 [1]。 该研究确定了P2X7受体顶部亚基界面处一个全新的 AZ10606120 变构结合口袋,为合理的药物开发提供了新靶点 [1]。 作者提出,AZ10606120 对P2X7R相对于其他P2X亚型的选择性并非源于与结合口袋中独特氨基酸的直接相互作用,而是间接通过调节变构口袋的动态结构和进入途径实现的,这些特征由P2X7R独特的残基所塑造 [1]。 使用 AZ10606120 拮抗P2X7受体被认为是治疗胶质母细胞瘤的一种潜在的新型有效替代疗法,在U251细胞中显示出优于替莫唑胺的肿瘤细胞杀伤效果 [2]。 AZ10606120是一种小分子P2X7受体拮抗剂。在1型糖尿病大鼠模型中,使用AZ10606120阻断P2X7R可完全逆转视网膜微血管通透性增加、VEGF积累和IL-6表达,表明P2X7R拮抗可能是治疗早期糖尿病视网膜病变微血管改变的一种有前景的策略 [3]。 AZ-10606120是一种有效的P2X7受体拮抗剂。在脂多糖诱导的快感缺乏模型中,急性AZ-10606120治疗显示出比选择性5-羟色胺再摄取抑制剂西酞普兰更高的效价。AZ-10606120的抗抑郁样效应依赖于P2X7受体的表达,因为在P2rx7基因敲除小鼠中该效应消失或减弱 [4]。 |
| 分子式 |
C25H34N4O2
|
|---|---|
| 分子量 |
422.573
|
| 精确质量 |
494.221
|
| 元素分析 |
C, 60.60; H, 7.32; Cl, 14.31; N, 11.31; O, 6.46
|
| CAS号 |
607378-18-7
|
| 相关CAS号 |
607378-18-7 (2HCl); 777851-64-6
|
| PubChem CID |
56972227
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
86.3
|
| 氢键供体(HBD)数目 |
6
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
33
|
| 分子复杂度/Complexity |
585
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
BVFONFUUWORSPO-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C25H34N4O2.2ClH/c30-9-8-26-6-7-27-23-5-4-20-21(28-23)2-1-3-22(20)29-24(31)16-25-13-17-10-18(14-25)12-19(11-17)15-25;;/h1-5,17-19,26,30H,6-16H2,(H,27,28)(H,29,31);2*1H
|
| 化学名 |
2-(1-adamantyl)-N-[2-[2-(2-hydroxyethylamino)ethylamino]quinolin-5-yl]acetamide;dihydrochloride
|
| 别名 |
AZ10606120 2HCl; AZ 10606120 DIHYDROCHLORIDE; AZ-10606120 dihydrochloride; 2-(Adamantan-1-yl)-N-(2-((2-((2-hydroxyethyl)amino)ethyl)amino)quinolin-5-yl)acetamide dihydrochloride; az10606120 2hcl; AZ10606120 dihydrochloride
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~8.33 mg/mL (~16.81 mM)
H2O : ~2 mg/mL (~4.04 mM) |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.3665 mL | 11.8324 mL | 23.6647 mL | |
| 5 mM | 0.4733 mL | 2.3665 mL | 4.7329 mL | |
| 10 mM | 0.2366 mL | 1.1832 mL | 2.3665 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|