| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
HBV/hepatitis B virus
|
|---|---|
| 体外研究 (In Vitro) |
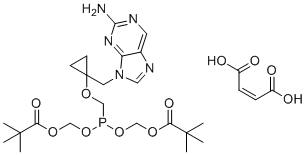
本文介绍了一种新型的膦酸酯核苷, 9-[1-(膦酰甲氧基环丙基)甲基]鸟嘌呤(PMCG,1),具有高效和选择性的抗HBV活性(EC50=0.5μM)。还描述了其口服候选药物9-[1-(膦酰甲氧基环丙基)甲基]-6-脱氧鸟嘌呤酯(贝西福韦酯(PMCDG酯),2)(图1)。
用转染HBV基因组的HepG2 2.2.15细胞评估这些合成化合物的抗HBV活性。如表1所示,1和16是最有效的(EC50=0.5μM)。其他修饰的鸟嘌呤碱类似物也表现出中等至高的抗HBV活性(EC50=1.5-8.0μM),而胸腺嘧啶碱类似物11和6-乙氨基鸟嘌呤类似物14在30μM时没有表现出抗HBV活性。在修饰的鸟嘌呤碱类似物中,8、15和16的抗HBV活性与1相当。化合物8、15和16很可能在细胞内通过氧化或水解转化为1。所有新型膦酸酯核苷类似物都显示出优异的细胞毒性特征,CC50>1.0 mM,在30μM时不会抑制HIV-1和HSV-1的复制[6]。
|
| 体内研究 (In Vivo) |
总之,在2'-位引入环丙基部分以限制无环膦酸酯核苷的构象流动性被证明可以产生高效、特异和选择性的抗HBV活性。口服候选药物贝西福韦酯(PMCDG Dipivoxil)(2)是PMCG(1)的双前体药物,在一项每天5 mg/kg的土拨鼠体内研究中,它大大降低了土拨鼠乙型肝炎病毒(WHBV)的DNA滴度。19候选药物2已成功完成I期,目前正在进行II期临床研究,以评估其对人类的疗效。[6]
口服前药 LB80380(30、60、120 和 240 mg)很快被吸收并转化为母体药物贝西福韦/Besifovir (LB80331)(血浆中未发现 LB80380)。对于Besifovir (LB80331),中位Tmax范围为给药后1.0-2.0小时。此后,血浆中LB80331的浓度呈单指数下降,平均t1/2为2.5-3.3小时。 背景:LB80380是一种在体外和土拨鼠模型中对抗乙型肝炎病毒(HBV)的强效抗病毒药物。它具有出色的临床前安全性,包括比阿德福韦更低的肾毒性。它对野生型和YMDD突变型HBV都有效。LB80380在口服吸收后转化为其母体药物Besifovir (LB80331),并进一步代谢为其活性形式LB80317。 目的/方法:这项LB80380的随机安慰剂对照I/II期临床研究旨在评估其母体药物Besifovir (LB80331)及其活性形式LB80317在29名慢性乙型肝炎e抗原阳性的亚洲成年人中的安全性、抗病毒活性和药代动力学。 结果:每天30、60、120和240毫克的平均最大HBV DNA减少量分别为3.05、4.20、3.67和3.68 log10拷贝/ml。病毒动力学分析表明,每天60mg或更高的剂量对HBV复制有高度的抑制作用。LB80380在所有剂量组均耐受良好,未报告与剂量相关的临床或实验室不良事件。 结论:LB80380是一种有效、安全的HBV抗病毒药物。所有剂量组均观察到明显的HBV DNA抑制。在28天的给药期内,60mg及以上剂量的HBV DNA抑制大致恒定。LB80380的剂量反应将在大型临床研究中进一步评估。[2] |
| 酶活实验 |
评估抗HBV活性和细胞毒性的程序。抗HBV活性。[6]
参考文章13,对上述化合物的抗HBV活性进行了评估。HepG2 2.2.15细胞,即产生乙型肝炎病毒(HBV)的细胞系,在37°C的Dulbecco's Modified Eagle's Medium(DMEM)中培养,DMEM补充了10%胎牛血清、1%抗生素抗真菌剂和400μg/mL Geneticin,并存在5%的CO2。将HepG2 2.2.15细胞以1.5×104个细胞/孔的密度铺在96孔板上,孵育2天。当融合度约为80-90%时,用含有2%FBS、1%ABAM和400μg/mL g 418的新鲜DMEM代替培养基。浓度为100、20、4、0.8、0.16和0μM的合成化合物每隔一天处理一次,持续9天。在第10天,收集培养基,煮沸并连续稀释。使用Rotor Gene 2000通过实时PCR分析样品。扩增引物为HBV2005F(5'-TCA GCT CTG TAT CGG GAA GCC TTA G-3')和HBV212R(5'-CAC CCA CCC AGG TAG CTA GAG TCA-3'),TaqMan探针为5'-6FAM-CCT CAC CAT ACT GCA CTC AGG CAA-BHQ-1-3'。PCR样品在94°C下变性10分钟,然后进行40个循环,94°C 30秒,55°C 30秒内,86°C 30 s。在86°C下检测到荧光,并使用PRISM对数据进行统计分析。 |
| 细胞实验 |
细胞毒性。[6]
在HepG2 2.2.15细胞系中测定每种化合物的50%细胞毒性浓度。在评估抗HBV活性的化合物处理后,96孔板的每个孔用0.5mg/mL的3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四氮唑(MTT)处理,并在37°C下孵育2小时。在培养期结束时,去除培养基,用酸性异丙醇(95%异丙醇中0.05%HCl)溶解转化的染料。在490nm下比色测量代谢的甲赞还原产物。 |
| 动物实验 |
方法:本研究为一项开放标签、单剂量、随机顺序、双药交叉试验,纳入32名韩国男性志愿者。受试者分别接受60 mg和90 mg游离碱LB80380片剂的组合治疗,或183 mg(其中150 mg为游离碱)马来酸LB80380片剂治疗。经过14天的洗脱期后,每位受试者接受另一种制剂治疗。采用经验证的液相色谱串联质谱法测定血浆和尿液中LB80331和LB80317(LB80380的活性代谢物)的浓度。对每位受试者进行安全性评估,包括生命体征、不良事件、心电图和临床实验室检查。[1]
结果:共纳入32名健康受试者,其中26名完成了研究。单次口服马来酸LB80380片剂与马来酸LB80380游离碱片剂相比,在安全性方面未观察到具有临床意义的差异。两种制剂(马来酸制剂与游离碱制剂)中LB80331的Cmax和AUClast几何平均比值的90%置信区间(CI)分别为0.986-1.1240和0.9848-1.0533。LB80317的Cmax和AUClast几何平均比值的90% CI分别为0.8379-0.9696和0.7224-0.9196。[1] 结论:在健康男性受试者中,183 mg马来酸LB80380片剂的药代动力学与60 mg和90 mg游离碱LB80380片剂相当。 |
| 药代性质 (ADME/PK) |
贝西福韦(LB80380)是一种相对较新的口服无环核苷酸膦酸盐。本文综述了LB80380的药代动力学特征,并探讨了其在慢性乙型肝炎病毒感染治疗中的作用。内容包括:LB80380是LB80331和LB80317的前体药物。口服后吸收迅速。贝西福韦剂量递增可使血浆浓度呈线性增加。60mg以上的剂量可有效抑制人体内的乙型肝炎病毒(HBV)。以60mg为例,LB80331在血浆中的最大浓度为397 ng/mL。达到血浆峰浓度所需时间和消除半衰期分别为2.0小时和3.0小时。贝西福韦及其代谢物主要经肾脏排泄。其抗病毒疗效不劣于每日0.5mg恩替卡韦(ETV)。就肾脏和骨骼毒性而言,贝西福韦总体上是安全的。最常见的不良反应是肉碱耗竭,几乎所有服用贝西福韦的患者都会出现这种情况,需要补充肉碱。专家意见:贝西福韦在人体中表现出可预测的药代动力学特征。目前关于贝西福韦的临床研究较少。预计未来将有更多数据,特别是针对特殊人群的数据。应监测长期用药后的不良反应。应开展大规模的头对头试验,比较贝西福韦与现有核苷(酸)类似物(尤其是替诺福韦艾拉酚胺)的疗效。[3]
|
| 毒性/毒理 (Toxicokinetics/TK) |
在整个研究期间,两组患者的总体不良事件发生率无显著差异(表3)。同样,在第48周至第96周期间,BSV-BSV组61例患者(53.5%)和TDF-BSV组57例患者(50.0%)新报告的不良事件数量也无显著差异。BSV-BSV组发生率≥5%的不良事件包括鼻咽炎、消化不良、恶心、背痛、头痛、头晕、疲乏和ALT升高;TDF-BSV组发生率≥5%的不良事件包括鼻咽炎、消化不良、胃炎、腹泻、瘙痒和荨麻疹。BSV组未报告消化不良,而TDF组在最初48周的治疗期间有7例患者(8.33%)发生8次消化不良。尽管研究期间未发生导致死亡的严重不良事件,但在最初的48周治疗期内,BSV组有1例肝细胞癌(HCC)患者,TDF组有2例HCC或肌酸磷酸激酶升高患者停止了研究药物治疗。此外,BSV-BSV组有1例患者发生结核性结肠炎,TDF-BSV组另有1例患者发生原发性血小板增多症,这两例患者均在延长治疗期内停止了研究药物治疗。https://pubmed.ncbi.nlm.nih.gov/30448598/
|
| 参考文献 |
[4]. Efficacy and Safety of Besifovir Dipivoxil Maleate Compared With Tenofovir Disoproxil Fumarate in Treatment of Chronic Hepatitis B Virus Infection. Clin Gastroenterol Hepatol.2018 Nov 15. pii: S1542-3565(18)31244-8;
[5]. Hepatitis B virus: new therapeutic perspectives. Liver Int.2016 Jan;36 Suppl 1:85-92. |
| 其他信息 |
贝西福韦酯是一种口服小分子乙型肝炎病毒(HBV)聚合酶抑制剂。HBV聚合酶是一种催化现有RNA链合成新RNA的酶。贝西福韦酯被认为通过干扰病毒的复制机制来抑制病毒增殖。
另见:贝西福韦(注释已移至此处)。 药物适应症 已研究用于治疗/治疗乙型肝炎(病毒性肝炎)。 作用机制 贝西福韦酯是一种HBV聚合酶抑制剂。它被认为通过干扰病毒的复制机制来抑制病毒增殖。 目前的抗病毒疗法已显著改善了慢性乙型肝炎病毒(HBV)感染患者的长期预后。干扰素(IFN)和核苷(酸)类似物(NA)治疗均已被证实能够减缓慢性乙型肝炎(CHB)患者的肝病进展。然而,持续存在的共价闭合环状DNA(cccDNA)可能导致抗病毒治疗停用后病毒复发。基于对乙型肝炎病毒(HBV)生命周期和病毒-宿主相互作用的广泛研究,目前正在开发多种针对病毒和宿主靶点的新型药物以期治愈HBV。新型聚合酶抑制剂,如替诺福韦艾拉酚胺和贝西福韦,为CHB患者提供了有效且更安全的治疗方案。靶向cccDNA的药物,例如基因工程改造的位点特异性核酸酶和RNA干扰疗法,有望消除cccDNA或抑制cccDNA转录。HBV核衣壳组装抑制剂能够抑制衣壳形成并阻止HBV DNA的合成。HBV进入抑制剂Myrcludex-B已被证实能够有效抑制cccDNA的扩增以及肝内感染的扩散。靶向增强先天性和适应性免疫反应的宿主因子的药物,包括淋巴毒素-β受体激动剂、Toll样受体激动剂、免疫检查点抑制剂和基于腺病毒的治疗性疫苗,可能在清除HBV感染细胞中发挥关键作用。凭借所有这些前景广阔的方法,我们希望在不久的将来实现治愈HBV的最终目标。9-[1-(膦甲氧基环丙基)甲基]鸟嘌呤(PMCG,1)是一类新型膦酸酯核苷的代表,在HepG2 2.2.15细胞原代培养中能以极高的效力(EC50 = 0.5 μM)抑制HBV复制。在浓度高达1.0 mM时,它在多种人类细胞系中均未表现出明显的细胞毒性。在 30 μM 浓度下,该化合物不抑制人类免疫缺陷病毒 (HIV-1) 或单纯疱疹病毒 (HSV-1) 的复制。化合物 1 的许多嘌呤碱基类似物也表现出对乙型肝炎病毒 (HBV) 的抑制活性,但嘧啶类似物在 30 μM 浓度下则不表现出抑制活性。化合物 1 的效力是用作阳性对照的 9-[2-(膦酰甲氧基)乙基]腺嘌呤 (PMEA) 的 4 倍 (EC50 = 2.0 μM)。化合物 1 2' 位上的特征性环丙基部分是通过钛介导的库林科维奇环丙烷化反应制备的。化合物 1 经修饰后得到口服有效的候选药物贝西福韦酯 (PMCDG Dipivoxil) (2)。在一项针对感染土拨鼠乙型肝炎病毒 (WHBV) 的土拨鼠的研究中,化合物 2 以 5 mg/kg/天的剂量给药时表现出优异的疗效。候选药物 2 已成功完成 I 期临床试验,目前正在进行 II 期临床研究以评估其疗效。 |
| 分子式 |
C26H38N5O12P
|
|
|---|---|---|
| 分子量 |
643.579988002777
|
|
| 精确质量 |
643.2254
|
|
| CAS号 |
1039623-01-2
|
|
| 相关CAS号 |
1039623-01-2(Besifovir maleate salt); 441785-26-8; 441785-25-7;
|
|
| PubChem CID |
24864125
|
|
| 外观&性状 |
Typically exists as solid at room temperature
|
|
| tPSA |
242 Ų
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
16
|
|
| 可旋转键数目(RBC) |
17
|
|
| 重原子数目 |
44
|
|
| 分子复杂度/Complexity |
924
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
P(COC1(CN2C=NC3C=NC(N)=NC2=3)CC1)(=O)(OCOC(C(C)(C)C)=O)OCOC(C(C)(C)C)=O.OC(/C=C\C(=O)O)=O
|
|
| InChi Key |
DXUDWHZKSUFXKH-BTJKTKAUSA-N
|
|
| InChi Code |
InChI=1S/C22H34N5O8P.C4H4O4/c1-20(2,3)17(28)31-12-34-36(30,35-13-32-18(29)21(4,5)6)14-33-22(7-8-22)10-27-11-25-15-9-24-19(23)26-16(15)27;5-3(6)1-2-4(7)8/h9,11H,7-8,10,12-14H2,1-6H3,(H2,23,24,26);1-2H,(H,5,6)(H,7,8)/b;2-1-
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5538 mL | 7.7690 mL | 15.5381 mL | |
| 5 mM | 0.3108 mL | 1.5538 mL | 3.1076 mL | |
| 10 mM | 0.1554 mL | 0.7769 mL | 1.5538 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。