| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
NMDA/N-methyl-D-aspartate receptor
|
|---|---|
| 体外研究 (In Vitro) |
在体外,CGP 37849 特异性地、可逆地抑制 NMDA 在海马切片中诱导的 CA1 锥体细胞放电率的上升。 CGP 37849 的浓度高达 10 μM,可抑制 CA1 神经元通过刺激浸泡在低 Mg2+ 培养基中的切片中的 Schaffer 侧副连合纤维而引起的爆发放电 [2]。在不改变初始群体峰值幅度的情况下观察到了这种效应。
CGP 37849和CGP 39551 的受体结合谱[2] CGP 37849对NMDA受体的高亲和力是根据其在粗PSD中NMDA敏感的L-[3H]-谷氨酸结合位点的活性确定的(Foster&Fagg,1987a;Fagg&Baud,1988),随后使用选择性放射性配体[3H]-CPP得到证实(Olverman等人,1986;Murphy等人,1987)。对一系列共膦酰基氨基酸类似物的系统分析表明,CGP 37849是L-[3H]-谷氨酸结合的高效抑制剂,其K类似于L-谷氨酸本身。抑制活性与APPA分子的反式构型有关(与天然存在的顺式异构体无关),与AP5(表1;Evans等人,1982)和其他NMDA受体拮抗剂(Watkins等人,1990)的情况一样,与D-立体异构体(CGP 40116)有关。饱和分析表明,CGP 37849与L-[3H]-谷氨酸结合位点的相互作用具有竞争性;增加阻断剂的浓度不会改变放射性配体标记的最大结合位点数量,但会逐渐降低L-[3H]-谷氨酸对受体的表观亲和力(图2)。CGP 37849抑制选择性NMDA受体拮抗剂[3H]-CPP与大鼠脑PSD的结合,Ki为35 nM(图3和表1),因此分别比拮抗剂CGS 19755、CPP和D-AP5强4、5和7倍。如使用L-[3H]-谷氨酸盐作为放射性配体时观察到的,发现活性基本上只存在于D-异构体中(CGP 40116,Ki 19 nM;表1),其亲和力比L-对映体(CGP 401 17)高出约150倍。乙酯CGP 39551在L-[3H]-谷氨酸盐(K;8.4 pM)和[3H]-CPP结合位点(Ki 0.31 pM)均显示出可测量的抑制活性,但弱于游离酸CGP 37849(表1)。CGP 37849和CGP 39551在18种其他神经递质或调节剂的受体结合试验中均较弱或无活性。在50 pM的浓度下,CGP 37849抑制士的宁不敏感[3H]-甘氨酸结合26+2%,CGP 39551抑制22+2%(平均值+标准误差平均值,n=3)。在剩余的17种受体测定中(见方法),在10pM的测试浓度下,两种化合物的结合抑制率均为20%或更低。因此,CGP 37849对NMDA受体识别位点的选择性比所检查的任何其他位点高出至少300倍[2]。 CGP 37849和CGP 39551的体外神经药理学作用[2] 使用海马切片制备的激动剂-拮抗剂相互作用电生理研究表明,CGP 37849没有表现出兴奋性活性,但在低至0.3 JM的浓度下,可以拮抗亚最大浓度NMDA诱导的CA1锥体细胞放电频率的增加(图4a)。这种效应起效和抵消都很快,并且是激动剂选择性的,因为奎奎特酸酯和红藻氨酸引起的反应不受影响。因此,CGP 37849作为NMDA受体反应拮抗剂的效力和选择性与其从放射性配体结合研究中确定的作用机制非常一致。 CGP 37849和CGP 39551对L-谷氨酸摄取和释放的影响[2] CGP 37849和CGP 39551(见下文)引起的突触功能改变可能不仅仅是由于它们与突触后NMDA受体的相互作用,还可能是由于谷氨酸摄取或释放的改变。在评估这些可能性的实验中,没有观察到化合物的影响。如其他研究人员所示(Davies&Johnston,1976;Johnston等人,1979),大鼠脑突触体以高亲和力(Km 11 pIM)积累L-[3H]-谷氨酸,其摄取受到参考化合物D-天冬氨酸和二氢红藻氨酸的抑制(IC50分别为7 pM和315 pM;平均值,2次单独实验)。然而,在1-10001pm的浓度下,CGP 37849和CGP 39551均未损害L-[3H]-谷氨酸的摄取。例如,在10pM CGP 37849或CGP 39551存在下,L-[3H]-谷氨酸摄取分别为对照值的104%和100%,在1mm药物存在下,分别为102%和106%(平均值,2个单独的实验,每个实验两次)。同样,CGP 37849和CGP 39551均未改变大鼠海马脑片内源性谷氨酸的电诱发释放。在这些实验中,基础谷氨酸释放通常在每部分组织含量的0.2-0.4%范围内,10Hz电场刺激使其增加了2.5+0.2倍。在对照条件下,比值S2/S1(由第二次刺激引发的释放/由第一次刺激诱发的释放)接近于1(1.2),并且该比值不会因在灌流介质中加入10pM CGP 37849(1.1)或CGP 39551(1.0)而改变(平均值,2个单独的实验,每个实验三份)[2]。 癫痫样活动[2] 先前已经证明,刺激浸泡在低Mg2I_培养基中的海马切片中的Schaffer连合侧支纤维会在CAI锥体神经元中引发多个群体尖峰,这让人联想到癫痫样爆发(Coan&Collingridge,1985;Lester等人,1988;见图4b,I)。在浴中施用浓度高达10pM的CGP 37849显著抑制了这种重复射击,但对爆发的第一次种群激增没有影响(图4bii)。这种效应是迅速可逆的,药物洗脱后10分钟内恢复爆裂的控制模式(图4b,iii)。在该实验范式中,CGP 39551也抑制了刺激诱导的突发放电,但比CGP 37849弱(未显示)。 |
| 体内研究 (In Vivo) |
在大鼠大脑中,CGP 37849对 NMDA 敏感的 l-[3H]-谷氨酸与突触后密度 (PSD) 成分的结合表现出强烈的竞争性抑制(Ki 为 220 nM)。选择性 NMDA 受体拮抗剂 [3H]-(±)-3-(2-羧基哌嗪-4-基)丙基-1-膦酸酯 (CPP) 被 CGP 37849 抑制,Ki 为 35 nM[2]。大鼠体内口服 CGP 37849 可以特异性抑制离子电渗 NMDA 引发的海马细胞放电,同时保持对 quilarate 和红藻氨酸的反应不变 [2]。小鼠口服CGP 37849的ED50为21 mg/kg,可预防小鼠电击引起的最大癫痫发作[2]。
在啮齿动物中研究了竞争性NMDA受体拮抗剂CGP 37849和CGP 39551的抗惊厥特性。在最佳预处理时间,CGP 37849抑制了小鼠和大鼠的电击诱导癫痫发作,口服后ED50为8至22mg/kg,静脉注射和腹腔注射后为0.4至2.4mg/kg。与CGP 37849相比,口服后CGP 39551的效力更强(ED50 3.7-8.1 mg/kg),静脉注射或腹腔注射治疗后效力较弱(ED50 2.7-8.7 mg/kg)。口服治疗后,CGP 37849的作用持续时间约为8小时,而CGP 39551在24小时后仍显示出良好的活性(ED50 8.7mg/kg,小鼠;21mg/kg,大鼠)。这两种化合物在低于明显行为副作用的剂量下都是抗惊厥药。CGP 39551在口服10mg/kg及以上的剂量下延迟了大鼠点燃的发展,并对戊四唑诱发的癫痫发作表现出较弱的抗惊厥活性。CGP 37849和CGP 39551是第一个在治疗有效剂量范围内显示出口服抗惊厥特性的竞争性NMDA拮抗剂,因此是人类新型抗癫痫治疗的有趣候选者。[1] 1.CGP 37849(DL-(E)-2-氨基-4-甲基-5-膦酰基-3-戊烯酸;4-甲基-APPA)及其羧乙酯CGP 39551,N-甲基-D-天冬氨酸(NMDA)受体拮抗剂2-氨基-5-膦酰基戊酸酯(AP5)的新型不饱和类似物,在啮齿动物脑中进行了体外和体内评估。2.放射配体结合实验表明,CGP 37849能有效地(Ki 220 nM)和竞争性地抑制NMDA敏感的L-[3H]-谷氨酸与大鼠脑突触后密度(PSD)组分的结合。它抑制选择性NMDA受体拮抗剂[3H]-((+/-)-3-(2-羧基哌嗪-4-基)丙基-1-膦酸酯(CPP)的结合,Ki为35 nM,分别比拮抗剂[+/-)-顺式-4-膦酰基甲基哌啶-2-羧酸(CGS 19755)、CPP和D-AP5强4、5和7倍。抑制活性仅与APPA分子的反式构型和D-立体异构体有关。CGP 39551在NMDA受体识别位点显示出较弱的活性,两种化合物在18个其他受体结合位点都较弱或无活性。CGP 37849和CGP 39551作为L-[3H]-谷氨酸摄入大鼠脑突触体的抑制剂没有活性,对电场刺激引起的大鼠海马脑片内源性谷氨酸的释放没有影响。4.在体外海马切片中,CGP 37849选择性和可逆地拮抗NMDA诱发的CA1锥体细胞放电频率的增加。在浸泡在含有低Mg2+水平的培养基中的切片中,CGP 37849的浓度高达10微M,抑制了通过刺激Schaffer侧支连合纤维在CA1神经元中诱发的突发放电,而不影响初始群体尖峰的幅度;CGP 39551具有相同的效果,但较弱。在体内,对大鼠口服CGP 37849或CGP 39551选择性地阻断了离子介导施加NMDA诱导的海马神经元放电,而不影响对奎司琼或红藻氨酸的反应。5.CGP 37849和CGP 39551分别抑制了ED50为21和4mg kg'-口服的小鼠的最大电击诱导癫痫发作。6.CGP 37849和CGP 39551是强效且竞争性的NMDA受体拮抗剂,在动物口服后显示出显著的中枢作用。因此,它们可能作为阐明NMDA受体在脑功能中作用的工具具有价值,并可能作为治疗人类癫痫和缺血性脑损伤等神经系统疾病的治疗剂。 CGP 37849和CGP 39551的抗惊厥特性[2] 与口服时无效的抗惊厥药AP5、AP7、CPP和CGS 19755相比,CGP 37849在口服给药后以21mgkg-1的ED50抑制了小鼠的最大电击诱导癫痫发作(表1)。与NMDA受体的放射性配体结合研究一致(见上文),发现抗惊厥活性存在于D-立体异构体中(CGP 40116;ED50 7mgkg-1)。然而,与体外研究不同,CGP 37849的乙酯(CGP 39551;ED50 4mgkg-1)比游离酸更有效。CGP 37849和CGP 39551抗惊厥特性的详细信息将在其他地方发表。 CGP 37849和CGP 39551在体内对NMDA诱发反应的拮抗作用[2] 由于CGP 37849和CGP 39551在口服给药后表现出抗惊厥活性,因此从了解其体内作用机制的角度来看,确定它们是否拮抗了此类治疗后的NMDA诱发反应是有意义的。图5显示这是7。6 5-CD a)“EL 3.-1n 2 a确实如此。在比口服抗惊厥药ED50大5-7倍的剂量下,这两种药物都选择性地阻断了海马神经元对离子传递施加的NMDA的反应,而不影响对奎司琼或红藻氨酸(或乙酰胆碱,未显示)的反应。对于CGP 37849,这种效应在给药后30-40分钟开始,75-85分钟后几乎完全阻断NMDA诱发反应。CGP 39551的起效潜伏期更长;口服后80-90分钟首次观察到NMDA反应的明显拮抗作用,110-120分钟后反应基本消除。 在慢性轻度应激抑郁模型中,研究了非竞争性NMDA受体拮抗剂MK-801(地佐西平)和竞争性NMDA-受体拮抗剂CGP 37849(DL-(E)-2-氨基-4-甲基-5-膦酰基-3-戊烯酸)及其(R)-对映体CGP 40116的抗抑郁特性。在该模型中,长时间受到各种轻度应激的动物表现出可口蔗糖溶液消耗的大幅减少(快感缺失)。之前已经证明,慢性轻度应激诱导的快感缺失可以通过各种抗抑郁药物的慢性治疗来逆转。在这项研究中,我们发现,通过MK-801(0.3mg/kg i.p.)、CGP 37849(5mg/kg i.p.)和CGP(25mg/kg p.o.)的慢性(4-5周)治疗,应激诱导的蔗糖摄入不足逐渐得到逆转。这种影响的程度及其时间过程与类似服用丙咪嗪(10mg/kg i.p.或p.o.)后观察到的效果相当。长期服用丙咪嗪和NMDA受体拮抗剂后蔗糖摄入量的增加是应激动物特有的;非应激对照组的行为未受任何测试药物的影响。这些结果证实了之前在“正常”动物身上进行的研究,表明NMDA受体拮抗剂可能具有抗抑郁作用。[3] 在这篇论文中,我们研究了苯二氮卓类受体拮抗剂氟马西尼(Ro 15-1788,10mg/kg)对竞争性N-甲基-D-天冬氨酸(NMDA)受体拮抗剂DL-(E)-2-氨基-4-甲基-5-膦酰基-3-戊烯酸(CGP 37849)和甘氨酸(B)受体部分激动剂1-氨基环丙烷羧酸(ACPC)在大鼠Vogel冲突饮酒试验中的抗冲突活性的影响。还研究了氟马西尼对大鼠CGP 37849的抗焦虑样(在正迷宫试验中)和抗惊厥(在最大电击诱导的癫痫发作中)活性的影响。地西泮被用作参考药物。CGP 37849(2。5-5mg/kg)、ACPC(50-200mg/kg)和地西泮(2.5-5mg/kg)显著且剂量依赖性地增加了冲突饮酒测试实验期间接受的电击次数。氟马西尼部分但显著降低了CGP 37849的抗冲突作用,并完全阻断了ACPC和地西泮的抗冲突效果。CGP 37849(2.5-5mg/kg)和地西泮(2.5-5mg/kg)在+迷宫测试中也表现活跃,因为它们显著增加了在+迷宫开放臂中花费和进入的时间百分比,这两种作用都被氟马西尼拮抗。在冲突饮酒和正迷宫测试中,单独使用氟马西尼都是无效的。在最大电击诱导的癫痫发作中,CGP 37849(2.5-5mg/kg)和地西泮(5-10mg/kg)都产生了抗惊厥作用,其中只有地西泮被氟马西尼拮抗。本研究的结果显示,氟马西尼对CGP 37849和ACPC的抗焦虑样作用具有拮抗作用,这表明苯二氮卓类受体分别参与了NMDA和甘氨酸(B)受体配体的这种活性,这可能是由于NMDA和GABA/苯二氮平系统之间可能的相互作用。苯二氮卓类拮抗剂对CGP 37849的抗惊厥活性没有影响,这表明苯二氮平受体参与NMDA拮抗剂的药理作用并不是一种普遍现象[4]。 |
| 酶活实验 |
NMDA受体测定[2]
如前所述(Foster&Fagg,1987a),从成年雄性Tif:RIAf(SPF)大鼠(180-250g)的大脑中分离出富含突触后密度(PSD)的亚细胞组分。简而言之,通过蔗糖密度梯度离心分离突触质膜,用0.4%Triton X-100处理,进行一次冻融循环,并在0.5 mm HEPES-KOH缓冲液(pH 7.0)中通过再悬浮和离心洗涤4次。所得粗PSD以悬浮液的形式在-800℃下储存,直至测定,此时将其解冻,再次洗涤并重新悬浮在测定缓冲液中。L-[3,4-3H]-谷氨酸(44.1Cimmol-')(Foster&Fagg,1987a)、[1,2-3H]-CPP(20 Ci mmol-1)(Olverman等人,1986;Murphy等人,1987)和[2-3H]-甘氨酸(43.5Cimmol-t)的结合基本上是根据之前发表的程序确定的。将粗PSD的等分试样(40-50pg蛋白质)与放射性配体(50 nM L-[3H]-谷氨酸盐;25 nM[3H]-CPP;20 nM[3H]-甘氨酸)在最终体积为0.5ml 50mM Tris-醋酸盐缓冲液(L-[3H]谷氨酸盐pH 6.9;[3H]-CPP pH 7.8;[3H]甘氨酸pH 7.5)中孵育三次,离心和抽吸上清液后测量膜结合放射性。L-[3H]-谷氨酸盐和[3H]-CPP在32°C下孵育30分钟,[3H]--甘氨酸在4°C下孵化20分钟。在0.5 mM L-谷氨酸盐、0.1 mM CPP或0.5 mM甘氨酸存在下测定非特异性结合,通常分别约为总结合的15%、30%和25%。在添加放射性配体之前,将潜在的抑制剂添加到培养管中。IC50值通过使用在VAX 8600计算机上操作的迭代曲线拟合程序 将数据拟合到逻辑方程来确定,Ki值根据以下关系计算:Ki=IC54/(l+F/Kd),其中F是放射性配体的自由浓度,Kd是其平衡解离常数(Kd值通过图2中所示类型的饱和分析来确定;这里使用的l-[3H]-谷氨酸盐的平均值为250nM,[3H]-CPP的平均值是130nM)。 其他受体[2] 放射受体测定是通过使用之前建立和记录的程序进行的(Foster等人,1981;Honore&Nielsen,1985;Lehmann等人,1988)。使用的检测方法(和放射性配体)如下:奎司琼酸盐(AMPA)、红藻氨酸(红藻氨酸)、GABAA(麝香醇)、苯二氮卓类(氟硝西泮)、GABAB(CGP 27492)、腺苷(环己基腺苷)、毒蕈碱胆碱受体(二氮杂烷和QNB)、xl肾上腺素受体(哌唑嗪)、a2肾上腺素受体(可乐定)、f0肾上腺素受体(二氢阿普洛尔)、5-HT1(5-HT)、5-HT2(酮色林)、组胺H1(多塞平)、组胺H2(噻替丁)、P物质(P物质)和神经降压素(neurotensin)。所有测定均使用标准参考化合物进行验证。运输研究通过Yunger等人(1984)描述的[3H]-GABA摄取方法,对从大鼠脑中分离出的粗突触体(P2)部分对L-[3,4-3H]-谷氨酸盐(52.6 Ci mmol'-;杜邦新英格兰核)的Na+依赖性摄取进行了研究,并进行了细微修改。简而言之,将P2级分(在0.32M蔗糖中以颗粒形式回收)悬浮在0.32M葡萄糖中,并用含有0.1mM异烟肼和L-蛋氨酸硫肟的Krebs-Ringer碳酸氢盐缓冲液(成分单位为mM:NaCl 118,KCI 4.8,CaCl2 2.7,MgSO4 1.2,KH2PO4 1.2,NaHCO3 25,最终葡萄糖浓度8,用02中5%的CO2平衡)稀释,以抑制L-[3H]-谷氨酸的代谢。在加入L-[3H]-谷氨酸盐(最终浓度为1 pM,Km测定除外)之前,将该P2悬浮液的等分试样在37°C下预孵育两次(酌情加入试验化合物)15分钟。“空白”试管在冰上孵育。再继续孵育3分钟,通过快速过滤(0.45 pm孔径)和用冰冷缓冲液洗涤两次来终止孵育。通过液体闪烁计数确定过滤器上保留的放射性。 发射器释放实验[2] 通过对Waldmeier等人(1988)描述的内源性GABA释放方法进行轻微修改,确定了大鼠海马脑片内源性谷氨酸的电诱发释放。将横切切片(约0.36 x 0.36 x 1 mm)悬浮在Krebs-Ringer碳酸氢盐缓冲液中(成分与上述转运研究相同,但CaCl2和D-葡萄糖的最终浓度分别为1.8mm和10mm),在°2中用5%的CO2平衡,并将等分试样转移到组织切片上下带有铂环电极的灌流室中。切片用含有0.5mm二氢红藻氨酸(抑制再摄取)的缓冲液(0.25 ml min-1,37°C)浸泡1小时,然后收集1.25 ml级分进行氨基酸分析。在用邻苯二甲醛进行柱前衍生化后,通过高效液相色谱法(h.p.l.c.)测定超磷酸盐和切片(在每次实验结束时收集)的谷氨酸含量,并将每个部分释放的谷氨酸表示为收集时组织含量的百分比(%分次释放)。先前的研究表明,在该系统中,内源性谷氨酸的诱发释放在2-40Hz范围内是频率依赖性的,并且完全依赖于Ca2f(Thedinga等人,1989)。对于这里描述的实验,在部分3(Sj和9(S2))期间传递了两列单相脉冲(10Hz,20mA,2ms,持续时间2min);第一次刺激总是单独在灌流缓冲液中进行,第二次刺激是在没有或存在测试化合物(20分钟前添加到缓冲液中)的情况下进行的。通过比较药物处理和对照切片中的S2/S1比值来确定药物对诱发释放的影响(Waldmeier等人,1988)。所有实验均一式三份。 电生理研究[2] 如前所述(Olpe&Lynch,1982),对由雄性Tif:RIAf(SPF)大鼠(体重150-200g)制备的横向海马切片(450pm)进行了体外实验。切片在湿润的界面室中稳定,随后在320℃下用生理盐溶液(成分单位为mM:NaCl 124、KCl 2.5、CaCl2 2.5、MgSO4 2、KH2PO4 1.25、NaHCO3 26、D-葡萄糖10;在02中用5%CO2充气)灌注(6 ml min-;相当于每分钟2个室体积)。使用填充有4M NaCl的玻璃微电极从CAI区域的金字塔层区域进行细胞外记录。进行了两个系列的实验:(1)在有和没有测试阻断剂的情况下,以5-10min的间隔施加亚最大浓度(10pM)的NMDA、奎司琼或红藻氨酸,并在图表记录器上绘制单个神经元的放电频率(5-10s区间的动作电位),从而研究激动剂-拮抗剂的相互作用。所有物质均通过灌注系统应用于浸没的海马切片。(2)使用Coan&Collingridge(1985)采用的方法评估了试验药物阻断突触诱发癫痫样活动的能力。通过刺激Schaffer侧支连合纤维(浸没切片),首先在CA1神经元中引发稳定的单群尖峰,然后将灌注介质的Mg2+浓度从2mm降低到标称0.1mm(降低NMDA受体离子通道电压依赖性阻断的条件)。随后的亚最大刺激(频率为0.125 Hz)诱发了群体尖峰的爆发,此前已被证明对NMDA受体拮抗剂的阻断敏感(Coan&Collingridge,1985;Lester等人,1988)。 |
| 动物实验 |
In vivo [2]
Male rats (Tif:RAII(SPF), 280-320g weight) were anaesthetized with chloral hydrate (400mg kg- 1, i.p.) and the tips of four-barrelled micropipettes were stereotaxically positioned in the region of the hippocampal CAI pyramidal neurones. Three barrels of the pipette contained NMDA, quisqualate and kainate (0.01 M, pH 10) and the fourth recording barrel 4 M NaCl. Excitatory amino acids were applied ionophoretically (currents 20-3OnA; adjusted to yield similar response amplitudes) for periods of 20-60s at constant intervals of 2-3min (retaining currents of 20nA were employed between drug applications). The number of action potentials in 5-lOs bins was plotted on a chart recorder, and responses to ionophoretically-applied agonists were monitored for up to 8h. Antagonists were dissolved in physiological saline and were administered cumulatively (3 h intervals) via a canula in the oesophagus. Anticonvulsant evaluation [2] Convulsions in mice were elicited by maximal electroshock (Bernasconi et al., 1986). Brief current pulses (16mA, 50 Hz, 0.2s) were applied via corneal electrodes and the number of animals displaying tonic hind limb extension seizures after saline or drug administration (5 animals per dose group) was determined. Test anticonvulsants were administered orally (via an oesophageal cannula) 2-4h before electroshock. ED50 values (dose which prevented seizures in 50% of animals) were determined by the method of Spearman-Kaerber. CGP 37849 wasdissolved in distilled water [4] Animals [4] The experiments were carried out on male Wistar rats weighing 180–190 g (electroshock-induced seizures test) or 220–250 g (conflict drinking test and elevated plus-maze test). The animals were kept in groups of eight in a cage (60×38×20 cm), at a room temperature of 20±1°C, and had free access to food (standard laboratory pellets) and water before the experiments Conflict drinking test (Vogel test) [4] A modification of the method of Vogel et al. (1971) was used. On the first day of the experiment the rats were adapted to the test chamber for 10 min. It was a plexiglass box (27×27×50 cm), equipped with a grid floor of stainless steel bars and with a drinking bottle containing tapwater. After the initial adaptation period, the animals were deprived of water for 24 h and were then placed in the test chamber for a further 10-min adaptation period during which they had free access to the drinking bottle. Afterwards, they were allowed a 30-min free-drinking session in their home cage. After another 24-h water deprivation period, the rats were placed again in the test chamber and were allowed to drink for 30 sec. Immediately afterwards, drinking attempts were punished with an electric shock (0.5 mA). The impulses were released every 2 sec (timed from the moment when a preceding shock was delivered) between the grid floor and the spout of the drinking bottle. Each shock lasted for 1 sec, and if a rat was drinking when an impulse was released, it received a shock. The number of shocks accepted throughout a 5-min experimental session were recorded. Behavioural responses were recorded by one experimenter unaware of the treatment the rats had received. Elevated plus-maze test [4] The construction and the testing procedure of an elevated plus-maze were based on a method described by Pellow and File (1986). Each rat was placed in the centre of the plus-maze, facing one of the enclosed arms immediately after a 5-min adaptation in a wooden box (60×60×35 cm). During a 5-min test period, two experimenters who were sitting in the same room approximately 1 m from the end of one of the open arms recorded the number of entries into the closed or the open arms, as well as the time spent in each type of arm. An entry with all four feet put into one arm was defined as an arm entry. At the end of each trial the maze was wiped clean. Electroshock-induced seizures [4] Seizures were induced according to the method of Swinyard et al. (1952). Electroshocks were delivered through ear-clip electrodes and were generated by a stimulator which produced an alternating current of 50 Hz and 150 mA for 0.5 sec. Each rat received a single electroshock only. The criterion for the occurrence of seizure activity was tonic extension of the hind limbs. |
| 参考文献 |
|
| 其他信息 |
CGP 37849(或 4-甲基-APPA)是一种新型的 NMDA 优先亚型兴奋性氨基酸受体竞争性拮抗剂,与其羧乙酯(CGP 39551)一起,是首个报道在动物口服给药后显示出显著中枢作用的此类药物。CGP 37849 的 NMDA 受体活性是基于其对大鼠脑 PSD(主要为 NMDA 敏感位点,参见 Foster & Fagg, 1987a; Fagg & Baud, 1988)中 L-[3H]-谷氨酸结合位点的高亲和力而确定的,并使用选择性 NMDA 受体放射性配体 [3H]-CPP 进行了验证(Olverman 等,1986;Murphy 等,1987)。在海马切片制备中,它没有表现出激动剂活性,但在抑制放射性配体与 NMDA 受体识别位点结合的浓度范围内,它拮抗了 NMDA 诱发的神经元放电增加;此外,它抑制 CAI 锥体神经元爆发放电的能力,而不影响快速兴奋性突触后电位 (epsp) 或群体尖峰,这与 NMDA 受体拮抗剂的特性一致,正如其他研究者所建立的那样(Collingridge 等,1983;Coan 和 Collingridge,1985;Lester 等,1988)。 CGP 37849 的选择性体现在其与多种其他神经递质受体结合位点的相互作用可忽略不计,包括奎斯奎酸和红藻氨酸兴奋性受体亚型的结合位点。此外,其在士的宁不敏感的甘氨酸结合位点上的弱活性进一步证实了其在 NMDA 受体上的主要作用位点确实是递质识别位点。体外和体内海马电生理研究也进一步证明了其选择性,结果表明,即使在降低或消除 NMDA 反应的剂量下,CGP 37849 也不会影响神经元对奎斯奎酸或红藻氨酸的反应。CGP 37849 在 [3H]-CPP 结合位点的 Ki 值为 35 nM,因此,与迄今为止报道的任何化合物相比,CGP 37849 对 NMDA 受体识别位点的亲和力和选择性更高。 NMDA 受体拮抗剂已被证明在对多种动物进行中枢或全身(腹腔或静脉)给药后具有抗惊厥活性(参见 Meldrum,1985;Lehmann 等,1987;1988;Patel 等,1988),CGP 37849 的口服疗效最初是通过其预防小鼠最大电休克诱发癫痫发作的能力而发现的;就此而言,其效力(口服ED50为21 mg/kg)与已知的抗惊厥药物相比处于治疗有效剂量范围内(参见Meldrum & Porter,1986),并且通过羧基酯化进一步增强(得到CGP 39551,口服ED50为4 mg/kg)(CGP 37849和CGP 39551的详细抗惊厥特性将在其他地方发表)。这些化合物口服后确实在中枢神经系统中作为NMDA受体拮抗剂发挥作用,这可以从观察到的对映体选择性(D-异构体具有活性,与所有已知的NMDA受体拮抗剂一样;参见Watkins等,1990)得到证实,并通过大鼠海马体内微离子电泳实验得到了更直接的证明。当剂量比其作为抗惊厥药的口服ED50高5-7倍时,这两种化合物均能消除神经元对NMDA的反应,而不影响对奎斯奎酸、红藻氨酸或乙酰胆碱的反应。在这方面,CGP 39551起效较慢。这一观察结果,结合CGP 39551在体外较弱的作用以及目前对NMDA受体构效关系的理解(Fagg & Baud, 1988; Watkins et al., 1990),可能表明酯化化合物在体内作为CGP 37849更易吸收的前药发挥作用。然而,需要确凿的证据来证明这两种物质在体内的前体-产物关系,以验证这一假设。 CGP 37849 和 CGP 39551 是首批报道在动物口服给药后显示出显著中枢效应的竞争性 NMDA 受体拮抗剂,因此有望用于治疗需要急性或慢性给药的人类神经系统疾病。尽管本文篇幅有限,无法对此进行深入探讨,但仍有必要考虑一些在实现这一目标之前必须解决的问题。主要问题集中在 NMDA 受体拮抗剂的治疗窗(达到一定剂量时会出现肌张力丧失;参见 Turski 等,1988)、其可能的致幻作用(基于非竞争性阻滞剂如 PCP 和氯胺酮在人体中的应用经验;参见 Domino 和 Luby,1981;Lodge 等,1988)以及其对学习的潜在不利影响(Morris 等,1986;Collingridge 和 Bliss,1987)。在这方面,最近的证据表明,竞争性 NMDA 受体拮抗剂可能比非竞争性阻滞剂具有显著优势(Meldrum,1985;Ferkany 等人,1988;Leander 等人,1988;France 等人,1989;Tricklebank 等人,1989)。本文描述的新型竞争性 NMDA 受体拮抗剂的研究表明,特别是 CGP 39551,其治疗窗口至少与临床使用的抗惊厥药物一样大(Fagg 等人,1989a;Schmutz 等人,未发表的观察结果),在抗惊厥剂量范围内没有对学习能力的直接损害(Mondadori、Buerki 和 Petschke,未发表),并且没有推广到恒河猴对氯胺酮或 MK801 的辨别刺激效应(France 和 Woods,个人交流)。由于毒理学特性良好,它们因此成为人体临床试验的主要候选药物。[2]
竞争性 N-甲基-D-天冬氨酸 (NMDA) 拮抗剂 DL-2-氨基-4-甲基-5-膦酰基-3-戊烯酸(CAS 127910-31-0,4-甲基-APPA,CGP 37849)及其乙酯(CAS 127910-32-1,CGP 39551)能有效阻断小鼠脊髓神经元原代分离细胞培养物中 NMDA 诱发的全细胞电流,IC50 (+/- SE) 值分别为 189 +/- 9 nmol/l (CGP 37849) 和 2100 +/- 220 nmol/l (CGP 39551)。化合物在口服给药2小时后,以剂量依赖的方式阻断了EL小鼠的前庭刺激诱发的惊厥,其ED50值(95% CI)分别为135 (78-236) μmol/kg (CGP 37849) 和65 (45-94) μmol/kg (CGP 39551)。在雄性瑞士白化小鼠中,被动回避实验的表现也以剂量依赖的方式受损,其ED50值(95% CI)分别为85 (56-157) μmol/kg (CGP 37849) 和27 (18-42) μmol/kg (CGP 39551)。此外,口服CGP 39551 2小时后,这些动物在转棒运动协调性测试中的表现受损,ED50(95% CI)为142(100-201)μmol/kg。这些结果表明,口服这些强效NMDA受体拮抗剂后具有抗惊厥活性,其中CGP 39551的相对效力更高。然而,治疗剂量与诱发记忆或运动障碍的剂量之间的不理想比例,支持了目前普遍的观点,即现有化合物的此类不良反应限制了NMDA受体拮抗剂作为长期治疗药物的应用。[https://pubmed.ncbi.nlm.nih.gov/9893924/] |
| 分子式 |
C6H12NO5P
|
|---|---|
| 分子量 |
209.14
|
| 精确质量 |
209.045
|
| 元素分析 |
C, 34.46; H, 5.78; N, 6.70; O, 38.25; P, 14.81
|
| CAS号 |
127910-31-0
|
| PubChem CID |
5950212
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.506 g/cm3
|
| 沸点 |
523.1ºC at 760 mmHg
|
| 闪点 |
270.2ºC
|
| LogP |
0.222
|
| tPSA |
130.66
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
13
|
| 分子复杂度/Complexity |
268
|
| 定义原子立体中心数目 |
0
|
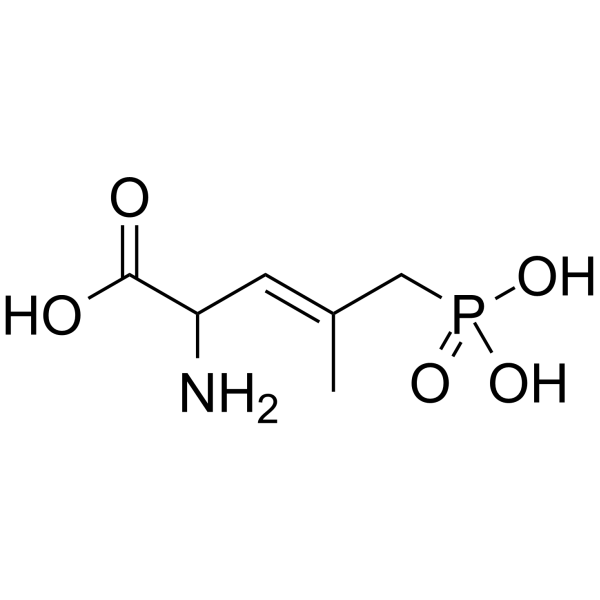
| SMILES |
C/C(=C\C(C(=O)O)N)/CP(=O)(O)O
|
| InChi Key |
BDYHNCZIGYIOGJ-DUXPYHPUSA-N
|
| InChi Code |
InChI=1S/C6H12NO5P/c1-4(3-13(10,11)12)2-5(7)6(8)9/h2,5H,3,7H2,1H3,(H,8,9)(H2,10,11,12)/b4-2+
|
| 化学名 |
(E)-2-amino-4-methyl-5-phosphonopent-3-enoic acid
|
| 别名 |
CGP-37849; CGP 37849; 127910-31-0; Cgp 37,849; Cgp-37,849; (E)-2-amino-4-methyl-5-phosphonopent-3-enoic acid; CGP37,849; 3-Pentenoic acid, 2-amino-4-methyl-5-phosphono-, (3E)-; 76IND1BS43; DTXSID40873634; CGP37849
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.7815 mL | 23.9074 mL | 47.8149 mL | |
| 5 mM | 0.9563 mL | 4.7815 mL | 9.5630 mL | |
| 10 mM | 0.4781 mL | 2.3907 mL | 4.7815 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。