| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Human Endogenous Metabolite
- Histamine exerts biological effects by binding to histamine receptors (H1, H2, H3, H4 receptors)[3] - Histamine induces gastric acid secretion through H2 receptors, which can be blocked by H2 receptor antagonists (e.g., cimetidine) [5] |
|---|---|
| 体外研究 (In Vitro) |
当存在组胺时,培养物中的人类关节软骨细胞增殖更多。许多细胞类型,包括软骨细胞、成纤维细胞、巨噬细胞、内皮细胞、上皮细胞和 T 细胞,在体外暴露于组胺时表现出行为改变。此外,组胺影响许多细胞因子受体的表达以及它们的产生量。组胺受体的表达使组胺能够控制各种细胞功能。组胺在体外刺激组氨酸脱羧酶 (HAC) 产生基质金属蛋白酶 (MMP)-13 和 -3(分别是胶原酶 3 和基质溶素-1)[1]。
- 恶性疟原虫(3D7株)体外培养实验:向培养体系中加入终浓度为0.1 μM、1 μM、5 μM、10 μM的组胺(Histamine),孵育48小时后,通过吉姆萨染色计数受感染红细胞数量。结果显示,组胺呈剂量依赖性抑制恶性疟原虫生长,上述浓度下的抑制率分别为50.2%±4.5%、65.8%±3.8%、78.1%±2.9%、85.3%±2.1% [2] - 人气道平滑肌细胞(HASMC)体外实验:向细胞培养基中加入终浓度为10 μM、50 μM、100 μM的组胺(Histamine),处理24小时后通过CCK-8法检测细胞增殖。结果显示,组胺显著促进HASMC增殖,与对照组相比,增殖率分别提高25.6%±3.2%、42.3%±4.1%、61.5%±5.3%。Western blot分析进一步显示,组胺可上调HASMC中ERK1/2的磷酸化水平 [3] |
| 体内研究 (In Vivo) |
组胺可用于构建动物疾病模型,如胃肠溃疡模型。静脉注射盐酸组胺后,肝脏和肝肿瘤组织中组胺的最大浓度和AUC高于皮下组织[4]
诱发胃肠道溃疡[5] 1) 致病原理 组胺可导致胃酸分泌增加、粘液分泌减少、胰腺反流、胃血流不良,最终导致胃溃疡。压力也会增加胃肠蠕动,使胃褶皱在接触酸时更容易受损 2) 具体方法 豚鼠:雄性•白化•360-420克 给药:5mg/kg•腹腔注射•单次剂量 3) 胃肠道溃疡模型成功构建的指标 溃疡呈点状或细长状。在解剖模型后,在显微镜下测量溃疡指数(病变长度)为3.4mm。 组胺是已知的过敏和炎症反应的贡献者,也是许多生理功能的关键调节因子,如血管生成、血管通透性和细胞增殖[1]。组胺会导致小静脉通透性增加,同时扩张血管系统并促进血液流动。血管内皮钙粘蛋白(VE-cadherin)在内皮细胞连接处的位置变化表明其破坏了小静脉的内皮屏障形成[3] - 小鼠哮喘模型实验:BALB/c小鼠经卵清蛋白(OVA)致敏后,腹腔注射组胺(Histamine),剂量为10 mg/kg,每日1次,连续7天。肺功能检测显示,与对照组相比,组胺使气道阻力(Raw)显著增加85.2%±7.6%,动态顺应性(Cdyn)降低42.1%±5.4%。支气管肺泡灌洗液(BALF)分析显示,组胺使嗜酸性粒细胞数量增加2.3倍,中性粒细胞数量增加1.8倍 [3] - 大鼠药代动力学实验:雄性Sprague-Dawley大鼠单次静脉推注组胺(Histamine),剂量为10 mg/kg。给药后5、15、30、60、120、240分钟采集血样和组织样本(肿瘤组织、肝、肾、肺),通过高效液相色谱(HPLC)检测样本中组胺浓度。结果显示,组胺快速分布至各组织,15分钟时肿瘤组织浓度最高(2.8±0.5 μg/g),为正常肺组织的2.3倍;血浆中组胺的消除半衰期(t1/2)为1.2±0.3小时,清除率(CL)为5.8±1.1 mL/min/kg [4] - 大鼠和犬胃溃疡模型实验:雄性Wistar大鼠皮下注射组胺(Histamine),剂量为50 mg/kg,每日1次,连续3天。处死后解剖胃部,测量溃疡面积,结果显示组胺诱导明显胃溃疡,平均溃疡面积为4.2±0.6 mm²。比格犬静脉注射组胺,剂量为10 mg/kg,诱导十二指肠溃疡,平均溃疡深度为0.8±0.2 mm [5] |
| 细胞实验 |
在 80 cm 2 培养瓶中,使用 10% 胎牛血清 (FCS) 和 Dulbecco 改良 Eagle 培养基 (DMEM) 使细胞生长至汇合。在第一次或第二次传代时,将细胞以大约 2×10 3 细胞/孔的密度接种到 96 孔培养板中。一天后,用 DMEM + 2% FCS(对照)或 DMEM + 2% FCS 加组胺(浓度为 1-100 μmol/l)处理细胞(每次处理至少需要 8 个孔)。每 48 小时更换一次培养基(无论是否含有),六天后计算细胞生长率。
- 恶性疟原虫培养及抑制实验:恶性疟原虫3D7株在含10%人血清、2%红细胞的RPMI 1640培养基中,37°C、5% CO₂条件下培养。当原虫血症达到5%时,向培养体系中加入组胺(Histamine),终浓度分别为0.1 μM、1 μM、5 μM、10 μM,同时设溶剂对照组。孵育48小时后制作薄血涂片,吉姆萨染色,显微镜下计数2000个红细胞,计算原虫血症和抑制率 [2] - 人气道平滑肌细胞(HASMC)培养及增殖实验:从人肺组织中分离HASMC,在含10%胎牛血清的DMEM培养基中,37°C、5% CO₂条件下培养。取对数生长期细胞以5×10³个/孔接种于96孔板,贴壁24小时后换为无血清DMEM,加入组胺(Histamine)至终浓度10 μM、50 μM、100 μM。处理24小时后每孔加入10 μL CCK-8溶液,孵育2小时后检测450 nm处吸光度,计算细胞增殖率。Western blot检测时,用RIPA裂解液裂解细胞,BCA法测定蛋白浓度;等量蛋白经SDS-PAGE分离后转移至PVDF膜,加入p-ERK1/2和ERK1/2一抗孵育,再加入二抗,ECL化学发光显影 [3] |
| 动物实验 |
新西兰成年健康白化兔皮下注射 50、100、200 μg/kg 组胺药 - 小鼠哮喘模型建立及治疗:BALB/c 小鼠(6-8 周龄)于第 0 天和第 7 天腹腔注射 100 μg 卵清蛋白 (OVA) 和 2 mg 氢氧化铝佐剂进行致敏。从第 14 天到第 20 天,小鼠每天腹腔注射一次组胺,剂量为 10 mg/kg。第 21 天,使用小动物肺功能仪检测肺功能。随后处死小鼠,用 0.5 mL 生理盐水冲洗肺部收集支气管肺泡灌洗液 (BALF)。使用血细胞计数器计数支气管肺泡灌洗液 (BALF) 中的炎症细胞数量,并通过 Wright-Giemsa 染色鉴定细胞类型 [3]
- 大鼠药代动力学研究方案:雄性 Sprague-Dawley 大鼠(250-300 g)在实验前禁食 12 小时,可自由饮水。将组胺溶于生理盐水中,配制成 10 mg/mL 的浓度,并以 10 mg/kg 的剂量经尾静脉注射给药。分别于给药后 5、15、30、60、120 和 240 分钟,从眼眶静脉采集 0.5 mL 血液至肝素化试管中,以 3000 rpm 离心 10 分钟分离血浆。在每个时间点处死大鼠,收集肿瘤组织、肝脏、肾脏和肺组织,用生理盐水洗涤,吸干水分,并称重。血浆和组织样本保存于-80°C直至进行高效液相色谱分析[4] - 大鼠和犬胃溃疡模型建立:雄性Wistar大鼠(180-220 g)随机分为对照组和组胺组。组胺组皮下注射组胺(溶于生理盐水),剂量为50 mg/kg,每日一次,连续3天;对照组注射等体积的生理盐水。第4天,处死大鼠,颈椎脱臼,取出胃,灌注10 mL 10%福尔马林溶液,固定30分钟。然后沿胃大弯切开胃壁,用游标卡尺测量溃疡面积。对于体重 8-10 kg 的比格犬,将组胺溶解于生理盐水中,配制成浓度为 5 mg/mL 的溶液,并以 10 mg/kg 的剂量进行静脉注射。24 小时后,处死犬只,解剖十二指肠,并使用带有测微器的显微镜测量溃疡深度 [5] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
肠外给药后易于吸收。 组胺肠外注射后易于吸收…… 各种代谢产物几乎没有或完全没有药理活性,经尿液排泄。 组胺和N-甲基组胺在组织中蓄积。 代谢/代谢物 主要在肝脏代谢。组胺通过甲基化和氧化迅速代谢。甲基化包括环甲基化,并由组胺-N-甲基转移酶催化,生成N-甲基组胺,后者主要转化为N-甲基咪唑乙酸。 2%~3%以游离组胺形式排出,4%~8%以N-甲基组胺形式排出,42%~47%以N-甲基咪唑乙酸形式排出,9%~11%以咪唑乙酸形式排出,16%~23%以咪唑乙酸核苷形式排出。 在人体内,组胺代谢主要有两条途径。其中一条更重要的途径涉及环甲基化,由组胺-N-甲基转移酶(咪唑-N-甲基转移酶,INMT)催化。大部分产物甲基组胺经单胺氧化酶转化为甲基咪唑乙酸(甲基IMAA)。 在另一条途径中,组胺主要在二胺氧化酶(DAO,也称“组胺酶”)催化下发生氧化脱氨反应……产物为咪唑乙酸(IMAA),最终生成其核苷。 ……/大量口服的组胺/会被肠道细菌转化为N-乙酰组胺。 - 吸收:尚未有关于口服组胺吸收的数据报道;在大鼠中静脉注射后,组胺迅速进入全身循环,注射后 5 分钟血浆浓度达到 15.6 ± 2.3 μg/mL [4] - 分布:在大鼠中静脉注射 10 mg/kg 组胺后,组胺迅速分布到各种组织,其中肿瘤组织浓度最高(15 分钟时为 2.8 ± 0.5 μg/g),其次是肝脏(1.9 ± 0.4 μg/g)、肾脏(1.5 ± 0.3 μg/g)和肺(1.2 ± 0.2 μg/g)。肿瘤组织中组胺的组织/血浆浓度比为2.3,表明其优先分布于肿瘤组织[4] - 药代动力学参数:在大鼠中,静脉注射10 mg/kg组胺后,其药代动力学参数如下:消除半衰期(t1/2)= 1.2 ± 0.3 小时,清除率(CL)= 5.8 ± 1.1 mL/min/kg,稳态分布容积(Vdss)= 0.42 ± 0.08 L/kg [4] |
| 毒性/毒理 (Toxicokinetics/TK) |
相互作用
在犬类中,甲胺(强效H2受体拮抗剂)对持续静脉输注组胺(最大有效剂量20 μmol/hr)引起的胃酸分泌的抑制作用在1.5小时后约为20%/10 μmol/kg。在同一项研究中,正常人也观察到了类似的效果。 /H2受体拮抗剂,摘自表格/ 豚鼠即使摄入极小剂量的组胺也会因窒息而死,但如果给予H1受体阻断剂,豚鼠即使摄入一百个致死剂量的组胺也能存活。在同一物种中,H1受体拮抗剂对过敏性支气管痉挛具有显著的保护作用,但对人类却并非如此……/H1受体拮抗剂/ |
| 参考文献 |
[1]. Ann Rheum Dis . 2003 Oct;62(10):991-4. [2]. Asian Pacific Journal of Tropical Medicine. 2010, 3(2): 112-116. [3]. PLoS One . 2015 Jul 9;10(7):e0132367. [4]. Histamine pharmacokinetics in tumor and host tissues after bolus-dose administration in the rat. Life Sci. 2002 Jan 11;70(8):969-76.[5]. Effects of cimetidine, a histamine H2-receptor antagonist, on various experimental gastric and duodenal ulcers. Am J Dig Dis. 1977 Aug;22(8):677-84. |
| 其他信息 |
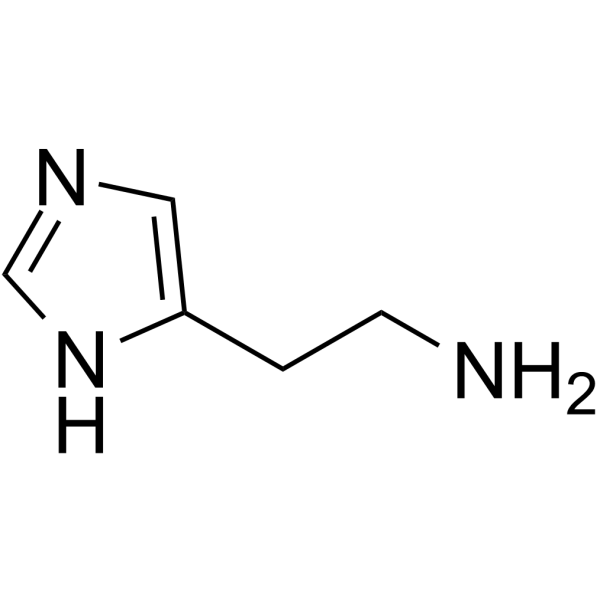
组胺是咪唑类化合物,其结构为1H-咪唑在C-4位被2-氨基乙基取代。它既是人体代谢产物,也是小鼠代谢产物,同时还是一种神经递质。组胺是一种芳烷基氨基化合物,属于咪唑类化合物。它是组胺的共轭碱。
组胺是一种由组氨酸酶促脱羧产生的镇静胺。它是一种强效的胃液分泌刺激剂、支气管平滑肌收缩剂、血管舒张剂,也是一种中枢神经递质。 据报道,组胺存在于白千层、日本商陆以及其他一些有相关数据的生物体中。 组胺是酿酒酵母的代谢产物,或由酿酒酵母产生。 组氨酸酶促脱羧产生的胺。它是一种强效的胃酸分泌刺激剂、支气管平滑肌收缩剂、血管扩张剂,也是一种中枢神经递质。 另见:盐酸组胺(有盐形式);磷酸组胺(有盐形式);氯化乙酰胆碱;组胺;血清素(成分)……查看更多…… 药物适应症 磷酸组胺适用于评估胃酸分泌功能的辅助诊断。 作用机制 组胺直接作用于血管,扩张动脉和毛细血管;这种作用由H1和H2受体介导。毛细血管扩张可引起面部潮红、全身血压下降和胃腺分泌增加,导致高酸性胃液分泌增多。毛细血管扩张伴随毛细血管通透性增加,导致血浆蛋白和液体渗出至细胞外间隙,淋巴液流量和蛋白含量增加,并形成水肿。此外,组胺对平滑肌具有直接的刺激作用,若激活H1受体则引起收缩,若激活H2受体则主要引起舒张。在人体中,组胺的刺激作用可引起肠道肌肉收缩。然而,组胺对子宫、膀胱或胆囊的影响甚微。组胺对十二指肠腺、唾液腺、胰腺、支气管腺和泪腺也具有一定的刺激作用。组胺还能与H3和H4受体结合,分别参与中枢神经系统/周围神经系统的神经递质释放和免疫系统的趋化作用。 ……它能收缩许多平滑肌,例如……支气管和肠道平滑肌,但……也能舒张另一些……细小血管的平滑肌。它是……胃酸分泌的强效刺激物,并能引发……其他外分泌。支气管收缩和肠道收缩……涉及 H1 受体……胃分泌……涉及 H2 受体的激活…… ……在细胞水平上,许多对组胺的反应显然归因于膜通透性的增加,这使得常见的无机离子(主要是阳离子)能够沿着电化学梯度流动并改变跨膜电位。毫无疑问,这解释了组胺对神经末梢或神经节细胞的刺激作用…… ……与细胞水平上的作用基本相似,这似乎可以解释分泌,至少在肾上腺髓质嗜铬细胞中是这样。组胺在此……模拟生理性促分泌剂乙酰胆碱(ACH)使血浆膜去极化。 组胺的作用机制……产生平滑肌松弛(包括血管舒张)的机制尚未明确。 经典的……抗组胺药……只能阻断……H1受体……H2受体……优先被H2受体拮抗剂抑制。 治疗用途 实验用途:在兽医学中,主要用于犬和猪的实验性溃疡诱导,偶尔也用于通过……来确定犬胃中盐酸的分泌状态。 “Diagnox Blue 测试”或“胃肠道测试”…… 实验用途:……曾尝试通过注射组胺来使患者对组胺过敏。但没有实验证据表明此类方案能诱导显著的耐受性……而且该方法尚未被普遍接受。 组胺的实际应用分为两类:第一类是作为诊断剂,其用途大多基于合理的生理学基础;其次,它在治疗中,尤其是在过敏性疾病的治疗中,具有争议性用途。 作为诊断试剂,它在检测胃腺功能方面具有价值。如果注射 0.25-0.5 毫克(通常以 1:1000 溶液形式)后没有胃酸分泌,则存在真正的胃无酸症。 有关组胺(共 10 种)的更多治疗用途(完整)数据,请访问 HSDB 记录页面。 药物警告 /当组胺以 0.1% 至 10% 的浓度局部用于眼部时,会导致/结膜血管扩张和水肿。 药效学 组胺刺激胃腺分泌,导致高酸性胃液分泌增加。这种作用可能主要归因于对壁细胞和主腺细胞的直接作用。 - 类风湿性关节炎 (RA) 患者滑液中的组胺水平显著高于健康对照组(12.5 ± 3.2 ng/mL 对 3.1 ± 0.8 ng/mL)。组胺水平与类风湿关节炎(RA)患者的疾病活动度评分(DAS28)呈正相关(r = 0.68,P < 0.01),提示组胺可能参与RA的发病机制[1]。组胺通过降低寄生红细胞内铁的可用性来抑制恶性疟原虫的生长,因为添加浓度为100 μM的铁离子(Fe³⁺)可逆转组胺的抑制作用(抑制率从85.3%降至32.1%)[2]。在哮喘模型中,组胺的促哮喘作用可被H1受体拮抗剂(氯雷他定,5 mg/kg)预处理阻断,使气道阻力降低62.3%。支气管肺泡灌洗液 (BALF) 中嗜酸性粒细胞计数降低了 58.7%,表明组胺的作用是通过 H1 受体介导的 [3]。组胺通过刺激胃酸分泌诱发胃溃疡和十二指肠溃疡。在大鼠中预先给予西咪替丁(一种 H2 受体拮抗剂)20 mg/kg 剂量,可使组胺诱发的溃疡面积减少 78.5%,证实了 H2 受体在组胺诱发的溃疡中的作用 [5]。 |
| 分子式 |
C5H9N3
|
|---|---|
| 分子量 |
111.1451
|
| 精确质量 |
111.079
|
| 元素分析 |
C, 73.52; H, 7.14; N, 9.03; O, 10.31
|
| CAS号 |
51-45-6
|
| 相关CAS号 |
51-45-6; 56-92-8 (HCl); 51-74-1 (phosphate)
|
| PubChem CID |
774
|
| 外观&性状 |
White to yellow solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
331.0±17.0 °C at 760 mmHg
|
| 熔点 |
83-84ºC
|
| 闪点 |
180.3±8.1 °C
|
| 蒸汽压 |
0.0±0.7 mmHg at 25°C
|
| 折射率 |
1.567
|
| LogP |
-0.92
|
| tPSA |
54.7
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
8
|
| 分子复杂度/Complexity |
64.7
|
| 定义原子立体中心数目 |
0
|
| SMILES |
N1([H])C([H])=NC([H])=C1C([H])([H])C([H])([H])N([H])[H]
|
| InChi Key |
NTYJJOPFIAHURM-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C5H9N3/c6-2-1-5-3-7-4-8-5/h3-4H,1-2,6H2,(H,7,8)
|
| 化学名 |
2-(1H-imidazol-5-yl)ethanamine
|
| 别名 |
LS82-556; LS 82-556; 2-(1H-imidazol-5-yl)ethanamine; 1H-Imidazole-4-ethanamine; Ergamine; Ergotidine; 2-(4-Imidazolyl)ethylamine; 5-Imidazoleethylamine; LS-82-556
|
| HS Tariff Code |
2934.99.03.00
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~22 mg/mL (~197.9 mM)
Water: ~22 mg/mL Ethanol: ~22 mg/mL |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 8.9969 mL | 44.9843 mL | 89.9685 mL | |
| 5 mM | 1.7994 mL | 8.9969 mL | 17.9937 mL | |
| 10 mM | 0.8997 mL | 4.4984 mL | 8.9969 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT00362999 | Active Recruiting |
N/A | Allergic Rhinitis | Children's Mercy Hospital Kansas City |
August 2006 | N/A |
| NCT05131555 | Active Recruiting |
Drug: Placebo: Placebo + exercise training. Drug: H1 blockade: H1 receptor antagonist + exercise training |
Exercise Histamine |
University Ghent | August 16, 2021 | Not Applicable |
| NCT06152497 | Recruiting | Drug: Placebo Behavioral: Resistance training |
Histamine | University Ghent | September 1, 2023 | Not Applicable |
| NCT06154824 | Recruiting | Other: Histamine Other: Cowhage |
Histamine Cowhage |
Aalborg University | December 15, 2023 | Not Applicable |
| NCT06081998 | Recruiting | Other: Histamine Other: Cowhage |
Histamine Cowhage Sleep Deprivation |
Aalborg University | November 1, 2023 | Not Applicable |
|
|
|