| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
Dopamine3 Receptor (D3 receptor)
|
|---|---|
| 体外研究 (In Vitro) |
苯并呋喃(+)-S 14297、苯甲酰胺萘烷酮、氨基茚满U-99194和芳基哌嗪GR 103691已被提出作为多巴胺D3受体与D2受体的“选择性”拮抗剂。在此,我们比较了它们与氨基四氢萘D3拮抗剂(+)-AJ 76和(+)-UH 232的体外亲和力和体内作用。通过使用混合的D2/D3拮抗剂[125I]-碘磺吡啶和优先的D3配体[3H]-(+)-PD 128、907和[3H]--(+)-S 14297,确定重组人(h)D3和/或hD2位点的亲和力。[3H]-(+)-PD 128907、[3H]--(+)-S 14297和[125I]-碘磺吡啶在D3位点产生了基本相同的位移模式,这表明它们识别相同的受体群体。效力的等级顺序(Ki值,单位为nM vs.[3H]-(+)-PD 128907)为GR 103691(0.4),约为萘呋啶(0.5)>氟哌啶醇(2),约等于(+)-UH 232(3),约大于(+)-S 14297(5)>(+)-AJ 76(26)>U-99194(160)。D3受体(标记为[3H]-PD 128907)与D2位点(标记为[125I]-碘磺吡啶)的优先顺序(Ki比,D2:D3)为(+)-S 14297(61),约GR 103691(60)>U-99194(14)>nafadotride(9),约(+)-UH 232(8),近(+)-AJ 76(6)>氟哌啶醇(0.2)。与hD4和hD1位点相比,(+)-S 14297和GR 103691在多巴胺hD3位点也显示出大于100倍的选择性。然而,GR 103691对血清素1A受体(5.8 nM)和α-1肾上腺素受体(12.6 nM)显示出明显的亲和力 [1]。
|
| 体内研究 (In Vivo) |
在体内,除GR 103691外,所有拮抗剂均能通过(+)-PD 128907(0.63 mg/kg皮下注射)和另一种优先的D3激动剂(+)-7-OH-DPAT(0.16 mg/kg皮下注射”)预防低温诱导。另一方面,氟哌啶醇、(+)-AJ 76、(+”-UH 232和那法多嗪均能诱导大鼠出现猝倒,而(+)-S 14297、U-99194和GR 103691则无活性。氟哌啶醇、(+)-AJ 76、(+”-UH 232、萘哌啶和(弱)U-99194也能增强催乳素分泌和纹状体多巴胺合成,而(+)-S 14297和GR 103691则没有活性。然而,尽管GR 103691(0.5mg/kg静脉注射)对5-HT1A受体和α-1肾上腺素受体具有很高的亲和力,这两种受体都存在于中缝定位的5-羟色胺能神经元上,但GR 103691未能影响它们的基础放电率或5-HT1A激动剂(+/-)-8-OH-DPAT(0.005mg/kg静脉注射)抑制它们的电活动,这一结果令人对其体内活性产生怀疑。总之,(+)-S 14297和GR 103691都是明显的选择性配体,可以在体外表征hD3与hD2受体的作用,但(+)-S14297似乎对评估其在体内的功能意义更有用。然而,为了更好地理解多巴胺D3和D2受体各自的作用,我们需要额外的、化学上不同的拮抗剂,以提高效力和选择性[1]。
|
| 酶活实验 |
放射性配体结合分析[2]
放射性配体饱和结合分析[2] 由表达多巴胺D2(25μg)或多巴胺D3受体(10μg)的Sf9细胞制备的膜蛋白在缓冲液2中与不同浓度的[3H]螺旋藻一起孵育,缓冲液2(20 mM HEPES、6 mM MgCl2、1 mM EDTA、1 mM EGTA、0.1%BSA,pH 7.4)在适当的情况下补充了100 mM NaCl或100 mM N-甲基-D-葡糖胺(NMDG)。在4 ml LP4试管(最终体积为1 ml)中进行三次反应,并通过加入膜蛋白启动反应。在(+)-丁卡醇(3μM)存在下测定非特异性结合。反应在25°C下孵育3小时,并使用Brandel细胞采集器通过Whatman玻璃微纤维GF/C过滤器快速过滤终止。用PBS(4°C)洗涤4次3ml后,将滤盘转移到闪烁瓶中,在2ml Ultima Gold™XR闪烁液中浸泡至少6小时,然后通过液体闪烁光谱法测定其放射性。通过减去非特异性结合和游离放射性配体浓度来计算特异性结合,并对计算出的配体耗竭进行校正。使用Prism对数据进行分析,并将其拟合为描述单结合位点模型的双曲线方程。 放射性配体竞争结合分析[2] 将由表达野生型或突变型受体的U-2 OS细胞(2μg)或Sf9细胞(25μg[D2]或10μg[D3])制备的膜蛋白与固定浓度的[3H]螺旋藻(0.25 nM[D2]或1 nM[D3])和一定浓度的竞争配体在补充有二硫苏糖醇(0.1 nM)和100 mM NaCl或100 mM NMDG的缓冲液2中(20 mM HEPES、6 mM MgCl2、1 mM EDTA、1 mM EGTA、0.1%BSA,pH 7.4)孵育。使用(+)-丁卡醇(3μM)代替竞争配体定义非特异性结合。在4 ml LP4试管(1 ml最终体积)[Sf9]或深孔96孔板(400μl最终体积)[U-2 OS]中进行三次反应。在存在(+)-丁卡醇(3μM)的情况下测定非特异性结合,在没有竞争配体的情况下确定总结合。按照“放射性配体饱和结合试验”所述,启动、孵育、终止反应并测量放射性。在减去非特异性结合后,数据以总结合的百分比表示。使用Prism对数据进行分析,并将其拟合为描述单结合位点模型的S形方程。当抑制率<100%时,通过数据外推计算参数。 |
| 细胞实验 |
膜制备[2]
在用磷酸盐缓冲盐水(PBS)洗涤后,通过与Versene孵育将U-2 OS细胞从烧瓶中分离出来。通过离心(200g,10分钟)收集U-2 OS和Sf9细胞,并将其重新悬浮在缓冲液1(20mM HEPES,1mM EDTA,1mM EGTA,pH 7.4,4°C)中。然后使用Ultra Turrax®T25均质器(24000 min-1,4 x 5s)破碎细胞,并通过离心(400g,5 min,4°C)去除细胞碎片。收集所得上清液并离心(47800g,60分钟,4°C)以收集细胞膜。使用Ultra Turrax®T25均质器将膜颗粒重新悬浮在缓冲液1中(6500 min-1,2 x 5s)。使用Lowry蛋白质测定法测定膜制剂的蛋白质浓度,BSA作为参考标准。 |
| 参考文献 |
[1]. Audinot V, et al. A comparative in vitro and in vivo pharmacological characterization of the novel dopamine D3 receptor antagonists (+)-S 14297, nafadotride, GR 103,691 and U 99194. J Pharmacol Exp Ther. 1998 Oct;287(1):187-97.
[2]. Examining the Effects of Sodium Ions on the Binding of Antagonists to Dopamine D2 and D3 Receptors. PLoS One. 2016 Jul 5;11(7):e0158808. |
| 其他信息 |
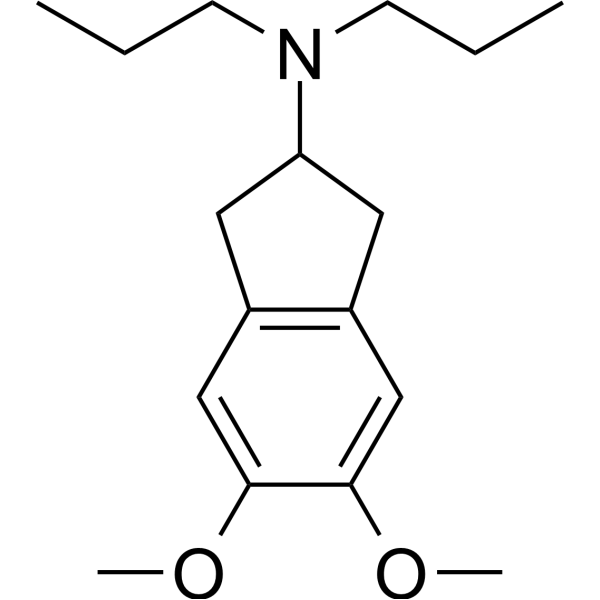
5,6-二甲氧基-N,N-二丙基-2,3-二氢-1H-茚-2-胺是茚满类化合物的一种。
许多G蛋白偶联受体已被证实对钠离子(Na+)敏感。我们利用放射性配体竞争结合实验,检测并比较了钠离子对多种结构不同的配体与人多巴胺D2和多巴胺D3受体亚型结合亲和力的影响。这两种受体是治疗精神疾病的重要靶点。在两种受体上,与使用有机阳离子N-甲基-D-葡糖胺(用于控制离子强度)相比,在钠离子存在下,拮抗剂/反向激动剂SB-277011-A、L,741,626、GR 103691和U 99194的结合亲和力均更高。相反,螺哌隆和(+)-丁氯莫尔的亲和力不受钠离子的影响。有趣的是,拮抗剂/反向激动剂氯氮平的结合受所用缓冲液离子强度变化的影响,而非特定阳离子的存在。两种受体对钠离子的敏感性相似,表明钠离子相互作用对受体构象的影响相似。然而,未观察到配体特性(例如亚型选择性)与钠离子敏感性之间存在明显的关联。因此,决定这种敏感性的性质仍不清楚。然而,这些发现确实强调了在体外实验中仔细考虑检测缓冲液组成以及比较不同研究数据时的重要性,并可能提示在体内配体结合方面需要进一步的控制。[2] |
| 分子式 |
C17H27NO2
|
|---|---|
| 分子量 |
277.4
|
| 精确质量 |
277.204
|
| 元素分析 |
C, 73.61; H, 9.81; N, 5.05; O, 11.54
|
| CAS号 |
82668-33-5
|
| PubChem CID |
5626
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| LogP |
3.293
|
| tPSA |
21.7
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
258
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O(C)C1C(=CC2=C(C=1)CC(C2)N(CCC)CCC)OC
|
| InChi Key |
UOLJKAPABHXFRE-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H27NO2/c1-5-7-18(8-6-2)15-9-13-11-16(19-3)17(20-4)12-14(13)10-15/h11-12,15H,5-10H2,1-4H3
|
| 化学名 |
5,6-dimethoxy-N,N-dipropyl-2,3-dihydro-1H-inden-2-amine
|
| 别名 |
JPC 211; JPC211; 82668-33-5; 1H-Inden-2-amine, 2,3-dihydro-5,6-dimethoxy-N,N-dipropyl-; U-99194; PNU-99194A free base; 5,6-dimethoxy-N,N-dipropyl-2,3-dihydro-1H-inden-2-amine; CHEMBL16410; 929J96FO8T; JPC-211
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.6049 mL | 18.0245 mL | 36.0490 mL | |
| 5 mM | 0.7210 mL | 3.6049 mL | 7.2098 mL | |
| 10 mM | 0.3605 mL | 1.8025 mL | 3.6049 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。