| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HCAR1/hydroxycarboxylic acid receptor 1; Endogenous Metabolite
|
|---|---|
| 体外研究 (In Vitro) |
乳酸和HCAR1靶向在葡萄膜黑色素瘤细胞系中发挥相反的作用
抑制乳酸摄取诱导葡萄膜黑色素瘤生长。
乳酸治疗增加葡萄膜黑色素瘤中HCAR1和乳酸转运蛋白。
乳酸重塑葡萄膜黑色素瘤代谢,增加参与线粒体代谢的基因mRNA水平。
补充乳酸可提高葡萄膜黑色素瘤细胞的常染色质率和静止性[1]。
葡萄膜黑色素瘤(Uveal melanoma, UM)是成人最常见的原发性眼内癌,是预后较差的肿瘤之一。最近,肿瘤代谢物乳酸盐的作用变得越来越有吸引力,因为它作为羟基羧酸受体1 (HCAR1)激活剂,作为诱导赖氨酸残基乳酸化的表观遗传调节剂,当然,作为糖酵解的最终产物,弥合了糖酵解和氧化磷酸化之间的差距。本研究的目的是利用已知的HCAR1和乳酸转运蛋白调节剂,在UM细胞系(92.1)中剖析乳酸作为代谢物或信号分子的作用。我们的研究结果表明,乳酸(20 mM)导致细胞增殖和迁移显著减少,并将细胞代谢转向氧化磷酸化。这些结果与UM细胞的常染色质含量增加和静止相结合。我们进一步在临床环境中发现,乳酸转运体MCT4和HCAR1的增加与UM的纺锤形组织学类型有关。总之,我们的研究结果表明,乳酸代谢可能作为UM进展的预后标记物,并可能作为潜在的治疗靶点。 |
| 体内研究 (In Vivo) |
乳酸通过CD8+ T细胞在多种肿瘤模型中促进抗肿瘤免疫。
乳酸治疗增加肿瘤浸润性CD8+ T细胞。
乳酸治疗增加MC38肿瘤中干细胞样CD8+ T细胞群。
乳酸增加体外扩增过程中TCF-1的表达,减少CD8+ T细胞的凋亡。
乳酸通过表观遗传调控诱导T细胞的干细胞性。
乳酸预处理的CD8+ T细胞过继转移在体内实现了有效的肿瘤生长抑制。[2]
乳酸是葡萄糖分子糖酵解代谢产生的关键代谢物,也是许多细胞类型的主要碳燃料来源。在肿瘤免疫微环境中,乳酸对癌症和免疫细胞的影响可能非常复杂且难以破译,这进一步被糖酵解的副产物酸性质子所混淆。本研究表明,乳酸能够增加CD8+ T细胞的干性,增强抗肿瘤免疫。皮下注射乳酸钠而非葡萄糖对移植MC38肿瘤小鼠产生CD8+ T细胞依赖性肿瘤生长抑制作用。单细胞转录组学分析显示,肿瘤内CD3+细胞中表达CD8+ T细胞的干细胞样tcf -1的比例增加,这一表型通过体外乳酸处理T细胞证实。从机制上讲,乳酸抑制组蛋白去乙酰化酶活性,导致Tcf7超级增强子位点H3K27乙酰化增加,导致Tcf7基因表达增加。体外乳酸预处理的CD8+ T细胞在过继转移到荷瘤小鼠后有效抑制肿瘤生长。我们的研究结果为乳酸在抗肿瘤免疫中的内在作用提供了证据,该作用独立于乳酸的ph依赖效应,并可能推进癌症免疫治疗。[2] |
| 细胞实验 |
细胞增殖的实时监测[1]
xCELLigence实验使用如前所述的实时细胞分析(RTCA)双板(DP)仪器进行。简单地说,通过细胞滴定和生长实验确定了最佳的播种数量。播种至最佳细胞数(3000个/孔)后,分别用乳酸、AZD3965、3,5- dhba和3- oba处理细胞,每15 min自动监测24 h。 药物治疗对细胞迁移的影响[1] 采用创面愈合实验检测细胞迁移。简单地说,细胞在24孔培养皿中播种并培养至融合。在这一阶段,在需要的地方加入乳酸、AZD3965、3,5- dhba或3- oba,并用200 mL微管尖端刮擦细胞培养物。分别于0、24、48 h检测创面闭合情况。利用ImageJ v1.37软件,以不同间隔测量创面未覆盖面积。 免疫细胞化学分析[1]< br > 免疫细胞化学按先前报道进行。简单地说,根据制造商的说明,用200 nM MitoTracker Red CMXRos探针在37°C下对线粒体进行30分钟的染色。细胞在37℃下用染料处理30分钟,30分钟后去除染料。在此阶段,细胞在磷酸盐缓冲盐水(PBS)中洗涤3次,以去除未结合的探针。根据制造商的说明,细胞核用NucBlue染色(每mL两滴),在37℃下染色15分钟。最后,用20 mM乳酸处理细胞。为了获取图像,我们使用了Operetta,将细胞保存在37°C,并在处理后24 h捕获图像。收集的数据用Harmony软件进行分析。 |
| 动物实验 |
肿瘤生长和治疗[2]
在第0天,将1 × 10⁶个MC38肿瘤细胞、1.5 × 10⁵个TC-1肿瘤细胞或1.5 × 10⁵个B16F10肿瘤细胞接种到C57BL/6 J小鼠的右侧腹部。将相同体积(2 mL)的等渗乳酸钠溶液(150 mM,pH 7.4)或葡萄糖溶液(278 mM,pH 7.4)皮下注射到颈部附近的背部皮肤下。对于MC38模型,动物从第8天开始,每天腹腔注射(ip)抗PD-1抗体(10 mg/kg,第7天和第10天),并联合葡萄糖或乳酸钠(皮下注射,分别为5 g/kg或1.68 g/kg)。对于TC-1肿瘤模型,动物从第12天开始,每天腹腔注射(ip)抗PD-1抗体(10 mg/kg,第11天和第14天)或PC7A疫苗(皮下注射0.5 μg E7肽,第11天和第16天),并联合葡萄糖或乳酸钠(皮下注射,分别为5 g/kg或1.68 g/kg)。对于B16F10肿瘤模型,动物从第6天开始,每天腹腔注射(ip)抗PD-1抗体(10 mg/kg,第5天和第8天),并联合葡萄糖或乳酸钠(皮下注射,分别为5 g/kg或1.68 g/kg)。在免疫细胞耗竭试验中,每三天腹腔注射一次抗CD8抗体、抗CD4抗体或抗NK1.1抗体(10 mg/kg)。在MC38肿瘤模型中,为了进行单细胞分析和体内流式细胞术分析,从第15天开始,每天腹腔注射抗PD-1抗体(10 mg/kg,第14天和第17天),并联合或不联合皮下注射乳酸钠(1.68 g/kg)。于第20天收集肿瘤及其引流淋巴结进行分析。使用游标卡尺测量肿瘤的长(L)、宽(W)和高(H),并计算肿瘤体积,公式为:肿瘤体积 = L×W×H/2。当肿瘤体积超过1500 mm³时,判定动物死亡。补充图7b中的体重研究使用了无肿瘤的C57BL/6J小鼠。 肿瘤间质液中乳酸浓度[2] 从新鲜切除的MC38肿瘤中收集肿瘤间质液。将样本在4℃下以300 g离心5分钟,使用70 μm细胞筛。将流出的组织间质液在4℃下以500 g离心5分钟。将上清液速冻后储存于-80℃,待批量分析。使用乳酸检测试剂盒,按照制造商的说明书测定乳酸浓度。 血浆中乳酸浓度[2] 使用K3 EDTA采血管,在不同时间点(乳酸注射后0、0.1、0.5、2、10和24小时)从乳酸处理的小鼠中采集1 mL血液。将血浆中的细胞通过离心(2000 g,4℃,10 分钟)去除。使用 BioProfile® FLEX2 测定血浆中的乳酸浓度。本实验使用无肿瘤的 C57BL/6J 小鼠。 血液 pH 值[2] 在不同时间点(乳酸注射后 0、0.1、2、10 和 24 小时)从乳酸处理的小鼠中采集 1 mL 血液,置于 1.5 mL Eppendorf 管中。采集后立即用 pH 计测量 pH 值。本实验使用无肿瘤的 C57BL/6J 小鼠。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
L-乳酸少量存在于人和动物的血液和肌肉液中;剧烈运动后,这些体液中乳酸的浓度会升高。L-乳酸也存在于肝脏、肾脏、胸腺、人羊水以及其他器官和体液中。 一项使用放射性L-乳酸在人体中进行的预输注研究显示,乳酸的虚拟分布容积为体重的49.4%。乳酸池大小和周转时间分别估计为0.029 g/kg和18.4分钟。 在体内,乳酸的分布与体液总量相当或略少于体液总量。它很容易通过细胞膜扩散,主要通过被动转运;在某些条件下,乳酸分布可能不均匀,或者乳酸池可能由几个具有不同速率常数的较小乳酸池组成。 使用大鼠测量了局部涂抹5% [14C]-乳酸(油包水乳膏)的经皮吸收情况。3天后,50%的涂抹乳酸已渗透皮肤。 有关乳酸(共6个)的更多吸收、分布和排泄(完整)数据,请访问HSDB记录页面。 采用单乳液法制备了平均粒径为75 nm、由聚乳酸(PLA)组成的可生物降解纳米颗粒(NP)。将这些颗粒滴入发情期小鼠的阴道后,它们会逆行穿过子宫颈到达子宫。将纳米颗粒注入阴道后进行的子宫冲洗表明,子宫内诱导产生了RANTES和TNF等促炎信号,这不利于妊娠的建立。这些纳米颗粒正被研究用于避孕。 通过在乳液/蒸发过程中将甲基丙烯酸缩水甘油酯(GMA)接枝共聚到聚乳酸(PLA)纳米颗粒上,制备了罗丹明B(RhB)标记的PLA纳米颗粒。RhB首先通过静电相互作用与十二烷基硫酸钠(SDS)结合形成疏水复合物(SDS-RhB)。由于SDS-RhB与GMA具有高亲和力,亲水性的RhB可以成功地结合到PLA纳米颗粒中。利用荧光显微镜技术研究了巨噬细胞对RhB标记的PLA纳米颗粒的内吞作用。研究了PLA纳米颗粒的表面性质和尺寸对内吞作用的影响。结果表明,粒径小于200 nm的PLA颗粒可以避免被吞噬细胞摄取。与表面修饰聚环氧乙烷-环氧丙烷共聚物(F127)或聚乙烯醇(PVA)的PLA颗粒相比,表面修饰聚乙二醇(PEG)的较大PLA颗粒(300 nm)被巨噬细胞内吞的程度更低。电化学阻抗谱技术揭示了PEG对PLA纳米颗粒的“隐形”作用,即由于其低蛋白吸附性,使其能够避免被巨噬细胞内吞。 黏膜免疫旨在病原体入侵门户诱导强烈的免疫反应。然而,与抗原共同给药的疫苗载体的命运机制仍未完全阐明,这限制了黏膜疫苗的进一步发展。因此,鉴于聚乳酸(PLA)纳米颗粒作为一种用途广泛的疫苗载体,我们分析了这些PLA纳米颗粒在体内和体外肠黏膜吸收过程中的命运,以阐明该过程中涉及的机制。我们首先设计了特异性荧光PLA纳米颗粒,这些纳米颗粒在包封6-香豆素或CellTrace BODIPY后表现出良好的胶体稳定性,然后在小鼠回肠结扎模型中监测其在黏膜中的转运。颗粒的转运过程似乎遵循三个步骤。大多数颗粒首先被黏液捕获。然后,它们仅通过M细胞穿过上皮屏障,最终在派氏淋巴集结(PP)中积聚。最后,我们观察到这些PLA纳米颗粒与PP中的B细胞和树突状细胞(DC)存在特异性相互作用。此外,我们证实,吞噬某些纳米颗粒的树突状细胞(DC)可表现出TLR8+特异性表达。对这两种细胞类型的特异性靶向作用有力地支持了将PLA纳米颗粒用作口服疫苗递送系统。事实上,在小鼠经口灌胃给予PLA纳米颗粒后,我们观察到了相同的生物分布模式,表明这些纳米颗粒能够特异性地到达口服免疫所需的免疫靶点。 代谢/代谢物 ……丙二醇……通过两条途径氧化为乳酸或丙酮酸。这两种代谢物随后被身体用作能量来源,一种是通过三羧酸循环氧化,另一种是通过糖酵解途径生成糖原。 乳酸扩散穿过肌肉组织,并通过血液循环运输到肝脏。在肝脏中,它通过糖异生作用转化为葡萄糖。乳酸还可以在乳酸循环(也称科里循环)中进一步分解代谢。 L-乳酸是大多数哺乳动物细胞和其他生物体(例如细菌)产生的正常代谢中间体;在人类、犬类和大鼠体内,L-乳酸的代谢优先于D-乳酸。乳酸在乳酸脱氢酶的作用下转化为丙酮酸。 在动物体内,厌氧代谢产生的乳酸可以被运输到其他需氧组织,例如肝脏,在那里它可以重新转化为丙酮酸。丙酮酸随后可进一步代谢,重新转化为游离葡萄糖等碳水化合物,或以糖原的形式储存。 有关乳酸(共8种代谢物)的更多代谢/代谢物(完整)数据,请访问HSDB记录页面。 2004年8月,美国食品药品监督管理局(FDA)批准了一种基于聚左旋乳酸(PLLA)的注射式医疗器械,用于恢复和/或矫正人类免疫缺陷病毒感染者面部脂肪流失(脂肪萎缩)的症状。因此,PLLA微粒的特性引起了医学界的广泛关注。聚乳酸在医疗应用中有着悠久的安全使用历史,例如用作钢钉、钢板、螺钉、骨内和软组织植入物,以及作为生物活性化合物缓释载体。聚乳酸的左旋异构体是一种可生物降解、生物相容性好、生物惰性的合成聚合物。推测,PLLA微粒的存在会引起正常的异物反应,从而启动胶原蛋白新生。随着时间的推移,胶原蛋白的积累会在注射部位形成体积,而PLLA微粒则会被代谢成二氧化碳和水,并通过呼吸系统排出体外。/聚左旋乳酸/ 聚乳酸(PLA)于1966年被引入用于可降解外科植入物。水解产物为乳酸,乳酸是碳水化合物代谢的正常中间产物。聚乙醇酸缝合线具有可预测的降解速率,与天然组织的愈合过程相吻合。 生物半衰期 (32)P-磷酸铬-聚左旋乳酸((32)P-CP-PLLA)的平均有效半衰期为11.8天。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
鉴别与用途:乳酸形成黄色至无色晶体或50%的糖浆状液体。它在染色浴中用途广泛,可用作羊毛制品的媒染剂、水不溶性染料的溶剂。它还用于羊毛媒染中还原铬酸盐,以及用于奶酪和糖果的生产。乳酸是婴儿配方奶粉的成分;饮料中的酸化剂;也用于酿造麦芽汁的酸化。它用于制备乳酸钠注射剂,以及作为化妆品成分和杀精凝胶的成分。其他用途:用于酵母生产中去除丁酸梭菌;用于脱毛、丰盈和脱钙皮革;作为甲酸纤维素的溶剂;作为软焊料的助焊剂。乳酸用于生产乳酸盐,乳酸盐用于食品、医药和作为溶剂。它也是一种增塑剂,是酚醛树脂浇铸的催化剂。人体暴露和毒性:其对眼睛的影响与其他中等强度的酸类似,会导致角膜和结膜上皮初期凝固,但如果及时用水冲洗,预后良好。在人类中,意外十二指肠内给予100毫升33%乳酸溶液,12小时内即可致死。高乳酸血症和乳酸性酸中毒是某些核苷类逆转录酶抑制剂治疗期间最危险、最危及生命的副作用之一。乳酸性酸中毒与遗传性和获得性代谢性疾病均相关。在糖异生、无氧糖酵解和酸碱平衡紊乱的情况下,乳酸代谢异常是许多疾病的主要因素。乳酸只能由丙酮酸生成;因此,增加丙酮酸浓度、增强乳酸生成或减少乳酸降解的疾病都会导致乳酸性酸中毒。先天性代谢缺陷伴随葡萄糖、丙酮酸、氨基酸和有机酸代谢途径紊乱,以及促进组织缺氧或线粒体损伤的毒性和全身性疾病,均可导致乳酸性酸中毒。动物实验:以标准方法将乳酸滴眼于兔眼,24小时后的反应评分为8分(1-10分制)。若乳酸溶液(原液和50%水溶液)长时间停留在兔眼上,均可导致角膜坏死和持续性基质瘢痕形成。将雄性大鼠分为若干组,每组5只,分别通过胃管给予0.5 mL浓度为130、650或1300 mg/2000 kg体重的乳酸溶液;对照组给予等体积的生理盐水。650 mg组有2只大鼠,1300 mg组有1只大鼠在给药后24小时内死亡。 8天后,大鼠被给予相同剂量的乳酸。1300 mg组的两只大鼠死亡;这些动物在给药后立即出现呼吸困难、流涕、呕吐和腹胀等症状。在饲料或饮用水中添加约3.6-18 g/kg乳酸,持续喂养猪长达5个月,未观察到明显的毒性反应。醉羊综合征被描述为羔羊D-乳酸酸中毒综合征。在一项发育研究中,12只小鼠在妊娠第6至15天每天灌胃给予570 mg/kg乳酸;13只小鼠作为对照组,给予蒸馏水。所有母鼠均在妊娠第18天处死。试验组和对照组动物的妊娠期体重增加无显著差异,但试验组的采食量显著低于对照组。此外,试验组母鼠的相对肝脏重量也显著低于对照组。对胎儿的唯一观察到的影响是顶骨骨化延迟的统计学显著增加。雌性兔每日两次口服0.1-0.2 g/kg乳酸(溶于100-150 mL水中),持续5个月;另有5只雌性兔每日两次口服0.1-0.7 g/kg乳酸(溶于50-100 mL水中),持续16个月(实际治疗13个月)。分别在5个月和16个月后均未报告肿瘤。使用经代谢活化的鼠伤寒沙门氏菌TA92、TA1535、TA100、TA1537、TA94和TA98菌株,通过Ames试验检测纯度为90.5%的乳酸在磷酸盐缓冲液中的致突变性,结果均为阴性。在未进行代谢活化的情况下,使用源自肺组织的中国仓鼠成纤维细胞克隆亚系,对浓度为 1000 μg/mL、11 mM 的乳酸进行 Ames 试验,结果为阴性。乳酸对染色体畸变的检测结果也为阴性。生态毒性研究:有研究表明,在富含碳水化合物、蛋白质或脂肪的饮食中,喂食 10% 乳酸会导致鸟类出现类似维生素 B1 缺乏的多发性神经炎危象。 鉴定和用途:聚乳酸 (PLA) 是一种生物可吸收聚合物。它应用于工业包装领域或生物相容性/生物可吸收医疗器械市场。PLA 于 1999 年首次在欧洲获准用于软组织填充,以改善疤痕和皱纹的美容效果。在美国,它被用于修复和/或矫正人类免疫缺陷病毒感染者面部脂肪流失(脂肪萎缩)的症状。人体暴露与毒性:2004年8月,美国食品药品监督管理局(FDA)批准了一种基于聚乳酸(PLA)的注射式医疗器械,用于修复和/或矫正人类免疫缺陷病毒(HIV)感染者面部脂肪流失(脂肪萎缩)的症状。因此,PLA微粒的特性引起了医学界的广泛关注。聚乳酸在医疗应用中有着悠久的安全使用历史,例如用作钢钉、钢板、螺钉、骨内和软组织植入物,以及作为生物活性化合物缓释载体。聚乳酸的L-异构体是一种可生物降解、生物相容且生物惰性的合成聚合物。据推测,PLA微粒的存在会引发正常的异物反应,从而启动胶原蛋白新生。随着时间的推移,胶原蛋白的积累会在注射部位形成体积,而PLA微粒则会被代谢为二氧化碳和水,并通过呼吸系统排出体外。已观察到注射聚左旋乳酸(PLA)后可能出现不良反应,主要包括血肿、瘀伤、水肿、不适、炎症和红斑。PLA最常见的不良反应是皮下丘疹的延迟出现,这些丘疹局限于注射部位,通常可触及、无症状且不可见。上市后观察到的不良反应包括:中枢神经系统——疲乏、疗效不佳、不适;皮肤——用药部位分泌物、睑外翻、皮肤肥大、注射部位脓肿、注射部位萎缩、注射部位脂肪萎缩、注射部位肉芽肿、注射部位反应、皮疹、皮肤粗糙、毛细血管扩张、可见结节(伴或不伴炎症或色素沉着异常)。其他不良反应包括:关节疼痛、过敏反应、血管性水肿、指甲脆弱、未另行规定的结肠炎、头发断裂、超敏反应、光敏反应、血管性水肿。动物研究:在大鼠研究中,PLA 具有良好的生物相容性,且所研究的组织对其耐受性良好,并未发现染色体致突变性。在体外培养条件下,使用大鼠上皮细胞研究了不同分子量聚乳酸对细胞增殖的影响。总体而言,PLA 表现出令人满意的生物相容性,但也观察到一些细胞抑制现象。在一些早期动物研究中,观察到 PLA 引起与慢性炎症相关的症状(巨噬细胞、成纤维细胞、巨细胞和淋巴细胞的存在)。这些炎症变化与细菌感染无关。 毒性数据 LC50(大鼠)= 7,940 mg/m3/4hr 相互作用 本研究探讨了局部心肌给药乳酸和低剂量依达拉奉联合用药的效果,以确定该组合是否具有与机械后处理类似的益处。我们将108只大鼠随机分为6组:假手术组、再灌注损伤组、后处理组(Post)、乳酸组(Lac)、低剂量依达拉奉组(Eda)和乳酸+低剂量依达拉奉组(Lac+Eda)。在给药前,将大鼠的左冠状动脉闭塞45分钟。在不同时间点处死大鼠,以检测梗死面积、心肌损伤和细胞凋亡的血清标志物以及信号通路标志物的表达。我们发现,缺血再灌注损伤引起的梗死面积在后处理和乳酸+依达拉奉注射后显著减少;血清心肌损伤标志物、细胞凋亡标志物和血流动力学参数也观察到类似的趋势。与后处理组相比,乳酸+依达拉奉组的血液pH值、活性氧水平、线粒体吸收值和信号通路标志物水平均相似。乳酸组和依达拉奉组部分模拟了这种保护作用。这些数据表明,局部心肌注射乳酸和低剂量依达拉奉可启动机械后处理的保护性信号通路,并复制心肌保护作用。 通过呼气和汗液排出的二氧化碳和L-乳酸为蚊子提供嗅觉信号,使其能够找到并叮咬人类;然而,不同种类的蚊子在这方面存在差异。本研究在实验室条件下,探究了亚洲重要的疟疾媒介——斯氏按蚊(迈索尔型)对二氧化碳和L-乳酸的逆风响应。结果表明,最低剂量的二氧化碳(90 ppm)即可激活蚊子,而10倍剂量的二氧化碳则会抑制其活动。单独使用L-乳酸并未产生显著效果,但当以6 μg/min的速率向90至410 ppm的二氧化碳溶液中添加L-乳酸时,蚊子会受到吸引。这些结果进一步支持了二氧化碳在嗜动物性蚊子的宿主寻找行为中发挥重要作用的假设,并提示L-乳酸在吸引斯氏按蚊方面可能比二氧化碳更为关键。 在肺水肿期……由于低氧血症导致乳酸生成增加,可能会发生代谢性酸中毒。 /NO2诱发的急性肺损伤/ 灼烧感和/或刺痛感是患者使用局部疗法治疗皮肤病时最常反映的问题之一。局部乳酸制剂常用于治疗干燥脱屑的皮肤。本研究比较了受试者在使用含锶的10%乳酸乳膏、12%乳酸铵乳液和鲸蜡硬脂醇乳液后报告的灼烧/刺痛程度。含锶的10%乳酸乳膏和鲸蜡硬脂醇乳液的平均灼烧/刺痛评分低于12%乳酸铵乳液(P<0.0001)。根据研究结果,含锶的10%乳酸乳膏比12%乳酸铵乳液引起的灼烧/刺痛感更轻。 有关乳酸(共6种)的更多相互作用(完整)数据,请访问HSDB记录页面。 一种新型环保抗菌包装的开发,是通过在聚乳酸(PLA)薄膜表面经电晕放电活化后涂覆月桂酸精氨酸酯(LAE)制成的。基于扫描电子显微镜(SEM)的分析证实了LAE成功涂覆在PLA表面。不同LAE涂覆量(0%至2.6%[w/w])的LAE/PLA薄膜的机械性能与纯PLA薄膜基本相同。通过改良的琼脂扩散定性试验和JIS Z 2801:2000定量方法,证实了LAE/PLA薄膜对单核细胞增生李斯特菌和鼠伤寒沙门氏菌(S. typhimurium)的抗菌活性。以LAE/PLA薄膜作为熟制腌制火腿的食品接触抗菌包装模型系统,结果表明,当需要高透明度时,在PLA上涂覆0.07% (w/w) LAE涂层可有效抑制火腿上的单核细胞增生李斯特菌和鼠伤寒沙门氏菌。储存7天后,每层薄膜上的病原菌生长量降低了2至3个对数单位,证实了这一点。然而,当LAE涂层含量达到2.6% (w/w)时,抗菌活性更强,但成品透明度有所降低。本文展示了如何利用电晕放电法在聚乳酸(PLA)表面涂覆激光辅助电晕放电(LAE)涂层,从而简便地开发出具有高效抗菌活性的功能性绿色食品包装。实际应用:本文验证了一种创新型抗菌LAE涂层PLA薄膜对食源性病原体的有效性。重要的是,LAE涂层PLA薄膜的制备可在现有薄膜生产线上进行定制。 注射类产品作为手术的替代方案,用于逆转面部衰老迹象,这种做法越来越受欢迎。2012年,美国进行了近500万例注射治疗。由于作用机制互补,玻尿酸(HA)、羟基磷灰石钙(CaHA)和聚左旋乳酸(PLLA)等容量填充产品通常与其他产品以及神经毒素联合使用,用于面部年轻化。本文介绍了两例病例报告,涉及两种不同的透明质酸(HA)产品(注射用聚左旋乳酸(PLLA)和钙化透明质酸(CaHA))与A型肉毒杆菌毒素(incobotulinumtoxinA或abobotulinumtoxinA)的患者特异性组合。HA、CaHA、PLLA和神经毒素的联合应用为许多患者带来了显著的疗效,且未发现联合治疗导致不良事件增加的临床证据。/聚左旋乳酸/ 可降解聚合物基材料在骨科和牙科领域具有吸引力,可作为金属植入物替代骨固定材料。本文将可降解聚合物聚乳酸(PLA)与新型碳纳米管(CNT)-磷酸钙(CP)混合纳米粉末结合,用于此应用。具体而言,我们利用离子修饰碳纳米管(mCNTs)溶液制备了CNTs-CP杂化纳米粉体(CNTs含量分别为0.1%和0.25%)。该mCNTs溶液经过特殊合成,具有良好的分散性,能够有效地吸附在CP纳米颗粒上。随后,我们将mCNTs-CP杂化纳米粉体与PLA(含量最高达50%)混合,制备了mCNTs-CP-PLA纳米复合材料。添加mCNTs-CP杂化纳米粉体显著提高了纳米复合材料的机械拉伸强度。此外,低浓度mCNTs(0.1%)的纳米复合材料在基因和蛋白质表达方面表现出显著的生物学效应,包括细胞增殖和成骨细胞分化。基于这项研究,将新型mCNT-CP杂化纳米粉末添加到PLA生物聚合物中,可被视为开发硬组织植入物的一种新型材料选择。 采用生物可吸收材料制成的临时性心血管支架装置可能减少晚期支架血栓形成。将一种含有磷酰胆碱基团的水溶性两亲性磷脂聚合物(PMB30W)与高分子量聚乳酸(PLLA)混合,以减少表面不良的组织反应。将PLLA植入物和聚合物混合物(PLLA/PMB30W)植入物分别植入大鼠皮下组织、大鼠肾下腹主动脉和兔颈内动脉。皮下植入6个月后,PLLA/PMB30W表面仍保持高密度的磷酰胆碱基团,且未发生明显的生物吸收。血管内植入后,对直径小于1.6 mm的聚合物管的横截面积进行组织形态计量学测量。与PLLA管相比,PLLA/PMB30W管在植入30天内显著减少了血栓形成。将人外周血单核细胞培养于PLLA和PLLA/PMB30W管上,以比较炎症反应。酶联免疫吸附试验(ELISA)定量分析显示,PLLA/PMB30W组中促炎细胞因子水平显著降低。它们与阴性对照组的水平几乎相同。因此,我们得出结论,磷酸胆碱基团能够显著降低体内和体外的组织反应,PLLA/PMB30W 是一种很有前景的用于制备临时性心血管支架装置的材料。 非人类毒性值 大鼠口服LD50:3730 mg/kg 豚鼠口服LD50:1810 mg/kg 小鼠皮下注射LD50:4500 mg/kg 小鼠口服LD50:4875 mg/kg 大鼠吸入LC50:7.94 mg/L/4 hr |
| 参考文献 | |
| 其他信息 |
乳酸是一种无色至淡黄色、无味的粘稠液体,对金属和组织具有腐蚀性。它用于生产发酵乳制品、作为食品防腐剂以及制造化学品。
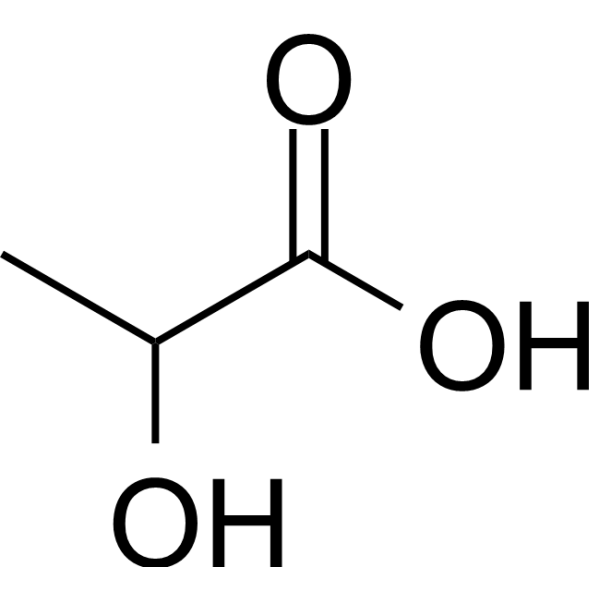
2-羟基丙酸是一种2-羟基单羧酸,它是丙酸中一个α-氢被羟基取代的产物。它是大型蚤(Daphnia magna)和藻类的代谢产物,在功能上与丙酸相关,并且是乳酸的共轭酸。 它是糖发酵(氧化、代谢)过程中的正常中间体。浓缩形式用于内服,以防止胃肠道发酵。(引自Stedman,第26版)乳酸钠是乳酸的钠盐,具有淡淡的咸味。乳酸是通过糖源(例如玉米或甜菜)发酵,然后中和生成的乳酸,得到分子式为NaC3H5O3的化合物而制成的。乳酸是Phexxi的活性成分之一,Phexxi是一种非激素避孕药,于2020年5月获得FDA批准。 据报道,果蝇、接骨木和其他一些有相关数据的生物体中都含有乳酸。 DL-乳酸是乳酸的消旋异构体,乳酸是人体内具有生物活性的同分异构体。乳酸或乳酸盐是在丙酮酸经乳酸脱氢酶发酵过程中产生的。该反应除了产生乳酸外,还会产生烟酰胺腺嘌呤二核苷酸(NAD),NAD随后用于糖酵解,生成能量来源三磷酸腺苷(ATP)。 它是糖发酵(氧化、代谢)过程中的正常中间产物。浓缩形式用于内服以防止胃肠道发酵。(摘自Stedman,第26版) 药物适应症 用作碱化剂。 作用机制 乳酸根离子最终代谢为二氧化碳和水,此过程需要消耗氢离子。 治疗用途 /临床试验/ ClinicalTrials.gov 是一个注册库和结果数据库,收录了全球范围内由公共和私人机构资助的人体临床研究。该网站由美国国家医学图书馆 (NLM) 和美国国立卫生研究院 (NIH) 维护。ClinicalTrials.gov 上的每条记录都提供了研究方案的概要信息,包括以下内容:疾病或病症;干预措施(例如,正在研究的医疗产品、行为或程序);研究标题、描述和设计;参与要求(资格标准);研究开展地点;研究地点的联系信息;以及其他健康网站的相关信息链接,例如美国国家医学图书馆 (NLM) 的 MedlinePlus(用于患者健康信息)和 PubMed(用于医学领域学术文章的引文和摘要)。数据库中包含乳酸。 (兽医):曾用作腐蚀剂,稀释后用于冲洗组织;用作肠道防腐剂和抗发酵剂。 10% 的溶液用作新生儿皮肤的杀菌剂。……16.7% 的溶液溶于柔性火棉胶中,用于去除疣和小的皮肤肿瘤。 酸化剂 缓释制剂;人工膜;牙科植入物;药物输送系统 用于恢复和/或矫正人类免疫缺陷病毒感染者面部脂肪流失(脂肪萎缩)的症状。 探索性治疗 我们报告了一例使用注射用聚左旋乳酸 (PLLA) 为一位45岁白人女性进行面部容量恢复的病例,该患者对其手部外观感到担忧。患者希望获得长期改善,并选择注射用PLLA,因为其已知疗效可持续2年,尽管她被告知注射用PLLA尚未获得FDA批准用于手部。将注射用PLLA与8 mL稀释剂和利多卡因混合后,将0.1-0.2 mL的等分试剂注射到选定的部位,每只手最多注射5 mL。患者接受了三次相同的治疗,注射后使用保湿霜并进行按摩;患者注意到在第二次和第三次治疗之间外观有所改善。矫正效果至少维持了18个月,未发生不良事件。我们还简要回顾了关于注射用聚左旋乳酸(PLLA)用于手部容量恢复的文献。/聚左旋乳酸/ 面部衰老的特征包括软组织萎缩、皮肤弹性丧失导致面部皮肤松弛以及面部软组织因重力作用下垂或上睑下垂。聚左旋乳酸(PLLA)是一种合成的可生物降解聚合物,它通过刺激炎症组织反应并随后促进胶原蛋白沉积来填充软组织。该论文讨论了面部衰老的特殊性,描述了一种正在接受美国食品药品监督管理局(FDA)批准的新型PLLA填充剂的作用机制和适应症……并详细介绍了该产品一项为期两年的非适应症试点研究的结果。在该产品接受FDA批准用于美容用途的试点研究期间,共有106名患者接受了PLLA的非适应症治疗。所有患者均接受了为期两年的随访,以帮助制定注射技术方案。本系列研究的患者年龄范围为40至78岁。其中男性3例,女性103例。患者平均每次接受1.6瓶注射,平均疗程2.3次,以达到泪沟、中面部、颧部、鼻唇沟、下颌前区、下颌缘和下颌角的容量填充。该研究实现了100%的随访率,患者满意度为99.1%。至少两年的随访期内,结节形成率为4.7%。由于其独特的作用机制,聚乳酸(PLLA)用于非手术面部年轻化需要精细的注射技术,并特别注意优化治疗效果和最大限度减少不良反应。聚左旋乳酸 如需了解聚左旋乳酸(共17种)的更多治疗用途(完整)数据,请访问HSDB记录页面。 药物警告 对于治疗区域或附近存在活动性皮肤炎症或感染的患者,应推迟使用聚左旋乳酸,直至炎症或感染得到控制。聚左旋乳酸应注射于真皮深层或皮下组织。避免浅表注射。在皮肤较薄的区域使用聚左旋乳酸时,应格外小心。聚左旋乳酸在眼周区域的治疗安全性和有效性尚未确定。 请勿过度矫正(过度填充)轮廓缺陷,因为随着聚左旋乳酸治疗效果的显现,凹陷会在几周内逐渐改善。 /聚左旋乳酸/ 有关聚乳酸(共16条)的更多药物警告(完整)数据,请访问HSDB记录页面。 药效学 乳酸产生代谢碱化作用。 |
| 分子式 |
C3H6O3
|
|---|---|
| 分子量 |
90.0779
|
| 精确质量 |
90.031
|
| CAS号 |
50-21-5
|
| 相关CAS号 |
Lactate calcium;814-80-2;Lactate sodium;72-17-3;Lactate potassium;996-31-6
|
| PubChem CID |
612
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
227.6±0.0 °C at 760 mmHg
|
| 熔点 |
18ºC
|
| 闪点 |
109.9±16.3 °C
|
| 蒸汽压 |
0.0±1.0 mmHg at 25°C
|
| 折射率 |
1.451
|
| LogP |
-0.7
|
| tPSA |
57.53
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
6
|
| 分子复杂度/Complexity |
59.1
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O([H])C([H])(C(=O)O[H])C([H])([H])[H]
|
| InChi Key |
JVTAAEKCZFNVCJ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C3H6O3/c1-2(4)3(5)6/h2,4H,1H3,(H,5,6)
|
| 化学名 |
2-hydroxypropanoic acid
|
| 别名 |
lactic acid; 2-hydroxypropanoic acid; DL-Lactic acid; 50-21-5; 2-hydroxypropionic acid; lactate; Milk acid; Tonsillosan
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~100 mg/mL (~1110.12 mM)
DMSO : ~100 mg/mL (~1110.12 mM) |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 11.1012 mL | 55.5062 mL | 111.0124 mL | |
| 5 mM | 2.2202 mL | 11.1012 mL | 22.2025 mL | |
| 10 mM | 1.1101 mL | 5.5506 mL | 11.1012 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。