| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
5-HT3 Receptor (IC50 = 0.33 nM)
|
|---|---|
| 体外研究 (In Vitro) |
在培养的大鼠皮质细胞中,当用贝司琼 (MDL7222) 阻断 5-HT3 受体时,过氧化氢诱导的神经毒性会减轻。在 1 μM 和 5 μM 浓度下,Bemisetron(0.01、0.1 和 1 μM,15 小时)和 Y25130(0.05、0.5 和 5 μM)分别将 H2O2 诱导的 MTT 还原降低 74.9±2.4 和 79.0 ±2.5%(浓度) -依赖。是最大影响,按此顺序 [2]。 Bemisetron (1 μM)、Y25130 (5 μM) 或 MK-801 (10 μM) 预处理 20 分钟可显着(但不是完全)降低 H2O2 引起的 [Ca2+]c 升高 [2]。使用贝司琼(1 μM,15 小时)可以显着阻断 H2O2 诱导的 caspase-3 免疫反应性升高 [2]。
本研究旨在使用培养的大鼠皮质神经元,研究5-羟色胺(5-HT)(3)受体拮抗剂对过氧化氢(H(2)O(2))诱导的神经毒性的神经保护作用。5-羟色胺(3)受体拮抗剂曲帕尼-3,5-二氯苯甲酸酯(MDL72222,0.1和1微M)和N-(1-氮杂二环[2.2.2.]辛-3-基)-6-氯-4-乙基-3-氧代-3,4-二氢-2H-1,4-苯并恶嗪-8-甲酰胺盐酸盐(Y25130,0.5和5微M)的预处理显著抑制了H(2)O(2)(100微M)诱导的神经元细胞死亡,如MTT法所评估的,并通过Hoechst 33342染色证明了凋亡核的数量。MDL72222(1微M)和Y25130(5微M)的保护作用被同时用100微M的5-羟色胺(3)受体激动剂1-苯基双胍治疗完全阻断,表明这些化合物的保护作用是由于5-羟色胺(4)受体阻断。此外,MDL72222(1微M)和Y25130(5微M)抑制了H(2)O(2)(100微M)诱导的细胞质Ca(2+)浓度升高([Ca(2+)](c))和谷氨酸释放、活性氧(ROS)的产生和半胱氨酸天冬氨酸蛋白酶-3活性。这些结果表明,5-HT(3)受体的激活可能部分参与了H(2)O(2)诱导的神经毒性,通过Ca(2+)内流的膜去极化。因此,MDL72222和Y25130阻断5-HT(3)受体可能通过干扰[Ca(2+)](c)的增加,进而抑制谷氨酸释放、ROS产生和半胱氨酸天冬氨酸蛋白酶-3活性来改善H(2)O(2)诱导的神经毒性[2]。 |
| 体内研究 (In Vivo) |
雄性成年白化小鼠腹腔注射贝美司琼,剂量为0.1、1和10 mg/kg。最低剂量的僵直症没有显着变化。另一方面,10 mg/kg 显着增加了这种发生率(从氟哌啶醇给药后 60 分钟起),而贝美司琼(1 mg/kg)显着降低了僵直症的发生率(从氟哌啶醇给药后 90 分钟起)。 )。给予氟哌啶醇后,最大的增效作用(约是对照值的4.5倍)在60分钟时出现,对僵直症的最大抑制作用(约75%)在120分钟后出现[3]。
典型的抗精神病药物(如氟哌啶醇)可以通过阻断纹状体DA受体在啮齿动物中诱导癫痫状态。研究表明,影响中枢5-羟色胺能(5-HTerg)机制的药物可以改变神经抑制剂诱导的嗜睡,这表明多巴胺能的传递是在5-HTerg的调节下进行的。本研究的目的是研究贝美司琼和格拉司琼这两种选择性5-羟色胺3受体拮抗剂对小鼠这种猝倒症的影响。用氟哌啶醇(1.5mg/kg,i.p.)诱导过敏反应,并通过棒试验以30分钟的间隔进行测量。在氟哌啶醇前20分钟腹腔注射药物(或生理盐水,作为对照),每只动物只使用一次。贝美司琼在1mg/kg的剂量下显著减轻了猝倒,而10mg/kg的剂量则加剧了这一现象,发现0.1mg/kg的剂量没有效果。格拉司琼在0.04和0.1mg/kg的剂量下抑制了猝倒,而4mg/kg的拮抗剂显著延长了猝倒的持续时间。这些数据表明,5-HT3受体在抗精神病药物诱导的猝倒中起作用。考虑到这两种拮抗剂对5-HT3受体的高度亲和力,人们很容易推测,高剂量的拮抗剂对痉挛的增强是由于非5-HT3受体机制[3]。 |
| 细胞实验 |
细胞活力测定 [2]
细胞类型: 原代皮层神经元细胞 测试浓度: 0.01-1 μM 孵育时间: 20 分钟(预处理); 15 小时(孵育后) 实验结果:H2O2 诱导的 MTT 还原减少呈浓度依赖性减少,在 1 μM 时显示为 74.9±2.4%,这是最大值影响。 蛋白质印迹分析[2] 细胞类型: 原代皮质神经元细胞 测试浓度: 1 μM 孵育持续时间: 15 小时 实验结果: 显着阻断 H2O2 诱导的 caspase-3 免疫反应性增加。 |
| 动物实验 |
动物/疾病模型: 雄性成年白化小鼠,体重 26-36 g[3]
剂量: 0.1-10 mg/kg 给药途径: 腹腔注射 (ip),20 分钟(预处理)+ 180 分钟(治疗) 实验结果: 剂量 1 mg/kg 时可明显减轻僵直症状,10 mg/kg 时可增强此现象,而 0.1 mg/kg 时无作用。 |
| 毒性/毒理 (Toxicokinetics/TK) |
大鼠静脉注射LD50为14 mg/kg,美国专利文献编号:4563465;小鼠口服LD50为90 mg/kg,美国专利文献编号:4563465;小鼠腹腔注射LD50为32 mg/kg,美国专利文献编号:4563465;小鼠静脉注射LD50为24 mg/kg,美国专利文献编号:4563465
|
| 参考文献 |
[1]. Peters JA, et al. An electrophysiological investigation of the properties of 5-HT3 receptors of rabbit nodose ganglion neurones in culture. Br J Pharmacol. 1993 Oct;110(2):665-76.
[2]. Lee HJ, et al. Blockade of 5-HT(3) receptor with MDL7222 and Y25130 reduces hydrogen peroxide-induced neurotoxicity in cultured rat cortical cells. Life Sci. 2005 Dec 5;78(3):294-300. [3]. Silva SR, et al. Effects of 5-HT3 receptor antagonists on neuroleptic-induced catalepsy in mice. Neuropharmacology. 1995 Jan;34(1):97-9. |
| 其他信息 |
1. 本研究采用膜片钳技术的全细胞和膜片钳外侧记录模式,测定了培养的兔结状神经节神经元中5-羟色胺(5-HT)诱发电流的生物物理和药理学特性。2. 在所研究的细胞中,49%的细胞在负钳制电位下灌注10⁻⁵ M 5-HT后诱发了内向电流。5-HT的全细胞反应在约-2 mV处发生反转(E5-HT),并表现出内向整流特性。3. 不同离子替代对E5-HT的影响表明,5-HT诱发的电流主要由Na⁺、K⁺混合阳离子电导介导,Cl⁻离子的贡献很小或几乎没有。从细胞外液中去除Ca²⁺和Mg²⁺可增强5-HT诱发电流的幅度。 4. 在离体膜片钳实验中,灌注10⁻⁶ M 5-HT可诱导单通道电流,在-70 mV时弦电导约为17 pS,在-100至-40 mV范围内平均斜率电导为19 pS。5-HT诱导的单通道表现出轻微的内向整流特性,其频率可被5-HT₃受体拮抗剂甲氧氯普胺(10⁻⁶ M)降低,但幅度不受影响。5. 在-60 mV电压钳制下,向全细胞灌注5-HT(3 × 10⁻⁷至3 × 10⁻⁵ M)可产生剂量依赖性的内向电流,该电流可被2-甲基-5-HT和1-苯基双胍模拟,二者相对于5-HT的等效摩尔比分别为2.5和32。 6. 局部施加 5-HT (10(-5) M) 引起的全细胞内向电流不受 10(-6) M 美西麦角、10(-6) M 酮色林或 10(-6) M 西酞普兰的影响,但可被选择性 5-HT3 受体拮抗剂托吡司琼 (IC50 = 4.6 x 10(-11) M)、昂丹司琼 (IC50 = 5.7 x 10(-11) M) 和贝美司琼 (IC50 = 3.3 x 10(-10) M) 浓度依赖性地拮抗。非选择性拮抗剂甲氧氯普胺(IC50 = 1.2 x 10(-8) M)、可卡因(IC50 = 8.3 x 10(-8) M)和(+)-筒箭毒碱(IC50 = 1.6 x 10(-7) M)也能阻断 5-HT 的反应。[1]
|
| 分子式 |
C15H17CL2NO2
|
|---|---|
| 分子量 |
314.206
|
| 精确质量 |
313.064
|
| 元素分析 |
C, 57.34; H, 5.45; Cl, 22.56; N, 4.46; O, 10.18
|
| CAS号 |
40796-97-2
|
| PubChem CID |
671690
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.344g/cm3
|
| 沸点 |
406.507ºC at 760 mmHg
|
| 闪点 |
199.648ºC
|
| 折射率 |
1.597
|
| LogP |
3.713
|
| tPSA |
29.54
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
355
|
| 定义原子立体中心数目 |
2
|
| SMILES |
O=C(O[C@@H]1C[C@@H](N2C)CC[C@@H]2C1)C3=CC(Cl)=CC(Cl)=C3
|
| InChi Key |
MNJNPLVXBISNSX-PBWFPOADSA-N
|
| InChi Code |
InChI=1S/C15H17Cl2NO2/c1-18-12-2-3-13(18)8-14(7-12)20-15(19)9-4-10(16)6-11(17)5-9/h4-6,12-14H,2-3,7-8H2,1H3/t12-,13+,14?
|
| 化学名 |
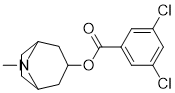
[(1S,5R)-8-methyl-8-azabicyclo[3.2.1]octan-3-yl] 3,5-dichlorobenzoate
|
| 别名 |
MDL72222; MDL-72222; BEMESETRON; 40796-97-2; 3-Tropanyl-3,5-dichlorobenzoate; MDL 72222; MDL-72222; MDL 72,222; Bemesetron (MDL 72222); CHEMBL1365455; MDL 72222
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~2 mg/mL (~6.37 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.1826 mL | 15.9129 mL | 31.8258 mL | |
| 5 mM | 0.6365 mL | 3.1826 mL | 6.3652 mL | |
| 10 mM | 0.3183 mL | 1.5913 mL | 3.1826 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。