| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Mitochondrial (mitochondria)-targeted redox cycling agent
|
|---|---|
| 体外研究 (In Vitro) |
MitoPQ由带电线粒体积累[1]
为了增强线粒体中超氧化物的产生,新开发的化合物必须在基质内迅速积累,以响应膜电位(图1)。因此,我们接下来测量了带电线粒体对它们的摄取(图5)。在与MitoPQ和TPMP一起孵育后,线粒体被制成丸状,并通过RP-HPLC进行评估,显示MitoPQ与TPMP均被广泛摄取,解偶联剂FCCP降低了摄取量(图5A)。为了量化摄取,我们还测量了累积比(ACR),即线粒体和上清液中化合物的相对量。最终淘汰管理计划和MitoPQ都有大量的ACRs,FCCP会降低这些ACRs(图5B)。以同样的方式对其他化合物进行评估表明,DMV、DBipy和TPP共轭衍生物Mito(C10)Bipy都是通过带电线粒体积累的(图5B)。有趣的是,虽然MitoPQ和Mito(C10)Bipy被吸收,但MitoPQC4和Mito。 MitoPQ刺激分离线粒体产生过氧化氢[1] 接下来,我们研究了被通电线粒体吸收的化合物是否可以启动基质内的氧化还原循环。MitoPQ显著增加了心脏线粒体中超氧化物歧化产物过氧化氢的产生(图6A)。当该分析扩展到其他化合物时,结果表明,正如预期的那样,类似浓度的PQ是无效的,DBipy是唯一一种增加过氧化氢流出的化合物,尽管其程度小于MitoPQ(图S1)。因此,MitoPQ是迄今为止分离线粒体产生过氧化氢最有效的物质,这可能是由于其膜电位依赖性积累(图5)和复合物I的氧化还原循环(图4)。因此,我们专注于通过MitoPQ进一步表征ROS的产生。 MitoPQ在诱导分离线粒体产生过氧化氢方面比PQ强几百倍(图6B),并且通过阻止FCCP摄取MitoPQ来消除这种过氧化氢的产生(图6C)。为了更直接地评估线粒体内MitoPQ的超氧化物形成,我们测量了超氧化物敏感基质酶乌头酶的失活。MitoPQ在降低乌头酶活性方面比PQ强几百倍(图6D),FCCP可以防止这种失活(图6E)。接下来,我们监测了过氧化物酶3(Prdx3)的单体和二聚体形式的相对量。这种线粒体基质抗氧化酶清除过氧化氢形成二硫键合的二聚体,单体形式的比例随着线粒体过氧化氢的增加而降低。MitoPQ(而非PQ)导致单体Prdx3的消失,这与基质过氧化氢的增加是一致的,FCCP可以防止这种情况的发生(图6F)。总的来说,这些数据支持线粒体通过复合物I的氧化还原循环驱动基质内的超氧化物产生,从而积累MitoPQ。 MitoPQ增加细胞内线粒体超氧化物的产生[1] 为了观察MitoPQ是否可以刺激细胞线粒体内的超氧化物产生,我们使用了MitoSOX荧光的增加,MitoSOX对线粒体基质中升高的超氧化物和过氧化氢有反应。MitoPQ增加了MitoSOX荧光(图7A),并且这种氧化随着时间的推移而增加(图7B)。相比之下,即使在比MitoPQ高一千倍的浓度下,PQ也无法在此时间范围内增加MitoSOX的氧化(图7C)。MitoPQ处理6小时降低了乌头酶活性,而相同浓度的PQ没有影响(图7D),这也与MitoPQ增加了细胞线粒体内的超氧化物产生相一致。 为了进一步评估细胞线粒体内MitoPQ超氧化物的产生,我们测量了MnSOD的表达水平,该水平随着对升高的基质超氧化物的适应而增加。MitoPQ以时间和剂量依赖的方式增加MnSOD蛋白水平,在12小时时达到最大诱导值约2倍(图S2)。通过扫描密度定量分析表明,1-5µM MitoPQ增加了MnSOD的表达,而需要1000倍的PQ浓度才能在相同程度上增强表达(图7E)。较高浓度的MitoPQ降低了MnSOD蛋白水平,这可能是由于过多的超氧化物产生对线粒体的损伤(图7E)。通过测量细胞存活率证实了MitoPQ的这种毒性作用,这表明MitoPQ增加了细胞死亡,而产生类似毒性需要高几百倍的PQ浓度(图7F和图S3)。这些数据共同表明,MitoPQ在细胞线粒体内选择性积累,产生超氧化物,诱导对升高的超氧化物的生物反应,并在更高浓度下导致细胞死亡。 |
| 体内研究 (In Vivo) |
MitoPQ破坏离体灌注心脏的线粒体功能[1]
接下来,我们评估了MitoPQ对离体灌注心脏功能的影响。为此,我们以等容Langendorff模式灌注跳动的小鼠心脏,并全程记录功能参数(收缩压、舒张末期压、冠状动脉流量和灌注压)(图8A-C)。初步实验表明,需要长时间灌注500µM PQ才能看到毒性作用,而5µM MitoPQ具有轻度损伤,因此我们详细评估了50µM MitaPQ的作用。平衡后,心脏被随机分配灌注50µM MitoPQ、PQ或TPMP(作为亲脂性阳离子非特异性作用的对照)。MitoPQ降低了LVDP(图8A),增加了舒张末期压(图8B),减少了冠状动脉流量(图8C),心率没有变化(数据未显示)。相比之下,相同浓度的PQ或TPMP没有影响(图8A-C)。这些数据与MitoPQ对心脏功能的损害远大于PQ一致。这种心脏损伤是由于其被心脏内的线粒体选择性摄取,随后对细胞器的氧化损伤导致细胞死亡和心脏功能紊乱。 MitoPQ在体内对苍蝇有毒[1] 为了将我们的研究扩展到整个生物体,我们通过显微注射将野生型黑腹果蝇暴露于一剂PQ或MitoPQ中,并监测它们的存活情况(图9D)。在一定浓度范围内,MitoPQ治疗对果蝇的毒性明显大于PQ(图8D)。这些数据证实,MitoPQ选择性靶向线粒体会增强体内相对于PQ的毒性。 |
| 细胞实验 |
蛋白质印迹[1]
为了检测过氧化物酶3,将RHM(2 mg蛋白质/mL)在30°C下在KCl缓冲液中孵育3分钟,在5 mM谷氨酸/苹果酸上呼吸,补充MitoPQ、PQ或赋形剂对照。在孵育结束时,加入100 mM N-乙基马来酰亚胺(NEM),继续孵育5分钟。然后通过离心(7500 x g,3分钟)将线粒体颗粒化,并将颗粒重新悬浮在缺乏还原剂的加载缓冲液中,在非还原性12%SDS-PAGE凝胶上分离出20µg蛋白质。然后使用BioRad TurboBlot转移装置将蛋白质转移到PVDF膜上。根据制造商的方案(Pierce Biotechnology),使用Memcode可逆蛋白质染色验证了蛋白质的等量装载和转移。在室温下用奥德赛阻断缓冲液阻断膜2小时。在4°C下用抗过氧化物酶3(Prdx3;兔多克隆;1:1000 v/v稀释)孵育过夜。 |
| 动物实验 |
离体灌注小鼠心脏实验[1]
C57BL/6J雄性小鼠(约25克)饲养于独立通风笼中,光照周期为12小时光照/12小时黑暗,湿度和温度受控(20-22℃),自由摄取标准饲料和水。小鼠通过腹腔注射戊巴比妥钠(约140毫克/公斤体重)进行安乐死。将跳动的心脏迅速切除,插管,并以等容 Langendorff 模式灌注,压力维持在 80 mmHg,由 STH 蠕动泵控制器反馈系统维持。灌注液为 Krebs-Henseleit (KH) 缓冲液,持续通入 95% O2/5% CO2 气体(pH 7.4,37 °C),其成分(单位:mM)为:NaCl 116、KCl 4.7、MgSO3.7H2O 1.2、NaHCO3 25、KH2PO4 1.2、CaCl2 1.4、葡萄糖 11。心脏以约 550 bpm 的频率持续起搏,并通过插入左心室 (LV) 的充满液体的保鲜膜球囊评估心脏功能,该球囊通过管路连接到压力传感器和 Powerlab 系统(英国 AD Instruments 公司)。使用1.0 mL注射器调节心室内球囊的容积,使初始左心室舒张压(LVDP)达到4–9 mmHg。在整个实验过程中,使用LabChart软件v.7(英国AD Instruments公司)记录功能参数(收缩压、舒张末期压、心率、冠状动脉血流量、灌注压)。LVDP由收缩压(SP)和舒张压(DP)之差计算得出。平衡20分钟后,将心脏随机分为三组(每组n=6),分别用50 μM PQ、MitoPQ或TPMP灌注20分钟。所有灌注方案结束后,立即使用预先在液氮中冷却的Wollenberger镊子将心脏速冻,并储存在–80 °C直至进一步分析。 果蝇饲养和实验[1] 野生型黑腹果蝇(白色达荷美品系)饲养于标准糖酵母琼脂培养基上,温度为25℃,湿度为65%,光暗周期为12:12小时。实验用果蝇由同步采集的卵以恒定密度饲养。7日龄雌性果蝇在温和的二氧化碳麻醉下,使用PicoSpritzer III(Parker)进行显微注射,方法如前所述[33],不同之处在于注射液中含有10% (v/v)乙醇或PQ/MitoPQ(由乙醇储备液配制于林格氏缓冲液[182 mM KCl、46 mM NaCl、3 mM CaCl2、10 mM Tris碱;pH 7.2 HCl]中),并添加了1 mg/mL亮蓝染料。注射后的果蝇恢复后,被放回装有食物的小瓶中,在25℃下孵育,并监测其存活情况。每组实验共注射约60-80只果蝇。 |
| 参考文献 | |
| 其他信息 |
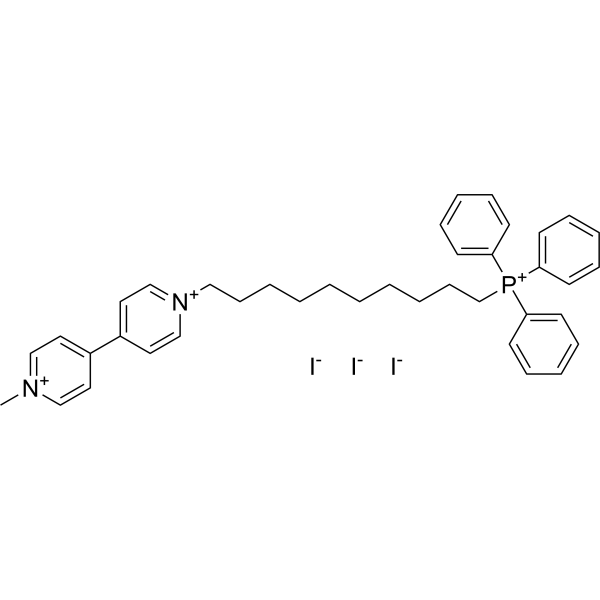
超氧化物是线粒体呼吸链产生的近端活性氧(ROS),在病理性氧化应激和氧化还原信号传导中发挥着重要作用。尽管目前已有检测或降低线粒体超氧化物水平的工具,但尚无任何方法能够快速且特异性地增加线粒体基质内的超氧化物生成。这一不足阻碍了相关研究的进展,使得准确评估线粒体超氧化物在细胞和体内的作用变得极具挑战性。为了解决这一难题,我们合成并表征了一种线粒体靶向氧化还原循环剂——MitoParaquat(MitoPQ)。MitoPQ由亲脂性三苯基膦阳离子与氧化还原循环剂百草枯偶联而成。在膜电位的驱动下,MitoPQ选择性地积累在线粒体基质中。在基质内,MitoPQ通过复合物I黄素位点的氧化还原循环产生超氧化物,从而选择性地增加线粒体内的超氧化物生成。 MitoPQ 能比非靶向百草枯更有效地增加分离线粒体和培养细胞中的线粒体超氧化物水平,其效果约为百草枯的千倍。MitoPQ 在离体灌注心脏和果蝇体内也比百草枯毒性更强。MitoPQ 能够选择性地在线粒体内生成超氧化物,是研究线粒体超氧化物在细胞和体内病理学和氧化还原信号传导中多种作用的有效工具。[1]
|
| 分子式 |
C39H46I3N2P
|
|---|---|
| 分子量 |
954.483128070831
|
| 精确质量 |
954.053
|
| 元素分析 |
C, 49.08; H, 4.86; I, 39.89; N, 2.93; P, 3.25
|
| CAS号 |
1821370-28-8
|
| PubChem CID |
129909777
|
| 外观&性状 |
Brown to reddish brown solid powder
|
| tPSA |
7.8
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
15
|
| 重原子数目 |
45
|
| 分子复杂度/Complexity |
646
|
| 定义原子立体中心数目 |
0
|
| SMILES |
[I-].[I-].[I-].[P+](C1C=CC=CC=1)(C1C=CC=CC=1)(C1C=CC=CC=1)CCCCCCCCCC[N+]1C=CC(C2C=C[N+](C)=CC=2)=CC=1
|
| InChi Key |
AOZZGHKENAZYTD-UHFFFAOYSA-K
|
| InChi Code |
InChI=1S/C39H46N2P.3HI/c1-40-30-25-35(26-31-40)36-27-32-41(33-28-36)29-17-6-4-2-3-5-7-18-34-42(37-19-11-8-12-20-37,38-21-13-9-14-22-38)39-23-15-10-16-24-39;;;/h8-16,19-28,30-33H,2-7,17-18,29,34H2,1H3;3*1H/q+3;;;/p-3
|
| 化学名 |
10-[4-(1-methylpyridin-1-ium-4-yl)pyridin-1-ium-1-yl]decyl-triphenylphosphanium;triiodide
|
| 别名 |
MitoPQ; 1821370-28-8; 1-Methyl-1'-(10-(triphenylphosphonio)decyl)-[4,4'-bipyridine]-1,1'-diium iodide; 10-[4-(1-methylpyridin-1-ium-4-yl)pyridin-1-ium-1-yl]decyl-triphenylphosphanium;triiodide; MitoParaquat; MitoPQ, MitoParaquat.; CHEMBL4750332; WXC37028;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~50 mg/mL (~52.38 mM)
DMSO : ~33.33 mg/mL (~34.92 mM) |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.0477 mL | 5.2385 mL | 10.4769 mL | |
| 5 mM | 0.2095 mL | 1.0477 mL | 2.0954 mL | |
| 10 mM | 0.1048 mL | 0.5238 mL | 1.0477 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。