| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 2mg |
|
||
| Other Sizes |
|
| 靶点 |
N-type Ca2+ channel
|
|---|---|
| 体外研究 (In Vitro) |
尾加压素 II (UII) 的作用受到 omega-芋螺毒素 GVIA (50 nM,50 nL) 的抑制 [1]。
|
| 体内研究 (In Vivo) |
本研究旨在揭示尾加压素II(UII)对延髓头端腹外侧区(RVLM)交感血管舒缩张力的影响。UII(0.3、3和30 nmol/L,50 nL)被微注射到RVLM中。测量血压(BP)、心率(HR)和肾交感神经活性(RSNA)以确定交感血管舒缩张力。将药物显微注射到RVLM后,同时记录BP、HR和RSNA。微量注射UII(0.3、3和30 nmol/L,50 nL)进入RVLM显著增加了BP、HR和RSNA。BIM23127预处理(300 nmol/L,50 nL),一种有效的UII受体GPR14拮抗剂,消除了UII的作用。先前微量注射PD98059(25 μmol/L,50 nL),一种ERK抑制剂,显著抑制UII的作用。预先注射N型Ca2+通道抑制剂ω-conotoxin GVIA(50 nmol/L,50 nL)抑制UII的作用。本研究表明,RVLM内微量注射UII可显著增加交感血管舒缩张力,这是由GPR14/ERK/N型Ca2+通道介导的。UII可能成为自主神经系统调节的一个新的治疗靶点,尤其是在高血压中。[1]
通过对天然分子丙氨酸取代类似物的结构、结合、体外和体内功能研究,阐明了N型钙通道阻滞剂ω-conotoxin GVIA(GVIA)的结构-功能关系。丙氨酸在序列中的所有非桥接位置被取代。在大多数情况下,通过1H NMR光谱显示类似物在水溶液中的结构是天然的。在某些情况下观察到的微小构象变化通过二维NMR进行表征。在三种功能测定(大鼠离体输精管、右心房和肠系膜动脉的交感神经刺激)和大鼠脑膜结合测定中,用Ala代替Lys2和Tyr13导致效力降低超过2个数量级。在功能测定中,用Ala(特别是Arg17、Tyr22和Lys24)取代其他几个残基导致效力显著降低(<100倍),但在结合测定中没有。类似物的效力在不同的功能测定之间有很强的相关性,但在功能测定和结合测定之间没有相关性。因此,本研究中采用的生理学相关测定表明,GVIA对N型钙通道的高亲和力是通道结合位点与毒素在比先前鉴定的Lys2和Tyr13更多的位点上相互作用的结果[2]。 |
| 酶活实验 |
结合测定[2]
通过Cruz和Olivera(29)的方法制备粗大鼠脑膜。使用Ultra-Turrax匀浆器(Janke和Kunkel)在10体积的缓冲液(0.32 m蔗糖,5 mm HEPES Tris,pH 7.4,0.1 mm苯甲基磺酰氟)中对个体大脑进行匀浆,并将匀浆在4°C下以1000×g离心10分钟。将颗粒重悬于另外10体积的缓冲液中,并再次旋转。然后将合并的上清液在4°C下以17000×。如上所述,将颗粒置于100体积的缓冲液中,但也含有50mg/l的溶菌酶。这得到了由约200μg组织/20μl匀浆衍生的膜。将悬浮液分成3毫升等分试样,并在−70°C下储存 结合测定在96孔微量滴定板中进行,底部有0.65μm过滤器,使用Cruz和Olivera以及Haack等人的方法进行修改,Kim等人也使用了该方法。3结合缓冲液含有0.32m蔗糖、5mm HEPES NaOH(pH 7.4)、0.1mm苯甲磺酰氟、0.3%牛血清白蛋白和50mg/l溶菌酶。洗涤缓冲液由150 mm NaCl、5 mm HEPES NaOH、pH 7.4、1.5 mm CaCl2和0.1%牛血清白蛋白组成。示踪剂溶液的制备如下:;将125I-[Tyr22]GVIA(杜邦NEN)的50μCi溶于1 ml水中,并分成50μl等分试样,在−15°C下储存。通过将一份等分试样(2.5μCi)稀释到用于测定的每个96孔微量滴定板的3.5ml结合缓冲液中,制备每个测定的示踪剂。孵育混合物(总体积100μl/孔)由50μl含有置换配体的结合缓冲液、20μl膜制剂和30μl稀释的125I-[Tyr22]GVIA示踪剂溶液组成,最终浓度0.13 nm。在存在1μm未标记的GVIA的情况下测定非特异性结合。测定在4°C下孵育90分钟,并通过真空过滤终止。每个孔用200μl洗涤缓冲液洗涤三次,然后在真空下放置10分钟以干燥过滤器。过滤器被冲压出来,并在γ计数器中计数。每个测量在一个实验中一式四份进行测定,每个实验至少重复三次。 |
| 细胞实验 |
Vas Deferens[2]
输精管被安装在5毫升的器官浴中,每个组织的顶部连接到等距力传感器(Grass FT03),底部连接到可移动的支架上,并跨在铂刺激电极上。用约10毫牛顿的被动力拉伸输精管,每20秒用单电场脉冲(100 V,0.2毫秒持续时间)刺激一次。由此产生的抽搐反应由交感神经介导,交感神经对胍乙啶(10μm)或河豚毒素(0.1μm)的抑制敏感,并记录在图表记录器上。GVIA(0.3–10 nm)导致大鼠输精管对电神经刺激的抽搐反应大小逐渐减少,这与浓度有关。亚最大有效浓度的GVIA引起抽搐的大小最初迅速下降,此后持续非常缓慢地下降超过90分钟。这种明显缓慢的平衡意味着,在没有抽搐反应自发消退的干扰的情况下,无法构建毒素完全平衡的浓度-反应曲线。为了解决这个问题,使用了连续浓度增量之间固定间隔20分钟的方案。GVIA或类似物的累积浓度响应曲线是通过将肽以从1nm开始的10倍浓度增量添加到浸泡输精管的溶液中而构建的。在每个组织中构建单个浓度响应曲线。 肠系膜动脉[2] 在解剖显微镜下,仔细解剖一条动脉(靠近进入肠道的动脉的三个分支级),去除其周围的脂肪和结缔组织,并将一段2毫米长的动脉段安装在Mulvany-Halpern式等长肌电图仪中的40μm导线上,并加热至37°C。动脉以大约四个步骤递增地径向拉伸,在每个步骤测量力和计算动脉周长,产生直径-力曲线,其中直径是在每个拉伸水平下与血管具有相同周长的圆的直径。然后使用标准计算将动脉的直径设置为100毫米汞柱膨胀压力预测直径的90%。在这些条件下建立的大鼠肠系膜动脉不会产生任何自发的主动收缩力。施用钾去极化溶液约2分钟以最大限度地激活动脉,并冲洗干净。在哌唑嗪(0.1μm)存在的情况下,用共价拮抗剂苯妥拉明(3μm,持续5分钟)阻断连接前的α2-肾上腺素受体,以保护连接后的α1-肾上腺素受体。然后冲洗拮抗剂,并应用去甲肾上腺素(10μm)来确认拮抗剂的冲洗。这个过程大大增加了对交感神经刺激的反应的大小。肌电描记器的每个颌部在距离动脉约1mm处安装有铂电极。用持续时间为0.25ms的单极电场脉冲在30V下刺激动脉壁中的交感神经,刺激参数产生的反应被河豚毒素阻断>95%。我们之前已经证明,这种反应被胍消除,因此由交感神经介导。交感神经的刺激产生收缩反应,其潜伏期短(<1s),并在刺激序列结束后迅速衰减。所有的反应都被测量为力的峰值变化。神经刺激以三组75个脉冲的形式施加,每组25 Hz,每组之间间隔60秒,连续刺激组之间间隔30分钟。GVIA或类似物以累积的方式应用,在每次测试刺激前接触30分钟。 右心房[2] 将右心房从心脏中分离出来,并将其置于37°C的5毫升器官浴中,支撑物上有两个与心房接触的细铂电极,用于收集表面电图,另一对电极用于电刺激。使用表面电图触发周期计连续测量自发收缩率。在阿托品(1μm)存在的情况下,测量交感神经介导的心动过速反应,以消除副交感神经刺激的影响。在两次对照刺激中的第二次刺激后立即施加增加浓度的GVIA或类似物,每次刺激前药物与组织接触30分钟。 |
| 动物实验 |
雄性哈兰·斯普拉格·道利大鼠经二氧化碳麻醉后断头处死,取出输精管、心脏和部分肠系膜肠段,置于盛有冰冷克氏液(成分:Na+ 144、K+ 5.9、Mg2+ 1.2、Ca2+ 2.5、HPO4− 1.2、Cl− 129、SO4− 1.2、HCO3− 25、葡萄糖 11、EDTA 0.026,通入 5% 二氧化碳/氧气混合气体)的培养皿中,以备进一步解剖[2]。
清醒兔实验。对新西兰白兔(雌雄不限,体重 2.5 ± 0.1 kg)进行局部麻醉(1% 盐酸利多卡因),分别在其中央耳动脉和耳缘静脉处插管,用于测量平均动脉压(MAP)和注射药物。瞬时血压信号触发心率计测量心率(HR)。瞬时动脉压、平均动脉压和心率均记录在Grass多导生理记录仪上。按照上述简要步骤操作后,将兔子固定在聚碳酸酯约束器中安静休息约40分钟。评估静脉注射选定的GVIA类似物对平均动脉压(MAP)、心率和压力反射的影响。压力反射的测量方法是:分别使用去氧肾上腺素和硝普钠诱发MAP交替的稳态升高和降低(基线±5–35 mmHg)。GVIA类似物的效价通过将其作用与10 μg/kg GVIA的作用进行比较来评估。GVIA类似物的初始给药剂量为3或10 μg/kg。监测平均动脉压 (MAP) 和心率 (HR) 60 分钟,如果其效果小于 10 μg/kg 静脉注射 GVIA,则增加类似物的剂量(累积半对数剂量递增)。在给予最高剂量肽后 60 分钟,重新评估压力反射曲线,并通过将压力感受器-心率反射曲线拟合到逻辑方程来获得反射参数(增益、位置和平台期)。[2] |
| 参考文献 | |
| 其他信息 |
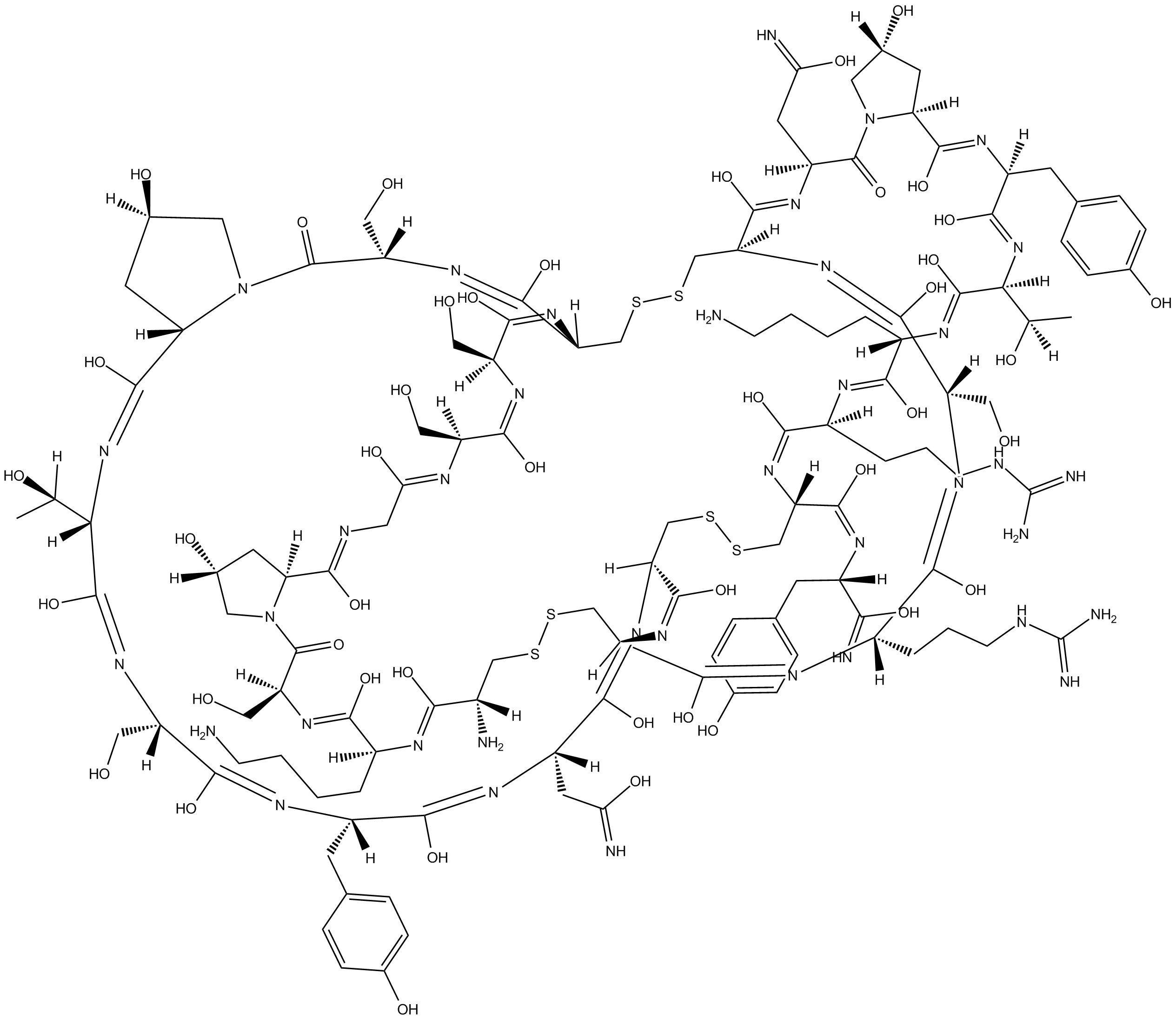
ω-芋螺毒素GVIA是一种异源环状多肽,由线性序列Cys-Lys-Ser-Hyp-Gly-Ser-Ser-Cys-Ser-Hyp-Thr-Ser-Tyr-Asn-Cys-Cys-Arg-Ser-Cys-Asn-Hyp-Tyr-Thr-Lys-Arg-Cys-Tyr-NH2组成,其中1-16、8-19和15-26位半胱氨酸残基之间形成三个二硫键。该毒素分离自以鱼类为食的芋螺(Conus geographus)的毒液。它具有毒液、神经毒素、钙通道阻滞剂和海洋代谢物等多种功能。它是一种多肽、异源环状肽、有机二硫化物和肽酰胺。
|
| 分子式 |
C120H182N38O43S6
|
|---|---|
| 分子量 |
3037.34787999999
|
| 精确质量 |
3035.15
|
| CAS号 |
106375-28-4
|
| 相关CAS号 |
106375-28-4
|
| PubChem CID |
16133838
|
| 序列 |
Cys-Lys-Ser-{Hyp}-Gly-Ser-Ser-Cys-Ser-{Hyp}-Thr-Ser-Tyr-Asn-Cys-Cys-Arg-Ser-Cys-Asn-{Hyp}-Tyr-Thr-Lys-Arg-Cys-Tyr-NH2 (Disulfide bridge: Cys1-Cys16; Cys8-Cys19; Cys15-Cys26)
|
| 短序列 |
CKS-{Hyp}-GSSCS-{Hyp}-TSYNCCRSCN-{Hyp}-YTKRCY-NH2 (Disulfide bridge: Cys1-Cys16; Cys8-Cys19; Cys15-Cys26)
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.71
|
| LogP |
-15.8
|
| tPSA |
1496.38
|
| 氢键供体(HBD)数目 |
49
|
| 氢键受体(HBA)数目 |
54
|
| 可旋转键数目(RBC) |
39
|
| 重原子数目 |
207
|
| 分子复杂度/Complexity |
6820
|
| 定义原子立体中心数目 |
31
|
| SMILES |
C[C@@H](O)[C@H]1C(N[C@H](C(NC(C(N[C@H](C(N[C@H](C(N)=O)CC2=CC=C(O)C=C2)=O)CSSC[C@H]3C(N[C@H]4CSSC[C@H](N)C(NC(C(N[C@H](C(N5C[C@H](O)C[C@H]5C(NCC(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N6C[C@H](O)C[C@H]6C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N3)=O)CC(N)=O)=O)CC7=CC=C(O)C=C7)=O)CO)=O)[C@H](O)C)=O)=O)CO)=O)CSSC[C@H](NC([C@@H](NC([C@@H](NC4=O)CCCNC(N)=N)=O)CO)=O)C(N[C@H](C(N8C[C@H](O)C[C@H]8C(N[C@H](C(N1)=O)CC9=CC=C(O)C=C9)=O)=O)CC(N)=O)=O)=O)CO)=O)CO)=O)=O)=O)CO)=O)CCCCN)=O)=O)=O)CCCNC(N)=N)=O)CCCCN)=O
|
| InChi Key |
DQZTPPHJRQRQQ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C120H182N38O43S6/c1-53(165)91-114(197)138-66(10-4-6-26-122)95(178)136-68(12-8-28-132-120(129)130)98(181)149-81(107(190)139-69(93(126)176)29-55-13-19-58(167)20-14-55)49-204-207-52-84-110(193)153-80-48-203-202-47-64(123)94(177)135-65(9-3-5-25-121)97(180)147-78(45-163)117(200)156-38-61(170)32-85(156)111(194)133-37-90(175)134-74(41-159)102(185)145-76(43-161)105(188)152-83(109(192)148-79(46-164)118(201)158-40-63(172)34-87(158)113(196)155-92(54(2)166)115(198)146-77(44-162)103(186)140-70(30-56-15-21-59(168)22-16-56)99(182)141-72(35-88(124)173)100(183)150-84)51-206-205-50-82(151-104(187)75(42-160)144-96(179)67(137-106(80)189)11-7-27-131-119(127)128)108(191)143-73(36-89(125)174)116(199)157-39-62(171)33-86(157)112(195)142-71(101(184)154-91)31-57-17-23-60(169)24-18-57/h13-24,53-54,61-87,91-92,159-172H,3-12,25-52,121-123H2,1-2H3,(H2,124,173)(H2,125,174)(H2,126,176)(H,133,194)(H,134,175)(H,135,177)(H,136,178)(H,137,189)(H,138,197)(H,139,190)(H,140,186)(H,141,182)(H,142,195)(H,143,191)(H,144,179)(H,145,185)(H,146,198)(H,147,180)(H,148,192)(H,149,181)(H,150,183)(H,151,187)(H,152,188)(H,153,193)(H,154,184)(H,155,196)(H4,127,128,131)(H4,129,130,132)
|
| 化学名 |
68-amino-36,71-bis(4-aminobutyl)-N-[1-amino-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]-22,51-bis(2-amino-2-oxoethyl)-33,60-bis(3-carbamimidamidopropyl)-8,47,78-trihydroxy-13,39-bis(1-hydroxyethyl)-4,16,57,74,86,89-hexakis(hydroxymethyl)-19,42-bis[(4-hydroxyphenyl)methyl]-2,5,11,14,17,20,23,32,35,38,41,44,50,53,56,59,62,69,72,75,81,84,87,90,97-pentacosaoxo-27,28,65,66,93,94-hexathia-3,6,12,15,18,21,24,31,34,37,40,43,49,52,55,58,61,70,73,76,82,85,88,91,96-pentacosazahexacyclo[52.37.4.225,63.06,10.045,49.076,80]heptanonacontane-30-carboxamide
|
| 别名 |
ω-CgTx GVIA, ω-Conotoxin GVIA,Conus geographus; omega-Conotoxin G via; 106375-28-4; Omega conopeptide GVIA (Conus);SNX124;SNX-124;SNX 124; Omega-Conotoxin GVIA trifluoroacetate salt; Omega-Conotoxin G Via TFA; DA-59381; Q27162637; H-D-Cys(1)-Lys-Ser-D-aHyp-Gly-D-Ser-D-Ser-Cys(2)-Ser-aHyp-D-aThr-Ser-D-Tyr-Asn-Cys(3)-Cys(1)-Arg-D-Ser-Cys(2)-Asn-D-aHyp-Tyr-aThr-D-Lys-Arg-Cys(3)-Tyr-NH2
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O: ~100 mg/mL (TFA salt)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.3292 mL | 1.6462 mL | 3.2923 mL | |
| 5 mM | 0.0658 mL | 0.3292 mL | 0.6585 mL | |
| 10 mM | 0.0329 mL | 0.1646 mL | 0.3292 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。