| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
Somatostatin receptor
|
|---|---|
| 体外研究 (In Vitro) |
这项工作致力于阿托西班,Mpa1-D-Tyr(OEt)-Ile-Thr-Asn-Cys6-Pro-Orn-Gly-NH2环状1,6二硫化物的大规模固相合成(SPS),这是临床上唯一使用的催产素受体拮抗剂。已经选择了在溶液和固相中关闭阿托西班分子中二硫键(S-S)的条件,同时尽量减少副产物的形成。在不同条件下对S-S键的形成进行了比较评估。在溶液和聚合物载体上研究了二硫键闭合过程中副产物的形成。所开发的技术允许在扩大的规模(10-20mmol)上合成阿托西班,包括在固相合成过程中使受保护的中间体环化并形成S-S键,同时尽量减少副产物的形成[1]。
|
| 体内研究 (In Vivo) |
肝糖原生成减少是非酒精性脂肪肝代谢异常的最重要原因之一。奥曲肽是一种生长抑素类似物,已被证明可以促进高脂肪饮食(HFD)诱导的肥胖小鼠的减肥和改善代谢紊乱。然而,奥曲肽是否影响肝脏糖原生成尚不清楚。本研究旨在验证奥曲肽对HFD诱导的肥胖大鼠肝脏糖原生成的影响。雄性Sprague-Dawley大鼠被喂食标准饮食或HFD 24周。HFD组的肥胖大鼠进一步分为HFD对照组和奥曲肽给药组。后一组大鼠注射奥曲肽8天。进行葡萄糖和胰岛素耐受试验,并计算曲线下面积(AUC)。处死后,测量其体重和身长、空腹血糖(FPG)、空腹胰岛素(FINS)、血清甘油三酯(TG)、总胆固醇(TC)、游离脂肪酸(FFA)、丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)水平。此外,还计算了李指数和稳态模型评估指数。首先测定肝脏TG、FFA水平和糖原含量。通过苏木精、伊红和油红O染色评估肥胖大鼠的肝脂肪变性。将人肝母细胞瘤HepG2细胞分为对照组、棕榈酸酯(PA)治疗组和PA+奥曲肽治疗组。通过油红O染色证实了使用HepG2细胞建立的体外脂肪肝模型。通过蛋白质印迹检测磷酸化Akt和糖原合酶激酶3β(GSK3β)的表达,通过逆转录定量聚合酶链式反应检测糖原合酶(GS)mRNA水平。与对照组相比,肥胖大鼠的体重、李指数、腹腔葡萄糖耐量试验和腹腔胰岛素耐量试验的AUC、FPG、FINS、TG、TC、FFA、ALT和AST水平以及HOMA指数值均显著升高。奥曲肽治疗后,体重、FPG和FINS水平以及HOMA指数显著降低,而Lee指数、ALT、AST、TC、TG和FFA血液水平以及AUC的降低没有达到统计学意义。与对照组相比,HFD诱导的肥胖大鼠的肝脏TG和FFA水平显著升高,肝糖原含量显著降低。奥曲肽干预恢复了这些改变。与对照组相比,HFD组磷酸化Akt和GSK3β蛋白表达的表达水平以及GS mRNA水平较低,而奥曲肽治疗逆转了这些降低。体外实验表明,奥曲肽治疗显著逆转了PA治疗组磷酸化Akt和GSK3β蛋白以及GS mRNA水平的降低。总之,结果表明,奥曲肽改善了HFD诱导的肥胖大鼠的肝脏糖原生成,降低了FPG浓度。这些机制可能与通过促进GSK3β磷酸化增加GS活性有关。因此,奥曲肽可被视为治疗HFD诱导的肥胖和肥胖相关代谢紊乱的新策略[2]。
|
| 参考文献 |
[1]. Optimal Method for Disulfide Bond Closure in the Synthesis of Atosiban—Antagonist of Oxytocin Receptors. Russian Journal of Bioorganic Chemistry volume 47, pages1241–1248 (2021)
[2]. Effects of octreotide on hepatic glycogenesis in rats with high fat diet?induced obesity. Mol Med Rep. 2017 Jul;16(1):109-118 |
| 其他信息 |
所开发的方法可以获得纯度超过 85% 的技术级阿托西班,二聚体产物含量低于 5%,这使得将该技术引入工业生产成为可能。[1]
|
| 分子式 |
C98H132N20O20S4
|
|---|---|
| 分子量 |
2038.48
|
| 精确质量 |
2151.877
|
| CAS号 |
1926163-80-5
|
| PubChem CID |
145707862
|
| 序列 |
H-D-Phe-Cys(1)-Phe-D-Trp-Lys-Thr-Cys(2)-Thr-ol.H-D-Phe-Cys(1)-Phe-D-Trp-Lys-Thr-Cys(2)-Thr-ol.TFA
D-phenylalanyl-L-cysteinyl-L-phenylalanyl-D-tryptophyl-L-lysyl-L-threonyl-L-cysteinyl-L-threoninol (2->2'),(7->7')-bis(disulfide) compound with D-phenylalanyl-L-cysteinyl-L-phenylalanyl-D-tryptophyl-L-lysyl-L-threonyl-L-cysteinyl-L-threoninol trifluoroacetic acid ({d-Phe}-Cys-Phe-{d-Trp}-Lys-Thr-Cys-{L-threoninol})2 (Disulfide bond: Cys2A-Cys2B; Cys7A-Cys7B) |
| 短序列 |
({d-Phe}-CF-{d-Trp}-KTC-{L-threoninol})2 (Disulfide bond: Cys2A-Cys2B; Cys7A-Cys7B)
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| tPSA |
803
|
| 氢键供体(HBD)数目 |
27
|
| 氢键受体(HBA)数目 |
33
|
| 可旋转键数目(RBC) |
34
|
| 重原子数目 |
149
|
| 分子复杂度/Complexity |
3820
|
| 定义原子立体中心数目 |
20
|
| SMILES |
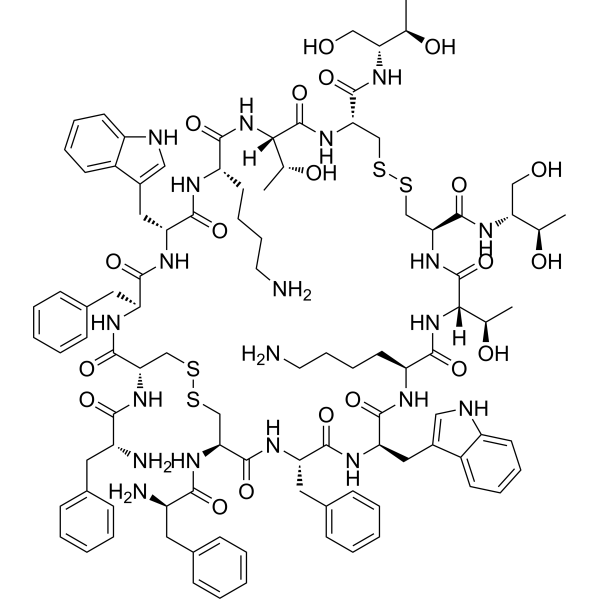
C[C@H]([C@H]1C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H](NC(=O)[C@@H](NC(=O)[C@H](CSSC[C@@H](C(=O)N[C@H](C(=O)N[C@@H](C(=O)N[C@H](C(=O)N1)CCCCN)CC2=CNC3=CC=CC=C32)CC4=CC=CC=C4)NC(=O)[C@@H](CC5=CC=CC=C5)N)NC(=O)[C@@H](CC6=CC=CC=C6)N)CC7=CC=CC=C7)CC8=CNC9=CC=CC=C98)CCCCN)[C@@H](C)O)C(=O)N[C@H](CO)[C@@H](C)O)C(=O)N[C@H](CO)[C@@H](C)O)O.C(=O)(C(F)(F)F)O
|
| InChi Key |
LUSPXROKXWWHOM-GZFVIQAPSA-N
|
| InChi Code |
InChI=1S/C98H132N20O20S4.C2HF3O2/c1-55(121)77(49-119)111-95(135)81-53-141-142-54-82(96(136)112-78(50-120)56(2)122)116-98(138)84(58(4)124)118-88(128)72(38-22-24-40-100)106-92(132)76(46-64-48-104-70-36-20-18-34-66(64)70)110-90(130)74(44-62-31-15-8-16-32-62)108-94(134)80(114-86(126)68(102)42-60-27-11-6-12-28-60)52-140-139-51-79(113-85(125)67(101)41-59-25-9-5-10-26-59)93(133)107-73(43-61-29-13-7-14-30-61)89(129)109-75(45-63-47-103-69-35-19-17-33-65(63)69)91(131)105-71(37-21-23-39-99)87(127)117-83(57(3)123)97(137)115-81;3-2(4,5)1(6)7/h5-20,25-36,47-48,55-58,67-68,71-84,103-104,119-124H,21-24,37-46,49-54,99-102H2,1-4H3,(H,105,131)(H,106,132)(H,107,133)(H,108,134)(H,109,129)(H,110,130)(H,111,135)(H,112,136)(H,113,125)(H,114,126)(H,115,137)(H,116,138)(H,117,127)(H,118,128);(H,6,7)/t55-,56-,57-,58-,67-,68-,71+,72+,73+,74+,75-,76-,77-,78-,79+,80+,81+,82+,83+,84+;/m1./s1
|
| 化学名 |
(4R,7S,10S,13R,16S,19R,24R,27S,30R,33S,36S,39R)-10,33-bis(4-aminobutyl)-19,24-bis[[(2R)-2-amino-3-phenylpropanoyl]amino]-16,27-dibenzyl-4-N,39-N-bis[(2R,3R)-1,3-dihydroxybutan-2-yl]-7,36-bis[(1R)-1-hydroxyethyl]-13,30-bis(1H-indol-3-ylmethyl)-6,9,12,15,18,25,28,31,34,37-decaoxo-1,2,21,22-tetrathia-5,8,11,14,17,26,29,32,35,38-decazacyclotetracontane-4,39-dicarboxamide;2,2,2-trifluoroacetic acid
|
| 别名 |
1926163-80-5; Octreotide trifluoroacetate salt (Dimer, Parallel); MFCD30748663
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.4906 mL | 2.4528 mL | 4.9056 mL | |
| 5 mM | 0.0981 mL | 0.4906 mL | 0.9811 mL | |
| 10 mM | 0.0491 mL | 0.2453 mL | 0.4906 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。