| 规格 | 价格 | |
|---|---|---|
| 1mg | ||
| 5mg | ||
| 10mg | ||
| Other Sizes |
| 靶点 |
AT1R-Gq fusion protein; Angiotensin II receptor type 1 (AT1R)
|
|---|---|
| 体外研究 (In Vitro) |
等摩尔比较清楚地将这些化合物(TRV120026、TRV120034、TRV120045、TRV12004-4和SGG)确定为β-arrestin偏置配体,而其他化合物似乎是平衡的(TRV120055、TRV120056、A1和S1C4)(图6A;补充图S4)。例如,SGG和TRV120044化合物被移到图的左侧,而平衡激动剂AngII和TRV120055都具有类似的双曲线形状,与β-arrestin募集试验相比,IP1试验中的扩增增加相一致(图6A)。这两种β-arrestin偏倚化合物的图表明,TRV120044(红色)比SGG(绿色)具有更多的β-arresten偏倚,尽管在这种定性分析中很难确定。然后使用等效方法计算所有化合物的偏差因子(图6B)。与等摩尔比较一致,TRV120026、TRV120034、TRV120044、TRV1020045和SGG化合物的偏差因子均与β-arrestin偏差一致,尽管其中一些化合物的较大误差导致差异在统计学上不显著。这是由于IP1浓度响应数据的拟合较差,其中许多化合物几乎没有信号活性[1]
第三,与Gq偏向激活βarr2的预测一致(图1C),Gq偏向激动剂TRV120055和TRV120056在AT1R Gq融合蛋白上的分子效率是AT1R-βarr2融合蛋白的10倍(图3C)。事实上,TRV120055和TRV120056的Gq分子效率是所有测试配体中最大的(表1)。这与它们在细胞中激活Gq的极高功效值是一致的(17)。第四,正如预测的那样(图1D),拮抗剂替米沙坦在两个传感器上都缺乏可检测的分子疗效(图3D)。[2] βarr2也观察到类似的关系。与AngII、TRV120055、TRV120056、TRV120023和SII促进AT1R在细胞内内化的能力相对应的效率(即经典的βarr依赖过程(4);图5C)与AT1R-βarr2融合蛋白计算的βarr2分子效率显著相关(双尾Pearson相关r2=0.7909,p=0.0435;图5D)。由于内化试验中的扩增水平较低,最大细胞反应(Emax)和βarr2分子效率之间也观察到了很强的一致性(双尾Pearson相关r2=0.9140,p=0.011)。效力和功效的排名顺序(以τ和Emax值计算)在较短的内化试验(30分钟)中保持不变,缓解了人们对3小时潜伏期内细胞贡献混淆内化测量的担忧[2]。 |
| 酶活实验 |
β-Arrestin招募检测。[1]
对于β2AR,如Barnea等人(2008)之前所述,通过Tango试验评估β-arrestin对受体的募集。在该试验中,人β2AR的C末端被V2加压素受体尾部的C末端尾部取代(以提高信噪比),然后是烟草蚀刻病毒(TEV)蛋白酶切割位点和tTA转录因子。该构建体与编码与TEV蛋白酶融合的β-arrestin 2的构建体一起在HEK293细胞中稳定转染。在配体刺激下,β-arrestin被募集到受体上,导致tTA从受体上切割。tTA转移到细胞核,在细胞核中转录稳定表达的萤光素酶报告基因。用这些构建体稳定转染的HEK293细胞以每孔2.5×104个细胞的速度接种在96孔板上。第二天,将磷酸盐缓冲盐水稀释的化合物加入孔中至终浓度,然后在37°C下孵育14至20小时。第二天将平板冷却至室温,并向每个孔中加入等量的Bright Glo萤光素酶检测试剂。5分钟后,在NOVOstar酶标仪上读取发光。为了确保使用该技术获得的结果不是与配体或V2R尾部过夜孵育的伪影,我们还使用了DiscoveRx的PathHunterβ-arrestin测定法(见下文),该测定法使用人类β2AR(在C末端添加Prolink肽)与配体的孵育时间更短(约30分钟),其代表性数据如补充图S5所示。[1] 对于AT1AR,我们使用了DiscoveRx的PathHunterβ-arrestin测定法,并在PheraStar阅读器上读取化学发光信号,如前所述(Violin等人,2010)。简而言之,β-半乳糖苷酶的互补半体在基因上与人AT1R和β-arrestin2的羧基末端融合。当共转染时,这两种融合蛋白充当接近传感器;当β-arrestin2转移到活性受体时,β-半乳糖苷酶片段相互作用形成一种功能酶,被化学发光底物检测到。 cAMP测定。[1] GloSensor cAMP生物传感器(Promega)使用含有cAMP结合基序的萤火虫荧光素酶的改良形式(Fan等人,2008)。cAMP结合后,构象变化导致酶互补,与萤光素酶底物孵育导致发光读数。在用Glosensor构建体和人β2AR稳定转染的HEK293细胞中进行cAMP积累分析。细胞以8×104个细胞/孔的速度接种在96孔白色透明底板中,在补充了10%胎牛血清[10%(v/v)]的最低必需培养基中。第二天,将GloSensor试剂[4%(v/v)]在室温下孵育2小时。然后用一系列β2 AR激动剂刺激细胞5分钟,并在NOVOstar酶标仪上读取发光增加。在用于β-arrestin募集试验的Tango细胞系中重复这些试验,并瞬时转染Glosensor构建体,尽管信噪比较差,但表现出相同的行为(补充图S6)。 肌醇1-磷酸盐测定。[1] 肌醇1-磷酸(IP1)是肌醇三磷酸的下游代谢产物,它本身是Gq信号传导的下游,如前所述,通过IP One Tb HTRF试剂盒检测到(Violin等人,2010)。使用时间分辨荧光比(665/620nm)在PheraStar阅读器上读取板。 血管紧张素II IA型受体竞争膜放射配体结合分析。[1] 通过在4°C下以400g离心30分钟,收获稳定表达大鼠(r)AT1受体的HEK293细胞,用平衡盐溶液洗涤一次,排斥,并将颗粒在液氮中快速冷冻。细胞颗粒在-80°C下储存,直到加工成膜。将颗粒重新悬浮在含有新鲜蛋白酶抑制剂、罗氏诊断公司的完整品牌蛋白酶片的缓冲液(50 mM HEPES,2 mM EDTA,pH 7.4)中,并在冰上用帕尔细胞破坏弹在1000 psi下进行氮气空化20分钟。在4°C下,将破裂的细胞在500g下沉淀10分钟,在48000g下洗涤含有细胞膜的上清液两次,持续15分钟。将细胞颗粒在4°C下重新悬浮在10倍体积的冰冷缓冲液A中,并在冰上空化。为了去除大颗粒,进行了低速离心(500g,4°C下30分钟),然后进行了高速离心(48000g,4℃下45分钟),在缓冲液和蛋白酶抑制剂混合物中重新悬浮,最后进行了最后的高速离心(48000 g,4癈下45分钟。使用Dounce均质器使用冰冷缓冲液重新悬浮最终颗粒。将膜悬浮液通过23号针,制备等分试样并储存在-80°C下。使用Pierce Biotechnology的Coomassie Plus试剂盒,以牛血清白蛋白为标准品,测定膜制剂的总蛋白浓度。[1] 在23°C下,将膜在测定缓冲液[50 mM HEPES、150 mM NaCl、5 mM MgCl2、Gpp(NH)p 10μM、pH 7.2]中稀释至1至3μg/孔的蛋白质浓度。通过向200μl[125I]Sar1Ile8-血管紧张素II(比活性,2200 Ci/mmol)中加入94μl膜悬浮液,以0.4至1倍的Kd和缓冲液中不同浓度的抑制剂,加上蛋白酶抑制剂和0.02%牛血清白蛋白的混合物,以减少非特异性放射配体结合,从而启动检测。将化合物在二甲亚砜中稀释,并在终浓度为1%的二甲基亚砜下进行测试(经测定对测定结果无影响)。在聚丙烯96孔板中进行与化合物(11点浓度)的竞争结合。非特异性结合是在10μM氯沙坦存在下定义的。在23°C下进行4小时的竞争分析,以便化合物和放射性配体有足够的时间达到结合平衡。通过使用Brandel细胞采集器在GF/B单滤器(聚乙烯亚胺处理)板上快速真空过滤培养混合物,实现了结合放射性配体与游离放射性配体的分离。用0.3ml冰冷的磷酸盐缓冲盐水(pH 7.0)洗涤过滤器两次,该盐水含有0.01%的Triton X-100。使用MicroBeta TriLux液体闪烁计数器对过滤器上的放射性进行定量。 放射性配体结合分析[2] 使用未融合和融合传感器的AT1R表达膜进行竞争性放射性配体结合分析,以促进严格分析(见“实验程序”)。在Gq测定缓冲液(50 mm Tris-HCl,pH 7.4,150 mm NaCl,12.5 mm MgCl2和0.2%BSA)中进行测量Gq分子功效的竞争结合测定,该缓冲液含有50 pm 125I-Sar1、Ile8-AngII、AT1R(0.5μg)或AT1R Gq(0.25μg)膜,并连续稀释测试配体。在βarr2测定缓冲液(50 mm Tris-HCl,pH 7.4,50 mm乙酸钾,150 mm NaCl,5 mm MgCl2和0.2%BSA)中进行测量βarr2分子功效的结合测定,该缓冲液含有50 pm 125I-Sar1、Ile8-AngII、AT1R+CAAX-GRK2(1μg)或AT1R-βarr2+CAAX-GRK2。在10μm替米沙坦存在下测定非特异性结合,而在没有竞争对手的情况下测定总结合。为了确保准确的低亲和力测定,在未融合的AT1R膜上进行的结合测定包括一种不可水解的GTP类似物5′-鸟苷酰亚胺二磷酸(GPP(NH)P),Gq测定为1μm,βarr2测定为100μm。在25°C下孵育1.5小时后,使用冷Gq洗涤缓冲液(50 mm Tris-HCl,pH 7.4)或冷βarr2洗涤缓冲液,在0.3%聚乙烯亚胺处理的GF/C过滤器上收集结合放射性。结合放射性在Packard Cobra伽马计数器上定量。如上所述,对AT1R Gq和AT1Rβarr2膜进行饱和结合分析,不同之处在于分别使用125I-AngII(5 pm至1 nm)和125I-Sar1,Ile8-AngII(6 pm至2 nm)的连续稀释液标记转导子偶联和总AT1R群体。 IP1累积[2] 如前所述,使用IP One Tb HTRF试剂盒 测量IP1积累(18)。 AT1R内化试验[2] 使用活化内吞试验测量βarr依赖性AT1R内化。简而言之,人AT1R在稳定表达酶受体标记的βarr2和内体定位的ProLink标记的U2OS细胞中瞬时表达。将细胞(20000个细胞/孔)在96孔板中孵育24小时,并在37°C下用测试配体(100μm至0.1 nm)刺激30分钟或3小时。AT1R内化被检测为内体内β-半乳糖苷酶片段(酶受体和ProLink)互补产生的发光。使用PathHunter检测试剂盒在NOVOstar平板阅读器上检测到发光。 βarr2招募试验[2] DiscoveRx 的PathHunterβarr测定测量了βarr2向AT1R的募集,用于细胞偏倚计算,如前所述。 ERK1/2磷酸化分析[2] 使用赛璐珞标记HTRF试剂盒测量ERK1/2磷酸化。在37°C下用1μm AngII刺激瞬时表达未融合AT1R、AT1R Gq或AT1R-βarr2融合蛋白的HEK 293细胞(50000个细胞/孔)10分钟。使用665 nm/615 nm的时间分辨荧光比在PheraStar阅读器上读取板。ERK1/2磷酸化被报道为-倍于基线反应。 |
| 细胞实验 |
共免疫沉淀【Nat Commun. 2017 Feb 9;8:14335.】
如前所述进行共免疫沉淀。HEK293细胞与Flag-AT1R-樱桃、TRPC3-GFP(野生型/截短型)和HA-β-arrestin1(野生型-截短型/突变体)共转染。转染48小时后,将细胞饥饿12小时,然后用Ang II(100 nM)、TRV120055(30 nM)或TRV120027(100 nM)刺激1分钟。随后,用冷PBS洗涤细胞,然后收集在冷裂解缓冲液中。使用不同的抗体偶联珠(Flag或HA偶联珠)对细胞裂解物进行免疫沉淀,在4°C下孵育过夜。用冷裂解缓冲液广泛洗涤含有AT1R或arrestin的免疫复合物至少五次,并用特异性抗体通过蛋白质印迹进行分析。 |
| 参考文献 | |
| 其他信息 |
七次跨膜受体(7TMR),通常被称为G蛋白偶联受体,构成了“可成药”基因组的很大一部分。7TMR可以同时通过平行通路传递信号,例如通过来自不同家族的异源三聚体G蛋白,或者,正如最近人们所认识到的,通过多功能衔接蛋白β-arrestin。偏向性激动剂能够以不同的效力激活受体的多个下游通路,是解析这种复杂信号传导的有效工具。这些化合物也可能具有治疗用途,因为它们与“平衡激动剂”具有不同的功能和治疗特性。尽管已经提出了一些识别偏向性配体的方法,但尚未对这些方法应用于同一组数据进行比较。因此,目前尚无公认的方法来量化不同配体的相对偏向性,这使得偏向性信号传导的研究变得困难。本文采用互补的计算方法来量化配体偏向性,并展示了其在两个著名的药物靶点——β2肾上腺素能受体和血管紧张素II 1A型受体——上的应用。本文概述的策略能够量化配体偏向性并识别弱偏向性化合物。这种通用方法有助于解析复杂的信号通路,并可能有助于开发新型偏向性治疗配体作为药物。[1]
“偏向性激动作用”的概念源于这样一种认识:激动剂诱导受体介导反应的能力(即“效力”)在源自同一GPCR的多个信号转导通路(例如G蛋白和β-arrestin (βarr))中可能存在差异。尽管偏向性激动作用具有治疗前景,但偏向性激动剂选择性激活信号通路的分子机制仍然难以捉摸。这很大程度上是由于量化细胞内配体效力所面临的挑战。为了解决这个问题,我们开发了一种无细胞方法,直接量化平衡型和偏向型配体对血管紧张素II 1型受体(AT1R,一种典型的G蛋白偶联受体)的转导器特异性分子效能。具体而言,我们以变构术语定义效能,将AT1R-Gq和AT1R-βarr2融合蛋白的配体亲和力变化(即KLo/KHi)与其激活Gq和βarr2的相应分子效能等同起来。与三元复合物模型预测一致,转导器特异性分子效能与激活Gq和βarr2的细胞效能密切相关。后续对不同转导器的比较表明,偏向型AT1R激动剂具有偏向性的分子效能,这与细胞实验中观察到的信号偏向性高度吻合。这些发现不仅代表了对不同换能器配体效力差异背后的热力学驱动力的首次测量,而且还支持了一种分子机制,即不同的换能器特异性分子效力会在 GPCR 上产生偏向性激动作用。[2] |
| 分子式 |
C43H65N13O12
|
|---|---|
| 分子量 |
956.06
|
| 精确质量 |
955.487
|
| CAS号 |
40678-47-5
|
| PubChem CID |
10533900
|
| 序列 |
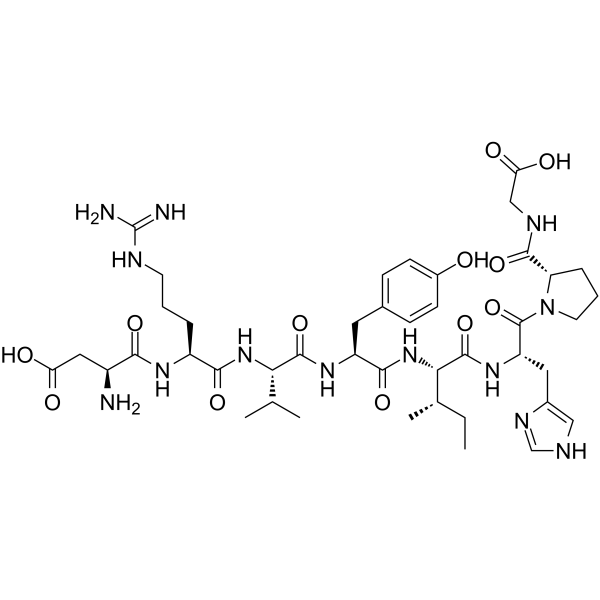
H-Asp-Arg-Val-Tyr-Ile-His-Pro-Gly-OH; L-alpha-aspartyl-L-arginyl-L-valyl-L-tyrosyl-L-isoleucyl-L-histidyl-L-prolyl-glycine
|
| 短序列 |
DRVYIHPG
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
-3.7
|
| tPSA |
409
|
| 氢键供体(HBD)数目 |
13
|
| 氢键受体(HBA)数目 |
15
|
| 可旋转键数目(RBC) |
27
|
| 重原子数目 |
68
|
| 分子复杂度/Complexity |
1790
|
| 定义原子立体中心数目 |
8
|
| SMILES |
C(N1CCC[C@H]1C(=O)NCC(=O)O)(=O)[C@@H](NC(=O)[C@]([H])([C@@H](C)CC)NC(=O)[C@@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](N)CC(=O)O)CC1C=CC(O)=CC=1)CC1N=CNC=1
|
| InChi Key |
LHGCUVPUBNGERS-FVSPLASQSA-N
|
| InChi Code |
InChI=1S/C43H65N13O12/c1-5-23(4)35(41(67)53-30(17-25-19-47-21-50-25)42(68)56-15-7-9-31(56)39(65)49-20-33(60)61)55-38(64)29(16-24-10-12-26(57)13-11-24)52-40(66)34(22(2)3)54-37(63)28(8-6-14-48-43(45)46)51-36(62)27(44)18-32(58)59/h10-13,19,21-23,27-31,34-35,57H,5-9,14-18,20,44H2,1-4H3,(H,47,50)(H,49,65)(H,51,62)(H,52,66)(H,53,67)(H,54,63)(H,55,64)(H,58,59)(H,60,61)(H4,45,46,48)/t23-,27-,28-,29-,30-,31-,34-,35-/m0/s1
|
| 化学名 |
(3S)-3-amino-4-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S,3S)-1-[[(2S)-1-[(2S)-2-(carboxymethylcarbamoyl)pyrrolidin-1-yl]-3-(1H-imidazol-5-yl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-oxobutanoic acid
|
| 别名 |
TRV120056; 40678-47-5; TRV-120056; CHEMBL4588454;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O: 33.33 mg/mL (34.86 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.0460 mL | 5.2298 mL | 10.4596 mL | |
| 5 mM | 0.2092 mL | 1.0460 mL | 2.0919 mL | |
| 10 mM | 0.1046 mL | 0.5230 mL | 1.0460 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。