| 规格 | 价格 | |
|---|---|---|
| 10mg | ||
| 500mg | ||
| 1g |
| 靶点 |
Phosphoglycerides
|
|---|---|
| 体外研究 (In Vitro) |
溶血磷脂酰肌醇(LPI)是一种众所周知的生物活性脂质,能够激活与细胞增殖、迁移、存活和肿瘤发生相关的信号级联。我们之前的工作表明,LPI参与了癌症的进展,因为它可以在Ras转化的成纤维细胞的培养基中释放,并可以作为细胞生长的自分泌调节剂。不同的研究小组已经确定,LPI是G蛋白偶联受体55(GPR55)的特异性和功能性配体,并且该GPR55-LPI轴能够激活与不同细胞功能相关的信号级联。我们实验室的工作最近揭示了一个自分泌回路,通过该回路,由细胞质磷脂酶A₂(cPLA₂)合成的LPI被ATP结合盒(ABC)转运蛋白C1(ABCC1)/多药耐药蛋白1(MRP1)泵出细胞,启动GPR55下游的信号级联。我们目前的工作表明,阻断这一途径可能是抑制癌症细胞增殖的一种新策略[1]。
|
| 体内研究 (In Vivo) |
最近的研究发现,在编码含7(MBOAT7)和跨膜通道样4(TMC4)的膜结合O-酰基转移酶结构域的两个基因附近存在一个遗传变异rs641738,这两个基因与病毒性肝炎感染者患非酒精性脂肪肝(NAFLD)、非酒精性脂性肝炎(NASH)、酒精相关性肝硬化和肝纤维化的风险增加有关(Buch等人,2015;Mancina等人,2016;Luukkonen等人,2016年;Thabet等人,2016)。基于肝脏表达定量性状位点分析,有人认为MBOAT7功能丧失会促进肝脏疾病进展(Buch等人,2015;Mancina等人,2016;Luukkonen等人,2016年;Thabet等人,2016,Viitasalo等人,2016),但这从未经过正式测试。在这里,我们表明,在高脂肪饮食的情况下,小鼠体内Mboat7的缺失,而不是Tmc4的缺失,足以促进NAFLD的进展。Mboat7功能丧失与其底物溶血磷脂酰肌醇(LPI)脂质的积累有关,直接给予LPI以Mboat7依赖的方式促进肝脏炎症和纤维化转录变化。这些研究揭示了MBOAT7驱动的LPI脂质酰化在抑制NAFLD进展中的新作用[2]。
|
| 酶活实验 |
溶血磷脂酰肌醇酰基转移酶生化测定[2]
[1-14C]-花生四烯酸辅酶A是商业获得的。酶测定中使用的溶血磷脂酰肌醇(LPI)底物(16:0 LPI、18:0 LPI和18:1 LPI)和脂质标准品是从商业获得的。从Mboat7-ASO和对照ASO处理的小鼠中分离出的肝微粒体用于测量LPIAT活性,这些小鼠同时食用食物和高脂肪饮食。测定缓冲液含有50 mM Tris-HCL(pH 8.0)、150 mM NaCl、50μM 18:0-LPI、20μM[1-14C]花生四烯酸辅酶a(0.025µCi)和15µg微粒体,总体积为100µL。底物在CHAPS(0.01mM终浓度)中制备。将测定混合物在37°C下孵育30分钟,通过加入1:2:1(v/v/v)氯仿:甲醇:2%正磷酸来停止反应。使用氯仿/丙酮/乙酸/甲醇/水(50:20:15:10:5,v/v)作为溶剂系统,在硅胶TLC板上提取和分离脂质。通过相对于标准物的迁移来鉴定单个脂质分子。通过放射自显影监测酶产物,从TLC板上刮下相应的斑点,用液体闪烁计数器定量放射性。 |
| 动物实验 |
小鼠肝脏脂滴的分离与鉴定[2]
肝脏脂滴的分离采用蔗糖梯度离心法,具体方法如我们之前所述(Ferguson et al., 2017)。取约100 mg组织,在冰冷的表面上用剃须刀片切碎。将切碎的组织转移至Potter-Elvehjem匀浆器中,然后加入200 μl 60%蔗糖溶液,冰上孵育10分钟。接着,加入800 μl裂解缓冲液并混匀,冰上孵育10分钟。用特氟龙研杵研磨5次,将样品匀浆后转移至2 ml离心管中。小心地将600 μl裂解缓冲液加于匀浆液上方,4℃下以20,000 g离心2小时。将离心管置于−80°C冷冻,并在1000 μl刻度线处剪开。离心管底部含有非脂滴组分,待其解冻后转移至新的离心管中。脂滴组分的收集方法为:从冰柱顶部切取约4–6 mm的冰滴,并将其置于新的2 ml离心管中。为提高脂滴组分的纯度,重复上述步骤一次。简而言之,向脂滴组分中加入200 μl 60%蔗糖溶液。随后,加入800 μl裂解缓冲液并混匀,再小心地加入600 μl裂解缓冲液进行分层,然后在4°C下以20,000 g离心2小时。再次置于−80°C冷冻后,剪开离心管,并从冰柱顶部切取约4–6 mm的冰滴,将其置于新的离心管中收集脂滴组分。蛋白质分析采用改良的Lowry法,如前所述(Ferguson等人,2017),Western印迹分析如下所述。LD组分中的MBOAT7底物(溶血磷脂酰肌醇)和产物(磷脂酰肌醇)脂质采用下述靶向LC-MS/MS方法提取和定量。 |
| 参考文献 |
[1]. Lysophosphatidylinositol: a novel link between ABC transporters and G-protein-coupled receptors. Biochemical Society transactions, 2014, 42(5), 1372-1377.
[2]. Obesity-linked suppression of membrane-bound O-acyltransferase 7 (MBOAT7) drives non-alcoholic fatty liver disease. eLife, 2019 Oct 17:8:e49882. |
| 其他信息 |
16:0 Lyso PI(1-棕榈酰-2-羟基-sn-甘油-3-磷酸肌醇)已被用作液相色谱-质谱(LC-MS)方法条件优化中的脂质标准品,也已被用作溶血磷脂酰肌醇(LPI)底物,用于溶血磷脂酰肌醇酰基转移酶生化测定,以检测肝微粒体的溶血磷脂酰肌醇酰基转移酶(LPIAT)活性。它还可以用作合成LPI,以比较其与肝脏来源的LPI在转铁蛋白(Tf)介导的内吞作用中的作用。
循环中L-α-溶血磷脂酰肌醇(LPI)水平升高与癌症相关,LPI是G蛋白偶联受体GPR55的强效配体。溶血磷脂酰肌醇 (LPI) 具有调节癌细胞迁移的能力,并能控制内皮细胞的功能。LPI 可作为细胞生长的自分泌调节因子,因此已知其参与癌症进展。它能刺激细胞存活、迁移和增殖所必需的信号通路。 |
| 分子量 |
589.653650283813
|
|---|---|
| CAS号 |
141553-69-7
|
| 相关CAS号 |
1425501-12-7 (free acid)
|
| 外观&性状 |
Typically exists as solids (or liquids in special cases) at room temperature
|
| SMILES |
O(C1C(C(O)C(O)C(O)C1O)O)P(O)(=O)OCC(O)COC(=O)CCCCCCCCCCCCCCC.N
|
| 化学名 |
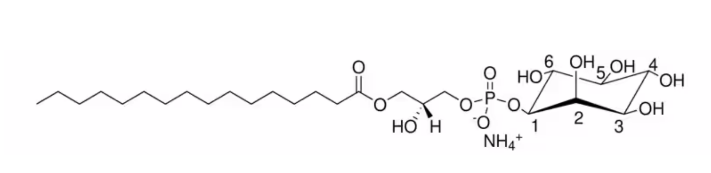
1-hexadecanoyl-2-hydroxy-sn-glycero-3-phospho-(1′-myo-inositol) (ammonium salt)
|
| 别名 |
16:0 Lyso PI ammonium salt; 1-palmitoyl-2-hydroxy-sn-glycero-3-phosphoinositol (ammonium salt); 141553-69-7
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6959 mL | 8.4796 mL | 16.9592 mL | |
| 5 mM | 0.3392 mL | 1.6959 mL | 3.3918 mL | |
| 10 mM | 0.1696 mL | 0.8480 mL | 1.6959 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。