| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
- CD88 (C5a receptor) – Potent antagonist (inhibits C5a-induced neutrophil myeloperoxidase release with IC50 of 22 nM; inhibits C5a-induced chemotaxis with IC50 of 75 nM) [2]
- Mas-related gene X2 (MrgX2) – Low-affinity agonist (induces degranulation at concentrations ≥30 nM) [1] |
|---|---|
| 体外研究 (In Vitro) |
- 在人LAD2肥大细胞中,PMX-53(1 μM)以剂量依赖性方式诱导脱颗粒(β-氨基己糖苷酶释放),最大释放率约为60%;PMX-53S(线性乱序肽)也诱导脱颗粒但程度较低;PMX-53C(Trp-Arg替换为Ala-dArg)即使在1 μM浓度下也不诱导脱颗粒 [1]
- 在LAD2肥大细胞中,PMX-53(100 nM和1 μM)诱导Ca²⁺动员;PMX-53C(100 nM)无活性,1 μM时仅诱导微小且不稳定的反应 [1] - 在HMC-1细胞中,PMX-53(10 nM)几乎完全抑制C5a(10 nM)诱导的Ca²⁺动员,但对C3a(10 nM)诱导的反应无影响;PMX-53C和PMX-53S对C5a或C3a诱导的反应均无影响 [1] - 在稳定表达CD88的RBL-2H3细胞中,PMX-53(10 nM)抑制C5a(1 nM)诱导的脱颗粒 [1] - 在LAD2细胞中,G蛋白拮抗剂2(GPA-2,1 μM,30分钟)显著抑制PMX-53诱导的脱颗粒;百日咳毒素(100 ng/mL,16小时)也抑制PMX-53介导的脱颗粒 [1] - PMX-53(≥30 nM)在LAD2肥大细胞、CD34⁺细胞来源的原代人肥大细胞以及稳定表达MrgX2的RBL-2H3细胞中诱导脱颗粒,但不激活表达MrgX1的RBL-2H3细胞 [1] - 在表达MrgX2的RBL-2H3细胞中,PMX-53(1 μM)引起持续的Ca²⁺动员,其幅度和持续时间与在LAD2细胞和CD34⁺来源肥大细胞中观察到的一致;PMX-53C无作用 [1] - 将Trp替换为Ala、Arg替换为dArg(PMX-53C)后,PMX-53抑制HMC-1细胞中C5a诱导的Ca²⁺动员以及诱导表达MrgX2的RBL-2H3细胞脱颗粒的能力均丧失 [1] |
| 体内研究 (In Vivo) |
- 在大鼠中,局部预给予PMX-53(每只爪子60或180 μg,足底内,刺激前30分钟)抑制酵母聚糖(每只爪子30 μg)诱导的机械性痛觉超敏反应;效果在酵母聚糖注射后持续6小时,24小时后减弱。治疗性给予PMX-53(每只爪子60 μg,酵母聚糖后3天给予)显著减少持续的酵母聚糖诱导的痛觉超敏反应 [2]
- PMX-53(每只爪子60 μg)抑制酵母聚糖激活血清(1:300稀释)和重组C5a(40 ng)诱导的痛觉超敏反应 [2] - PMX-53(每只爪子60 μg)抑制LPS(每只爪子0.5 μg)和角叉菜胶(每只爪子100 μg)诱导的机械性痛觉超敏反应 [2] - PMX-53(每只爪子60 μg)预给药减少了先前免疫大鼠中抗原(卵清蛋白,每只爪子25 μg)激发诱导的痛觉超敏反应 [2] - PMX-53(每只爪子60 μg)不改变PGE₂(100 ng)或多巴胺(3 μg)诱导的痛觉超敏反应 [2] - PMX-53(每只爪子60 μg)减少酵母聚糖、酵母聚糖激活血清和C5a诱导的中性粒细胞迁移(通过髓过氧化物酶活性测定),但不减少角叉菜胶或LPS诱导的迁移 [2] - 在小鼠中,全身给予PMX-53(0.3、1或3 mg/kg,皮下,刺激前30分钟)以剂量依赖性方式减少酵母聚糖(关节内30 μg)诱导的关节痛觉超敏反应 [2] - PMX-53(3 mg/kg,皮下,刺激前30分钟)减少酵母聚糖诱导的中性粒细胞向胫跗关节的迁移(通过MPO活性测定),并减少TNF-α(关节内100 pg)诱导的关节痛觉超敏反应 [2] - 在ApoE⁻/⁻小鼠(正常饮食)中,慢性给予PMX-53(3 mg/kg皮下,每周3次,加饮水中约1 mg/kg/天口服,从5周龄至30周龄)减少头臂动脉病变大小(内膜面积和内膜/中膜比值减少约40%,P<0.05),并减少斑块脂质含量(P<0.05)[5] - PMX-53治疗ApoE⁻/⁻小鼠不影响体重或血清胆固醇水平 [5] - 在ApoE⁻/⁻小鼠中,PMX-53治疗使升主动脉正面染色显示的富脂质病变面积平均减少约40%,但由于未治疗对照组内变异性较大,未达到统计学显著性 [5] |
| 细胞实验 |
- 脱颗粒测定:LAD2细胞(每孔5×10³个)或CD34⁺来源肥大细胞在含人IgE(1 μg/mL)的96孔板中铺板过夜。细胞洗涤后与不同浓度肽孵育30分钟。将20 μL上清液与20 μL 1 mM对硝基苯基-N-乙酰基-β-D-氨基葡萄糖苷在37°C孵育1.5小时,测定β-氨基己糖苷酶释放。加入250 μL 0.1 M Na₂CO₃/NaHCO₃缓冲液终止反应,在405 nm处读取吸光度 [1]
- 钙动员测定:细胞(0.2×10⁶个人肥大细胞或10⁶个RBL-2H3细胞)与1 μM indo-1乙酰氧甲酯和1 μM Pluronic酸F-127在室温下避光孵育30分钟。细胞洗涤后重悬于HEPES缓冲盐水中。使用分光光度计在激发波长355 nm、发射波长410 nm处测定Ca²⁺动员 [1] - 稳定表达MrgX1或MrgX2的RBL-2H3细胞:通过核转染将编码HA标签受体质粒转入RBL-2H3细胞,在G418(1 mg/mL)存在下培养,使用抗HA抗体进行细胞分选 [1] - RT-PCR检测MrgX1和MrgX2:使用TRIzol从肥大细胞中提取总RNA,经DNase I处理,反转录为cDNA,用特异性引物扩增。人β-肌动蛋白引物作为内参 [1] |
| 动物实验 |
- 大鼠机械性痛觉超敏反应测试:成年雄性Wistar大鼠(180-200 g)接受足底内注射(100 μL)。使用恒压大鼠足测试(施加20 mmHg压力于足底表面)测定机械性痛觉超敏反应。测量刺激前(零时)和刺激后的冻结反应潜伏期。痛觉超敏强度以反应时间减少量量化 [2]
- 大鼠痛觉超敏研究给药方案:PMX-53(每只爪子60或180 μg,足底内)在酵母聚糖(30 μg)、LPS(0.5 μg)、角叉菜胶(100 μg)或卵清蛋白(免疫大鼠中25 μg)刺激前30分钟给予。治疗性研究中,PMX-53(每只爪子60 μg)在酵母聚糖注射后第3天给予。对于ZAS和C5a研究,PMX-53(每只爪子60 μg)在ZAS(1:300稀释)或C5a(40 ng)前30分钟给予 [2] - 中性粒细胞耗竭:大鼠在刺激足底内注射前72小时静脉注射长春碱硫酸盐(0.8 mg/kg)[2] - 小鼠关节痛觉超敏模型:雄性C57BL/6小鼠(20-25 g)轻度麻醉,将酵母聚糖(30 μg于5 μL)或TNF-α(100 pg于5 μL)注射入右侧胫跗关节。使用配备改良大尖端(4.15 mm²)的电子压力计施加于足底表面诱导胫跗关节背屈,测定机械性痛觉超敏反应。PMX-53(0.3、1或3 mg/kg,皮下)或溶剂(生理盐水)在刺激前30分钟给予 [2] - MPO测定:组织在EDTA/NaCl缓冲液(pH 4.7)中匀浆,4°C下3000g离心15分钟。沉淀重悬于0.5%十六烷基三甲基溴化铵缓冲液(pH 5.4),液氮冷冻解冻三次,4°C下3000g离心15分钟。上清液用于MPO测定,使用1.6 mM四甲基联苯胺、80 mM NaPO₄、0.5 mM过氧化氢。加入4 M H₂SO₄终止反应,在450 nm处读取吸光度 [2] - ELISA测定细胞因子:足底皮肤在含蛋白酶抑制剂的缓冲液中匀浆。微孔板包被羊抗大鼠TNF-α或IL-1β抗体,4°C过夜。加入标准和样品室温孵育2小时,然后加入生物素化多克隆抗体(1:500)孵育1小时,再加入亲和素-辣根过氧化物酶(1:5000)孵育30分钟。加入OPD底物15分钟,H₂SO₄终止反应,在490 nm处读取吸光度 [2] - ApoE⁻/⁻小鼠动脉粥样硬化模型:纯合雌性ApoE⁻/⁻小鼠(C57BL/6J背景)自由进食正常饮食。PMX-53溶于高压灭菌水(6 mg/L)用于口服给药,溶于无菌5%葡萄糖溶液(3 mg/mL)用于皮下给药。小鼠从5周龄至30周龄接受PMX-53治疗:饮水中给药(约每日口服剂量1 mg/kg/天)加每周三次皮下注射PMX-53(3 mg/kg)。对照组接受溶剂(无菌水中的5%葡萄糖)注射和高压灭菌饮用水 [5] - 头臂动脉组织学分析:动脉用4%缓冲甲醛灌注固定,包埋于冷冻保护剂包埋介质中,冷冻后切成10 μm横切片。切片经Miller弹性蛋白Van Gieson染色、Gabe醛品红染色、天狼星红染色(胶原)和油红O染色(脂质)。使用ImageJ软件进行形态计量学分析。测量外弹性膜、内弹性膜和管腔围成的面积,计算血管总面积、中膜面积和内膜/中膜比值 [5] - 升主动脉正面染色:主动脉根部和升主动脉纵向切开,油红O染色,用微针固定在蜡上,病变面积(红色染色)表示为血管总面积的百分比 [5] - 头臂动脉免疫组化:切片用含5%山羊血清的PBS封闭30分钟,与一抗(抗CD68标记巨噬细胞、抗von Willebrand因子标记内皮细胞、抗α-SM肌动蛋白标记平滑肌细胞、抗CD88、抗C5L2)4°C孵育过夜,然后与Alexa Fluor偶联的二抗(1:500)孵育显色。阴性对照用无关IgG替换一抗 [5] - 主动脉细胞流式细胞术:从25周龄ApoE⁻/⁻小鼠取主动脉,用Liberase Blendzyme TL在37°C酶解离30分钟。单细胞悬液用抗小鼠CD88-Alexa Fluor 647和抗小鼠CD31-PE或抗小鼠F4/80-PE在冰上染色30分钟,用抗CD16/CD32抗体封闭,在流式细胞仪上分析 [5] |
| 毒性/毒理 (Toxicokinetics/TK) |
- PMX-53在I期和IIa期临床试验中显示出安全性和耐受性 [5]
- 这三篇文献中未描述PMX-53的LD50、肝毒性、肾毒性、药物-药物相互作用或血浆蛋白结合数据 [1][2][5] |
| 参考文献 |
|
| 其他信息 |
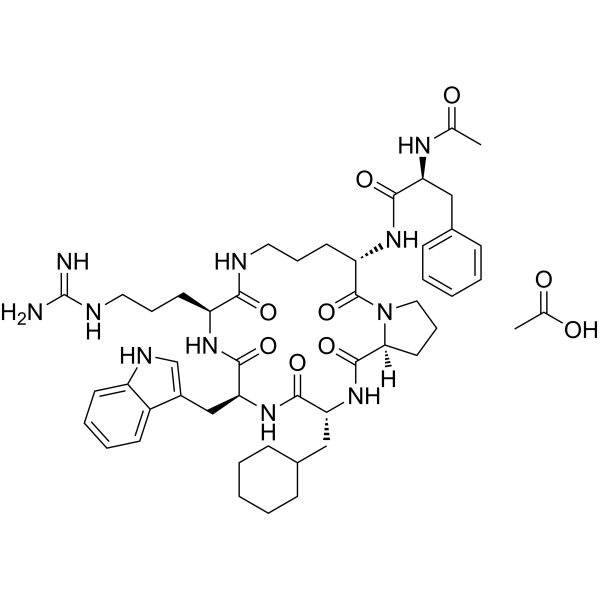
- PMX-53是一种环状六肽(Ac-Phe-[Orn-Pro-dCha-Trp-Arg]),基于C5a的末端氨基酸序列设计,以天然人C5a的C末端区域为模型 [1][2][5]
- PMX-53是一种强效的小分子肽类受体拮抗剂,对CD88具有高度选择性 [5] - PMX-53抑制C5a诱导的中性粒细胞髓过氧化物酶释放和趋化作用,IC50值分别为22 nM和75 nM [2] - PMX-53在多种小鼠和大鼠炎症性疾病模型中有效,包括类风湿关节炎、炎症性肠病、缺血再灌注损伤和神经退行性疾病 [2][5] - PMX-53已被证明能有效减少C5a介导的炎症反应和多种炎症性疾病的病理发展 [5] - PMX-53目前正在进行治疗骨关节炎的临床试验 [1] - PMX-53是一种双功能分子:是CD88的高亲和力拮抗剂,但却是MrgX2的低亲和力激动剂。低浓度时,PMX-53作为CD88拮抗剂阻断炎症;较高浓度(≥30 nM)时,通过MrgX2模拟防御素对肥大细胞的激活作用,促进先天免疫 [1] - PMX-53的CD88拮抗活性和MrgX2激动活性均需要Trp和Arg残基 [1] - 不表达MrgX2的小鼠肥大细胞对PMX-53的激活无反应,表明PMX-53对人MrgX2具有特异性 [1] |
| 分子式 |
C49H69N11O9
|
|---|---|
| 分子量 |
956.14
|
| CAS号 |
852629-88-0
|
| 相关CAS号 |
219639-75-5
|
| 序列 |
Ac-Phe-{Orn}-Pro-{dCha}-Trp-Arg (Lactam bridge: Orn2-Arg6)
|
| 短序列 |
Ac-Phe-Orn(1)-Pro-D-Cha-Trp-Arg-(1).CH3CO2H
|
| 外观&性状 |
Typically exists as solids at room temperature
|
| SMILES |
O=C1[C@@H]2CCCN2C([C@H](CCCNC([C@H](CCC/N=C(\N)/N)NC([C@H](CC2=CNC3C=CC=CC2=3)NC(C(CC2CCCCC2)N1)=O)=O)=O)NC([C@H](CC1C=CC=CC=1)NC(C)=O)=O)=O.OC(C)=O
|
| 别名 |
3D53 monoacetate; PMX-53 acetate; 852629-88-0; PMX 53 acetate(219639-75-5 free base); PMX 53 (monoacetate); orb1296311;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.0459 mL | 5.2294 mL | 10.4587 mL | |
| 5 mM | 0.2092 mL | 1.0459 mL | 2.0917 mL | |
| 10 mM | 0.1046 mL | 0.5229 mL | 1.0459 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。