| 规格 | 价格 | |
|---|---|---|
| 50mg |
| 靶点 |
GlyT1 (IC50=18 ~ 30 nM)
|
|---|---|
| 体外研究 (In Vitro) |
在人 SK-N-MC 和大鼠 C6 细胞中,SSR504734(15 nM-86 μM;10 分钟)可降低甘氨酸摄取[1]。
SSR504734阻断体外[14C]甘氨酸摄取[1] RT-PCR产物的Southern印迹分析显示,人SK-N-MC细胞仅表达GlyT1 mRNA亚型a。在该细胞系中未检测到其他GlyT1 mRNA异构体b和c(数据未显示)。[14C]甘氨酸在SK-N-MC细胞中的摄取是饱和的,钠和氯依赖性的(数据未显示),Km=21±4 μM和Vmax=667±186 pmol/min/106个细胞(n=4个独立实验)。比吸收率通常为总放射性的90%。这与之前描述的这些转运蛋白的特征是一致的(Mallorga等人,2003)。 SSR504734抑制了人SK-N-MC和大鼠C6细胞对[14C]甘氨酸的摄取,IC50值分别为18±6和15±2 nM(表1)。(R,R)对映体SSR506204在阻断[14C]甘氨酸摄取方面的效力大约是人和大鼠GlyT1的10倍。 SSR504734无活性(在1℃时抑制率低于50%) μM)对抗约120个靶点,包括甘氨酸、谷氨酸、DA、5-HT、肾上腺素、去甲肾上腺素、组胺和毒蕈碱受体、酶如MAO,以及摄取系统如DA、5-羟色胺和去甲肾上腺素转运体(由法国Celle l'Evescolt的Cerep进行的检测,数据可应要求提供)。SSR504734也没有影响(IC50>1 μM)对人GlyT2和D-丝氨酸转运蛋白以及小鼠脯氨酸、谷氨酸和GABA转运蛋白的影响(数据可应要求提供)。 SSR504734拮抗CB1受体激动剂WIN55212-2[1] 诱导的前额叶皮层神经元放电率降低 内侧PFC细胞的基线放电主要发生在约1.5的2-4个尖峰的爆发中 ms持续时间和0.2 自发(对照)频率范围为0.3至6.0的mV振幅 赫兹(平均值±扫描电镜:2.5±0.3 Hz,n=20;图7a,左面板最前面的左栏)。静脉注射WIN55212-2(0.1mg/kg)导致记录的五个PFC细胞中有四个的放电频率受到抑制。抑制最大(52.5±6.6%;图7b,左起第二条)5 给药后分钟,在接下来的20天内,F(8,24)=9.69,P<0.01,仍具有统计学意义 在返回基线之前。 |
| 体内研究 (In Vivo) |
SSR504734 的口服生物利用度(腹腔注射和口服;1-100 mg/kg;一次)良好[1]。 SSR504734(腹腔注射;30 mg/kg;一次)可快速显着降低特定甘氨酸摄取量[1]。 (腹腔注射;10 mg/kg;一次)可提高大鼠自由移动的前额皮质 (PFC) 中的细胞外甘氨酸水平[1]。
非竞争性N-甲基-D-天冬氨酸(NMDA)阻断剂在人类中诱导精神分裂症样症状,可能是通过损害谷氨酸能传递。因此,通过增加甘氨酸(谷氨酸的必要共激动剂)的细胞外水平来增强这种神经传递的化合物可能具有抗精神病活性。阻断甘氨酸转运蛋白-1(GlyT1)应该通过增加细胞外甘氨酸水平来增强谷氨酸能神经传递。SSR504734是一种选择性可逆的人、大鼠和小鼠GlyT1抑制剂(IC50分别为18、15和38 nM),可快速且长时间可逆地阻断甘氨酸的离体摄取(小鼠皮质匀浆:ID50:5 mg/kg i.p.)。在体内,它增加了大鼠前额叶皮层(PFC)中甘氨酸的细胞外水平(最小有效剂量(MED):3mg/kg i.p.)。这导致谷氨酸能神经传递增强,因为SSR504734增强了大鼠海马切片中NMDA介导的兴奋性突触后电流(EPSCs)(最低有效浓度(MEC):0.5微M)和小鼠纹状体内甘氨酸诱导的旋转(MED:1 mg/kg i.p.)。它使海马和PFC功能减退的大鼠模型中的活动正常化(通过激活突触前CB1受体):它逆转了海马切片中电诱发[3H]乙酰胆碱释放的减少(MEC:10 nM)和PFC神经元放电的减少(MED:0.3 mg/kg静脉注射)。SSR504734分别预防了氯胺酮诱导的小鼠边缘区代谢激活,并逆转了MK-801诱导的小鼠和大鼠多动和EEG光谱能量增加(MED:10-30mg/kg i.p.)。在精神分裂症模型中,它使DBA/2小鼠的自发预脉冲抑制缺陷正常化(MED:15mg/kg i.p.),并逆转了对d-苯丙胺运动效应的超敏反应和对新生儿用苯环利定治疗的成年大鼠的选择性注意力缺陷(MED:1-3mg/kg i.p.)。最后,它增加了大鼠PFC中的细胞外多巴胺(MED:10 mg/kg i.p.)。该化合物在抑郁/焦虑模型中显示出额外的活性,例如小鼠的慢性轻度应激(10mg/kg i.p.),与母亲分离的大鼠幼崽的超声波求救信号(MED:1mg/kg s.c.),以及大鼠反常睡眠潜伏期的增加(MED:30mg/kg i.p.)。总之,SSR504734是一种强效且选择性的GlyT1抑制剂,在精神分裂症、焦虑和抑郁模型中表现出活性。通过针对精神分裂症的主要原因之一(低血糖症),预计它不仅对阳性症状有效,而且对阴性症状、认知缺陷和合并抑郁/焦虑状态也有效[1]。 SSR504734阻断小鼠皮质匀浆中[14C]甘氨酸的体外摄取。 SSR504734增加自由运动大鼠前额叶皮层中甘氨酸的细胞外水平。 SSR504734增强大鼠海马切片中NMDA介导的兴奋性突触后电流。 SSR504734增加小鼠纹状体微量注射甘氨酸诱导的对侧旋转次数。 SSR504734对CB1受体激动剂WIN55212-2诱导的大鼠海马切片[3H]乙酰胆碱释放减少的拮抗作用。 SSR504734对CB1受体激动剂WIN55212-2诱导的前额叶皮层神经元放电率降低的拮抗作用。 SSR504734增加自由运动大鼠前额叶皮层细胞外多巴胺水平。 SSR504734阻断氯胺酮诱导的小鼠脑代谢活性增加。 SSR504734对MK-801诱导的小鼠运动亢进的拮抗作用。 SSR504734逆转MK-801诱导的大鼠皮层α1带绝对功率的增加。 SSR504734对新生儿期用苯环利定治疗的成年大鼠新奇辨别能力的损害和对d-苯丙胺急性攻击的超敏性的拮抗作用。 SSR504734逆转DBA/2小鼠启动反射脉冲前抑制的自发缺陷。 SSR504734可减少大鼠幼崽的超声波痛苦发声。 SSR504734改善慢性轻度应激小鼠的身体状态退化。 SSR504734降低大鼠矛盾睡眠[1]。 |
| 酶活实验 |
SSR504734及其(R,R)对映体SSR506204对体外[14C]甘氨酸摄取的影响[1]
人神经母细胞瘤(SK-N-MC)和大鼠星形细胞瘤(C6)细胞系在含有10%胎牛血清的生长培养基(SK-N-M细胞为MEM,C6细胞为HAM-F12)中,在37°C、5%CO2的加湿空气中进行单层培养。通过胰蛋白酶收集的细胞每周传代两次。Gomeza等人(1995)报道了C6细胞中GlyT1的存在。在SK-N-MC细胞中,GlyT1的存在评估如下:使用Trizol试剂分离细胞的总RNA,然后逆转录并进行PCR扩增(在93°C下进行1小时的初始变性步骤 在94°C下持续30分钟,共35个循环 s、 55°C,30 s、 1的温度为72°C min)在存在对三种已知GlyT1亚型之一特异性的两个引物的情况下进行(Kim等人,1994)。a亚型的有义引物为5′-TGC CAA AGG GAT GCT GAA TG-3′,b和c亚型的无义引物均为5′-GCG GCT CAT GGA CCT GTG-3′。这三种亚型共有的反义引物序列为5′-CGC AGA TGA GCA TGA TG-3′。为了确认,使用对每种人类GlyT1亚型特异的32P标记的内部寡核苷酸探针通过Southern印迹分析RT-PCR产物。印迹用Storm Phosphorimager扫描。 At 48 在[14C]甘氨酸摄取实验前h,细胞以20 000–30 000 对于SK-N-MC细胞,在预先涂有纤维连接蛋白或C6细胞涂有聚-D-赖氨酸的96孔培养皿中。200℃下进行了37°C的检测 μl HEPES缓冲液(HB),含有(以mM计)NaCl(147)、KCl(5)、MgCl2(2)、CaCl2(2,HEPES(10)、D-葡萄糖(10)和l-丙氨酸(5),pH 7.4。移除生长培养基,用HB洗涤后,将细胞孵育10分钟 用测试化合物进行测试。通过添加10开始摄取 μM[14C]甘氨酸(112.4 mCi/mmol;法国巴黎NEN生命科学产品公司)。非特异性摄取用10 mM未标记的甘氨酸。10之后 min,用HB洗涤细胞两次,并向孔中加入闪烁液。放射性是通过Wallac MicroBeta计数器中的液体闪烁来测量的。 结果表示为抑制50%(IC50)特异性[14C]甘氨酸摄取所需的药物浓度,并通过非线性回归分析获得。 SSR504734的受体选择性 通过使用标准方案或内部研究评估了SSR504734与约120种不同受体、离子通道、酶或转运蛋白的相互作用。 |
| 细胞实验 |
细胞活力测定[1]
细胞类型:人神经母细胞瘤 (SK-N-MC) 和大鼠星形细胞瘤 (C6) 细胞 测试浓度: 15 nM -86 μM 孵育时间:10 分钟 实验结果:对人 SK-N-MC 和大鼠 C6 细胞的 IC50 值分别为 18 和 15 nM , 分别。 |
| 动物实验 |
动物/疾病模型:雄性SD(Sprague-Dawley)大鼠[1]
剂量:1-100 mg/kg 给药途径:腹腔注射(ip)和灌胃(po);1-100 mg/kg;一次 实验结果:腹腔注射和灌胃给药的ID50值分别为5.0和4.6 mg/kg。 动物/疾病模型:雄性SD(Sprague-Dawley)大鼠[1] 剂量:30 mg/kg 给药途径:腹腔注射(ip);30 mg/kg; 实验结果:给药后1至7小时内抑制率维持在80%左右。 动物/疾病模型:雄性SD(Sprague-Dawley)大鼠[1] 剂量:10 mg/kg 给药途径:腹腔注射(ip);10 mg/kg;一次 实验结果:可快速且持续地提高前额叶皮层(PFC)细胞外甘氨酸水平。 SSR504734和SSR506204对离体[14C]甘氨酸摄取的影响[1] 雄性OF1小鼠(20-25 g)分别在腹腔注射(ip)或口服(po)给药后30分钟或60分钟处死。皮质组织被迅速解剖,并在冰上使用Polytron匀浆器进行匀浆(1 g组织对应10倍体积的冷HB缓冲液)。对新鲜匀浆进行测定时,首先向20 μl组织匀浆中加入10 μM [14C]甘氨酸(最终蛋白浓度:0.8–0.9 mg/ml)。非特异性摄取用10 mM未标记甘氨酸测定。摄取反应在25°C下进行10分钟,然后用MultiScreen真空歧管将匀浆液抽吸到MultiScreen玻璃纤维滤板上终止反应。滤板用冰冷的HB缓冲液洗涤两次,干燥后浸入闪烁液中。使用 Wallac MicroBeta 计数器通过液体闪烁法测量放射性。 口服 30 mg/kg SSR504734 后,分别在 5 分钟、15 分钟、1 小时、4 小时、7 小时、16 小时和 24 小时进行时间进程研究,采用上述方案。 结果以 [14C]甘氨酸摄取量相对于对照组(载体处理组)的百分比表示,并以通过非线性回归分析计算的抑制 50% 摄取量的化合物剂量 (ID50) 表示。对于时间进程实验,数据采用单因素方差分析(ANOVA)进行分析,随后进行事后Dunnett检验。 SSR504734对自由活动大鼠前额叶皮层细胞外甘氨酸水平的影响[1] 雄性Sprague-Dawley大鼠(280-330 g)每笼饲养两只。在透析测量前2天,用氯醛水合物(400 mg/kg,腹腔注射,10 ml/kg体重)麻醉大鼠,并将其固定于立体定位仪上。手术过程中,根据需要追加氯醛水合物以维持麻醉。通过直肠探针监测体温,并使用恒温毯将其温度调节至37±1°C。为了将引导套管植入内侧前额叶皮层(PFC),打开了颅骨和硬脑膜。其坐标为:前囟前2.5 mm,中线外侧0.6 mm,硬脑膜下1.3 mm。使用牙科水泥帽固定套管,并用三颗螺钉将水泥帽固定在颅骨上。术后,将大鼠单独饲养,并在实验开始前恢复2天。实验当天,将动物放入微透析碗中,移除套管的闭塞器,并将3 mm的微透析探针插入引导套管。使用微量注射泵以 1 μl/min 的恒定流速灌注探针,灌注液为含气林格氏液,成分为(mM):NaCl (145)、KCl (2.7)、CaCl2 (1.2)、MgCl2 (1)、Na2HPO4 (2.3) 和 NaH2PO4 (0.45);pH 7.4。探针置入 PFC 120 分钟后开始微透析取样。探针出口连接至在线衍生化系统(如前所述 (Bert 等,1996)),可直接分析每 15 分钟收集一次的透析液样品。 使用毛细管电泳 (CE) 结合激光诱导荧光检测法测定 15 μl 透析液样品中的甘氨酸水平。分析前,样品按照先前描述的方法(Bert et al, 1996)使用萘-2,3-二甲醛和氰化钠进行衍生化。毛细管电泳实验在P/ACE MDQ毛细管电泳系统上进行,该系统与外部Zetalif荧光检测器联用。激发光源为波长442 nm的Omnichrome氦镉激光器,激发功率为30 mW。发射强度在490 nm波长处测量。分离采用内径50 μm、外径375 μm、总长度55 cm、有效长度38.9 cm的熔融石英毛细管,施加电压为25 kV(即电流为65 μA)。使用pH 10.5、含β-环糊精(1 mM)的硼酸盐缓冲液(75 mM)进行毛细管电泳 (CE)。实验结束后,通过探针注入天蓝色溶液,并用戊巴比妥钠过量处死动物。取出脑组织,冷冻后用冰冻切片机切取50 μm厚的切片,以验证微透析探针的正确放置。将各组分样本中的甘氨酸水平转化为治疗前90分钟基线测量平均值的百分比。采用双因素方差分析 (ANOVA) 分析SSR504734和SSR506204对甘氨酸水平的时间进程影响,其中治疗作为组间因素,采样时间作为组内因素,随后进行Dunnett事后检验。通过比较药物或赋形剂腹腔注射后前 180 分钟的曲线下面积来评估 SSR504734 的剂量效应。采用单因素方差分析 (ANOVA) 和 Dunnett 事后检验进行统计分析。 SSR504734 对大鼠海马切片中诱发的 NMDA 介导的兴奋性突触后电流的影响 [1] 将 Sprague-Dawley 大鼠(17-22 日龄)处死,取出其脑组织,并在人工脑脊液 (aCSF) 溶液中用 Campden 752M 微型切片机将其切成冠状切片(厚度为 0.3 mm)。aCSF 溶液的成分为(单位:mM):NaCl (126)、KCl (3)、MgCl2 (1)、KH2PO4 (1)、CaCl2 (1)、NaHCO3 (25) 和葡萄糖 (11),pH 7.35,温度约为 0°C,并用 95% O2 和 5% CO2 混合气体进行通气。在室温下用人工脑脊液 (aCSF) 浸泡至少 1 小时后,将脑片转移至记录室,并持续用 30–32°C 的 aCSF 灌流。使用硼硅酸盐玻璃电极(电阻:4–7 MΩ)进行 CA1 层锥体细胞的膜片钳全细胞记录,电极内填充 290 mosmol 的溶液,该溶液含有(单位:mM)KMeSO4 (130)、EGTA (10)、ATP (2)、GTP (0.5) 和 QX314 (5);pH 7.2。SSR504734 和 SSR506204 对小鼠纹状体内微量注射甘氨酸诱导的对侧旋转的影响[1] 实验前 1 周,将雌性 CD1 小鼠(25–27 g)以每笼 10 只为一组饲养。微注射程序的详细信息已在其他地方发表(Poncelet 等人,1993)。在纹状体内微注射甘氨酸(0.001 ng,亚阈值剂量)前 30 分钟,腹腔注射 SSR504734、SSR506204 或载体。在另一项实验中,在注射SSR504734(1 mg/kg ip)或载体前15分钟,注射MK-801(0.03 mg/kg ip)或载体,30分钟后,微量注射0.001 ng甘氨酸。 SSR504734和SSR506204对WIN55212-2诱导的大鼠海马切片中[3H]乙酰胆碱释放减少的影响[1] 雄性OFA大鼠(250-350 g)被断头处死,迅速取出脑组织,并在冰冷的铝块上解剖海马。解剖后,使用振动切片机将组织切成350 μm厚的切片,并将切片转移至20 ml Krebs缓冲液(pH 7.4)中,该缓冲液饱和95% O₂和5% CO₂,并含有20 μM [³H]胆碱(86 Ci/mmol)。在37°C下与放射性标记物孵育30分钟后,将切片转移至18个灌流室(每个灌流室3片)。在37°C下,以0.5 ml/min的流速,用含10 μM半胆碱的氧合Krebs缓冲液灌流切片,以防止[³H]胆碱的再摄取。45分钟的冲洗期后开始收集样品。随后收集两个3分钟的馏分,以测量基础释放量。在第五个采集期加入大麻素-1 (CB1) 受体激动剂 WIN55212-2 (10⁻⁶ M),并持续至实验结束。在加入 WIN55212-2 前 9 分钟加入 SSR504734。用电刺激(矩形脉冲,2 Hz,2 ms,1 mA)诱导 [³H]乙酰胆碱 ([³H]ACh) 释放 3 分钟,之后加入原始的 Krebs 缓冲液以恢复基础释放水平。结果以对照组抑制百分比表示。数据采用单因素方差分析 (ANOVA) 和 Dunnett 事后检验进行分析。使用加权线性曲线拟合程序,通过四参数逻辑模型确定了SSR504734作用的IC50值。 SSR504734和SSR506204对WIN55212-2诱导的前额叶皮层神经元放电率降低的影响[1] 雄性Sprague-Dawley大鼠(280-400 g)用水合氯醛(400 mg/kg,腹腔注射)麻醉后,固定于立体定位仪上。实验过程中,通过追加水合氯醛维持麻醉深度。使用电加热垫将动物体温维持在37±0.1°C。手术完成后,在待探查区域上方的颅骨上钻取小孔。使用尖端直径为1 μm的玻璃微电极进行细胞外记录,电极内填充1 M NaCl溶液或含2% Pontamine Sky Blue的0.5 M醋酸钠溶液(100 Hz时阻抗为4–7 MΩ)。电极指向内侧前额叶皮层(PFC)细胞:分别位于前囟前方2.9–3.2 mm和外侧0.6–0.8 mm处,皮层表面下方2.2–3.6 mm处(Paxinos和Watson,1998)。液压微驱动器可实现精细的三维电极移动。动作电位(尖峰)经放大、滤波(400 Hz–5 kHz)后,在数字示波器和音频放大器上进行监测。将电位输入窗口鉴别器,并使用连接至运行 CED“Spike2”软件的 PC 的“μ1401 智能实验室接口”进行在线分析。 放电率直方图以连续模式运行(10 秒窗口大小)。在首次静脉注射 SSR504734、SSR506204 或载体(50 μl 1 N HCl + 蒸馏水,剂量为 1 ml/kg v/w)之前,允许放电率稳定 10-15 分钟。在注射测试药物(或载体)10 分钟后,静脉注射 WIN55212-2(0.1 mg/kg)。然后至少再监测 30 分钟的放电率。每只大鼠记录一个细胞。所有静脉注射均在 1 分钟内完成。 SSR504734 对自由活动大鼠前额皮质多巴胺细胞外水平的影响[1] 注:一些作者(Kapur 和 Remington,1996)认为,某些非典型抗精神病药物增强前额皮质多巴胺能神经传递的能力,是其对精神分裂症患者的阴性症状和认知缺陷产生有益影响的基础。因此,我们也测量了SSR504734增强该结构中细胞外多巴胺张力的能力。 SSR504734对氯胺酮诱导的小鼠脑代谢活性增加的影响[1] 实验前1周,将雄性OF1小鼠(28-37 g)每笼饲养10只。实验当天,在给药前至少1小时将它们单独饲养在笼中。在腹腔注射溶剂或SSR504734,注射前30分钟腹腔注射氯胺酮(30 mg/kg)或生理盐水(选择氯胺酮而不是PCP或MK-801,是因为它是Duncan等人1998a年首项研究中使用的化合物)。在注射氯胺酮或生理盐水2分钟后,将2-脱氧-D-[1-14C]葡萄糖(2-DG)溶液(13 μCi溶于0.3 ml生理盐水中,20秒内)缓慢注入小鼠尾静脉。静脉注射2-DG 5分钟后,将小鼠断头处死。取出脑组织后,浸入冷却的异戊烷(−45°C)中冷冻,然后储存在约−80°C直至切片。 SSR504734 和 SSR506204 对 MK-801 诱导的小鼠运动过度症的影响 [1] 雄性瑞士小鼠(18–21 g)被单独隔离在盒子中,并预先腹腔注射 SSR504734、SSR506204 或载体,随后立即腹腔注射载体或 MK-801(0.2 mg/kg)。第二次注射后 30 分钟,将小鼠放入活动记录仪(直径 20 cm,高 9.5 cm;Apelex,法国)中,该活动记录仪配备两束垂直光束,光束距离地面 1.5 cm。将小鼠放入活动记录仪后,记录其运动活性(光束中断次数),持续 30 分钟。数据采用单因素方差分析 (ANOVA) 进行分析,随后进行 Dunnett 事后检验。 SSR504734 对 MK-801 诱导的大鼠 Alpha1 波段光谱能量增加的影响 [1] 雄性 Sprague-Dawley 大鼠(220-240 g)用戊巴比妥钠(50 mg/kg,腹腔注射)麻醉,并固定在立体定位仪上。皮层电极(直径 0.9 mm 的小型不锈钢螺钉)被旋入感觉运动皮层(位于正中缝外侧 1.5 mm,额顶缝后方 1.5 mm)、视觉皮层(位于正中缝外侧 1.5 mm,顶枕缝前方 1.5 mm)和小脑(参考电极)的骨骼中。皮层电极焊接至用牙科水泥固定于颅骨上的微型连接器。 术后恢复 3 周后,将动物置于有机玻璃圆筒(直径 60 cm)中,可自由获取食物和水。为了研究 SSR504734 对 MK-801 诱导的 α1 频谱能量增加的影响,在进行 15 分钟脑电图 (EEG) 记录后(第一阶段:对照组),腹腔注射载体或 SSR504734,15 分钟后腹腔注射 MK-801 (0.2 mg/kg)。脑电信号经放大和滤波 (1–100 Hz) 后,使用计算机系统(“Coherence 32”软件,Deltamed,巴黎,法国)自动进行连续频谱分析。信号以 128 Hz 的采样率进行傅里叶变换,从而计算功率变量 (μV²)。每隔30秒计算一次脑电信号的绝对功率谱,频率范围为0.5至32 Hz,步长为0.5 Hz,并分别计算以下频段的功率谱:δ波段(0.5–3.5 Hz)、θ波段(θ1:4–6 Hz;θ2:6.5–8 Hz)、α波段(α1:8.5–11 Hz;α2:11.5–13.5 Hz)和β波段(14–32 Hz)。由于MK-801在0.2 mg/kg腹腔注射剂量下可显著增加α1波段的绝对功率,因此本研究采用该剂量进行测试。 在给予MK-801前15分钟,以及注射后1小时内每隔10分钟,对α1波段的脑电功率谱进行平均。通过计算腹腔注射前后绝对功率的比值来评估药物引起的改变。在对照期(设为100%)注射SSR504734或载体对绝对功率的影响,并以对照期功率的百分比表示。 SSR504734对新生期苯环利定处理的成年大鼠新奇辨别能力受损的影响[1] 在出生后第3天(PN 3)获得10只雄性幼鼠,均为雌性Wistar Han大鼠。在PN 7、9和11,幼鼠分别接受10 mg/kg PCP(皮下注射,1 ml/100 g体重)或载体处理。同一窝的幼鼠接受相同的处理。母鼠和幼鼠共同饲养至PN 21断奶,断奶后幼鼠每笼饲养5只,直至行为实验开始前2周,之后改为单独饲养。行为实验在幼鼠达到成鼠期(出生后第60天至第108天之间)后进行。 实验在黑暗期进行,采用红外照明(15勒克斯)。幼鼠在放入成年鼠的笼子前先隔离30分钟。笼子置于摄像机下方,移除网状顶盖并更换为有机玻璃盖。首先将一只(熟悉的)幼鼠放入装有成年鼠的笼子中,持续30分钟。30分钟后,放入第二只(陌生的)幼鼠。在放入陌生幼鼠后的5分钟内,由位于隔壁房间的观察员通过视频监视器手动记录成年鼠与两只幼鼠之间的探索行为(嗅闻、嗅探、梳理毛发、追逐幼鼠)。在成年大鼠接触第一只幼鼠前 30 分钟,腹腔注射 SSR504734 或载体。每只成年大鼠接受四次处理:一次载体处理和三次 SSR504734 处理。每次处理间隔 1 或 2 天。 SSR504734 对新生期接受苯环利定治疗的成年大鼠急性 d-苯丙胺激发超敏反应的影响 [1] 本实验中使用的成年大鼠与新奇辨别实验中使用的大鼠相同。实验开始前 1 小时,将动物放入实验室。然后将它们放入活动箱(40 × 40 × 30 cm 的有机玻璃箱)中,活动箱内装有红外光束(光束间距 2.5 cm,距地面 2.5 cm)。首先评估其基础运动活性,持续30分钟(适应期)。适应期结束后,腹腔注射SSR504734或溶剂,并放回活动记录仪中。30分钟后,再次腹腔注射d-安非他明(2 mg/kg)或溶剂,并测量其运动活性90分钟。每只大鼠接受五种处理:两种溶剂处理(单独使用和与d-安非他明联合使用)和三种剂量的SSR504734与d-安非他明联合使用。两次治疗之间至少间隔3天。数据以红外光束中断的平均次数表示,并采用重复测量双因素方差分析进行分析,其中新生儿期治疗作为组间因素,成年期急性治疗作为组内因素,随后进行适当的事后检验。 SSR504734对DBA/2小鼠惊吓反射预脉冲抑制自发性缺陷的影响[1] 雄性DBA/2J小鼠(22-26克)以4只为一组饲养于笼中。小鼠到达后13天进行选择实验(见下文)。小鼠在六个惊吓箱中进行测试。惊吓反射由位于惊吓平台下方的压电加速度计检测和转换,并由运行SR-LAB软件(该软件也控制所有其他事件)的微型计算机进行数字化和存储。首先将小鼠置于固定在惊吓平台顶部的有机玻璃约束圆筒(长3.7厘米,宽12.8厘米)内。然后开始选择实验:经过5分钟的适应期后,施加20次刺激(刺激间隔可变:5-25秒,以5秒为步长)——17次惊吓脉冲刺激(P;持续时间40毫秒,强度120分贝),穿插3次强度为30分贝的预脉冲,随后施加一次脉冲刺激(p30/P)。对于最后三个刺激,预脉冲持续时间为20毫秒,强度为88分贝(即比58分贝的背景噪声高30分贝),脉冲与上述相同,预脉冲结束与脉冲开始之间间隔100毫秒。音频刺激使用声级计(型号CDA 830,Chauvin Arnoux,法国)进行校准(±2分贝,A标度)。惊吓平台使用SR-LAB校准器标准化单元进行校准,平台间差异小于3%。在惊吓刺激出现后的100毫秒内记录惊吓反射(采样间隔:1毫秒)。惊吓幅度定义为受惊小鼠对平台施加的向下力的峰值幅度。实验过程中,小鼠均处于黑暗环境中。本次筛选环节用于将小鼠按基础惊吓反应水平相似进行分组,以便后续测试。 第二天(测试环节),小鼠在放入约束筒前30分钟腹腔注射载体或SSR504734。测试环节首先进行5分钟的适应期,随后单独给予4个脉冲(P)。之后进行两组相同的刺激:每组包含26个刺激,分为五种条件:10个无预脉冲的惊吓脉冲(P)、4个前有6 dB预脉冲的惊吓脉冲(p6/P)、4个前有18 dB预脉冲的惊吓脉冲(p18/P)、4个前有30 dB预脉冲的惊吓脉冲(p30/P)以及4个无预脉冲且无脉冲的刺激(nop/noP)。五种条件以伪随机顺序呈现。除此之外,所有其他参数均与上述选择阶段的参数相同。 SSR504734 和 SSR506204 对幼鼠超声波应激发声的影响 [1] 从出生后第 3-4 天(PN 3-4)的雌性 Sprague-Dawley 大鼠中获取 10 只雄性幼鼠。实验流程参考 Gardner (1985) 的方法,具体如下:首先将每只幼鼠(PN 7)与母鼠和同窝幼鼠分开,皮下注射 0.1 ml SSR504734 或载体,然后放回母鼠身边。30 分钟后,将幼鼠放入隔音笼中。使用 Ultravox 系统记录超声波发声(UV,频率范围为 40 kHz)。首先,使用连接到驻极体麦克风(放置在幼犬旁边)的改良型超声波探测器(Mini-3蝙蝠模型)将超声波转换为可听声音。然后,对信号进行滤波(用户定义频率范围和振幅阈值),并将其发送到电脑,UltraVox软件记录3分钟测试期间的每次超声波发声。 SSR504734在小鼠慢性轻度应激程序中的作用[1] 慢性轻度应激(CMS)方案最初由Willner等人(1992)描述用于大鼠,该方案改编自Kopp等人(1999)描述的用于小鼠的方案。该实验包括依次施加一系列轻度应激,例如束缚、强迫游泳、剥夺水和/或食物、与另一只受应激动物配对,每种应激持续2至24小时不等,整个实验周期为3周,并根据需要重复进行直至实验结束。 在慢性应激(CMS)开始2周后,开始腹腔注射SSR504734(10 mg/kg)。该剂量已在神经化学和行为模型中证实对小鼠有效。动物(BALB/c雄性小鼠,实验开始时体重21-28克)每天腹腔注射一次,直至所有实验完成(33天)。 SSR504734和SSR506204对自由活动大鼠睡眠/觉醒周期的影响[1] 手术步骤的详细信息如“SSR504734对MK-801诱导的大鼠α1波段频谱能量增加的影响”一文中所述。 记录在连续3天的11:00至17:00进行:预对照(第1天)、药物激发(第2天)和后对照(第3天)。以小脑电极为参考电极记录感觉运动皮层和视觉皮层的脑电活动。睡眠分为三个阶段:清醒期(W;以低电压脑电活动为特征)、慢波睡眠期(SWS;以脑电活动增强为特征,即高振幅慢波伴有少量睡眠纺锤波爆发)和异相睡眠期(PS;以视觉皮层θ节律过度同步为特征)。脑电信号分析由计算机系统自动完成,该系统利用频谱频率分析区分不同的睡眠阶段(“Coherence 32”软件,Deltamed,巴黎,法国)。在记录前15分钟,分别腹腔注射载体(第1天和第3天)、SSR504734或SSR506204(第2天)。在 6 小时内分析了化合物对 W、SWS、PS 期间所花费的时间、PS 发作次数以及进入 PS 的潜伏期的影响,并以第 1 天获得的对照值的百分比表示。对于每种处理,使用单因素重复测量方差分析对原始值进行统计分析,然后进行 Dunnett 事后检验(第 1 天作为对照)。 |
| 药代性质 (ADME/PK) |
外周给药SSR504734可剂量依赖性地抑制小鼠大脑皮层对离体特异性[14C]甘氨酸的摄取。腹腔注射和口服给药的ID50值分别为5.0和4.6 mg/kg,口服/腹腔注射比值接近于1,表明其具有良好的口服生物利用度(图2a)。[1]
|
| 毒性/毒理 (Toxicokinetics/TK) |
SSR504734 的安全性概况 [1]
SSR504734 在小鼠腹腔注射剂量高达 30 mg/kg 时未引起僵直(数据未显示),表明其不会引起患者锥体外系症状;在这方面,它与目前常用的非典型抗精神病药物(如氯氮平、氨磺必利、奥氮平和喹硫平)相符。此外,它不会升高大鼠的催乳素水平(腹腔注射剂量高达 30 mg/kg;数据未显示),而催乳素升高是大多数抗精神病药物的常见副作用。 |
| 参考文献 | |
| 其他信息 |
SSR504734 是一种强效、选择性强且口服有效的 GlyT1 抑制剂,在精神分裂症和焦虑/抑郁症动物模型中均显示出活性。大量体外、离体和体内试验表明,其活性具有对映选择性,因为其 (R,R) 对映体 SSR506204 活性较低或无作用。其作用机制针对被认为是精神分裂症主要病因之一的谷氨酸能低下状态。因此,预计它不仅对阳性症状有效,而且对阴性症状和认知缺陷以及共病的抑郁和焦虑状态也有效。一项最新的双盲安慰剂对照研究结果进一步强化了GlyT1抑制剂作为治疗精神分裂症新疗法的潜在用途。该研究表明,弱效GlyT1抑制剂肌氨酸与利培酮联合使用,可显著减轻精神分裂症的阳性症状、阴性症状和认知症状,其疗效与之前使用完全甘氨酸位点激动剂D-丝氨酸所观察到的疗效相当(Tsai等,2004)。[1]这是首篇详细阐述新型选择性可逆GlyT1抑制剂SSR504734的神经化学、电生理和药理学特性的报告。文献中已报道过其他 GlyT1 阻断剂,但它们的亲和力极低(肌氨酸、十二烷基甘氨酰酰胺)或阻断作用的不可逆性(ALX5407)使得它们在 GlyT1 的药理学研究中吸引力不足。
SSR504734 是一种体外和离体选择性 GlyT1 阻断剂 [1] SSR504734 能有效阻断表达 GlyT1a 亚型的天然人 SK-N-MC 细胞系以及含有 GlyT1 的大鼠 C6 细胞系中 [14C]甘氨酸的摄取。SSR504734 的这种作用具有立体选择性,因为其 (R,R) 对映体 SSR506204 的效力远低于前者。 SSR504734 抑制人源和鼠源 GlyT1 转运蛋白上的甘氨酸转运(IC50 约为 20 nM),其效力介于 ALX5407(3 nM,Atkinson 等,2001;220 nM,Herdon 等,2001,均针对 hGlyT1c;26 nM,针对 hGlyT1b,Smith 等,2004;10 nM,针对 rGlyT1a,Kinney 等,2003)和 ORG 24598(120 nM,针对 hGlyT1b,Brown 等,2001)之间,远高于肌氨酸或十二烷基甘氨酰酰胺这两种早期的 GlyT1 抑制剂(IC50 大于 10 μM;本研究结果;Javitt 和 Frusciante)。 1997)。SSR504734 在小鼠中也表现出类似的效力(IC50:38±5 nM,在皮质匀浆中,未在“材料与方法”和“结果”部分报告),这一点我们通过在多项实验中使用小鼠进行了验证。SSR504734 在体外对 GlyT2、谷氨酸、GABA、DA 和 5-羟色胺转运体均无活性。与目前的抗精神病药物不同,它对 DA 受体以及其他与各种副作用相关的受体没有亲和力,例如体重增加(5-HT2c、组胺能 H1 受体)、低血压(α 肾上腺素能受体)、口干/便秘/认知障碍(毒蕈碱受体)和镇静(组胺能受体)等等。 离体实验表明,腹腔注射和口服给药后,SSR504734 可阻断小鼠皮质匀浆中甘氨酸的摄取。对离体阻断甘氨酸摄取的时间进程分析表明,与ALX5407(未发表数据)相反,SSR504734的抑制作用是可逆的。在体外实验中也观察到了SSR504734的可逆性(海马切片中EPSC的增强),而ALX5407则不具有这种可逆性。 SSR504734 对 GlyT1 阻断作用的可逆性至关重要,因为不可逆阻断可能构成该化合物在临床应用中的一个潜在缺点。 SSR504734 对 GlyT1 的阻断作用可增强前额叶皮层中甘氨酸和多巴胺的细胞外水平 [1] 在微透析实验中,SSR504734(10 mg/kg,腹腔注射)提高前额叶皮层(PFC)甘氨酸基础水平的效力和功效至少与 ALX5407(10 mg/kg,腹腔注射或口服;未发表数据;Atkinson 等,2001)相当。SSR504734 提高大鼠前额叶皮层(PFC)中甘氨酸和多巴胺细胞外水平的能力预计会产生多种后果。在与精神分裂症表现密切相关的脑结构中,前额叶皮层(PFC)占据着特殊的地位。越来越多的证据表明,PFC功能减退与阴性症状和认知缺陷的产生密切相关(Goldman-Rakic和Selemon,1997),而这些症状和缺陷越来越被认为是精神分裂症病理的核心。至少有两种神经递质系统的缺陷被认为是导致PFC功能减退的原因:NMDA/谷氨酸能系统和多巴胺能系统(Goldman-Rakic和Selemon,1997)。SSR504734增强前额叶甘氨酸能张力有望增强NMDA/谷氨酸能传递(见下文),并进一步平衡这种神经递质传递的不足。此外,现有抗精神病药物增强前额叶多巴胺(DA)张力的能力被认为是其缓解患者阴性症状和认知症状的神经化学标志物(Kapur和Remington,1996)。综上所述,这些数据表明,SSR504734凭借其双模式神经化学机制,可能有效对抗精神分裂症患者的阴性/认知缺陷。最后,前额叶皮层(PFC)多巴胺系统活性不足被认为会导致皮层下多巴胺能系统功能亢进,进而引发精神分裂症的阳性症状(Grace,1991)。由于SSR504734能够增强前额叶皮层(PFC)的多巴胺(DA)传递(从而降低皮层下DA张力),预计它对阳性症状也具有直接的益处,这一假设已得到行为学数据的进一步证实(见下文)。 SSR504734增强中枢甘氨酸能张力对中枢谷氨酸能神经传递具有功能性影响[1] SSR504734诱导的中枢甘氨酸水平升高对中枢谷氨酸能神经传递具有功能性影响,无论是在体外还是体内。在体外,SSR504734增强了大鼠海马切片中NMDA介导的兴奋性突触后电流(eEPSC)。与这些结果一致,Wilcox及其合作者(1996)的研究表明,从海马神经元记录到的NMDA受体介导的eEPSC可以被甘氨酸显著增强。一些证据表明,精神分裂症患者的海马体在细胞结构和神经化学水平上均存在异常(Heckers和Konradi,2002)。海马体与多种认知功能相关,其中包括情景记忆,而情景记忆在精神分裂症患者中受到影响(Rushe等,1999)。本研究数据,结合SSR504734(论文撰写中)以及两种GlyT1抑制剂NFPS(Kinney等,2003)和CP 802,079(Martina等,2004)在体内增强海马体长期增强作用的实验结果,提示GlyT1抑制剂可能对精神分裂症中海马依赖性记忆缺陷具有有益作用。此外,在麻醉大鼠中,SSR504734增强了由杏仁核电刺激诱发的伏隔核多巴胺伏安信号。由于该多巴胺信号已被证实依赖于NMDA受体,因此这种增强作用为SSR504734阻断GlyT1后NMDA神经传递的增强提供了补充证据(Leonetti等人,投稿中)。 全身给药SSR504734可剂量依赖性地增加小鼠纹状体内注射亚阈剂量甘氨酸诱发的对侧旋转次数,并且发现单独单侧微量注射SSR504734到纹状体也能诱发对侧旋转。 SSR504734 的作用可被 MK-801 拮抗,而 MK-801 本身在该剂量下并无作用,这进一步表明行为输出的增强(旋转次数增加)是谷氨酸能/NMDA 神经传递增强的结果。 这些体外和体内实验结果共同强化了以下观点(Bergeron 等,1998;Chen 等,2003):NMDA 受体附近的甘氨酸浓度由 GlyT1 维持在亚饱和水平,而通过阻断该转运蛋白增加甘氨酸浓度会导致 NMDA 介导的功能增强。 SSR504734 可使两个被认为与精神分裂症相关的脑结构中 NMDA/谷氨酸能系统的功能低下恢复正常 [1] 在被怀疑与精神分裂症相关的脑结构中,在精神分裂症的病因学中,海马和前额叶皮层(PFC)占据着重要地位。研究反复表明,海马在患者中存在细微的神经解剖学异常(Heckers和Konradi,2002),而前额叶皮层功能减退被认为在阴性症状的发生中发挥作用(Goff和Evins,1998)。两者都与认知功能(特别是记忆和注意力过程)的控制有关,而这些认知功能在精神分裂症的病理过程中会受到影响。突触前CB1受体负向调节兴奋性突触传递,这可能是通过阻断神经递质(特别是谷氨酸)的释放来实现的(综述见Schlicker和Kathmann,2001)。CB1受体激动剂,例如WIN55212-2,已被证明可以抑制大鼠海马切片中[3H]ACh的释放(Gifford和Ashby,1996)。本研究表明,在类似的体外海马制备模型中,SSR504734几乎完全逆转了WIN55212-2介导的[3H]ACh外流减少。使用10⁻⁵ M NMDA或10⁻⁴ M甘氨酸也获得了类似的逆转效果(数据未显示),这强烈提示SSR504734的作用与NMDA受体的激活有关。考虑到胆碱能系统在记忆过程中的重要性(Gold,2003),SSR504734能够重建中枢胆碱能传递的正常水平,预示着该化合物可能具有治疗记忆障碍的活性,不仅在精神分裂症中,而且可能在其他疾病(例如阿尔茨海默病)中也有效。总而言之,这些数据补充了eEPSCs实验中获得的数据(见上文),并提供了强有力的实验证据,表明SSR504734可以分别对基础或降低的海马神经元活动产生促进或正常化作用。 在麻醉大鼠中,WIN55212-2诱导的前额叶皮层(PFC)神经元自发放电率降低,可通过给予SSR504734完全逆转。PFC的正常功能密切依赖于谷氨酸能神经传递,主要通过谷氨酸/NMDA系统,而该系统的紊乱与精神分裂症有关(参见Konradi和Heckers,2003年的综述)。体外实验表明,CB1受体激动剂可以抑制包括PFC在内的多个脑区的谷氨酸能突触传递(Auclair等,2000)。 SSR504734 对降低的前额叶皮层 (PFC) 神经元活动的恢复,进一步证实了通过阻断 GlyT1 增强甘氨酸能张力可以逆转该结构的功能减退(至少在电生理参数方面)。因此可以预期,这种化合物能够重建精神分裂症患者疑似功能减退的大脑结构(前额叶皮层)的正常神经元活动。需要强调的是,可以排除SSR504734在这两项实验([3H]ACh海马流出和PFC自发放电率)中的有益作用源于其对CB1受体的直接拮抗活性,因为该化合物未显示出对CB1受体的亲和力(IC50>1 μM)。SSR504734在多种预测抗精神病活性的测试中均显示出活性[1] 在多种神经化学和行为学测试中获得了SSR504734潜在抗精神病活性的证据,这些测试被认为可以检测其对精神分裂症阳性症状和/或阴性症状的疗效。 2-DG摄取增加被认为反映了代谢率的增加,即神经元活性的增强。 SSR504734 可使小鼠急性亚麻醉剂量氯胺酮诱导的前额叶皮层 (PFC) 和其他皮层下边缘区域的 2-DG 摄取相对增加恢复正常。文献报道了氯胺酮诱导的类似 2-DG 摄取增加模式(Duncan 等,1998a,1998b;Miyamoto 等,2000)。急性给予非典型抗精神病药物(如氯氮平)可完全阻断这些增加,但典型抗精神病药物(如氟哌啶醇)则无效(Duncan 等,1998b)。临床研究表明,志愿者氯胺酮诱发的精神病症状与额叶皮层代谢活动增强呈正相关(Breier 等,1997;Vollenweider 等,1997)。 SSR504734 能降低小鼠皮层代谢活动的增强(这种增强是由谷氨酸能低下状态引起的),这表明该化合物可能具有对抗花斑症状的活性。 在行为学层面,SSR504734 能拮抗 MK-801 诱导的小鼠多动症以及大鼠皮层 α1 波段频谱能量的增加。Harsing 等人 (2003) 报道了 NFPS 和/或 ORG 24461 对 PCP 诱导的小鼠多动症和大鼠脑电图频谱功率变化具有类似的作用。在我们看来,MK-801 诱导的过度活跃和脑电图模式改变对氟哌啶醇和氯氮平敏感,这可能表明这些测试中的活动仅能预测对阳性症状的疗效,因为氟哌啶醇对阴性症状和认知缺陷的疗效较差。 如先前报道(Olivier 等,2001;Kinney 等,2003),DBA/2 小鼠的惊吓反射 PPI 基础水平较低。换句话说,它们表现出自发性 PPI 缺陷。SSR504734 呈剂量依赖性地增强了 PPI 水平,即减少了这种先天性 PPI 缺陷。在DBA/2小鼠中,氯氮平、氟哌啶醇和利培酮治疗后也报道了类似的逆转效应(McCaughran等,1997;Olivier等,2001),最近,NFPS的活性更强的对映体(+)NFPS也具有类似的逆转效应(Kinney等,2003)。此外,甘氨酸和ORG 24598(ORG 24461的活性R(−)对映体)也被发现能够逆转新生期腹侧海马损伤成年大鼠的PPI缺陷(Le Pen等,2003)。所有这些数据都强调了促甘氨酸能策略在逆转不同性质的PPI缺陷方面的潜力。已知精神分裂症患者存在前脉冲抑制(PPI)缺陷(Braff等人,1978),这被认为是潜在信息处理能力异常的外显表现。SSR504734的作用表明,该化合物可能缓解这种异常,而这种异常被认为是该病理表现的关键因素。 新生儿PCP模型基于精神分裂症的神经发育概念(Weinberger,1986;Lieberman等人,1997)。Wang及其同事(2001,2003)的研究表明,给幼鼠注射高剂量PCP会导致其在青春期或成年期出现与神经元改变相关的长期行为改变。研究发现,SSR504734 对新生期接受 PCP 处理的成年大鼠在两个与病理相关的行为方面具有有益作用:(1) 对 d-安非他明急性刺激的超敏反应(在精神分裂症患者急性精神病发作期间曾有报道;Laruelle,2000);(2) 选择性注意缺陷(一种在精神分裂症中严重受损的认知过程,被认为是该疾病的主要特征;Brébion 等,2000)。SSR504734 对前者的有益作用与最近的研究结果相一致,即长期使用 NFPS 或甘氨酸可阻止 PCP 长期给药引起的纹状体中 d-安非他明诱导的多巴胺释放增强(Javitt 等,2004)。如果这种对右旋安非他明的超敏反应反映了皮层下多巴胺系统的异常敏感性,从而导致精神分裂症患者出现明显的症状(Laruelle,2000),那么SSR504734的抑制作用则为该化合物可能具有对抗阳性症状的活性提供了额外的实验证据。SSR504734能够使大鼠选择性注意障碍和DBA/2小鼠自发性PPI(一种信息处理的潜在标志物)缺陷恢复正常,这表明SSR504734有望对精神分裂症患者受损的认知过程产生有益作用。此外,最近的研究表明,直接甘氨酸激动剂D-丝氨酸能够逆转新生大鼠在空间记忆任务中因类似PCP处理而产生的有害影响(Andersen和Pouzet,2004),这进一步支持了这样一种观点:促甘氨酸能策略可能对精神分裂症的多种认知缺陷产生积极影响。这一方面值得进一步研究。 SSR504734具有额外的抗抑郁/抗焦虑样活性[1] SSR504734在预测抗抑郁和/或抗焦虑活性的测试中表现出活性。急性给药后,它能减少与母鼠分离的幼鼠的超声波求救信号,这与抗抑郁药氟西汀以及苯二氮卓类和5-HT1A受体激动剂等抗焦虑药的效果相似(Gardner,1985;Fish等,2000)。 SSR504734还能延长进入异相睡眠阶段的潜伏期,这种效应通常见于氟西汀和丙咪嗪等抗抑郁药(Slater等,1978;Kleinlogel,1982)。此外,长期服用SSR504734还能预防接受慢性应激(CMS)的小鼠出现生理退化,这种效应与其他已知的或潜在的抗抑郁/抗焦虑化合物(如氟西汀或促肾上腺皮质激素释放因子(1)受体拮抗剂SSR125543)相似(Griebel等,2002)。总而言之,这些药理学数据与最近一份初步报告的结果相符,该报告指出GlyT1杂合敲除小鼠的焦虑水平有所降低(Vanhoof等人,2004)。 SSR504734的抗抑郁/抗焦虑潜力似乎与其他临床前数据相矛盾,后者显示抗谷氨酸能化合物,如PCP和MK-801(非竞争性拮抗剂),或CCP、CPPene和CGS 19755(竞争性拮抗剂),在某些焦虑动物模型中具有疗效(参见Bergink等人,2004的最新综述)。然而,这些抗谷氨酸能化合物的抗焦虑潜力不仅尚未在临床层面得到证实,甚至有迹象表明这些化合物可能具有致焦虑特性。一项针对焦虑症患者的MK-801开放性试验因大多数患者症状加重而中止(Reimherr等人,1986)。此外,据报道CPPene会引起躁动不安,而CGS 19755(selfotel)会引起头晕、焦虑、烦躁和意识混乱(参见Muir和Lees,1995年的综述)。鉴于这些临床考量,增强NMDA/谷氨酸能传递的化合物(例如SSR504734)可能具有抗焦虑/抗抑郁活性,这种可能性并非完全不合理。目前正在对SSR504734在其他预测抗抑郁和/或抗焦虑活性的模型中的特征进行更深入的研究。无论如何,焦虑和抑郁状态是精神分裂症患者常见的两种共病因素,被认为是该疾病发作间期的关键因素,因此积极治疗这些因素可以延缓和/或减轻后续发作的严重程度,并有助于更好地稳定病情。 |
| 分子式 |
C20H20CLF3N2O
|
|---|---|
| 分子量 |
396.833814620972
|
| 精确质量 |
396.121
|
| 元素分析 |
C, 60.53; H, 5.08; Cl, 8.93; F, 14.36; N, 7.06; O, 4.03
|
| CAS号 |
742693-38-5
|
| 相关CAS号 |
615571-23-8
|
| PubChem CID |
9954540
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
4.7
|
| tPSA |
41.1
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
496
|
| 定义原子立体中心数目 |
2
|
| SMILES |
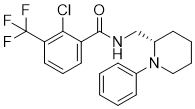
ClC1C(C(F)(F)F)=CC=CC=1C(N[C@@H](C1C=CC=CC=1)[C@@H]1CCCCN1)=O
|
| InChi Key |
MEZRZVWPLXVLSO-WMZOPIPTSA-N
|
| InChi Code |
InChI=1S/C20H20ClF3N2O/c21-17-14(9-6-10-15(17)20(22,23)24)19(27)26-18(13-7-2-1-3-8-13)16-11-4-5-12-25-16/h1-3,6-10,16,18,25H,4-5,11-12H2,(H,26,27)/t16-,18-/m0/s1
|
| 化学名 |
2-chloro-N-[(S)-phenyl-[(2S)-piperidin-2-yl]methyl]-3-(trifluoromethyl)benzamide
|
| 别名 |
615571-23-8; SSR504734; SSR 504734; SSR 504734 hydrochloride; SSR-504734; L297UZF32G; 2-chloro-3-(trifluoromethyl)-N-((S)-phenyl((S)-piperidin-2-yl)methyl)benzamide hydrochloride; 2-Chloro-N-[(S)-phenyl-[(2S)-piperidin-2-yl]methyl]-3-(trifluoromethyl)benzamide;hydrochloride;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮和光照。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5200 mL | 12.5999 mL | 25.1997 mL | |
| 5 mM | 0.5040 mL | 2.5200 mL | 5.0399 mL | |
| 10 mM | 0.2520 mL | 1.2600 mL | 2.5200 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。