| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Histone demethylase KDM2/7
|
|---|---|
| 体外研究 (In Vitro) |
在MALDI试验中,TC-E 5002/compound 9对KDM7B的活性是6的20倍。化合物9在KDM7B活性位点的对接表明,化合物9的环丙基通过CH−π或环丙基−π相互作用与Phe 250的苯基相互作用(图2)。此外,化合物9抑制KDM2A(也称为JHDM1A, FBXL11), KDM7A(也称为JHDM1D, KIAA1718)和KDM7B,显示出对所有KDM2/7亚家族成员的抑制作用(表2和3)。化合物9对KDM2/7的选择性超过KDM4A (IC50 > 120 μM), KDM4C (IC50 = 83 μM), KDM2/7的选择性高于KDM4A (IC50 > 120 μM), KDM4C (IC50 = 83 μM)。KDM5A (IC50 = 55 μM)和KDM6A(也称为UTX) (IC50 > 100 μM);但请注意使用不同的测定条件(见实验部分)。因此,化合物9是酶分析中发现的最有效的KDM7B抑制剂。此外,化合物13对KDM2A的选择性高于KDM7B和其他同工酶。由于分子模型表明KDM7B疏水口袋中9环丙烷环周围的空间不是很大(图2),因此带有苯基环的化合物13可能很难形成能有效与口袋中的Phe相互作用的构象。另一方面,KDM2A具有比KDM7B更宽敞的疏水口袋(支持信息图S2),其中的苯环可以有效地与KDM2A的疏水氨基酸残基相互作用。这可能是化合物13对KDM2A比KDM7B具有选择性的原因。[1]
为了研究TC-E 5002/化合物9是否作为KDM7A和KDM7B的抑制剂在细胞中具有活性,我们使用Western blot分析进行了细胞实验。由于已知KDM7可以催化H3K27me2,10,11的去甲基化,因此我们分析了细胞中H3K27的甲基化水平。在这项研究中,我们使用N2a细胞,因为有报道称KDM7在细胞中表达如图3所示,在9的存在下,H3K27me2的水平呈剂量依赖性升高。尽管对全局组蛋白n -甲基化状态变化的解释可能很复杂,但H3K27me2水平的升高与KDM7抑制一致。这些结果表明细胞中H3K27me2的去甲基化受到化合物9的抑制,并且它看起来可以作为探测KDM7.的生物学作用的工具[1]。 虽然有报道称rnai介导的KDM7B的敲低抑制了一些癌细胞的生长,但目前尚不清楚KDM7B的去甲基化酶功能是否与这种抑制有关,因为rnai介导的KDM7B的敲低不仅会导致去甲基化酶功能的丧失,还会导致KDM7B的其他功能的丧失,12包括与非催化结合域有关的功能。首先,我们研究了TC-E 5002/化合物9对N2a细胞生长的抑制活性。在Western blot分析(图3)检测到明显H3K27甲基化的浓度范围内,化合物9对N2a细胞生长的抑制作用被观察到(GI50 = 86 μM)(图4)。因此,这可能表明KDM7的去甲基化酶功能参与了这种细胞生长,然而,需要更有效和选择性的化合物来充分阐明这一事实。接下来,我们使用HeLa细胞和KYSE150细胞对化合物9以及前药1、2和3进行了细胞生长抑制实验(表3)。也有报道称,KDM4C抑制剂2、3(表3)和它们的甲酯前药(GI50 bb0 500 μM)虽然是细胞膜透性的,但对所测试的癌细胞的生长抑制没有任何影响。这些结果表明,至少在某些细胞类型中,KDM4C的去甲基化酶活性与癌细胞生长没有直接关系。另一方面,KDM2/7亚家族抑制剂9在KYSE150和HeLa细胞系中观察到细胞生长抑制(图5)。此外,化合物9在HeLa细胞和KYSE150细胞中均引起H3K27甲基化,在细胞生长抑制的浓度范围内(图6)。表3所示的数据表明,KDM2/7抑制剂值得作为候选抗癌药物进行评估[1]。 最近一项研究报道,KDM7B激活HeLa细胞中E2F1转录因子的转录,从而促进细胞周期的进展因为TC-E 5002/化合物9降低了H3K27me2积累的HeLa细胞的生长(表3;图5和图6),我们通过定量RT-PCR检测化合物9是否下调了HeLa细胞中E2F1的表达。如图7所示,化合物9显著降低80 μM时E2F1 mRNA水平,影响HeLa细胞的生长。这些数据提示kdm7b介导的E2F1基因表达调控可能是某些癌细胞生长调控的机制之一[1] 。 |
| 酶活实验 |
KDM7B抑制试验[1]
KDM7B (0.5 mg/mL)与150 mM KCl、2.5%甘油、0.5 mM二硫苏糖醇、0.05 mM PMSF、2.5 mM谷胱甘肽还原形式、20 μM (+)-Fe(II)-l-抗坏血酸、20 μM ZnCl2、0.5 mM抗坏血酸、0.5 mM 2-氧葡萄糖酸和5 μM H3K4me3K9me2 (ART(Kme3)QTAR(Kme2)STGGKAPRKQL-Cys)在8 μL 10 mM Tris-HCl缓冲液(pH 8.0)中37℃孵育1小时。加入75 μL的基质溶液(5 mg/mL α-氰基-4-羟基肉桂酸、37%乙腈、0.12%三氟乙酸)停止反应,超声30 s。将1 μL的反应混合物点染在样品板上,干燥后使用Voyager-DE PRO进行基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS)分析。测试化合物的KDM7B抑制活性由H3K9me2的残留量计算。测试化合物的50%抑制浓度(IC50)计算为去除一半H3K9me2的浓度与添加酶时去除的浓度(辅助信息图S7)。 KDM4C抑制试验[1] 用0.6 mg/mL酶测定kdm4c抑制活性。这些化合物溶解在二甲基亚砜中。反应混合物中DMSO的终浓度均小于3.3%,证实了3.3%的DMSO对KDM4C活性没有影响。与DMSO单独反应也作为对照。反应混合物(94.6 μL),除H3K9me3肽和2-氧戊二酸外,其余物质均含有,预孵育5min,然后加入5.4 μL的0.93 mM H3K9me3肽和3.7 mM 2-氧戊二酸溶液开始反应。酶活性测定方法如上所述。在抑制剂存在的情况下,测量的酶活性与对照组的酶活性之比根据log [inhibitor]绘制。为了证实测试化合物对KDM4C活性的降低不是由于抑制偶联酶FDH,我们检查了测试化合物对FDH活性的影响。反应混合物(0.1 mL)中含有HEPES-KOH 20 mM、pH 7.5、甲醛50 μM、3-乙酰吡啶腺嘌呤二核苷酸1 mM、还原性谷胱甘肽1 mM、牛血清白蛋白0.1 mg/mL、FDH 0.1 mg/mL和固定浓度123 μM的测试化合物。FDH活性是通过监测APADH的形成来测量的,如上所述。存在试验化合物时的FDH活性与不存在试验化合物时相似。 KDM4A抑制试验[1] KDM4A活性的测定采用了KDM4C的fdhh偶联法,不同之处是反应在384孔板(Nunc)中以30 μL的终体积进行,KDM4A的终浓度为0.37 mg/mL。 KDM5A抑制试验[1] KDM5A活性测定采用与KDM4C相同的fdh偶联法,不同之处是与H3K4me3肽在384孔板(Nunc)中以30 μL的终体积进行反应,KDM5A终浓度为0.64 mg/mL。 KDM2A抑制试验[1] 实验化合物对KDM2A的抑制活性根据文献(4)报道的方法进行测定。 KDM6A抑制试验[1] KDM6A酶检测采用表观igenase JMJD3/UTX去甲基酶活性/抑制测定试剂盒。根据供应商的方案,将随试剂盒提供的材料、100 μM的测试化合物和KDM6A (300 ng/孔)添加到涂覆三甲基化组蛋白底物的孔中。在37℃下孵育120分钟。酶反应后,每孔与捕获抗体反应60分钟,与检测抗体反应30分钟。最后,依次将显影液和停止液加入孔中,用ARVO X3酶标仪测量每孔的吸光度(450 nm)。根据吸光度值计算受试化合物的KDM6A抑制活性。 KDM7A抑制试验[1] 使用MALDI和K27me2肽作为底物,在与文献(4)相同的条件下进行KDM7A测定。 |
| 细胞实验 |
RNA的分离与半qrt - pcr [1]
以浓度为30 μM和80 μM的0.238% DMSO或TC-E 5002/化合物9处理HeLa细胞48 h。按照制造商的方案,使用RNAzol从HeLa细胞中分离总RNA。利用ReverTra Ace从总RNA合成第一链cDNA。利用2720热循环器 进行半定量PCR (semi-qPCR)分析。引物是针对被测基因的特异性引物,其序列如下: GAPDH 450bp引物(F): 5 ' -TCCACCACCCTGTTGCTGTA-3 ‘ (20mer)引物(R): 5 ’ - accacagtccatgccatca3 ' (20mer) E2F1 435bp引物(F): 5 ' -ACTCCTCGCAGATCGTCATCATCT-3 ‘ (24mer)引物(R): 5 ’ - ggacgttggtgatgtcatagatggcg -3 ' (25mer) 循环参数为94°C 2 min,然后是28 (E2F1), 20 (GAPDH)循环,98°C 10 s, 60°C 30 s, 68°C 30 s,最后延长至68°C 1 min。 流式细胞仪分析[1] 细胞(5 × 105)用TC-E 5002/化合物9在指定浓度的RPMI 1640和10%胎牛血清中处理24 h,然后通过胰蛋白酶化收获。离心收集细胞,用70%乙醇冷冻固定,用磷酸盐缓冲盐水洗涤,用0.5 mL含碘化丙啶(10 μg/mL)和RNase A (0.2 mg/mL)的磷酸盐缓冲盐水重悬。最终在25°C孵育30分钟后,使用JSAN流式细胞仪分析细胞。每个样本总共统计了30000个事件。使用FlowJo软件对数据进行分析。 |
| 参考文献 | |
| 其他信息 |
组蛋白N(ε)-甲基赖氨酸去甲基酶KDM2/7已被确定为潜在的癌症治疗靶点。基于KDM7B的晶体结构,我们设计并制备了一系列带有烷基链的羟肟酸类似物。酶活性测定表明,化合物9能有效抑制KDM2A、KDM7A和KDM7B,其IC50值分别为6.8、0.2和1.2 μM。虽然KDM4抑制剂对所测试的癌细胞没有显示出任何作用,但KDM2/7亚家族抑制剂9表现出抗增殖活性,表明KDM2/7抑制剂具有作为抗癌药物的潜力。我们鉴定了一种新型KDM2/7亚家族抑制剂9,它有望作为先导化合物用于开发更有效、更具选择性的KDM2/7抑制剂。此类抑制剂既可作为抗癌药物的候选药物,也可作为研究 KDM2/7 亚家族在细胞中生物学作用的工具。[1]
|
| 分子式 |
C15H27NO4
|
|---|---|
| 分子量 |
285.38
|
| 精确质量 |
285.194
|
| 元素分析 |
C, 63.13; H, 9.54; N, 4.91; O, 22.42
|
| CAS号 |
1453071-47-0
|
| PubChem CID |
71735843
|
| 外观&性状 |
White to off-white solid powder
|
| 熔点 |
87 °C
|
| LogP |
3.209
|
| tPSA |
77.84
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
12
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
302
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
NEHSERYKENINRH-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C15H27NO4/c17-14(16(20)12-11-15(18)19)8-6-4-2-1-3-5-7-13-9-10-13/h13,20H,1-12H2,(H,18,19)
|
| 化学名 |
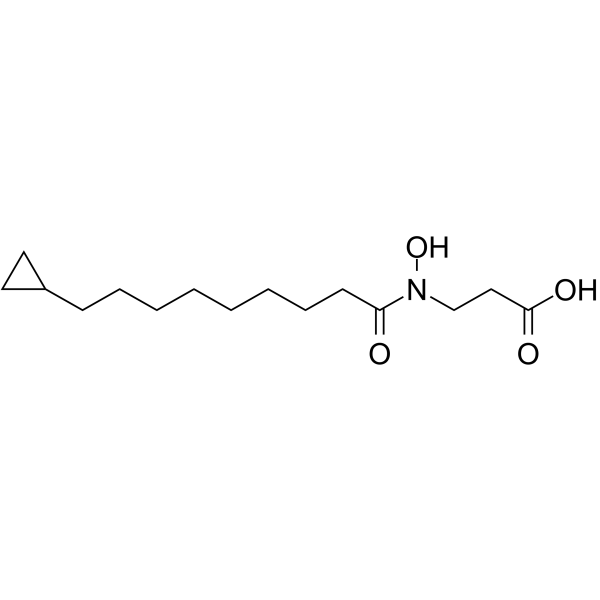
3-[9-cyclopropylnonanoyl(hydroxy)amino]propanoic acid
|
| 别名 |
TCE 5002; TC E 5002; 1453071-47-0; TC-E 5002; N-(9-Cyclopropyl-1-oxononyl)-N-hydroxy-beta-alanine; 3-(9-CYCLOPROPYL-N-HYDROXYNONANAMIDO)PROPANOIC ACID; KDM2/7-IN-1; CHEMBL2424812; NCDM-64; MFCD28166486; TC-E 5002
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.5041 mL | 17.5205 mL | 35.0410 mL | |
| 5 mM | 0.7008 mL | 3.5041 mL | 7.0082 mL | |
| 10 mM | 0.3504 mL | 1.7520 mL | 3.5041 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。