| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
| 靶点 |
VEGF receptors
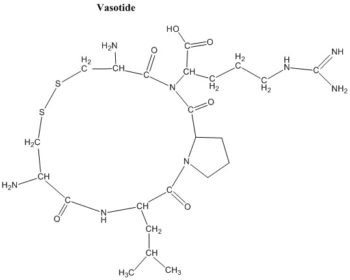
Researchers have evaluated a small cyclic retro-inverted peptidomimetic, D(Cys-Leu-Pro-Arg-Cys) [D(CLPRC)], and hereafter named Vasotide, that inhibits retinal angiogenesis by binding selectively to the VEGF receptors VEGFR-1 and neuropilin-1 (NRP-1). [1] |
|---|---|
| 体外研究 (In Vitro) |
研究人员评估了一种小环逆转录-倒转肽模拟物D(Cys-Leu-Pro-Arg-Cys) [D(CLPRC)],以下命名为Vasotide,它通过选择性地结合VEGF受体VEGFR-1和neuropilin-1 (NRP-1)来抑制视网膜血管生成。[1]
CPQPRPLC 肽的环状逆向反转肽模拟物衍生物,即 Vasotide (p(CLPRC)),被证明是比原始线性肽序列更强的 VEGFR-1 和 NRP-1 配体,并且在体内稳定性增强。[1] 核磁共振分析确定 Arg-Pro-Leu (RPL) 是与 VEGFR-1 和 NRP-1 受体双配体结合所必需且足够的最小三肽基序。[1] |
| 体内研究 (In Vivo) |
Vasotide减少ROP小鼠血管丛的形成。
Vasotide在激光诱导的猴子AMD模型中减少血管生成。 静脉注射Vasotide可减少小鼠vldlr RAP模型的血管生成。 VEGF受体靶向的原型拟肽血管肽可减少两种人类视网膜疾病的临床前小鼠模型和一种非人灵长类动物模型:小鼠ROP模型、vldlr敲除小鼠视网膜血管生成增殖模型(RAP)和激光诱导湿性AMD猴模型的病理血管生成。每种疾病类型都显示出常见和独特的血管生成特征。这表明,像目前fda批准的抗vegf治疗药物一样,Vasotide可能对一系列涉及血管生成的人类视网膜疾病有价值。事实上,使用Vasotide的结果与之前报道的在同一灵长类动物群体中使用贝伐单抗的治疗反应大致相似,这些动物的眼睛受到激光诱导的光凝损伤。需要对Vasotide进行更详细的药代动力学/治疗分析,以确定其他特征,如疗效持续时间、安全性、便利性和成本。 [1] 在三种动物模型中,通过滴眼液或腹腔注射给药Vasotide可以减少视网膜血管瘤性增生(RAP)的小鼠AMD亚型基因敲除模型和小鼠氧诱导的ROP模型的视网膜血管生成。这种原型候选药物是一种有前景的新的VEGF配体双受体抑制剂,有可能转化为更安全、更微创的应用,以对抗视网膜疾病的病理性血管生成。[1] 在小鼠氧诱导视网膜病变模型中,于缺氧期腹腔注射或滴眼给予 Vasotide,可显著减少病理性血管簇的形成。视网膜无血管区面积未受显著影响。[1] 在激光诱导的非洲绿猴脉络膜新生血管模型中,滴眼给予 Vasotide 能显著降低具有临床意义的 CNV 病灶的发生率和大小,并减少荧光素渗漏。组织学分析显示炎症细胞浸润、CNV 和纤维增生明显减少。[1] 在 vldlr 基因敲除小鼠视网膜血管瘤样增生模型中,腹腔注射 Vasotide 能显著抑制病理性血管生成,包括降低视网膜内、外层血管密度,减少血管簇的数量和大小,并阻止血管长入光感受器细胞层。[1] |
| 酶活实验 |
最初使用消减噬菌体展示库筛选策略鉴定出 CPQPRPLC 肽是 VEGFR-1 和 NRP-1 的选择性配体。[1]
随后进行了结构分析以确定最小结合基序。[1] |
| 细胞实验 |
对视网膜组织进行了免疫组织化学和免疫荧光分析。使用荧光标记的 IB4 凝集素染色血管。使用 CD31、CD68/F4/80 和 GR1 抗体进行共染色以鉴定特定细胞类型并评估炎症。使用荧光显微镜和共聚焦显微镜成像。[1]
对于视网膜全铺片,固定眼球,解剖视网膜,用荧光 IB4 染色,通常用有机碘剂增加透明度,然后平铺进行成像。采集全视网膜厚度的图像栈进行三维分析。[1] |
| 动物实验 |
对猴子进行眼药水给药[1]
将浓度为120 mg/ml的Vasotide肽局部制剂滴入猴子的眼内。在第1天进行激光光凝后,将试验药物Blink Gel Tears(本文中简称GelTears)用滴管滴入猴子的双眼(每次50 µl),每日两次,持续5天,之后每日一次,持续16天。以相同方式滴入赋形剂(50 µl)。治疗方案如表S1所示。猴子在仰卧位给药。 人类视网膜血管瘤增生症 (RAP) 的小鼠 vldlr 基因敲除 (敲除) 模型 [1] 在标准化条件下饲养和繁殖了 vldlr 基因靶向敲除的突变小鼠 (B6;129S7-Vldlrtm1Her/J; vldlr KO)。使用年龄匹配的 C57BL/6J 小鼠作为正常野生型对照。将 vldlr KO 小鼠随机分为三组:未治疗的 vldlr KO 组、给予对照肽 D(CAPAC) 的 vldlr KO 组和给予治疗性肽 Vasotide 的 vldlr KO 组。在出生后第 12-18 天 (P12-P18)、第 48-54 天 (P48-P54)、第 108-114 天 (P108-P114) 和第 208-214 天 (P208-P214),每天腹腔注射 (ip) 20 µg/µl PBS 的肽溶液,剂量为 40 µg/g 体重。小鼠饲养遵循视觉与眼科研究协会关于眼科研究中动物使用的声明。 小鼠氧诱导视网膜病变(OIR)模型:将C57BL/6J小鼠幼崽及其母鼠置于75%氧气环境中,从出生后第7天(P7)至P12,以抑制正常的视网膜血管发育。P12时,将小鼠放回室温空气(21% O2)环境中,启动低氧期,促进病理性血管生成。药物治疗在P12至P18期间进行。Vasotide或对照肽通过腹腔注射(每日8 µg/g或40 µg/g体重)或滴眼液(200 µg溶于2 µl Systane溶剂中,每日三次)给药。在P19时分析视网膜。 [1] 猴子激光诱导脉络膜新生血管(CNV)模型:成年雄性非洲绿猴接受激光光凝治疗(每眼六个光斑)以破坏布鲁赫膜并诱导CNV。激光治疗后第1天开始,猴子接受局部滴眼液治疗,滴眼液中含有Vasotide(120 mg/ml,每眼50 µl),溶于GelTears凝胶中,或仅含凝胶。给药方案为每日两次,持续5天,然后每日一次,持续6-21天。在第29天进行眼科影像学检查(荧光血管造影、光学相干断层扫描),并在第34天进行组织病理学评估。[1] 小鼠Vldlr基因敲除RAP模型:使用Vldlr基因敲除小鼠和野生型对照小鼠。在特定治疗期间(P12-P18、P48-P54、P108-P114 和 P208-P214),每日通过腹腔注射(40 µg/g 体重,溶于 PBS)给予 Vasotide 或对照肽 D(CAPAC)。在 P16 至 P270 期间的多个时间点收集并分析视网膜。[1] |
| 药代性质 (ADME/PK) |
先前研究的初步数据显示,滴眼液中给药的线性三肽p(LPR)(一种前体)可以转移到小鼠眼的玻璃体腔,并直接接触形成病理性簇状结构的内视网膜表面。[1] 环状反向肽模拟物Vasotide的设计旨在提高其体内稳定性,优于其线性对应物。[1] 该手稿指出,需要进行更精细的药代动力学/治疗分析,以确定其他特性,例如疗效持续时间。[1]
|
| 毒性/毒理 (Toxicokinetics/TK) |
在猴模型中,治疗组和对照组均观察到下角膜轻微混浊,这归因于局部用药制剂的低pH值。但这并未影响眼底镜检查或图像分析。[1]
|
| 参考文献 |
[1]. The peptidomimetic Vasotide targets two retinal VEGF receptors and reduces pathological angiogenesis in murine and nonhuman primate models of retinal disease. Sci Transl Med . 2015 Oct 14;7(309):309ra165.
[2]. The potential of anti-VEGF (Vasotide) by eye drops to treat proliferative retinopathies. Ann Transl Med . 2016 Oct;4(Suppl 1):S41. d |
| 其他信息 |
本文介绍了一种名为Vasotide™的新型小分子候选药物,该药物由工程化氨基酸构成,能够阻断眼部视网膜血管的异常过度生长,从而预防视力丧失。该药物的显著特点是只需滴眼即可给药。Vasotide能够独特地阻止一种名为VEGF的血管生长促进分子与血管内皮细胞上的两种不同受体分子结合,从而抑制动物模型中主要视网膜疾病(如老年性黄斑变性、早产儿视网膜病变以及可能与此类似但尚未经过验证的糖尿病视网膜病变)的病理过程。[1] 血管生成(血管从现有血管生长)是许多严重疾病的根本原因,包括早产儿视网膜病变(ROP)和老年性黄斑变性(AMD)等主要致盲性视网膜疾病。这一发现推动了抗体抑制剂的研发,这些抑制剂能够阻断血管内皮生长因子(VEGF)这一AMD的关键因子与其受体VEGFR-1(尤其是VEGFR-2)的结合。然而,部分患者对现有的抗VEGF药物不敏感或产生耐药性,而且这些大分子药物需要反复进行玻璃体内注射,费用昂贵且临床应用存在诸多问题。[1]
总的来说,Sidman及其同事的研究结果表明,像Vasotide这样的药物具有治疗多种以新生血管为特征的眼部疾病的潜力,这些药物能够抑制VEGFR-1和NRP-1。Vasotide并未与目前美国食品药品监督管理局(FDA)批准的药物(如阿柏西普、雷珠单抗和贝伐珠单抗,这些药物靶向VEGF-A和VEGFR-2)进行直接比较。这项评估不仅对于了解Vasotide的相对疗效至关重要,而且对于确定VEGF通路中哪些成分对减弱眼部新生血管最为关键也至关重要,这些发现可能对目前抗VEGF药物耐药的患者尤为重要。局部给药或许是未来治疗眼部新生血管和血管通透性最有前景的方向之一。如果能够证实并优化其对视网膜和脉络膜的渗透性,并获得可靠的药代动力学和安全性数据,那么滴眼液将优于目前每月一次的玻璃体内注射,并可能显著节省成本。[2]Vasotide是一种小环状逆向肽模拟物,p(Cys-Leu-Pro-Arg-Cys)或p(CLPRC)。它是一种原型候选药物,旨在通过阻断VEGF配体与VEGFR-1和NRP-1的结合来抑制病理性血管生成。 [1] 其作用机制与目前主要靶向VEGF-A与VEGFR-2结合的抗VEGF-A疗法(例如雷珠单抗、贝伐珠单抗)不同。Vasotide可能对现有疗法无效或耐药的患者有益。[1] 研究表明,Vasotide也可能影响血管生成性视网膜病变中涉及的炎症和免疫机制,治疗组猴子的炎症浸润减少即证明了这一点。[1] 潜在的给药途径包括局部滴眼和腹腔注射,其中滴眼可能比反复玻璃体内注射更安全、创伤更小、更方便。[1] 文中还讨论了与其他作用机制不同的抗血管生成药物联合治疗的可能性。[1] |
| 外观&性状 |
Typically exists as solid at room temperature
|
|---|---|
| 别名 |
Vasotide; D(Cys-Leu-Pro-Arg-Cys); D(CLPRC)
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Effects ofVasotideon the vasculature and tuft formation in ROP mice.Sci Transl Med.2015 Oct 14;7(309):309ra165. |
Fluorescein angiograms, OCT images, and histopathology of choroidal neovessels in monkey retinas.(A) Representative 6-minute fluorescein angiograms (FA) from eye drop-treated monkeys containing vehicle (left) orVasotide(right), at 29 days post laser-induced photocoagulation.Sci Transl Med.2015 Oct 14;7(309):309ra165. |
Histopathologyof vldlr-nullmouse retinas treated with control peptide orVasotide.(A) Representative 6-minute fluorescein angiograms (FA) from eye drop-treated monkeys containing vehicle (left) orVasotide(right), at 29 days post laser-induced photocoagulation.Sci Transl Med.2015 Oct 14;7(309):309ra165. |
Confocal image series at 10-mmintervals through the full retinal thickness at P48 in WT and vldlr-nullmice.Sci Transl Med.2015 Oct 14;7(309):309ra165. |
Blood vessel growth in the outer retina of vldlr-null mice treated with control peptide orVasotideat P16 to P270.(A) Tuft formation in the pooled outer retinal areas of WT mice or vldlr-null (KO) mice treated with control D(CAPAC) peptide orVasotidewas visualized by confocal microscopy with a 20Å~ microscope objective. Scale bar, 25 mm. |
Vascular tufts in OIR mice extend from the retina into the vitreous.(A) IB4-stained branched vessels and tufts in horizontal retinal scans in normal mice and mice with oxygen-induced retinopathy (OIR) treated withD(CAPAC) control peptide orVasotide. (A’) Scans rotated 90°, showing tufts above dashed lines, innermost retina below.Sci Transl Med.2015 Oct 14;7(309):309ra165. |