| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 药代性质 (ADME/PK) |
代谢/代谢物
L-半胱氨酸是人体硫代谢的核心化合物。在蛋白质中,半胱氨酸巯基之间形成二硫键对蛋白质的三级结构和酶活性起着重要作用;然而,半胱氨酸总是以半胱氨酸的形式掺入多肽链中。L-半胱氨酸通过两步降解为丙酮酸:一步是脱硫,另一步是转氨作用。半胱氨酸可以通过半胱氨酸亚磺酸途径代谢生成牛磺酸和二氧化碳,该途径的第一步是半胱氨酸氧化为半胱氨酸亚磺酸。这一步骤由半胱氨酸双加氧酶催化。半胱氨酸亚磺酸盐可脱羧生成牛磺酸,或经由假定的中间体β-亚磺酰丙酮酸代谢为丙酮酸和亚硫酸盐,最终生成二氧化碳和硫酸盐。氨基酸分解代谢对于调节游离氨基酸库的大小至关重要,并参与能量产生和营养物质的再利用。碳骨架通常转化为三羧酸循环的前体或中间体。对于半胱氨酸而言,源自巯基的还原硫也必须被氧化,以防止其积累至毒性浓度。本文介绍了一种线粒体硫分解代谢途径,该途径催化L-半胱氨酸完全氧化为丙酮酸和硫代硫酸盐。 L-半胱氨酸经转氨作用生成3-巯基丙酮酸后,其巯基通过硫转移酶1转移至谷胱甘肽,并被硫双加氧酶ETHE1氧化为亚硫酸盐。随后,硫转移酶1添加第二个过硫化物基团,将亚硫酸盐转化为硫代硫酸盐。该途径在早期胚胎发育和光照限制条件下的营养生长中最为重要。对拟南芥ETHE1和硫转移酶1的T-DNA插入系产生的双突变体进行表征发现,ETHE1依赖途径的中间体(很可能是过硫化物)会干扰氨基酸分解代谢并诱导早期衰老。 尿毒症毒素往往因饮食过量或肾脏滤过不良而在血液中积累。大多数尿毒症毒素是代谢废物,通常通过尿液或粪便排出体外。 |
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概要
在目前的使用方法和浓度下是安全的。成分、浓度和使用信息可在以下网址查阅:https://cir-reports.cir-safety.org 识别和用途:半胱氨酸形成白色或无色晶体。它用于生物化学和营养研究,也可用作面包面团中的还原剂(最高浓度为 90 ppm)。它还可用作增味剂和药物,包括兽药。人体暴露和毒性:3% 的半胱氨酸溶液对人眼无刺激性。动物研究:单次向兔子眼部滴入 0.1 克 L-半胱氨酸,产生轻微刺激作用,该作用在 48 小时内完全可逆。单次向三只兔子皮肤涂抹 0.5 克 L-半胱氨酸,未显示刺激或腐蚀作用。接受高剂量半胱氨酸治疗的大鼠产仔数减少,这与排卵的未受精卵和胚胎的退化和/或死亡有关,并伴有透明带的改变,而卵巢中的透明带已受到影响。妊娠小鼠和大鼠在妊娠最后一天皮下注射1.2 mg/g的半胱氨酸,一天后在胎儿中观察到脑退化。使用中国仓鼠V79细胞系,L-半胱氨酸被认为对HPRT基因座无致突变性。L-半胱氨酸不会诱导V79中国仓鼠细胞系的染色体结构畸变。生态毒性研究:本研究旨在确定半胱氨酸对鲤鱼(Cyprinus carpio)解冻后精子活力、精子活力持续时间、DNA损伤和生育力的影响。补充半胱氨酸可提高受精率和孵化率,并减少DNA损伤。 尿毒症毒素(如半胱氨酸)可通过有机离子转运蛋白(尤其是OAT3)主动转运至肾脏。尿毒症毒素水平升高可刺激活性氧的产生。这似乎是由尿毒症毒素直接结合或抑制NADPH氧化酶(尤其是肾脏和心脏中含量丰富的NOX4)介导的(A7868)。活性氧可诱导多种不同的DNA甲基转移酶(DNMTs),这些酶参与KLOTHO蛋白的沉默。KLOTHO已被证实对抗衰老、矿物质代谢和维生素D代谢具有重要作用。多项研究表明,在急性或慢性肾脏疾病中,由于局部活性氧水平升高,KLOTHO mRNA和蛋白水平会降低(A7869)。尽管半胱氨酸被归类为非必需氨基酸,但它对婴儿、老年人以及患有某些代谢疾病或吸收不良综合征的个体而言可能至关重要。在正常的生理条件下,如果蛋氨酸充足,人体通常可以合成半胱氨酸。由于硫醇能够发生氧化还原反应,半胱氨酸具有抗氧化特性。半胱氨酸的抗氧化特性通常体现在三肽谷胱甘肽中,谷胱甘肽存在于人体和其他生物体中。口服谷胱甘肽(GSH)的系统生物利用度极低;因此,它必须由其组成氨基酸——半胱氨酸、甘氨酸和谷氨酸——生物合成。谷氨酸和甘氨酸在大多数工业化国家的饮食中都很容易获得,但半胱氨酸的供应可能成为限制性底物。半胱氨酸也是人体代谢中硫化物的重要来源。铁硫簇和固氮酶中的硫化物是从半胱氨酸中提取出来的,半胱氨酸在此过程中转化为丙氨酸。在1994年五大卷烟公司联合发布的一份报告中,半胱氨酸是卷烟599种添加剂之一。然而,与大多数卷烟添加剂一样,其用途或目的尚不明确。在卷烟中添加半胱氨酸可能带来两方面益处:一是作为祛痰剂,因为吸烟会增加肺部黏液的产生;二是增加有益的抗氧化剂谷胱甘肽(吸烟者体内谷胱甘肽含量较低)。 非人类毒性值 大鼠经皮LD50 >2000 mg/kg 体重 大鼠经口LD50 1890 mg/kg 大鼠经腹腔LD50 1620 mg/kg 大鼠经皮LD50 1550 mg/kg 有关半胱氨酸(共7种)的更多非人类毒性值(完整)数据,请访问HSDB记录页面。 |
| 其他信息 |
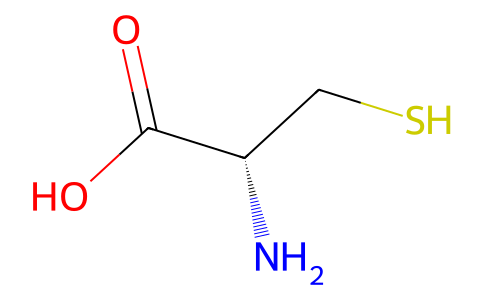
L-半胱氨酸是具有L构型的旋光性半胱氨酸。它可用作面粉处理剂、人体代谢产物和EC 4.3.1.3(组氨酸解氨酶)抑制剂。它是一种丝氨酸家族氨基酸、蛋白质合成氨基酸、半胱氨酸和L-α-氨基酸。它是L-半胱氨酸的共轭碱。它是L-半胱氨酸(1-)的共轭酸。它是D-半胱氨酸的对映异构体。它是L-半胱氨酸两性离子的互变异构体。
半胱氨酸是一种含硫醇的非必需氨基酸,氧化后可生成胱氨酸。 L-半胱氨酸是大肠杆菌(K12菌株、MG1655菌株)中发现或产生的代谢产物。 据报道,木蓝、石榴和其他一些有相关数据的生物体中也含有半胱氨酸。 半胱氨酸是人体必需的含硫氨基酸,与胱氨酸相关。半胱氨酸对蛋白质合成、解毒和多种代谢功能至关重要。半胱氨酸存在于β-角蛋白中,β-角蛋白是指甲、皮肤和毛发的主要蛋白质,半胱氨酸对胶原蛋白的生成以及皮肤的弹性和质地都非常重要。半胱氨酸也是合成牛磺酸的必需氨基酸,同时也是抗氧化剂谷胱甘肽的组成部分,并在辅酶A、肝素和生物素等重要生化物质的代谢中发挥作用。(NCI04) 半胱氨酸是一种尿毒症毒素。根据其化学和物理特性,尿毒症毒素可分为三大类:1) 小分子、水溶性、非蛋白结合化合物,例如尿素;2) 小分子、脂溶性和/或蛋白结合化合物,例如酚类;3) 较大的所谓中分子,例如β2-微球蛋白。长期接触尿毒症毒素可导致多种疾病,包括肾损伤、慢性肾病和心血管疾病。 半胱氨酸是一种天然存在的含硫氨基酸,存在于大多数蛋白质中,但含量很少。在20种天然氨基酸中,半胱氨酸的独特之处在于它含有一个巯基。巯基可以发生氧化还原反应;半胱氨酸被氧化后可以形成胱氨酸,胱氨酸是由两个半胱氨酸残基通过二硫键连接而成。该反应是可逆的:还原该二硫键可以再生两个半胱氨酸分子。胱氨酸的二硫键对于许多蛋白质的结构至关重要。半胱氨酸通常参与电子转移反应,并帮助酶催化反应。半胱氨酸也是抗氧化剂谷胱甘肽的组成部分。N-乙酰-L-半胱氨酸 (NAC) 是半胱氨酸的一种形式,其中乙酰基连接到半胱氨酸的氮原子上,并作为膳食补充剂出售。半胱氨酸的名称来源于胱氨酸,胱氨酸一词源于希腊语 kustis,意为膀胱——胱氨酸最初是从肾结石中分离出来的。由于半胱氨酸含有巯基,因此它可以发生氧化还原反应。半胱氨酸的氧化可以与其他硫醇形成二硫键,或进一步氧化生成亚磺酸或磺酸。半胱氨酸的硫醇基团也具有亲核性,可以发生加成反应和取代反应。硫醇基团电离后活性显著增强,蛋白质中的半胱氨酸残基的pKa值接近中性,因此在细胞内通常以活性硫醇盐的形式存在。硫醇基团对重金属具有很高的亲和力,含半胱氨酸的蛋白质能够紧密结合汞、铅和镉等金属。由于其能够发生氧化还原反应,半胱氨酸具有抗氧化特性。半胱氨酸是人体代谢中重要的硫来源,虽然它被归类为非必需氨基酸,但对于婴儿、老年人以及患有某些代谢疾病或吸收不良综合征的个体而言,半胱氨酸可能是必需的。未来,半胱氨酸可能会被认定为必需氨基酸或条件必需氨基酸。半胱氨酸在能量代谢中发挥着重要作用。它以胱氨酸的形式存在,是许多组织和激素的结构成分。半胱氨酸的临床应用范围广泛,从治疗脱发、银屑病到预防吸烟引起的咳嗽都有涉及。在某些情况下,口服半胱氨酸疗法已被证明对治疗哮喘非常有效,可以帮助患者停用茶碱和其他药物。此外,半胱氨酸还能增强外用银盐、锡盐和锌盐预防龋齿的效果。未来,半胱氨酸可能在治疗钴中毒、糖尿病、精神病、癌症和癫痫方面发挥作用。 半胱氨酸是一种含硫醇的非必需氨基酸,氧化后形成胱氨酸。 另见:盐酸半胱氨酸(有盐形式)……查看更多…… 药物适应症 用于预防对乙酰氨基酚过量引起的肝肾损伤 作用机制 在正常生理条件下,如果蛋氨酸充足,人体通常可以合成半胱氨酸。半胱氨酸通常在人体内蛋氨酸充足时合成。半胱氨酸具有抗氧化特性,并参与氧化还原反应。半胱氨酸的抗氧化特性通常体现在三肽谷胱甘肽中,谷胱甘肽存在于人体和其他生物体中。由于谷胱甘肽 (GSH) 在体内的生物利用度有限,通常需要由其组成氨基酸——半胱氨酸、甘氨酸和谷氨酸——进行生物合成。谷氨酸和甘氨酸在大多数工业化国家的膳食中含量丰富,但半胱氨酸的供应可能成为限制性底物。在人体代谢中,半胱氨酸作为前体参与铁硫簇和固氮酶中硫化物的生成。在1994年五家顶级卷烟公司发布的一份报告中,半胱氨酸是卷烟中599种添加剂之一。然而,与大多数卷烟添加剂一样,其用途或目的尚不清楚。在卷烟中添加半胱氨酸可能带来两个益处:一是作为祛痰剂,因为吸烟会增加肺部黏液的产生;二是增加有益的抗氧化剂谷胱甘肽(吸烟者体内谷胱甘肽含量较低)。 |
| 分子式 |
C3H7NO2S
|
|---|---|
| 分子量 |
121.15
|
| 精确质量 |
121.019
|
| CAS号 |
52-90-4
|
| 相关CAS号 |
62488-11-3;7048-04-6 (Hydrochloride)
|
| PubChem CID |
5862
|
| 外观&性状 |
Colorless crystals
White crystals |
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
293.9±35.0 °C at 760 mmHg
|
| 熔点 |
260 °C decomposes
; 220 °C
|
| 闪点 |
131.5±25.9 °C
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
| 折射率 |
1.550
|
| LogP |
0.23
|
| tPSA |
102.12
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
7
|
| 分子复杂度/Complexity |
75.3
|
| 定义原子立体中心数目 |
1
|
| SMILES |
S([H])C([H])([H])[C@@]([H])(C(=O)O[H])N([H])[H]
|
| InChi Key |
XUJNEKJLAYXESH-REOHCLBHSA-N
|
| InChi Code |
InChI=1S/C3H7NO2S/c4-2(1-7)3(5)6/h2,7H,1,4H2,(H,5,6)/t2-/m0/s1
|
| 化学名 |
(2R)-2-amino-3-sulfanylpropanoic acid
|
| 别名 |
Cysteinum; FEMA No. 3263; Cysteine
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 8.2542 mL | 41.2712 mL | 82.5423 mL | |
| 5 mM | 1.6508 mL | 8.2542 mL | 16.5085 mL | |
| 10 mM | 0.8254 mL | 4.1271 mL | 8.2542 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT06622577
Conditions:Classical HomocystinuriaLink: https://clinicaltrials.gov/ct2/show/NCT06278948
Conditions:MelasmaLink: https://clinicaltrials.gov/ct2/show/NCT04939792
Conditions:Vitamin D Deficiency
Title:Effects of Dietary Amino Acids on Serum and Macrophage Atherogenicity
Status:Unknown status
updateDate:2017-06-08
Ctid:NCT03180775
Link: https://clinicaltrials.gov/ct2/show/NCT03180775
Conditions:Atherosclerosis|Diet Modification|Serum; DiseaseLink: https://clinicaltrials.gov/ct2/show/NCT02462746
Conditions:HealthyLink: https://clinicaltrials.gov/ct2/show/NCT02050139
Conditions:Uremia
|
|
|