| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Staphylococcus aureus Sortase A (SrtA) (IC50 = 24.17 µM)[4]。
|
|---|---|
| 体外研究 (In Vitro) |
天然产物 Dryocrasin ABBA 被鉴定为金黄色葡萄球菌分选酶A (SrtA) 的有效抑制剂。在荧光共振能量转移 (FRET) 实验中,Dryocrasin ABBA 能显著降低由SrtA切割模型底物肽 (Dabcyl-QALPETGEE-Edans) 所产生的荧光信号,表明其抑制了SrtA的催化活性。其半数抑制浓度 (IC50) 测定为24.17 µM[4]。
分子动力学模拟和突变实验揭示了其抑制的分子机制。Dryocrasin ABBA 直接结合在SrtA的活性位点,主要与氨基酸残基Ala104、Glu105、Val166、Gly167、Val168、Ile182和Trp194相互作用。关键结合作用包括与Val166和Val168的范德华力,以及与Gly167的强氢键。野生型SrtA与Dryocrasin ABBA 复合物的结合自由能 (ΔGbind) 计算为-25.8 ± 2.8 kcal/mol[4]。 为验证结合位点,构建了点突变体V166A-SrtA和V168A-SrtA。在FRET实验中,Dryocrasin ABBA (40 µM) 对这些突变体的抑制效果相较于野生型SrtA显著减弱。突变体的结合自由能也更弱:V166A为-19.2 ± 3.1 kcal/mol,V168A为-15.3 ± 1.9 kcal/mol,这证实了Val166和Val168是Dryocrasin ABBA 结合并抑制其活性的关键残基[4]。 |
| 体内研究 (In Vivo) |
在感染了金刚烷胺耐药的高致病性禽流感H5N1毒株(A/Chicken/Hebei/706/2005)的小鼠模型中,口服给予 Dryocrassin ABBA 能以剂量依赖性的方式显著提高存活率。感染后第14天,33、18和12.5 mg/kg/天治疗组的存活率分别为87%、80%和60%,而金刚烷胺(20 mg/kg/天)组为53%,未治疗的病毒对照组为20%。[1]
与未治疗组相比,Dryocassin ABBA 治疗组小鼠体重显著增加[2]。 感染后第 7 天,33 和 18 mg/kg Dryocassin ABBA 治疗组的肺病毒载量显著低于未治疗组[2]。 感染后第 7 天,33 和 18 mg/kg Dryocassin ABBA 治疗组支气管肺泡灌洗液中促炎细胞因子(IL-6、TNF-α、IFN-γ、IL-12)显著降低,抗炎细胞因子(IL-10、MCP-1)显著升高,与金刚烷胺组和未治疗组相比均有显著差异[2]。 Dryocassin ABBA 治疗组肺指数较未治疗组降低,但与金刚烷胺组相比无显著差异[2]。 |
| 酶活实验 |
采用荧光共振能量转移 (FRET) 实验测定 Dryocrasin ABBA 对金黄色葡萄球菌分选酶A (SrtA) 的抑制活性。将重组SrtA蛋白(野生型或突变型)与不同浓度的Dryocrasin ABBA 或对照溶剂在反应缓冲液 (50 mM Tris-HCl, 5 mM CaCl2, 150 mM NaCl, pH 7.5) 中于37°C预孵育30分钟。随后,向96孔板的每个孔中加入荧光肽底物 (Dabcyl-QALPETGEE-Edans) 以启动酶促反应。混合物在37°C下继续孵育1小时。SrtA切割底物会解除荧光淬灭,导致荧光强度增加。使用酶标仪在激发波长350 nm、发射波长520 nm下测量荧光信号。与对照组相比,Dryocrasin ABBA 存在时荧光信号的降低表明其对SrtA活性的抑制[4]。
同时,采用荧光淬灭法测定了Dryocrasin ABBA 与SrtA的结合亲和力(结合常数,K_A)。在Dryocrasin ABBA 浓度递增的条件下,记录SrtA在激发波长280 nm(带宽5 nm)、发射波长345 nm(带宽10 nm)下的荧光发射光谱。根据淬灭数据计算结合常数[4]。 |
| 动物实验 |
Mouse Efficacy Study against H5N1: Specific pathogen-free (SPF) female BALB/c mice (n=20 per group) were infected intranasally with 10^4.5 ELD50 of the amantadine-resistant H5N1 virus (A/Chicken/Hebei/706/2005) in 100 µl saline. Starting from day 2 post-infection, mice received Dryocrassin ABBA via oral gavage once daily for 7 consecutive days (days 2 to 8). Three dose groups were used: 12.5, 18.0, and 33 mg/kg body weight per day. The positive control group received amantadine hydrochloride at 20 mg/kg/day via the same route and schedule. The untreated virus control and normal control groups received equivalent volumes of physiological saline. Mice were monitored daily for 14 days for body weight, activity, and mortality. On days 7 and 14 post-infection, subsets of mice were euthanized to collect lungs for lung index calculation and virus titration. [1]
Cytokine Analysis: On day 7 post-infection, mice were euthanized, and lungs were lavaged with sterile saline to obtain bronchoalveolar lavage fluid (BALF). The BALF supernatant was collected after centrifugation. Cytokine concentrations (IL-12, IL-6, IL-10, INF-γ, MCP-1, TNF-α) were measured using a commercial cytokine bead array kit and flow cytometry. [1] SPF BALB/C female mice were inoculated intranasally with 10^4.5 ELD50 of H5N1 virus in 100 µL saline[2]。 Starting from day 2 post-infection, mice were orally administered Dryocassin ABBA at doses of 12.5, 18, and 33 mg/kg body weight, or amantadine hydrochloride at 20 mg/kg body weight, once daily for 7 days[2]。 Control groups received equivalent volumes of physiological saline[2]。 Body weight, activity, mortality, and survival time were monitored daily for 14 days[2]。 On days 7 and 14, mice were euthanized to collect lungs for lung index calculation and virus load determination[2]。 Bronchoalveolar lavage fluid was collected on day 7 for cytokine analysis using a flow cytometry-based cytokine kit[2]。 |
| 毒性/毒理 (Toxicokinetics/TK) |
This article cites a previous study that indicated that the maximum toxic dose (MTD) of Dryocrassin ABBA in Sprague-Dawley rats was up to 2000 mg/kg body weight and that it was considered a non-toxic substance according to the European Pharmacopoeia 7.0. [1] In this mouse study, no significant adverse reactions or toxicities were reported after administration of Dryocrassin ABBA at the test dose (up to 33 mg/kg/day). [1] It has been reported that the maximum toxic dose of Dryocrassin ABBA in Sprague-Dawley rats was 2000 mg/kg body weight and that it was considered a non-toxic substance according to the European Pharmacopoeia 7.0 (cited in another study, not this article) [2].
|
| 参考文献 |
|
| 其他信息 |
Dryocrassin ABBA is a phloroglucinol compound and the main active ingredient isolated from the traditional Chinese medicine Rhizoma Dryopteridis Crassirhizomatis (RDC). [1] Rhizoma Dryopteridis Crassirhizomatis is traditionally used to treat inflammatory and infectious diseases. [1] Dryocrassin ABBA has shown protective effects against lethal infection with amantadine-resistant H5N1 avian influenza virus in mouse models. [1] Its mechanism of action is believed to be immunomodulation rather than direct viral inhibition. This protective effect is associated with the reduction of lung lesions, the decrease in viral load, and the shift of the cytokine spectrum from pro-inflammatory to anti-inflammatory (decreased levels of IL-6, TNF-α, IFN-γ, and IL-12; increased levels of IL-10 and MCP-1). [1] Dryocrasin ABBA is considered a potential novel lead compound for the development of therapies against amantadine-resistant avian influenza virus. [1]
Dryocrasin ABBA is a phloroglucinol compound isolated from Rhizoma Dryopteridis Crassirhizomatis (RDC)[2]. In a mouse model, it exhibited antiviral activity against amantadine-resistant H5N1 avian influenza virus, possibly through modulation of inflammatory cytokine responses[2]. This compound is considered a potential lead compound for the treatment of drug-resistant avian influenza infections[2]. Dryocrasin ABBA is a flavonoid natural product. This study found that Dryocrasin ABBA is a novel inhibitor of Staphylococcus aureus sorting enzyme A (SrtA). SrtA is a key virulence factor enzyme that anchors surface proteins to the bacterial cell wall. Inhibiting SrtA is an antiviral strategy that could potentially inactivate the bacteria without killing them, thereby reducing the selective pressure of antibiotic resistance. The results suggest that Dryocrasin ABBA is a promising candidate drug for the treatment of Staphylococcus aureus infection[4]. |
| 分子式 |
C43H48O16
|
|---|---|
| 分子量 |
820.8316
|
| 精确质量 |
820.294
|
| CAS号 |
12777-70-7
|
| PubChem CID |
3082025
|
| 外观&性状 |
Light yellow to green yellow solid powder
|
| 密度 |
1.5±0.1 g/cm3
|
| 沸点 |
1089.0±65.0 °C at 760 mmHg
|
| 闪点 |
626.1±30.8 °C
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
| 折射率 |
1.673
|
| LogP |
8.08
|
| tPSA |
304.72
|
| 氢键供体(HBD)数目 |
10
|
| 氢键受体(HBA)数目 |
16
|
| 可旋转键数目(RBC) |
14
|
| 重原子数目 |
59
|
| 分子复杂度/Complexity |
1760
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
PRVKSKWNDSLRBY-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C43H48O16/c1-9-11-24(46)28-32(50)18(30(48)20(34(28)52)14-22-36(54)26(16(3)44)40(58)42(5,6)38(22)56)13-19-31(49)21(35(53)29(33(19)51)25(47)12-10-2)15-23-37(55)27(17(4)45)41(59)43(7,8)39(23)57/h48-57H,9-15H2,1-8H3
|
| 化学名 |
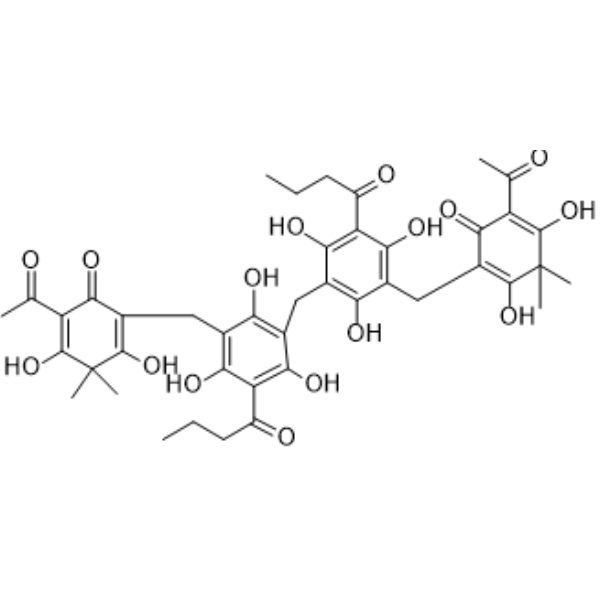
2-acetyl-4-[[3-[[3-[(5-acetyl-2,6-dihydroxy-3,3-dimethyl-4-oxocyclohexa-1,5-dien-1-yl)methyl]-5-butanoyl-2,4,6-trihydroxyphenyl]methyl]-5-butanoyl-2,4,6-trihydroxyphenyl]methyl]-3,5-dihydroxy-6,6-dimethylcyclohexa-2,4-dien-1-one
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.2183 mL | 6.0914 mL | 12.1828 mL | |
| 5 mM | 0.2437 mL | 1.2183 mL | 2.4366 mL | |
| 10 mM | 0.1218 mL | 0.6091 mL | 1.2183 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。