| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Inducible nitric oxide synthase (iNOS) (Steady-state Kd < 40 nM; IC50 vs human iNOS: 0.69 ± 0.09 µM after 15 min preincubation; Selectivity: >5800-fold vs human eNOS, >114-fold vs human nNOS; In rat tissues: ED50 = 1.15 ± 0.6 µM, selectivity >260-fold vs eNOS and 219-fold vs nNOS)
Endothelial nitric oxide synthase (eNOS) (Ki = 185 ± 32 µM) Neuronal nitric oxide synthase (nNOS) (Ki = 4.57 ± 0.23 µM)[1] |
|---|---|
| 体外研究 (In Vitro) |
GW274150 以时间依赖性方式抑制 J774 细胞的胞内 iNOS,IC50 值为 0.2 μM [1]。在大鼠组织中,GW274150 对 iNOS 的选择性分别是 eNOS 和 nNOS 的 260 倍和 219 倍。与人类 eNOS 和 nNOS 相比,人类 iNOS 分别增加 >100 倍和 >80 倍 [1]。
GW274150 是一种强效、时间依赖性、高选择性的人诱导型一氧化氮合酶 (iNOS) 抑制剂。预孵育15分钟后,其对重组人iNOS的IC50为 0.69 ± 0.09 µM。该化合物与L-精氨酸竞争性结合iNOS,表现Ks为 1.12 ± 0.1 µM。抑制作用呈时间依赖性,并且在NADPH存在下基本不可逆,计算出的稳态Kd <40 nM。在稳态下,相对于人内皮型NOS (eNOS) 和神经元型NOS (nNOS) 的选择性分别 >5800倍和 >114倍。在用IFNγ和LPS刺激表达iNOS的小鼠J774巨噬细胞中,GW274150 以时间依赖性的方式抑制细胞内NO的产生,在24小时内达到稳态IC50 0.2 ± 0.04 µM。[1] |
| 体内研究 (In Vivo) |
一次腹腔注射 GW274150(一种长效(大鼠半衰期为 5 小时)iNOS 抑制剂)可防止 14 小时后 LPS 介导的血浆 NO2 和 NO3 水平升高(ED50 = 3 mg/kg)[2] 。 GW274150(腹膜内注射;2.5、5 和 10 mg/kg)以剂量相关的方式减轻角叉菜胶引起的肺损伤程度。大鼠胸膜腔内的水肿发展和中性粒细胞浸润也显着且呈剂量依赖性减少[2]。口服(30 mg/kg,每天两次,持续 7 天)时,GW274150 显着保护神经元;然而,在帕金森病 (PD) 中,与 6-OHDA 结合使用时,它具有类似钟声的神经保护作用。在小鼠模型中,高剂量时无效[3]。
在LPS诱导的内毒素血症小鼠模型中,于LPS注射后4小时腹腔注射 (i.p.) GW274150 (30 或 100 mg/kg) 能有效抑制血浆硝酸盐/亚硝酸盐 (NOx) 水平的升高。在14小时(LPS后18小时)抑制血浆NOx的ED50为 3.2 ± 0.7 mg/kg (i.p.)。口服给药显示出相似的效力,ED50为 3.8 ± 1.5 mg/kg,表明其具有较高的口服生物利用度。GW274150 (高达 50 mg/kg i.v.) 在正常的、长期插管的小鼠中未显著影响血压,这与其对iNOS相对于eNOS的高选择性一致。在内毒素休克小鼠中,它能选择性地升高平均动脉血压。在大鼠小脑中体内抑制nNOS的作用较弱,仅在高达 100 mg/kg i.v. 的剂量下才观察到显著抑制 (47%)。[1] |
| 酶活实验 |
采用氧合血红蛋白法测定NOS酶活性。测定混合物包含HEPES缓冲液 (100 mM, pH 7.4)、二硫苏糖醇 (100 µM)、MgCl2 (0.8 mM)、氧合血红蛋白 (5 µM)、L-精氨酸 (30 µM)、NADPH (100 µM)、FAD (1 µM)、FMN (1 µM)、钙调蛋白 (100 nM) 和四氢生物蝶呤 (BH4, 10 µM)。通过分光光度法监测NO将氧合血红蛋白转化为高铁血红蛋白的过程。IC50值在37°C下于特定时间段(如0-10分钟,15-30分钟)测定。人NOS亚型使用杆状病毒系统在昆虫细胞中表达。对于详细的动力学研究,使用纯化的人iNOS(在大肠杆菌中表达)。通过将数据拟合到积分速率方程来分析GW274150时间依赖性抑制的进程曲线。通过将iNOS与GW274150和NADPH预孵育,然后大量稀释到含有过量L-精氨酸的测定混合物中来测试抑制的可逆性。[1]
|
| 细胞实验 |
在小鼠J774单核细胞白血病细胞中评估细胞内iNOS的抑制。将细胞铺板并用小鼠干扰素-γ (5 U/mL) 和LPS (1 µg/mL) 刺激24小时以诱导iNOS表达。洗涤后,将细胞与测试化合物和荧光NO指示剂 (DAF-2DA, 20 µM) 在含有L-精氨酸 (200 µM)、干扰素-γ和LPS的培养基中共同孵育。通过在不同时间点(长达24小时)测量荧光(激发492 nm,发射515 nm)来监测NO的产生。GW274150的IC50值根据时间依赖性抑制曲线确定。[1]
|
| 动物实验 |
动物/疾病模型: SD大鼠[2]
剂量: 2.5、5和10 mg/kg;单次给药 给药途径: 角叉菜胶注射前5分钟腹腔注射 (ip) 实验结果: 对角叉菜胶诱导的急性炎症肺损伤模型具有保护作用。 在体内疗效研究中,雄性CD-1小鼠经静脉注射LPS(大肠杆菌,3 mg/kg)。4小时后,以指定剂量(例如,3.2至100 mg/kg)腹腔注射 (ip) 或口服 (po) 给予GW274150(溶于生理盐水)或载体。在不同时间点(例如,LPS 注射后 18 小时用于测定 ED50)通过麻醉状态下的心脏穿刺采集血浆,用于测定硝酸盐/亚硝酸盐 (NOx) 水平。血压研究中,对清醒小鼠进行慢性插管。通过静脉注射大肠杆菌 LPS 诱导内毒素休克。静脉注射 GW274150 或载体,并监测平均动脉血压。为研究脑内 nNOS 抑制,向大鼠静脉注射 GW274150(20-200 mg/kg)或生理盐水。30 分钟后,收集小脑,冷冻后分析 NOx 含量。[1] 药代动力学研究中,向健康大鼠和小鼠静脉或口服给予 GW274150(1 或 10 mg/kg)。在不同时间点采集血样,并采用高效液相色谱-质谱联用技术测定母体化合物的血浆浓度。[1] |
| 药代性质 (ADME/PK) |
在健康大鼠中,静脉注射 10 mg/kg 剂量的 GW274150 后,其表现出双相药代动力学特征,末端半衰期 (T1/2) 约为 6.5 小时,清除率 (CL) 为 0.14 L/h/kg,稳态分布容积 (Vss) 为 1.04 L/kg。在小鼠中,静脉注射 1 mg/kg 剂量后,末端 T1/2 约为 5.7 小时。大鼠和小鼠的口服生物利用度均较高 (>90%)。与类似物 GW273629 相比,GW274150 的最大血浆浓度 (Cmax) 较低,而全身暴露量 (AUC) 较高,这预示着其体内作用持续时间更长。[1]
|
| 参考文献 |
|
| 其他信息 |
GW274150 已用于哮喘、偏头痛、偏头痛相关疾病以及关节炎和类风湿性关节炎的治疗和预防试验。
GW274150 是一种新型乙酰胺氨基酸衍生物,被鉴定为诱导型一氧化氮合酶 (iNOS) 的高选择性抑制剂。其对组成型一氧化氮合酶 (eNOS 和 nNOS) 的高选择性对于避免对血压调节和神经功能产生不良影响至关重要。该化合物是一种时间依赖性、机制性抑制剂,需要 NADPH 才能实现完全且几乎不可逆的抑制。它显示出作为治疗药物的潜力,可用于治疗涉及病理性 iNOS 激活的疾病,例如炎症性疾病(如关节炎、哮喘、术后肠梗阻)和感染性休克。 GW274150的特点是其体内作用持续时间长,这归因于其药代动力学特性及其酶抑制的不可逆性。[1] |
| 分子式 |
C8H16N2O3S
|
|---|---|
| 分子量 |
220.28924
|
| 精确质量 |
219.104
|
| CAS号 |
210354-22-6
|
| 相关CAS号 |
GW274150 phosphate;438542-15-5;GW274150 dihydrochloride;438542-17-7
|
| PubChem CID |
9797017
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
1.198
|
| tPSA |
121.21
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
14
|
| 分子复杂度/Complexity |
209
|
| 定义原子立体中心数目 |
1
|
| SMILES |
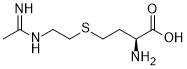
CC(=NCCSCC[C@@H](C(=O)O)N)N
|
| InChi Key |
MOLOJNHYNHBPCW-ZETCQYMHSA-N
|
| InChi Code |
InChI=1S/C8H17N3O2S/c1-6(9)11-3-5-14-4-2-7(10)8(12)13/h7H,2-5,10H2,1H3,(H2,9,11)(H,12,13)/t7-/m0/s1
|
| 化学名 |
L-Homocysteine, S-(2-((1-iminoethyl)amino)ethyl)-
|
| 别名 |
GW-274150; GW 274150; GW274150.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~456.00 mM)
H2O : ≥ 62 mg/mL (~282.72 mM) |
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.5395 mL | 22.6974 mL | 45.3947 mL | |
| 5 mM | 0.9079 mL | 4.5395 mL | 9.0789 mL | |
| 10 mM | 0.4539 mL | 2.2697 mL | 4.5395 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。