| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
RETWT (IC50 = 14.0 nM); RETV804M (IC50 = 24.1 nM); RETG810R (IC50 = 530.7 nM)
|
|---|---|
| 体外研究 (In Vitro) |
Selpercatinib (LOXO-292) 是一种口服生物可利用的、有效的、选择性的 RET 激酶抑制剂。
Selpercatinib抑制Ba/F3 RETΔ898-901和RET C634R的细胞生长,其半数最大抑制浓度(IC50)约为3 nM。[3] Selpercatinib能够非常有效地抑制Ba/F3-RETΔ898-901和Ba/F3-RET C634R细胞的细胞增殖,两种细胞系的IC50剂量约为3 nM。因此,在这些细胞中,塞帕替尼同样抑制了RETΔ898-901和RET C634R磷酸化(图4B)。与RET C634R突变体(IC50,91 nM;图4C)相比,Vandetanib在抑制RETΔ898-901突变体促进的细胞生长方面的效果低约五倍(IC50,564 nM)。[3] |
| 体内研究 (In Vivo) |
Selpercatinib(LOXO-292;10 mg/kg;ig;0-2 小时)在 FVB/NRj 小鼠口服灌胃后表现出良好的药代动力学[1]。
12个月后,患者对vandetanib表现出主要耐药性,对selpercatinib表现出次要耐药性。在selpercatinib期间对进展性病变进行的全面下一代测序显示,没有额外的RET突变,但CDKN2A、CDKN2B和MTAP基因获得性完全遗传缺失。随后用卡博扎替尼和5-FU-达卡巴嗪治疗疗效不佳。[3] 总共有212名患者在意向治疗的pembrolizumab人群中接受了随机分组。在预先计划的中期疗效分析时,中位无进展生存期为24.8个月(95%置信区间[CI],16.9至不可估计),使用塞帕替尼,11.2个月(95%CI,8.8至16.8),使用对照治疗(进展或死亡的风险比为0.46;95%CI为0.31至0.70;P<0.001)。使用selpercatinib的患者中,有客观反应的患者比例为84%(95%CI,76至90),使用对照治疗的患者中有65%(95%CI为54至75)。影响中枢神经系统的进展时间的病因特异性危险比为0.28(95%CI,0.12至0.68)。总体意向治疗人群(261名患者)的疗效结果与意向治疗pembrolizumab人群的疗效结果相似。使用塞帕替尼和对照治疗发生的不良事件与之前报告的一致。 结论:在晚期RET融合阳性NSCLC患者中,使用selpercatinib治疗的无进展生存期明显长于使用或不使用pembrolizumab的铂类化疗[4]。 |
| 细胞实验 |
在 ALKAL2 或 GDNF 刺激前两小时将 LOXO292 (1 µM) 添加到细胞中。
生长曲线和细胞活力测定[3] 将RET C634R和RETΔ898-901转化的NIH3T3细胞接种在6孔板中(10000/孔)。NIH3T3转染子在2.5%的CS中生长。每2天计数三次细胞。将RET C634R和RETΔ898-901转化的Ba/F3接种在6孔板中(300000个/孔)。在接种后的第二天,对细胞进行计数,并将不同浓度的药物或载体加入培养基中。连续4天每天对细胞进行三次计数,并使用相对于实验最后一天的细胞数量来计算生长抑制。使用Prism软件对生长曲线的最后一天进行曲线拟合分析,计算细胞生长的半最大抑制浓度(IC50)剂量[3]。 |
| 动物实验 |
雌性裸鼠(nu/nu BALB/c)
3 mg/kg og 本研究使用雌性裸鼠(nu/nu BALB/c)。所有操作均在异氟烷气体麻醉下进行。所有小鼠均未出现消瘦或其他毒性症状。将2 × 10⁵个RET C634R或RET Δ898-901转化的NIH3T3细胞皮下接种到4只小鼠的两侧腹部(每种细胞系2只小鼠)。14天后,用游标卡尺测量肿瘤大小。小鼠采用颈椎脱臼法处死;切除肿瘤并立即置于液氮中速冻。然后使用Mixer Mill MM300匀浆器在裂解缓冲液中匀浆冷冻肿瘤组织。样品经10,000×g离心两次澄清。蛋白质磷酸化水平按照标准Western blot方法进行检测。 [3] 患者被随机分配接受以下治疗:selpercatinib(160 mg,每日两次),连续21天为一个周期;或培美曲塞(500 mg/m²体表面积)联合维生素补充剂,以及研究者选择的铂类化疗(卡铂[浓度-时间曲线下面积,5;最大剂量,750 mg]或顺铂[75 mg/m²]),并联合或不联合帕博利珠单抗(200 mg),每21天一次。患者按地理区域(东亚与其他地区)、基线时脑转移情况(无或未知与有)以及研究者在随机分组前是否计划使用帕博利珠单抗或不使用帕博利珠单抗进行分层。最初,符合条件的患者按 1:1 的比例随机分配至 selpercatinib 组或对照组;然而,在方案修订后,患者按 2:1 的比例随机分配至 selpercatinib 组或对照组,因此最终的随机分组比例为 1.6:1。在完成四个疗程的对照治疗且病情未进展后,对照组患者可继续接受培美曲塞治疗,可联合或不联合帕博利珠单抗。帕博利珠单抗最多使用 35 个疗程。由于各组治疗方案存在差异,该试验对患者和研究者均采用开放标签设计。然而,申办方并未审查或分析汇总数据和疗效评估,也未审查或分析由盲法独立中心审查和研究者根据RECIST 1.1.13版进行的疾病进展评估。如果患者在疾病进展后获益,经研究者判断并获得申办方批准,患者可以继续接受selpercatinib治疗。随机分配至对照组且经盲法独立中心审查确认疾病进展的患者,可以选择交叉接受selpercatinib治疗。本文未报告交叉治疗患者的疗效和安全性结果。[4] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
局部晚期或转移性实体瘤患者每日两次服用160 mg selpercatinib,约7天后达到稳态血药浓度,Cmax为2,980(CV 53%),AUC0-24h为51,600(CV 58%)。绝对生物利用度为60%至82%(平均73%),中位tmax为2小时。食物对selpercatinib的AUC或Cmax无明显影响。肝功能损害患者的 AUC0-INF 值均出现相应升高,轻度(7%)、中度(32%)和重度(77%)肝功能损害患者的 AUC0-INF 值均升高。 健康个体单次服用 160 mg 塞帕替尼后,药物主要经粪便(69%,其中 14% 为原形)和尿液(24%,其中 12% 为原形)排出。 塞帕替尼的表观分布容积为 191 L;分布容积随体重增加而增加。 塞帕替尼的表观清除率为 6 L/h;清除率随体重增加而增加。 代谢/代谢物 塞帕替尼主要在肝脏中通过 CYP3A4 代谢。 生物半衰期 塞帕替尼在健康个体中的半衰期为 32 小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在塞帕替尼治疗甲状腺癌和非小细胞肺癌患者的上市前临床试验中,肝功能异常较为常见,但通常程度较轻。高达 55% 的塞帕替尼治疗患者出现不同程度的 ALT 升高,其中 10% 至 12% 的患者 ALT 值超过正常值上限 (ULN) 的 5 倍,且大多在治疗的最初几个月内出现;中位发病时间为 6 周,但范围从 1 天到 2 年以上不等。在纳入 531 例患者的注册前试验中,血清转氨酶升高导致 5% 至 6% 的患者暂停用药或调整剂量,但完全停药的患者不足 1%。ALT 水平受到密切监测,未导致出现黄疸等临床症状的肝损伤或肝病死亡。因此,selpercatinib 治疗与较高的短暂性血清酶升高发生率相关,但尚未明确证实其与出现临床表现明显的肝损伤(伴有黄疸)病例相关。selpercatinib 的产品说明书建议在治疗前进行常规肝功能检查,治疗的前 3 个月每 2 周检查一次,之后根据临床需要每月检查一次。 可能性评分:E(未经证实但怀疑是临床表现明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用 selpercatinib 的信息。由于 selpercatinib 与血浆蛋白的结合率为 97%,因此其在乳汁中的含量可能很低。然而,制造商建议母亲在接受 selpercatinib 治疗期间以及最后一次给药后 1 周内不要进行母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白质结合 Selpercatinib 的体外蛋白质结合率为 97%,与浓度无关,血浆浓度比为 0.7。 |
| 参考文献 | |
| 其他信息 |
药效学
Selpercatinib 通过抑制 RET 酪氨酸激酶的突变形式,在特定癌症中发挥抗肿瘤活性。由于其对 RET 的特异性高于其他酪氨酸激酶,因此与其它多激酶抑制剂相比,Selpercatinib 被认为具有更好的安全性。尽管如此,Selpercatinib 治疗仍与肝毒性、高血压、QT 间期延长、出血事件、伤口愈合受损风险以及胚胎-胎儿毒性相关;部分患者也可能对 Selpercatinib 产生超敏反应。 Selpercatinib 是一种激酶抑制剂,与其他 RTK 类别相比,它对 RET 酪氨酸激酶受体 (RTK) 具有更高的特异性。RET(转染重排)癌基因表达增强是许多癌症的标志。尽管包括卡博替尼、帕纳替尼、索拉非尼、舒尼替尼和凡德他尼在内的多激酶抑制剂已显示出对RET驱动型癌症的疗效,但由于其缺乏特异性,通常伴有显著的毒性。塞帕替尼(LOXO-292)和普拉替尼(BLU-667)是第一代用于治疗RET驱动型癌症的特异性RET RTK抑制剂。尽管塞帕替尼目前仍在临床试验NCT04211337中进行研究,但它已于2020年5月8日获得FDA加速批准,用于治疗特定的RET驱动型癌症适应症。目前,它由Loxo Oncology Inc.以RETEVMO™的商品名上市销售。塞帕替尼也已获得欧盟委员会的批准。 塞帕替尼是一种激酶抑制剂。塞帕替尼的作用机制是作为转染重排(RET)抑制剂、细胞色素P450 2C8抑制剂、细胞色素P450 3A抑制剂、P-糖蛋白抑制剂、乳腺癌耐药蛋白抑制剂以及多药和毒素外排转运蛋白1抑制剂。 塞帕替尼是一种口服选择性酪氨酸激酶受体抑制剂,该受体由RET(转染重排)编码。RET是一种原癌基因,在多种癌症(例如甲状腺髓样癌和非小细胞肺癌)中发生突变或改变。服用塞帕替尼治疗期间,血清转氨酶升高较为常见,可能导致剂量调整或停药,但尚未见报道因服用塞帕替尼而出现临床上明显的肝损伤和黄疸。 塞帕替尼是一种口服生物利用度高的选择性抑制剂,可抑制原癌基因受体酪氨酸激酶(RET)的野生型、突变型和融合产物,具有潜在的抗肿瘤活性。口服塞帕替尼后,可选择性地结合并靶向野生型RET以及各种RET突变体和含RET的融合产物。这可抑制RET活性增强的肿瘤细胞的生长。此外,selpercatinib靶向、结合并抑制血管内皮生长因子受体1(VEGFR1)和3(VEGFR3),以及成纤维细胞生长因子受体1(FGFR1)、2(FGFR2)和3(FGFR3)。RET过表达、激活突变和融合导致各种癌细胞类型中RET酪氨酸激酶活性的上调和/或过度激活; RET活性失调在这些癌症的发生发展中起着关键作用。 SELPERCATINIB是一种小分子药物,其临床试验阶段最高为IV期(涵盖所有适应症),于2020年首次获批,目前有7项已获批适应症和3项在研适应症。 背景:Selpercatinib是一种高选择性、强效且能穿透血脑屏障的RET抑制剂,在一项非随机I/II期研究中,已证实其对RET融合阳性晚期非小细胞肺癌(NSCLC)患者有效。方法:在一项随机III期试验中,我们评估了一线Selpercatinib治疗与对照治疗(铂类化疗联合或不联合帕博利珠单抗,由研究者决定)相比的疗效和安全性。主要终点是无进展生存期,由盲法独立中心审查在帕博利珠单抗治疗意向人群(即,如果患者被分配到对照组,医生计划使用帕博利珠单抗治疗的患者)和总体意向治疗人群中进行评估。如果在接受对照治疗期间,经盲法独立中心审查评估,出现疾病进展,则允许从对照组交叉到塞帕替尼组。[4] |
| CAS号 |
2306313-13-1
|
|---|---|
| 相关CAS号 |
2152628-33-4; 2306313-17-5 (mesylate); 2306313-13-1 (HCl); 2306313-14-2 (sulfate); 2306313-23-3; 2306313-16-4; 2306313-19-7 (besylate); 2306313-28-8 (fumarate); 2306313-27-7 (tartrate); 2306313-29-9 (citrate)
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| LogP |
2.5
|
| tPSA |
112
|
| 化学名 |
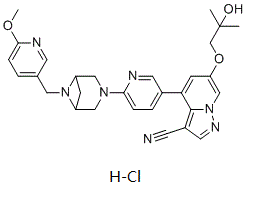
6-(2-hydroxy-2-methylpropoxy)-4-[6-[6-[(6-methoxypyridin-3-yl)methyl]-3,6-diazabicyclo[3.1.1]heptan-3-yl]pyridin-3-yl]pyrazolo[1,5-a]pyridine-3-carbonitrile hydrochloride
|
| 别名 |
LOXO-292 HCl; ARRY 192 HCl; LOXO292 HCl; LY-3527723 HCl; CEGM9YBNGD; Serpercatinib; Ret inhibitor loxo-292; LY3527723; ARRY192; LOXO 292; ARRY-192; Selpercatinib; Retevmo
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04280081 | Active Recruiting |
Drug: Selpercatinib | Solid Tumor Medullary Thyroid Cancer |
Loxo Oncology, Inc. | March 16, 2020 | Phase 2 |
| NCT05906836 | Recruiting | Drug: Rosuvastatin Drug: Selpercatinib |
Healthy | Eli Lilly and Company | July 27, 2023 | Phase 1 |
| NCT05668962 | Recruiting | Drug: Selpercatinib Drug: rhTSH |
Thyroid Cancer Thyroid Carcinoma |
Massachusetts General Hospital | March 1, 2023 | Phase 2 |
| NCT03157128 | Recruiting | Drug: LOXO-292 | Colon Cancer Any Solid Tumor |
Loxo Oncology, Inc. | May 2, 2017 | Phase 1 Phase 2 |
| NCT03899792 | Recruiting | Drug: LOXO-292 | Soft Tissue Sarcoma Infantile Fibrosarcoma |
Loxo Oncology, Inc. | June 13, 2019 | Phase 1 Phase 2 |