| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
mTORC1
Target: NV-5138 selectively targets brain mammalian target of rapamycin complex 1 (mTORC1) and exerts effects by directly activating mTORC1; the EC50 for activating phosphorylation of mTORC1 downstream substrates in vitro is approximately 0.3 μM [1] - Target: NV-5138 acts as a Sestrin modulator, specifically activating brain mTORC1 by relieving Sestrin-mediated inhibition of mTORC1 [2] |
|---|---|
| 体外研究 (In Vitro) |
NV-5138调节细胞中Sestrin2-Gator2相互作用并激活mTORC1。 [1]
NV-5138缺乏蛋白生成能力[1] NV-5138不被支链氨基转氨酶(BCAT)代谢。[1] NV-5138对Sestrin1/2具有选择性[1]。 NV-5138产生类似氯胺酮的抗抑郁行为反应。[1] < br > NV-5138具有与氯胺酮相似的长效抗抑郁作用[1] nv -5138诱导的抗抑郁作用需要mTORC1信号通路[1] NV-5138增加mPFC锥体神经元突触数量和功能。 mTORC1激活活性:NV-5138 剂量依赖性激活mTORC1,在原代皮质神经元中,1 μM浓度可使mTORC1下游底物S6核糖体蛋白(Ser235/236位点)磷酸化水平升高2.8倍,4E结合蛋白1(Thr37/46位点)磷酸化水平升高2.1倍 [1] - Sestrin-mTORC1相互作用调控:在过表达Sestrin2的HEK293T细胞中,NV-5138 (1 μM)可破坏Sestrin2与GATOR2的结合,解除Sestrin2对mTORC1的抑制,使p-S6水平较对照组升高3.2倍 [2] - 突触可塑性相关分子调控:原代海马神经元经NV-5138 (0.3-3 μM)处理24小时后,突触后致密蛋白95(PSD95)和突触素(Synapsin I)的蛋白表达水平分别升高1.5-2.3倍和1.4-2.1倍,提示促进突触发生 [2] - 抗抑郁相关体外效应:在皮质酮处理的原代神经元中,NV-5138 (1 μM)可逆转皮质酮诱导的p-S6水平降低(从对照组的42%恢复至91%),同时上调脑源性神经营养因子(BDNF)mRNA表达水平1.8倍 [2] |
| 体内研究 (In Vivo) |
研究发现,NV-5138 基本上具有 100% 的口服生物利用度,在大鼠静脉内和口服给药后测定的血浆消除半衰期约为 3 小时[1]。在 PFC 突触体制剂中,NV-5138(160 mg/kg,口服,单剂量)显着提高磷酸化 mTOR 及其下游靶标磷酸化 p70S6K1 和磷酸化 4EB-P1 的水平[2]。此外,NV-5138(80 mg/kg,口服,每天一次,共 7 天)具有抗抑郁特性[2]。
重复低剂量NV-5138 (80 mg/kg)也有抗抑郁作用。[2] 低剂量NV-5138(40或80 mg/kg, p.o)每天给药共7天(从第0天开始)的抗抑郁效果也进行了测试(图2F)。由于氯胺酮的抗抑郁作用在7天(24天)后开始逆转,因此每隔一天给予氯胺酮(10mg /kg, i.p)作为6天的阳性对照。结果表明,80mg /kg的NV-5138分别显著减少FST和NSFT的静止时间和进食潜伏期,显示出抗抑郁作用,而不改变运动活动或HCF(图2,G-J)。这与单次给药后24小时评估该剂量缺乏疗效形成鲜明对比(图1、B和D)。氯胺酮给药也分别对FST和NSFT的静止时间和进食延迟产生显著影响(图2、G和J)。 NV-5138可快速逆转慢性应激引起的行为和突触缺陷[2] 快感缺乏是抑郁症的一个核心症状,伴随着慢性不可预测压力(CUS)的暴露,需要一种典型抗抑郁药的慢性治疗来逆转这种影响,这使得CUS成为抑郁症最有效的模型之一(25,26)。CUS模型也为速效抗抑郁药提供了严格的测试,单剂量氯胺酮可快速逆转CUS诱导的快感缺乏,这是蔗糖偏好测试(SPT)确定的(8)。目前的研究结果表明,重复暴露于CUS(21天)可降低蔗糖偏好,单剂量NV-5138可快速逆转这一效应(图3、a和B)。NV-5138给药不影响非应激对照大鼠的蔗糖偏好(图3B)。两组的总饮水量和总液体消耗量无显著差异(补充图1、A、B;本文提供的在线补充材料;https://doi.org/10.1172/JCI126859DS1)。在第26天继续暴露于CUS,进行随后的行为测试和组织取样。在NSFT(第22天)中,暴露于CUS增加了进食延迟,而NV-5138迅速逆转了这一效应(图3C)。在NSFT后立即进行的实验中,没有发现CUS或NV-5138对HCF的影响(图3D),这表明NV-5138的影响不是由于喂食量的普遍增加。慢性应激暴露可显著降低体重,这是慢性应激暴露的预测结果(图3E)。 NV-5138的抗抑郁作用需要BDNF [2] 先前的研究表明,氯胺酮和其他速效抗抑郁药(包括东莨菪碱和rapastine)的抗抑郁作用需要脑源性神经营养因子(BDNF),通过输注BDNF中和的Ab (nAb)或BDNF突变小鼠来确定(33-38)。在这里,我们使用这两种方法评估了BDNF在NV-5138抗抑郁作用中的作用。大鼠在NV-5138 (160 mg/kg p.o)前30分钟在mpfc内输注BDNF (nAb) (0.5 μg/侧),24小时后开始行为测试(图5A)。在注射igg的对照大鼠中,NV-5138分别显著减少了FST和NSFT的静止时间和进食潜伏期,但BDNF nAb完全阻断了这些作用(图5、B和D);单独使用BDNF nAb对FST或NSFT、运动活动或HCF均无影响(图5,B-E)。 脑内mTORC1激活与组织分布:C57BL/6小鼠口服NV-5138 (30 mg/kg)后1小时,前额叶皮质、海马和纹状体中p-S6(Ser235/236)水平分别升高2.5倍、2.3倍和1.9倍,外周组织(肝脏、肾脏、肌肉)中无明显激活效应 [1] - 抗抑郁样行为学效应:慢性不可预测温和应激(CUMS)诱导的抑郁模型小鼠,口服NV-5138 (10 mg/kg,每日1次,连续7天)后,强迫游泳实验不动时间从218秒缩短至124秒,悬尾实验不动时间从196秒缩短至112秒;单次口服30 mg/kg后24小时,即可观察到类似抗抑郁效应,且效应持续至72小时 [2] - 突触可塑性改善:抑郁模型小鼠经NV-5138 (30 mg/kg,口服,连续14天)治疗后,海马CA1区突触密度较模型组增加35%,PSD95和BDNF蛋白表达水平分别升高42%和38% [2] - 血脑屏障穿透能力:小鼠口服NV-5138 (30 mg/kg)后,脑内药物浓度达峰时间为1小时,峰浓度(Cmax)为1.2 μM,脑-血浆浓度比为0.8 [1] |
| 酶活实验 |
体外药理筛选[1]
NV-5138在300µM浓度下进行了一式两份的测试,以检测其与107个药物不良反应靶点的潜在相互作用,包括21个转运体、受体、离子通道和中枢神经系统表达的酶。排除显著相互作用的阈值设置为绑定/响应bbb50 %。 BCAT酶促测定[1] 测定缓冲条件为:α -酮戊二酸酯(5 mM)、NADH (0.075 mM)、吡哆醛5′-磷酸(5µM)、亮氨酸脱氢酶(0.95 U)、硫酸铵(50 mM)、DTT (5 mM)和载药(水)、l -亮氨酸、精氨酸和NV-5138。将检测缓冲液分配到96孔板中,加热至37°C 10 min,然后在0.1 M磷酸钾缓冲液中加入BCAT1或BCAT2 (72 ng)。然后在RT下使用Envision平板读取器每分钟读取340 nm处的吸光度,持续30分钟。使用的每种试剂的来源可在补充信息中找到。 14c -亮氨酸蛋白掺入试验[1] 用PBS洗涤HeLa细胞一次,然后在含有CHX (10 ug/ml)或DMSO(1%终值)的饥饿培养基(亮氨酸和无血清DMEM)中37℃孵育2.5 h。孵育后,用PBS洗涤一次细胞,然后在含有14c -亮氨酸(2µCi/ml)的标记培养基中与NV-5138或非放射性亮氨酸在37℃下孵育30分钟。孵育后,收集细胞并在Tris/HCl 10 mM pH 7.4 + 1% NP40中裂解。将裂解液与水和20%三氯乙酸(1:1:2)混合,在冰上孵育2小时,沉淀蛋白质。通过离心收集蛋白质,在NaOH中溶解,置于闪烁液中,在Wallac Microbeta Trilux 2450上读取,计数2分钟。闪烁值被归一化为dmso处理井中计数的百分比。 等温滴定热法(ITC)[1] 由于NV-5138是天然配体l -亮氨酸的类似物,并且已知亮氨酸似乎与Sestrin212共同纯化,因此开发了一种将内源性亮氨酸从结合位点置换为较弱的Sestrin2配体L-Methionine24的程序。蛋氨酸后来被亮氨酸和类似物取代,用于直接结合测量。NV-5138合成和ITC蛋白制备的详细信息可参见补充信息。 mTORC1活性检测实验:原代皮质神经元接种后培养7天,加入系列浓度NV-5138 (0.01-10 μM)孵育24小时。提取细胞总蛋白,经Western blot检测p-S6(Ser235/236)、p-4EBP1(Thr37/46)及总S6、总4EBP1蛋白表达,以p-S6/总S6比值作为mTORC1激活指标,通过非线性回归分析计算EC50 [1] - Sestrin-GATOR2结合干扰实验:构建Sestrin2和GATOR2亚基(WDR24)的表达载体,共转染HEK293T细胞。加入NV-5138 (0.1-3 μM)孵育16小时后,进行免疫共沉淀实验(以Sestrin2抗体沉淀复合物),Western blot检测复合物中WDR24的含量,分析NV-5138 对两者结合的干扰效果 [2] |
| 细胞实验 |
细胞培养[1]< br >
所有细胞系在添加10% FBS的DMEM中培养,并在37°C和5% CO2中保持。如前所述,产生了稳定表达Flag-WDR24的HEK-293T细胞。对于亮氨酸饥饿,细胞用不含亮氨酸的DMEM和添加10% dFBS孵育50分钟,然后用NV-5138、亮氨酸或载体处理10分钟。用于细胞培养的试剂的详细信息可在补充信息中找到。
<人力资源>
免疫沉淀(IP)免疫印迹(Western blotting): [1]
如前所述制备细胞裂解物24。裂解物在4°C下13200 rpm离心8 min后被清除。对于抗flag的IPs,将FLAG-M2亲和凝胶加入约2mg的裂解物中,在4°C下旋转孵育3小时。IP后,用含有500 mM NaCl的Triton洗涤缓冲液洗涤一次。在基于裂解物的蛋白相互作用实验中,IPs以指定剂量重悬于含有载体、NV-5138或亮氨酸的细胞质缓冲液中10分钟。化合物孵育后,离心收集IPs。免疫沉淀蛋白变性,SDS-PAGE分离。使用LI-COR成像系统对膜进行成像。所用试剂和抗体在补充信息中列出。 <人力资源> 细胞热移试验(CETSA)[1] CETSA的执行方法如前所述23。简单地说,HEK293T细胞在不含亮氨酸的培养基中孵育1小时,然后加入NV-5138(300µM)、亮氨酸(300µM)或载体(水)再孵育30分钟。收集细胞,300g室温(RT)离心3min, PBS洗涤,再次离心,最后用1ml含EDTA-free蛋白酶抑制剂片(Roche)的RT PBS重悬。每个细胞悬液在指定温度下加热100µl,加热3 min,样品在RT下放置在工作台上3 min,然后在液氮中快速冷冻。为了使细胞溶解,样品经过两个循环的冻融,然后在4°C下20000 g离心20分钟。所得上清80µl变性,SDS-PAGE分离。使用LI-COR成像系统对膜进行成像。使用的抗体在补充信息中列出。 原代神经元培养与mTORC1激活检测:从胚胎18天大鼠大脑分离皮质或海马神经元,接种于包被后的培养板,培养7-10天。加入NV-5138 处理指定时间后,提取蛋白进行Western blot分析,或固定细胞进行免疫荧光染色(检测p-S6的细胞定位)[1] - 突触相关蛋白表达检测:原代海马神经元经NV-5138 (0.3-3 μM)处理24小时后,提取总蛋白,通过Western blot检测PSD95、Synapsin I的表达水平,以β-肌动蛋白为内参,ImageJ软件定量条带灰度值 [2] - 皮质酮诱导神经元损伤模型实验:原代皮质神经元培养7天后,加入皮质酮(200 μM)建立损伤模型,同时加入NV-5138 (0.1-3 μM)共孵育24小时。提取RNA逆转录为cDNA,qPCR检测BDNF mRNA表达水平;提取蛋白检测p-S6和总S6表达 [2] |
| 动物实验 |
体重 250-260 g 的雄性 Sprague-Dawley 大鼠[2]。
40、80、160 mg/kg。 口服,单次剂量 (160 mg/kg) 或每日一次,连续 7 天 (40、80 mg/kg)。 动物和给药。[2] 除慢性不可预测应激 (CUS) 实验外,大多数研究均使用体重 250-260 g 的雄性 Sprague-Dawley 大鼠。CUS 实验由于研究持续时间较长,使用了体重 120-140 g 的大鼠。此外,还使用了先前描述的 BDNF Val66Met 突变敲入小鼠(8-12 周龄的 Val/Val WT、杂合 Val/Met 和纯合 Met/Met 小鼠)来测试 BDNF 的作用。动物单独饲养,置于标准条件下,光照/黑暗周期为 12 小时/12 小时,并可自由摄取食物和水。大鼠单次口服给予赋形剂(0.5% 甲基纤维素和 0.1% Tween 80)、NV-5138(40、80 或 160 mg/kg,口服,Navitor Pharmaceuticals Inc.)、氯胺酮(10 mg/kg,腹腔注射)、DMSO(0.5%;1 ml/kg,腹腔注射)或 NBQX(10 mg/kg,腹腔注射,Tocris Bioscience)。在重复给药研究中,每日口服给予NV-5138(40或80 mg/kg),共7天;每隔一天腹腔注射氯胺酮(10 mg/kg),共6天。 NV-5138在大鼠体内的药代动力学分析[1] 为确定口服生物利用度,雄性SD大鼠分别静脉注射1 mg/kg和口服5 mg/kg的NV-5138(溶于0.5% MC/0.1% Tween80溶液中)(每组每个时间点n=3)。口服组大鼠禁食过夜,静脉注射组大鼠可自由摄取食物和水。给药后,在指定时间点采集尾静脉血至K2EDTA抗凝管中,并以2000 g离心5分钟收集血浆。为了测定脑组织和血浆中NV-5138的浓度,将大鼠经口给予160 mg/kg的NV-5138(n = 5),给药1小时后断头处死,采集躯干血和一侧脑半球。将血浆与含有普瑞巴林作为内标的乙腈混合并离心,脑组织和心脏样本直接在乙腈中匀浆。采用液相色谱-串联质谱法(LC-MS/MS)定量分析NV-5138的浓度。使用 WinNonlin V 6.2 统计软件,采用非房室模型生成药代动力学参数。 mTORC1 信号通路和突触蛋白的蛋白质印迹分析[1] SD 大鼠经口灌胃给予 NV-5138、亮氨酸或赋形剂(50 mg/ml,溶于含 0.5% MC 和 0.1% Tween80 的水中),剂量和时间点如所示。给药后,立即用断头台处死动物。迅速显微解剖特定脑区,收集组织,并立即液氮速冻。外周组织和所有脑组织均使用MP匀浆器在裂解缓冲液(细胞裂解缓冲液:1% Triton X-100、50 mM HEPES pH 7.4、100 mM NaCl、2 mM EDTA、10 mM β-甘油磷酸钠、10 mM 焦磷酸钠和1%蛋白酶抑制剂)中于4℃下匀浆。各脑区突触蛋白和mTORC1的分析均按照先前描述的方法16在粗突触体制备物上进行。每个样本等量的总蛋白经变性后,通过SDS-PAGE电泳分离。使用LI-COR成像系统对膜进行成像。蛋白质水平以微管蛋白或GAPDH水平进行标准化,并进一步以载体处理的对照组大鼠的水平进行标准化。所用抗体列于补充信息中。 脑内 mTORC1 激活和药代动力学分布实验:将 8 周龄 C57BL/6 小鼠随机分组,分别口服 NV-5138(10、30 mg/kg)或载体(0.5% 甲基纤维素 + 0.1% Tween 80)。分别于给药后 0.5、1、2、4 和 8 小时处死小鼠,收集血浆和脑组织(前额叶皮层、海马、纹状体、肝脏、肾脏)。将脑组织匀浆,并通过 LC-MS/MS 检测药物浓度;同时,提取脑组织蛋白,并通过Western blot检测p-S6水平[1] - 慢性抑郁模型(CUMS)疗效实验:将8周龄C57BL/6小鼠进行CUMS处理(包括食物剥夺、饮水剥夺、笼子倾斜、昼夜颠倒等,每天一次刺激,连续4周)。造模后,每天一次口服NV-5138(10、30 mg/kg)或阳性对照药物,连续7天。在给药期间进行行为测试:强迫游泳测试(记录 6 分钟内的不动时间)、悬尾测试(记录 6 分钟内的不动时间)、新奇抑制进食测试(记录首次进食潜伏期)[2] - 单剂量抗抑郁作用实验:正常 C57BL/6 小鼠或 CUMS 模型小鼠单次口服 NV-5138 (30 mg/kg) 或载体。在给药后 24、48 和 72 小时进行强迫游泳和悬尾试验,以评估抗抑郁药作用的持续时间 [2] - 突触可塑性检测动物实验:将 CUMS 模型小鼠用 NV-5138(30 mg/kg,连续 14 天口服)治疗后,处死小鼠并收集海马组织,制备冰冻切片,采用免疫荧光染色检测 PSD95(突触后标记物)和突触蛋白 I(突触前标记物)的荧光强度。使用 ImageJ 软件分析突触密度 [2] |
| 药代性质 (ADME/PK) |
口服NV-5138后的药代动力学(PK)和药效学(PD)[1]
研究发现,NV-5138的口服生物利用度接近100%,在大鼠静脉和口服给药后,其血浆消除半衰期约为3小时(补充表3和图4a)。鉴于NV-5138良好的药代动力学特性,我们希望确定口服NV-5138是否能够激活自由摄食大鼠脑和其他器官中的mTORC1,并以mTORC1下游底物磷酸化S6 (S240/244pS6)作为该复合物激活状态的替代药效学参数。如图 3a 和补充图 5a 所示,给药 1 小时后,从大脑前额叶皮层 (PFC) 分离的突触体中 S240/244pS6 的含量呈剂量依赖性增加,在 160 mg/kg 剂量组观察到较溶剂对照组显著增加约 2 倍,在 80 mg/kg 剂量组观察到增加趋势。基于此结果,我们决定使用 160 mg/kg 口服剂量进行后续实验,结果显示血浆和全脑提取物中的药代动力学特征相似,表明脑暴露量较高(补充图 4b)。单次口服 NV-5138 一小时后,除前额叶皮层外,包括纹状体、海马、新皮层在内的多个脑区均观察到 mTORC1 的显著激活,但小脑未见激活(图 3b 和补充图 5b)。 口服生物利用度和血浆代谢:小鼠口服 NV-5138 (30 mg/kg) 的生物利用度为 42%,血浆峰时间 (Tmax) 为 1 小时,Cmax 为 1.5 μM,末端半衰期 (t1/2) 为 3.8 小时,AUC0-∞ 为 8.7 μM·h [1] - 组织分布和血脑屏障穿透:给药后 1 小时,NV-5138 在各个脑区(前额叶皮层、海马、纹状体)的浓度为脑血浆浓度比为0.8,血血浆浓度比为0.9-1.2 μM;肝脏和肾脏浓度分别为2.3 μM和1.8 μM,肌肉浓度仅为0.3 μM,表明其具有脑靶向性[1] - 代谢和排泄:人肝微粒体实验表明,NV-5138主要通过CYP3A4代谢生成2种主要的氧化代谢物;小鼠给药后48小时内,尿液排泄量占给药剂量的32%,粪便排泄量占58%,其中原药分别占尿液和粪便排泄量的12%和25%[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
急性毒性:小鼠单次口服剂量高达 200 mg/kg 的 NV-5138,14 天内未出现死亡或明显的毒性症状(体重、行为和食物摄入量正常),半数致死量 (LD50) >200 mg/kg [1]
- 重复给药毒性:大鼠连续 28 天每日一次口服 NV-5138 (30, 100 mg/kg),体重增加正常,血常规、肝肾功能(ALT、AST、肌酐、尿素氮)和电解质指标均在正常范围内;病理切片显示,心脏、肝脏、脾脏、肺脏、肾脏和脑等主要器官未见明显病理损伤[1] - 血浆蛋白结合率:体外实验确定,NV-5138 的人血浆蛋白结合率为 82%-86%,小鼠血浆蛋白结合率为 78%-83%[1] - 安全性:在抗抑郁有效剂量(10-30 mg/kg)下,未观察到明显的镇静、运动协调障碍或认知功能障碍,也未观察到血糖或血脂异常[2] |
| 参考文献 | |
| 其他信息 |
雷帕霉素靶蛋白复合物1 (mTORC1) 与多种重要的慢性疾病相关,其中许多疾病与年龄增长有关。mTORC1 的完全激活需要多种输入信号,包括氨基酸亮氨酸。胞质蛋白 Sestrin1 和 Sestrin2 特异性地结合多蛋白复合物 GATOR2,并将亮氨酸充足状态传递给 mTORC1 通路激活复合物。本文报道了一种新型口服生物利用度高的化合物 NV-5138,它能与 Sestrin2 结合,并在体外和体内激活 mTORC1。与亮氨酸类似,NV-5138 可在多种外周组织中短暂激活 mTORC1,但与亮氨酸不同的是,由于 NV-5138 不参与蛋白质合成,因此它仅在大脑中激活该复合物。因此,NV-5138 将有助于探索尚未满足的医疗需求领域,包括与 mTORC1 激活状态相关的神经精神疾病和认知障碍。[1]临床前研究表明,包括氯胺酮在内的速效抗抑郁药需要刺激 mTORC1 信号通路。该通路受神经元活动、内分泌和代谢信号的调控,尤其是氨基酸亮氨酸,它通过与上游调节因子 sestrin 结合来激活 mTORC1 信号通路。在此,我们研究了 NV-5138 的抗抑郁作用,NV-5138 是一种新型高选择性小分子 sestrin 调节剂,能够穿透血脑屏障。结果表明,单次注射 NV-5138 即可产生快速且持久的抗抑郁作用,并能迅速逆转慢性应激引起的快感缺失。 NV-5138 的抗抑郁作用需要 BDNF 的释放,因为将 BDNF 中和抗体注入内侧前额叶皮层 (mPFC) 或在敲入阻断活性依赖性 BDNF 释放的 BDNF 多态性的小鼠中,行为反应均被阻断。NV-5138 给药还能迅速增加 mPFC 中的突触数量和功能,并逆转慢性应激引起的突触缺陷。综上所述,这些结果表明 NV-5138 通过激活 mTORC1 通路和 BDNF 信号通路产生快速的突触和抗抑郁行为反应,提示对 sestrin 进行药理学调控是开发速效抗抑郁药的一种新方法。[2]
药物分类和研发背景:NV-5138 是首个被发现的选择性脑 mTORC1 激活剂,是一种分子量为 412.5 Da 的小分子化合物。经过结构优化后,NV-5138 具有良好的脑渗透性和口服生物利用度[1] - 作用机制:NV-5138 通过两条途径激活脑内 mTORC1:一条途径是直接与 mTORC1 的调节结构域结合,增强其激酶活性;另一条途径是作为 Sestrin 调节剂,干扰 Sestrin 与 GATOR2 之间的相互作用,解除 Sestrin 介导的 mTORC1 抑制,最终促进突触可塑性和神经营养因子表达,从而发挥抗抑郁作用[2] - 适应症相关潜力:基于动物实验结果,NV-5138 具有快速起效的抗抑郁作用潜力。单次给药后24小时即可观察到其抗抑郁样作用,且无传统抗抑郁药起效延迟的问题,为抑郁症的治疗提供了一种新的策略[2] - 选择性特征:NV-5138对mTORC2无激活或抑制作用,对其他激酶(如PI3K、Akt、ERK)无明显影响,且在外周组织中对mTORC1的激活作用较弱,从而降低了全身性副作用的风险[1] |
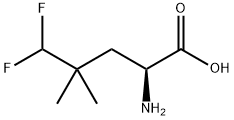
| 分子式 |
C7H13F2NO2
|
|---|---|
| 分子量 |
181.1804292202
|
| 精确质量 |
181.09
|
| 元素分析 |
C, 46.40; H, 7.23; F, 20.97; N, 7.73; O, 17.66
|
| CAS号 |
2095886-80-7
|
| 相关CAS号 |
NV-5138 hydrochloride;2639392-70-2
|
| PubChem CID |
129050791
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
-1
|
| tPSA |
63.3
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
12
|
| 分子复杂度/Complexity |
171
|
| 定义原子立体中心数目 |
1
|
| SMILES |
CC(C)(C[C@@H](C(=O)O)N)C(F)F
|
| InChi Key |
HRFIMCJTDKEPPV-BYPYZUCNSA-N
|
| InChi Code |
InChI=1S/C7H13F2NO2/c1-7(2,6(8)9)3-4(10)5(11)12/h4,6H,3,10H2,1-2H3,(H,11,12)/t4-/m0/s1
|
| 化学名 |
Pentanoic acid, 2-amino-5,5-difluoro-4,4-dimethyl-, (2S)-
|
| 别名 |
NV 5138; NV-5138; 2095886-80-7; 4-(difluoromethyl)-L-leucine; (2S)-2-amino-5,5-difluoro-4,4-dimethylpentanoic acid; 06CA9QMG6Z; Pentanoic acid, 2-amino-5,5-difluoro-4,4-dimethyl-, (2S)-; ((S)-2-Amino-5,5-difluoro-4,4-dimethylpentanoic acid; NV5138
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~10 mg/mL (~55.2 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 5.5194 mL | 27.5969 mL | 55.1937 mL | |
| 5 mM | 1.1039 mL | 5.5194 mL | 11.0387 mL | |
| 10 mM | 0.5519 mL | 2.7597 mL | 5.5194 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05066672 | Recruiting | Drug: NV-5138 Drug: matched placebo |
Treatment Resistant Depression | Navitor Pharmaceuticals, Inc. | February 28, 2022 | Phase 2 |