| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
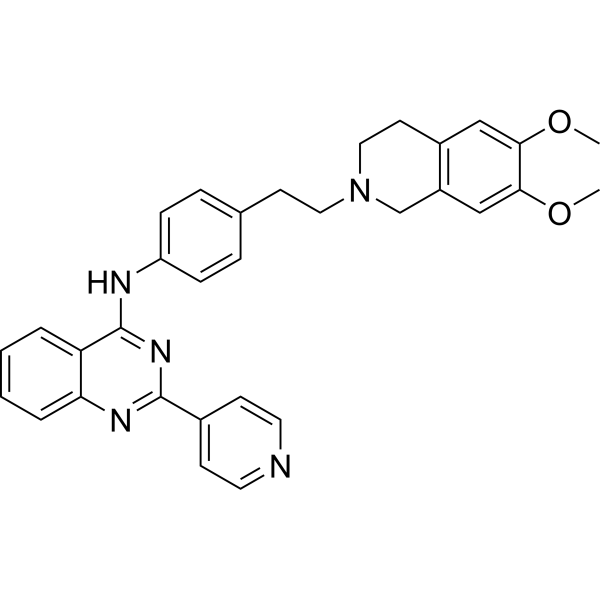
The target of the compound 12k (a derivative of N-(4-(2-(6,7-Dimethoxy-3,4-dihydroisoquinolin-2(1H)yl)ethyl)phenyl)quinazolin-4-amine) is P-glycoprotein (P-gp, also known as ATP Binding Cassette Transporter, Subfamily B, Member 1, ABCB1). It exhibits inhibitory activity against P-gp, with an EC₅₀ value of 57.9 ± 3.5 nM in reversing doxorubicin (DOX) resistance in K562/A02 cells. Additionally, it inhibits P-gp ATPase activity without affecting CYP3A4 activity or P-gp expression[1]
|
|---|---|
| 体外研究 (In Vitro) |
P-gp 抑制剂 1 (12k) 可逆转 K562/A02 细胞中的阿霉素 (DOX) 耐药性 80 分钟,具有高效 (EC50=57.9±3.5 nM)、最小的细胞毒性和延长的活性持续时间 (1 μM)[1]。 P-gp抑制剂1还可以阻断Pgp介导的Rh123外排,增加DOX的积累,抑制K562/A02 MDR细胞中P-gp ATP酶的活性(0.1、1、5μM,1小时),并增强其他药物的效力具有不同结构的MDR相关细胞毒性药物[1]。
1. 逆转K562/A02细胞DOX耐药性:化合物12k在K562/A02细胞中表现出强效的DOX耐药逆转活性,EC₅₀为57.9 ± 3.5 nM,且在发挥耐药逆转作用的有效浓度下,对K562/A02细胞的细胞毒性较低[1] 2. 增强其他MDR相关细胞毒性药物的药效:12k可提高多种不同化学结构的MDR相关细胞毒性药物在K562/A02细胞中的药效,增强其对耐药细胞生长的抑制作用[1] 3. 增加细胞内DOX蓄积:K562/A02细胞经12k处理后,细胞内DOX的蓄积量显著升高,这一现象归因于12k对P-gp介导的药物外排功能的抑制[1] 4. 阻断P-gp介导的Rh123外排:12k可阻断P-gp的底物罗丹明123(Rh123)从K562/A02细胞中外排。经12k处理后,细胞内Rh123的滞留量增加,表明P-gp的外排功能受到抑制[1] 5. 抑制P-gp ATP酶活性:12k可抑制K562/A02细胞中P-gp的ATP酶活性,这与P-gp药物转运功能的抑制密切相关(P-gp依赖ATP水解驱动药物外排)[1] 6. 不影响CYP3A4活性及P-gp表达:相关细胞经12k处理后,细胞色素P450酶CYP3A4的活性未发生改变,且P-gp的表达水平(蛋白及mRNA水平均无变化)也未受影响[1] |
| 体内研究 (In Vivo) |
1. 药代动力学特性:化合物12k具有良好的体内药代动力学特性,包括较长的半衰期(t₁/₂)和良好的口服生物利用度,这为其临床口服给药应用提供了支持[1]
2. 对DOX代谢的影响:12k在体内对DOX的代谢无影响。这一特性至关重要,可避免因代谢改变导致细胞毒性药物(如DOX)血浆浓度升高而引发的副作用[1] |
| 酶活实验 |
1. P-gp ATP酶活性测定:首先从K562/A02细胞中制备含P-gp的样品(如分离富含P-gp的细胞膜)。随后,将样品与不同浓度的12k及定量的ATP(P-gp ATP酶的底物)共同孵育。孵育过程中,P-gp催化ATP水解为ADP和无机磷酸(Pi)。反应结束后,采用特定检测方法(如比色法或荧光法)检测生成的Pi含量(ATP酶活性的指标)。通过比较加入与未加入12k时的Pi生成量,评估12k对P-gp ATP酶活性的影响,Pi生成量减少表明12k抑制了P-gp ATP酶活性[1]
2. CYP3A4活性测定:构建包含重组CYP3A4酶、特异性CYP3A4底物(如荧光或发光底物)及CYP3A4活性所需辅因子的酶反应体系。向体系中加入不同浓度的12k,在适宜温度下孵育一定时间。孵育结束后,采用合适的分析方法(如高效液相色谱法或荧光检测法)检测底物生成的代谢产物量(反映CYP3A4活性)。通过比较加入与未加入12k时的代谢产物生成量,确定12k对CYP3A4活性无影响[1] |
| 细胞实验 |
蛋白质印迹分析[1]
细胞类型: K562/A02 细胞 测试浓度: 0.1、0.5 或 2.0 μM 孵育时间: 72 hrs(小时) 实验结果: 12k 的 MDR 逆转不是由蛋白质表达减少引起的,而很可能是由于直接抑制 P-gp 流出所致[1]。 1. K562/A02细胞耐药逆转测定(MTT法):将K562/A02细胞以适宜密度接种于96孔板,培养一定时间使细胞贴壁。向孔中加入不同浓度的12k,随后加入固定浓度的DOX(K562/A02细胞对其耐药的细胞毒性药物)。共孵育特定时间(如48小时)后,向各孔中加入MTT试剂并继续孵育。活细胞生成的甲臜结晶用溶解液溶解,通过酶标仪测定特定波长下的吸光度值。根据吸光度值计算细胞存活率,通过分析量效关系确定12k逆转DOX耐药的EC₅₀值[1] 2. 细胞内DOX蓄积测定:收集对数生长期的K562/A02细胞,用适宜缓冲液重悬并调整细胞浓度。向细胞悬液中加入不同浓度的12k,预孵育一定时间后,加入DOX至终浓度并孵育特定时间。孵育结束后,用冰浴缓冲液洗涤细胞,去除细胞外的DOX和12k。采用流式细胞仪检测细胞内DOX的荧光强度,通过比较加入与未加入12k时的荧光强度,计算细胞内DOX的相对蓄积量[1] 3. Rh123外排测定:收集对数生长期的K562/A02细胞,用缓冲液重悬。向细胞悬液中加入Rh123至终浓度,37°C孵育一定时间使Rh123进入细胞。用冰浴缓冲液洗涤细胞去除细胞外Rh123后,向细胞悬液中加入不同浓度的12k。37°C孵育特定时间后,采用流式细胞仪检测细胞内Rh123的荧光强度。通过比较加入与未加入12k时的荧光强度,评估Rh123的外排速率,进而确定12k阻断P-gp介导Rh123外排的能力[1] 4. 12k单独细胞毒性测定:将K562/A02细胞以适宜密度接种于96孔板,培养一段时间后,向孔中加入不同浓度的12k(不含DOX),孵育48小时。后续步骤同上述MTT法,计算细胞存活率,评估12k单独对K562/A02细胞的细胞毒性[1] 5. P-gp表达检测(western blot及PCR):用不同浓度的12k处理K562/A02细胞一定时间。western blot分析时,用裂解液裂解细胞提取总蛋白,测定蛋白浓度。将等量蛋白通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,转移至聚偏氟乙烯(PVDF)膜上。膜经封闭液封闭后,加入抗P-gp一抗及辣根过氧化物酶(HRP)标记的二抗孵育。采用增强化学发光(ECL)检测系统显影蛋白条带,通过密度分析定量P-gp蛋白的相对表达水平。PCR分析时,用RNA提取试剂盒提取处理后细胞的总RNA,逆转录合成互补DNA(cDNA)。使用P-gp特异性引物及内参管家基因引物进行PCR扩增,扩增产物经琼脂糖凝胶电泳分析,通过与内参条带强度对比,确定P-gp mRNA的相对表达水平[1] |
| 动物实验 |
1. 大鼠体内化合物 12k 的药代动力学研究:选取雄性 Sprague-Dawley 大鼠,并在实验前使其适应实验环境一段时间。将化合物 12k 配制成合适的口服剂型(例如,悬浮于含增溶剂的溶液中)和静脉注射剂型。口服给药组大鼠通过灌胃给予特定剂量的化合物 12k。静脉注射组大鼠通过尾静脉注射特定剂量的化合物 12k。分别于给药后不同时间点从眼眶静脉丛采集血样,置于肝素化试管中。离心分离血浆后,采用灵敏的分析方法(例如,液相色谱-串联质谱法,LC-MS/MS)测定血浆中化合物 12k 的浓度。采用药代动力学软件[1]计算半衰期(t₁/₂)、口服生物利用度(F)、浓度-时间曲线下面积(AUC)、血浆峰浓度(Cₘₐₓ)和达峰时间(Tₘₐₓ)等药代动力学参数。
2. 体内研究12k对阿霉素(DOX)代谢的影响:将雄性Sprague-Dawley大鼠随机分为两组,包括对照组(单独给予DOX)和实验组(12k联合DOX)。实验组按特定剂量和频率(例如,连续数日每日一次灌胃)给予12k,并在特定日期通过静脉注射或其他途径给予特定剂量的DOX。在DOX给药后不同时间点采集血样,并分离血浆。采用液相色谱-串联质谱法(LC-MS/MS)或其他合适的方法测定血浆中阿霉素(DOX)及其代谢物的浓度。比较两组受试者血浆中阿霉素的药代动力学参数,以评估12k是否对阿霉素的代谢产生影响[1] |
| 药代性质 (ADME/PK) |
1. 半衰期 (t₁/₂):12k在大鼠口服或静脉注射后均具有良好的半衰期[1]
2. 口服生物利用度 (F):12k在大鼠中表现出良好的口服生物利用度[1] 3. 对药物代谢的影响:12k不影响体内阿霉素的代谢[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 体外细胞毒性:化合物 12k 在逆转耐药性的有效浓度下对 K562/A02 细胞显示出较低的细胞毒性[1]
2. 药物相互作用:化合物 12k 不影响 CYP3A4 的活性,表明其与 CYP3A4 底物发生药物相互作用的可能性较低[1] |
| 参考文献 | |
| 其他信息 |
1. 背景:P-糖蛋白(P-gp)介导的多药耐药性(MDR)是癌症化疗成功的主要障碍。12k是一种新型的P-gp抑制剂,具有喹唑啉骨架,在合成的衍生物中被认为是最有希望进行深入研究的候选药物[1]。
2. 作用机制:12k主要通过抑制P-gp的外排功能(阻断DOX和Rh123等底物的外排)和抑制P-gp ATPase活性来逆转P-gp介导的MDR,而不改变P-gp的表达或影响CYP3A4的活性[1]。 |
| 分子式 |
C32H31N5O2
|
|---|---|
| 分子量 |
517.620846986771
|
| 精确质量 |
517.247
|
| CAS号 |
2050747-49-2
|
| PubChem CID |
132822387
|
| 外观&性状 |
Light yellow to brown solid powder
|
| LogP |
5.8
|
| tPSA |
72.4
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
8
|
| 重原子数目 |
39
|
| 分子复杂度/Complexity |
742
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O(C)C1C(=CC2=C(C=1)CN(CCC1C=CC(=CC=1)NC1C3C=CC=CC=3N=C(C3C=CN=CC=3)N=1)CC2)OC
|
| InChi Key |
TXKOCTPGTLRGNL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C32H31N5O2/c1-38-29-19-24-14-18-37(21-25(24)20-30(29)39-2)17-13-22-7-9-26(10-8-22)34-32-27-5-3-4-6-28(27)35-31(36-32)23-11-15-33-16-12-23/h3-12,15-16,19-20H,13-14,17-18,21H2,1-2H3,(H,34,35,36)
|
| 化学名 |
N-[4-[2-(6,7-dimethoxy-3,4-dihydro-1H-isoquinolin-2-yl)ethyl]phenyl]-2-pyridin-4-ylquinazolin-4-amine
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~16.67 mg/mL (~32.21 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9319 mL | 9.6596 mL | 19.3192 mL | |
| 5 mM | 0.3864 mL | 1.9319 mL | 3.8638 mL | |
| 10 mM | 0.1932 mL | 0.9660 mL | 1.9319 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。