| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 体外研究 (In Vitro) |
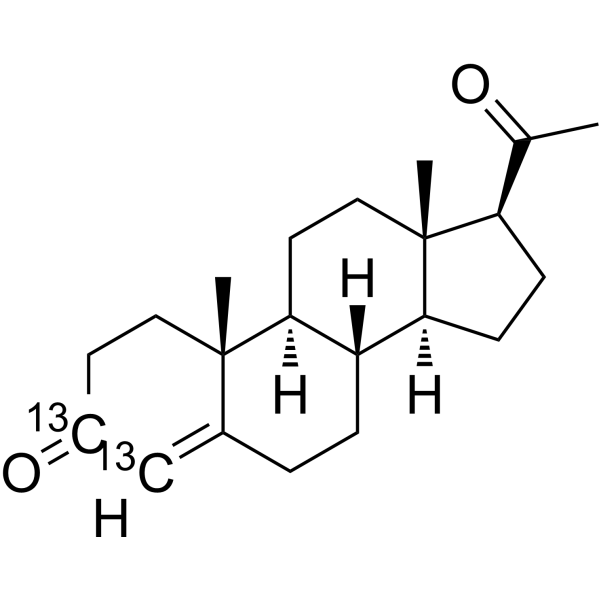
药物化合物包括碳、氢和其他元素的稳定重同位素,在药物开发过程中主要作为定量示踪剂。由于氘化可能会影响药物的药代动力学和代谢特性,因此值得关注[1]。
|
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期使用概述 由于母乳中孕酮的报道含量较低,即使使用高剂量产品,婴儿摄入的量也很少,预计不会对母乳喂养的婴儿造成任何不良影响。某些国家/地区提供的孕酮阴道环可使母体血液中的孕酮水平低于排卵期女性。大多数研究表明,孕酮不会对乳汁分泌或哺乳期持续时间产生不利影响。似乎无需采取特殊预防措施。 在俄罗斯,孕酮凝胶(Progestogel - Besins Healthcare;美国未上市)曾被用于局部涂抹于乳房,用于治疗产后乳房胀痛,尤其是在其他保守治疗无效的情况下。一项后续研究未能检测到在乳房胀痛的母亲使用孕酮凝胶 20 分钟后乳房硬度有任何降低。该用途的安全性和有效性尚未得到充分研究,Progestogel 的生产商建议哺乳期妇女避免使用该药物。 ◉ 对母乳喂养婴儿的影响 84 名妇女在产后 30 至 35 天之间植入了 6 个皮下植入剂,每个植入剂含有 100 毫克孕酮,作为避孕措施。与接受安慰剂或铜 T 宫内节育器的妇女相比,她们的婴儿在产后前 6 个月的生长速度没有差异。 192 名母亲在产后第 60 天植入了 6 个皮下植入剂,每个植入剂含有 100 毫克孕酮,作为避孕措施。本研究比较了60名纯母乳喂养6个月的婴儿与母亲分别接受安慰剂(第30天时n=68)或铜T宫内节育器(第30天时n=64,第60天时n=49)的婴儿的体重增长情况。结果显示,3组婴儿在6个月大时的平均体重增长无显著差异。 128名妇女在产后约60天植入了释放孕酮的阴道环。其中两种阴道环分别释放孕酮:一种为每日7.5毫克,90天后递减至4.5毫克;另一种为每日15毫克,90天后递减至7毫克。产后前12个月,使用孕酮环的母亲所生的纯母乳喂养婴儿与使用铜T宫内节育器避孕的对照组母亲所生的纯母乳喂养婴儿的体重增长无差异。 120名哺乳期妇女在产后第5至7周开始使用阴道环,该阴道环每日释放约10毫克孕酮,持续90天。与正常人群相比,母乳喂养婴儿的生长发育或发育里程碑均无差异。 187名哺乳期妇女在产后第57天左右开始使用阴道环,该阴道环每日释放约10毫克孕酮。一项研究比较了100名产后29至64天使用阴道环(每日释放约10毫克孕酮)的女性和262名产后5至9周开始使用宫内节育器(Copper T)的女性,结果发现,在产后第一年,两组女性的母乳喂养婴儿体重增长无差异。在为期14个月的观察期内,两组母乳喂养婴儿的体重增长没有差异。 一项比较产后妇女使用孕酮环(n = 459)和铜T宫内节育器(n = 330)的研究发现,孕酮环对婴儿的母乳喂养或生长发育没有不良影响。 ◉ 对泌乳和母乳的影响 84名妇女在产后30至35天之间植入了6个皮下植入物,每个植入物含有100毫克孕酮,作为避孕措施。与接受安慰剂或铜T宫内节育器的妇女相比,产后前9个月的母乳喂养率没有差异。产后1年,铜T组的母乳喂养妇女人数多于孕酮组或安慰剂组。 246名妇女在产后约60天植入了释放孕酮的阴道环。三种类型的阴道环分别每日释放5、10或15毫克孕酮。对照组妇女使用铜T宫内节育器。产后6个月和12个月时,孕酮组和铜T组的母乳喂养婴儿比例无显著差异。 120名哺乳期妇女在产后5至7周开始使用每日释放约10毫克孕酮的阴道环。孕酮阴道环组的断奶率高于使用左炔诺孕酮或炔诺酮植入剂进行产后避孕的妇女组。 在一项多中心研究中,802名在产后第29至63天开始使用每日释放约10毫克孕酮的阴道环的妇女与734名使用铜T宫内节育器的妇女进行了比较。产后第一年,两组女性的母乳喂养率无差异。 一项研究比较了285名产后5至9周开始使用每日释放约10毫克孕酮的阴道环的女性和262名产后5至9周开始使用铜T宫内节育器的女性。在14个月的观察期内,两组女性的母乳喂养率无差异。 另一项观察性研究追踪了192名产后54至64天开始使用每日释放10毫克孕酮的阴道环的女性。所有受试者均使用阴道环至少4个月;90%的受试者在产后6个月仍在继续使用,73%的受试者在产后9个月仍在继续使用。母乳喂养持续时间和婴儿生长情况与对照组相似。 一项双盲安慰剂对照试验将46名产后戒烟妇女随机分为两组,分别口服微粒化黄体酮200毫克,每日两次,或服用安慰剂,疗程4周,以评估戒烟率。所有受试者均在母乳喂养稳定后方可入组。各组间母乳喂养天数无统计学差异。 一项比较产后妇女使用孕酮环(n = 459)和铜T宫内节育器(n = 330)的研究发现,孕酮环组的哺乳期闭经持续时间(405天)长于宫内节育器组(120天)。 一位跨性别女性服用螺内酯50毫克,每日两次以抑制睾酮;多潘立酮10毫克,每日三次,后增至20毫克,每日四次;口服微粒化孕酮200毫克,每日一次;口服雌二醇8毫克,每日一次;并每天吸奶6次以诱导泌乳。治疗3个月后,雌二醇方案改为每日0.025毫克贴片,孕酮剂量降至每日100毫克。两周后,她开始纯母乳喂养伴侣的新生儿。纯母乳喂养持续了6周,期间婴儿的生长发育和排便习惯均正常。患者继续部分母乳喂养婴儿至少6个月。 一位跨性别女性服用螺内酯100毫克,每日两次;孕酮200毫克,每日一次;雌二醇5毫克,每日一次。为了增加乳汁分泌,她开始服用多潘立酮10毫克,每日三次。开始服用一个月后,她每天能够挤出3至5盎司的乳汁。8周后,由于乳汁分泌减少,多潘立酮的剂量增加到30毫克,每日三次。她的乳汁分泌恢复到每天3至5盎司。到6个月时,尽管她的血清催乳素水平仍然升高,但她的乳汁分泌减少到每天约5毫升。 一位跨性别女性服用雌二醇2毫克,每日两次,已有14年。在伴侣预产期前107天,她开始服用多潘立酮,每次10毫克,每日四次,以及黄体酮,每日100毫克。同时,雌二醇的剂量增加至每次4毫克,每日两次。在预产期前94天,多潘立酮的剂量增加至每次20毫克,每日四次;黄体酮的剂量增加至每日200毫克;雌激素改为经皮雌二醇,每日25微克。在预产期前34天,她停用了黄体酮。从预产期前34天开始,她开始挤奶并储存母乳。到产后27天,她已经能够每天两次给婴儿哺乳,每天挤出150毫升母乳,并且能够将多潘立酮的剂量减少至每次20毫克,每日三次。降低剂量导致乳汁分泌减少。 一位跨性别女性正在接受性别肯定治疗,她每天两次舌下含服雌二醇4毫克、螺内酯100毫克,睡前服用孕酮200毫克。为了迎接伴侣怀胎的婴儿的出生,她将舌下含服雌二醇的剂量增加到每天两次,每次6毫克,并将孕酮的剂量增加到睡前400毫克。同时,她开始服用多潘立酮10毫克,每天两次,以提高血清催乳素水平,之后剂量增加到每天四次,每次20毫克。在预产期前,她停用了孕酮,螺内酯的剂量减少到每天100毫克,雌二醇改为经皮给药,每次25微克。产后第59天,雌二醇改为舌下含服,每次2毫克,螺内酯的剂量增加到每天两次,每次100毫克。该患者每日可分泌高达 240 毫升的乳汁,其中含有典型的宏量营养素和寡糖水平。 一位希望母乳喂养的跨性别女性接受了每日 150 微克雌二醇透皮贴剂和每日口服 100 毫克孕酮的治疗。之后,加用了每日 100 微克雌二醇喷雾剂和每日 4 次、每次 10 毫克多潘立酮。随后,多潘立酮剂量加倍至每日 4 次、每次 20 毫克,孕酮剂量加倍至每日 2 次、每次 100 毫克。在进一步调整雌二醇和孕酮剂量后,通过吸奶器吸出了7毫升乳汁,但在婴儿出生两周后,应患者要求停止了催乳。 一位50岁的跨性别女性希望母乳喂养她的孙子,她接受了基础治疗,每72小时使用0.3毫克雌二醇透皮贴剂,并每日口服一次200毫克微粒化孕酮。为了启动泌乳,她的雌二醇剂量增加到每72小时使用0.4毫克透皮贴剂,并开始进行乳头刺激。之后,患者的孕酮剂量增加到每日300毫克,并开始口服甲氧氯普胺10毫克,每日三次。她总共泌乳两周,并多次哺乳这位四个月大的婴儿。她的乳汁高峰期,右侧较大的乳房产奶量为30毫升,左侧较小的乳房产奶量为8毫升。 |
| 参考文献 |
| 分子式 |
C21H30O2
|
|---|---|
| 分子量 |
314.46
|
| 精确质量 |
316.231
|
| CAS号 |
82938-07-6
|
| 相关CAS号 |
Progesterone;57-83-0
|
| PubChem CID |
163196495
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
3.9
|
| tPSA |
34.1
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
23
|
| 分子复杂度/Complexity |
589
|
| 定义原子立体中心数目 |
6
|
| SMILES |
CC(=O)[C@H]1CC[C@@H]2[C@@]1(CC[C@H]3[C@H]2CCC4=[13CH][13C](=O)CC[C@]34C)C
|
| InChi Key |
RJKFOVLPORLFTN-PIWOXAIRSA-N
|
| InChi Code |
InChI=1S/C21H30O2/c1-13(22)17-6-7-18-16-5-4-14-12-15(23)8-10-20(14,2)19(16)9-11-21(17,18)3/h12,16-19H,4-11H2,1-3H3/t16-,17+,18-,19-,20-,21+/m0/s1/i12+1,15+1
|
| 化学名 |
(8S,9S,10R,13S,14S,17S)-17-acetyl-10,13-dimethyl-1,2,6,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthren-3-one
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.1801 mL | 15.9003 mL | 31.8005 mL | |
| 5 mM | 0.6360 mL | 3.1801 mL | 6.3601 mL | |
| 10 mM | 0.3180 mL | 1.5900 mL | 3.1801 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。