| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
GLP-1 receptor
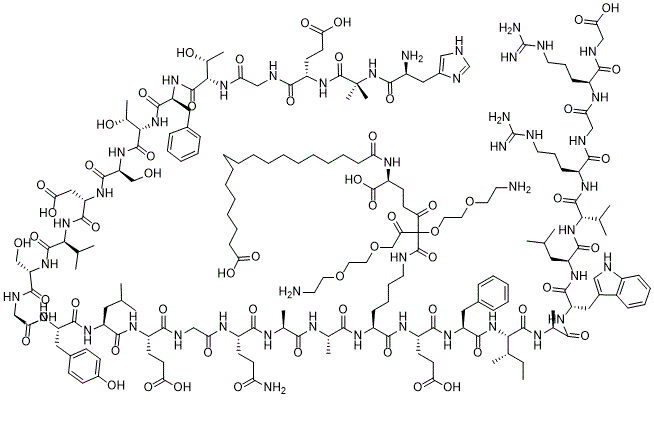
Semaglutide is derivatized at lysine 26 and differs from human GLP-1 in two amino acid substitutions (Aib8, Arg34). Semaglutide has an affinity for GLP-1R of 0.38±0.06 nM[1]. A GLP-1 analogue that is 94% sequence similar to human GLP-1 is semaglutide [3]. |
|---|---|
| 体外研究 (In Vitro) |
索马鲁肽在第 26 位赖氨酸处衍生化,与人 GLP-1 的不同之处在于两个氨基酸取代(Aib8、Arg34)。索马鲁肽对 GLP-1R 的亲和力为 0.38±0.06 nM[1]。与人 GLP-1 94% 序列相似的 GLP-1 类似物是索马鲁肽 [3]。
|
| 体内研究 (In Vivo) |
小型猪皮下给药后索马鲁肽的 MRT 为 63.6 小时,静脉给药后小型猪的血浆半衰期为 46 小时[1]。索马鲁肽可改善 1-甲基-4-苯基-1,2,3,6-四氢吡啶 (MPTP) 引起的运动障碍。索马鲁肽还通过挽救酪氨酸羟化酶(TH)水平的降低、减少脂质过氧化、减轻炎症、抑制细胞凋亡途径和增加自噬相关蛋白的表达来保护黑质和纹状体中的多巴胺能神经元。此外,索马鲁肽(一种长效 GLP-1 类似物)在大多数参数上均优于利拉鲁肽[2]。索马鲁肽通过促进胰岛素的释放来降低体重和血糖[3]。
在具有高心血管风险的2型糖尿病患者中,与安慰剂相比,每周一次皮下注射司美格鲁肽(0.5 mg或1.0 mg)在中位治疗2.1年后,显著降低了主要复合结局(心血管死亡、非致死性心肌梗死或非致死性卒中)的风险。风险比(HR)为0.74(95% CI,0.58至0.95;非劣效性P<0.001;优效性P=0.02)。24个月内为防止发生一次主要结局事件需要治疗的人数(NNT)为45。[1] 主要结局风险的降低主要源于非致死性卒中显著降低39%(HR 0.61;95% CI,0.38至0.99;P=0.04)以及非致死性心肌梗死非显著性降低26%(HR 0.74;95% CI,0.51至1.08;P=0.12)。两组间心血管死亡率相似(HR 0.98;95% CI,0.65至1.48;P=0.92)。[1] 与安慰剂相比,司美格鲁肽治疗还降低了新发或恶化肾病的风险(HR 0.64;95% CI,0.46至0.88;P=0.005),但增加了糖尿病视网膜病变并发症的风险(HR 1.76;95% CI,1.11至2.78;P=0.02)。[1] 观察到血糖控制和体重显著改善。第104周时,司美格鲁肽组糖化血红蛋白自基线8.7%下降了1.1%(0.5 mg)和1.4%(1.0 mg),而安慰剂组下降了0.4%。司美格鲁肽组体重下降了3.6 kg(0.5 mg)和4.9 kg(1.0 mg),而安慰剂组下降了0.5-0.7 kg。[1] |
| 酶活实验 |
HEK293‐SNAP‐GLP‐1R细胞在悬浮液中用SNAP‐Lumi4‐Tb(40 nM,Cisbio,Codelet,France)在室温下在完全培养基中培养1小时。在含有0.1%牛血清白蛋白和代谢抑制剂(20 mmol/L 2-脱氧葡萄糖和10 mmol/L NaN3)以防止GLP‐1R内化,如前所述,使用exendin(9‐39)和异硫氰酸荧光素(FITC)安装在K12位置,通过时间分辨förster共振能量转移(FRET)进行结合实验。[4]
|
| 细胞实验 |
Semagulide激活胰腺β细胞中的GLP-1受体,导致葡萄糖依赖性胰岛素释放。它还能减少胰高血糖素的分泌,减缓胃排空,促进饱腹感。
|
| 动物实验 |
小鼠:本研究全程使用10周龄(20-25 g)雄性C57BL/6小鼠。将小鼠随机分为六组(每组n=12)。各处理组如下:(i)对照组仅给予生理盐水;(ii)NN-2211组给予生理盐水和NN-2211(25 nmol/kg,腹腔注射,每日一次,连续7天);(iii)索玛鲁肽组给予生理盐水和索玛鲁肽(25 nmol/kg,腹腔注射,每日一次,连续7天);(iv)MPTP组仅给予MPTP(20 mg/kg,腹腔注射,每日一次,连续7天);(v)MPTP(20 mg/kg,腹腔注射,每日一次,连续7天)处理后立即给予NN-2211(25 nmol/kg,腹腔注射,每日一次,连续7天)。 (vi) MPTP(20 mg/kg,腹腔注射,每日一次,连续7天)组紧随其后,随后给予索玛鲁肽(25 nmol/kg,腹腔注射,每日一次,连续7天)治疗。在药物治疗结束后,测量行为变化、神经元损伤、炎症标志物和其他生物标志物。[2]
使用10周龄雄性C57BL/6小鼠。通过腹腔注射MPTP(20 mg/kg,每日一次,连续7天)建立帕金森病模型。 治疗组中,索玛鲁肽溶于生理盐水,以25 nmol/kg的剂量腹腔注射,每日一次,连续7天。治疗在每日MPTP注射后立即开始。 在MPTP注射开始后的第8天进行行为学评估(旷场实验、转棒实验、足迹实验)。 第9天,处死小鼠。收集脑组织(黑质和纹状体)用于后续的免疫组织化学和蛋白质印迹分析。免疫组织化学实验中,用生理盐水灌注脑组织,并用多聚甲醛固定。蛋白质印迹实验中,解剖脑组织并冷冻于-80°C。[2] |
| 药代性质 (ADME/PK) |
吸收:在一项临床试验中,司美格鲁肽的Cmax为10.9 nmol/L,AUC为3123.4 nmol·h/L,Tmax为56 h,1-3天内即可达到。绝对生物利用度为89%。口服片剂的稳态浓度在4-5周内达到。司美格鲁肽的平均稳态浓度是指0.5mg至1mg剂量给药后的平均稳态浓度,范围为16 nmol/L至30 nmol/L。
消除途径:该药物主要经肾脏清除,并可通过尿液和粪便排出。主要消除途径是尿液,约占摄入放射性标记剂量的53%,其次是粪便,约占18.6%。少量(3.2%)通过呼气排出。肝功能损害似乎不影响该药物的清除率,肝功能减退的患者无需调整剂量。 分布容积:索玛鲁肽的分布容积为 8 升至 9.4 升。它能透过大鼠胎盘。 清除率:根据一项临床研究,索玛鲁肽的清除率为 0.039 升/小时。FDA 标签显示,2 型糖尿病患者的索玛鲁肽清除率约为 0.05 升/小时。 代谢/代谢物:索玛鲁肽在肽链骨架处被裂解,随后脂肪酸链发生 β-氧化。天然存在的 GLP-1 可被二肽基肽酶-4 (DPP-4) 和其他酶快速代谢,这些酶广泛存在于人体组织中。化学结构修饰使索玛鲁肽不易被胃肠道DPP-4酶降解。它代谢缓慢而广泛,约83%的给药剂量以原形药物形式存在于血浆中。神经内肽酶(NEP)是另一种代谢该药物的酶。DPP-4通过截断N端片段使索玛鲁肽失活,而NEP则水解肽键。在人血浆中已鉴定出六种不同的索玛鲁肽代谢物。主要代谢物P3约占摄入剂量的7.7%。生物半衰期:索玛鲁肽的主要特性之一是其长达168小时的半衰期。这种长半衰期归因于其与白蛋白的结合。这降低了肾清除率,并保护索玛鲁肽免受代谢分解。 索玛鲁肽是一种长效GLP-1类似物,每周一次皮下注射,用于治疗2型糖尿病。它是利拉鲁肽的改良版,旨在抵抗蛋白酶降解,从而延长生物半衰期。本研究未提供具体的药代动力学参数(例如,半衰期、Cmax、AUC)。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性 在大型临床试验中,与安慰剂或对照药物相比,索玛鲁肽治疗组的血清酶升高发生率并不更高,且未报告任何临床上明显的肝损伤病例。事实上,索玛鲁肽和其他GLP-1类似物治疗通常可改善血清转氨酶水平(以及肝脂肪变性),使其成为非酒精性脂肪肝的潜在治疗方法。自上市以来,尚未有关于索玛鲁肽引起肝毒性的病例报告发表,且产品说明书中也未将肝损伤列为不良事件。因此,索玛鲁肽引起的肝损伤即使发生,也必定十分罕见。 可能性评分:E(不太可能引起临床上明显的肝损伤)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于索玛鲁肽在哺乳期临床应用的信息。由于司美格鲁肽是一种分子量为4113道尔顿的肽类分子,且其蛋白结合率超过99%,因此其在乳汁中的含量可能非常低。婴儿吸收该药物的可能性也很小,因为药物很可能在婴儿的胃肠道内被破坏。在获得更多数据之前,哺乳期妇女应谨慎使用司美格鲁肽,尤其是在哺乳新生儿或早产儿时。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 查看更多◈ 什么是司美格鲁肽? 蛋白质结合 索玛鲁肽与血浆白蛋白具有高亲和力结合,从而保证了药物的高稳定性。其与白蛋白的结合率超过 99%。 在 SUSTAIN-6 试验中,索玛鲁肽 组的胃肠道疾病(例如恶心、呕吐、腹泻)发生率(50.7%-52.3%)高于安慰剂组(35.2%-35.7%),导致因不良事件而中断治疗的比例更高。 |