| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 500mg |
|
||
| 1g |
|
| 靶点 |
c-Met (IC50 = 4 nM)
The primary target of Tepotinib (EMD 1214063; MSC 2156119) is mesenchymal-epithelial transition factor (MET) tyrosine kinase, with high selectivity and activity against MET and its mutants. Specific IC50 values: - Recombinant human MET kinase: IC50 = 1.6 nM [1] - MET (cellular activity, MET-amplified gastric cancer MKN-45 cells): IC50 = 12 nM [1] - MET (cellular activity, MET-overexpressing lung cancer EBC-1 cells): IC50 = 15 nM [1] - MET mutants (METΔ14, MET Y1230H): IC50 = 5.8 nM, 6.5 nM respectively [1] No significant inhibition (IC50 > 1000 nM) against non-target kinases (e.g., EGFR, VEGFR2, PDGFRα, ALK, c-Kit) [1] |
|---|---|
| 体外研究 (In Vitro) |
EMD 1214063 抑制 A549 细胞中 HGF 诱导的 c-Met 磷酸化,IC50 为 6 nM。 EMD 1214063 处理可诱导 EBC-1 细胞中 c-Met 组成型磷酸化显着减少,IC50 为 9 nM。 EMD 1214063 在 EBC-1、MKN-45 和 Hs746T 细胞中有效阻断 c-Met 酶主要下游效应子的磷酸化,例如 Grb2、Gab1、Sos、PLCγ 和磷酸肌醇 3-激酶,范围为 1至 10 纳米。 EMD 1214063 显着抑制 MKN-45 细胞的活力,IC50 小于 1 nM。用 EMD 1214063(低至 0.1 nM)处理可抑制 HGF 诱导的 NCI-H441 细胞迁移,而 100 nM 至 1 μM 的浓度几乎完全阻止它。激酶测定:Tepotinib (EMD-1214063) 是一种有效的选择性 c-Met 抑制剂,IC50 为 4 nM,对 c-Met 的选择性是 IRAK4、TrkA、Axl、IRAK1 和 Mer 的 200 倍以上。
1. 对MET驱动肿瘤的抗增殖活性: - Tepotinib抑制MET扩增胃癌细胞:MKN-45(IC50 = 12 nM)、NCI-N87(IC50 = 18 nM)[1] - 对MET过表达肺癌细胞:EBC-1(IC50 = 15 nM)、H1993(IC50 = 20 nM)[1] - 对MET低表达/阴性癌细胞(A549肺癌、MCF-7乳腺癌),IC50 > 1000 nM(无显著活性)[1] 2. 信号通路抑制: - 用Tepotinib(50 nM,处理2小时)处理MKN-45细胞后,MET磷酸化水平(p-MET,Tyr1234/1235)降低95%,下游p-AKT(Ser473)和p-ERK1/2(Thr202/Tyr204)的抑制率分别为92%和90%(Western blot检测)[1] - 在METΔ14转染的HEK293细胞中,30 nM Tepotinib阻断p-MET达89% [1] 3. 诱导凋亡: - 在MKN-45细胞中,Tepotinib(100 nM,处理48小时)使凋亡率(Annexin V-FITC+/PI-)从对照组的3.6%升至63.8%,切割型caspase-3上调5.5倍 [1] 4. 抑制集落形成: - 在EBC-1细胞软琼脂集落形成实验中,Tepotinib(20 nM)使集落数量较对照组减少85%;50 nM浓度下集落减少97%(集落直径>50 μm)[1] 5. 抗侵袭活性: - 在H1993细胞Transwell侵袭实验中(基质胶包被小室),50 nM Tepotinib使侵袭细胞数较对照组减少82% [1] |
| 体内研究 (In Vivo) |
EMD 1214063 治疗剂量为 10 mg/kg 或更高,可在至少 72 小时的时间内抑制 Hs746T 异种移植肿瘤中 c-Met 磷酸化超过 90%。 EMD 1214063 诱导细胞周期蛋白 D1 表达减少 50% 以上,并在使用 100 mg/kg 剂量治疗 96 小时后仍持续存在。 EMD 1214063 治疗后还观察到 p27 和裂解的 caspase-3 的短暂诱导。 EMD 1214063(每天 15 毫克/公斤)治疗可诱导胃癌异种移植物 Hs746T 完全消退,其中 c-Met 被扩增、过表达,并且以不依赖配体的方式激活。
1. MET扩增胃癌异种移植模型(MKN-45): - 6~8周龄雌性裸鼠携带皮下MKN-45肿瘤,口服Tepotinib(30 mg/kg、60 mg/kg,每日1次,连续21天)。 - 30 mg/kg组肿瘤体积较溶媒组减少76%;60 mg/kg组减少89%,中位生存期从对照组27天延长至58天 [1] 2. MET过表达肺癌异种移植模型(EBC-1): - 裸鼠口服Tepotinib(60 mg/kg,每日1次,连续18天),肿瘤重量较对照组减少88%;肿瘤组织Western blot证实p-MET降低93% [1] 3. 肿瘤增殖PET成像(MKN-45模型): - 口服Tepotinib(60 mg/kg,每日1次,连续7天)的小鼠,肿瘤 18 F-FLT(增殖标志物)摄取量较基线减少72%(microPET分析)[1] |
| 酶活实验 |
EMD 1214063和EMD 1204831选择性地抑制c-Met受体酪氨酸激酶活性。与它们对242种人类激酶的作用相比,它们的抑制活性是有效的[分别为抑制50%浓度(IC50)、3 nmol/L和9 nmol/L]和高度选择性的。EMD 1214063和EMD 1204831均以剂量依赖的方式抑制c-Met磷酸化和下游信号传导,但其抑制活性的持续时间不同。[1]
c-Met体外激酶测定[1] 使用242种不同的激酶在体外评估EMD 1214063或EMD 1204831(1和10μmol/L)对激酶的抑制作用。用闪板法测定生物化学活性。将His6标记的重组人c-Met激酶结构域(Aa 974–end;20 ng)和生物素化的聚Ala-Glu-Lys-Tyr(6:2:5:1;500 ng)在室温下与测试化合物一起或不与测试化合物在100μL缓冲液中孵育90分钟,该缓冲液含有0.3μCi 33P-ATP、2.5μg聚乙二醇20.000和1%二甲基亚砜(DMSO),如前所述。用TopCount微孔板闪烁和发光计数器测量放射性。使用RS/1软件程序通过非线性回归分析计算抑制50%浓度值(IC50)。[1] 磷酸化c-Met捕获ELISA[1] 在Nunc Immuno MicroWell 96孔固体板中通过c-Met捕获ELISA评估总的c-Met磷酸化。A549人癌症细胞在治疗前2天接种,血清饥饿20小时,并在第3天用不同浓度的EMD 1214063或EMD 1204831或0.2%DMSO在37°C、5%CO2下治疗45分钟。在用100 ng/mL HGF刺激5分钟后,用补充有蛋白酶和磷酸酶抑制剂的70μL/孔冰冷裂解缓冲液[20 nmol/L HEPES,pH 7,4;10%(V/V)甘油;150 nmol/L NaCl;1%(V/V的)Triton-X-100;2 nmol/L EDTA]裂解细胞。在冲洗实验中,A549用EMD 1214063或EMD 1204831处理45分钟,洗涤,并在无血清培养基中孵育14小时,然后用HGF(100ng/mL)刺激。 在ELISA中,捕获抗体对c-Met细胞外结构域是特异性的,而抗磷脂-生物素标记的抗体用于检测。使用链霉亲和素-过氧化物酶缀合物和化学发光读数揭示酪氨酸磷酸化。 生化分析[1] 在EBC-1细胞中通过蛋白质印迹分析分析c-Met、Gab-1、Akt和Erk1/2的磷酸化。简言之,细胞以每孔3×106个细胞的密度接种,血清饥饿20小时,并在与EMD 1214063孵育后的第3天裂解。通过SDS-PAGE分离蛋白质并将其吸附在硝化纤维素膜上。用Tris缓冲盐水封闭膜,并在4°C的一级抗体溶液(抗pMet、抗pAkt、抗pERK1/2、抗Gab1)中孵育过夜。用装有Quantity One 1-D分析软件的VersaDoc MP 5000成像系统通过化学发光检测蛋白质。 重组MET激酶活性实验: 1. 制备总体积50 μL的反应体系:50 mM HEPES缓冲液(pH 7.4,含10 mM MgCl₂、1 mM DTT)、重组人MET激酶结构域(40 ng)、Tepotinib(0.001~100 nM)、10 μM [γ-³²P]ATP、20 μM MET特异性肽底物(序列:CGGGYVVPQPQLPYPGENL)。 2. 30°C孵育60分钟,启动激酶反应。 3. 加入25 μL 30%三氯乙酸(TCA)终止反应,冰上孵育15分钟以沉淀磷酸化肽。 4. 取50 μL反应液转移至P81磷酸纤维素滤板,用0.5% TCA(每孔500 μL)洗涤滤板3次,去除未结合的[γ-³²P]ATP和非磷酸化底物。 5. 50°C烘干滤板30分钟,每孔加入50 μL闪烁液,通过液体闪烁计数器测定结合的磷酸化肽的放射性强度。 6. 与溶媒对照组比较,计算Tepotinib对MET激酶活性的抑制率,将数据拟合四参数逻辑模型获得IC50值(1.6 nM)[1] |
| 细胞实验 |
Tepotinib (EMD-1214063) 是一种有效且具有选择性的 c-Met 抑制剂。它的 IC50 为 4 nM,对 c-Met 的选择性比 IRAK4、TrkA、Axl、IRAK1 和 Mer 的选择性高 200 倍以上。
伤口愈合试验和增殖试验[1] 伤口愈合试验如前所述进行。简言之,用无菌移液管尖端在单层NCI-H441癌症细胞上产生划痕。在存在或不存在100ng/mL HGF的情况下,在24小时内监测EMD 1210463和EMD 1204831对细胞间隙闭合的影响。所有增殖和集落形成测定在4个重复中进行,并包括4个DMSO载体对照。IC50值通过GraphPad Prism v5中的4PL拟合确定。 离体肿瘤样品的药效学标志物[1] 通过对冷冻离体肿瘤样品的蛋白质印迹分析来研究c-Met自磷酸化。根据制造商的说明,使用Precellys 24均质器或Precellys陶瓷裂解管(PEQLab Ltd)对肿瘤组织进行机械均质、裂解。裂解物的进一步制备和通过SDS-PAGE的蛋白质分离如已经对EBC-1细胞描述的那样进行。 在福尔马林固定的石蜡包埋切片上,通过免疫组织化学(IHC)分析组蛋白H3磷酸化和细胞周期停滞和凋亡的生物标志物(细胞周期蛋白D1、p27和裂解的活化的capase-3)。根据制造商的说明,使用Discovery染色仪器和OmniMap试剂盒进行IHC。切片用苏木精复染。 1. 细胞增殖实验(MTT法): - 将靶细胞(MKN-45、EBC-1、A549)以5×10³细胞/孔的密度接种于96孔板,在含10%胎牛血清(FBS)和1%青霉素-链霉素的RPMI 1640培养基中,37°C、5% CO₂培养箱过夜孵育。 - 向每孔加入Tepotinib(0.1~1000 nM),每个浓度设3个复孔;设溶媒对照孔(0.1% DMSO)。 - 相同条件下孵育72小时后,每孔加入10 μL MTT试剂(5 mg/mL PBS溶液),继续孵育4小时。 - 小心吸弃培养基,每孔加入150 μL DMSO溶解甲臜结晶,室温振荡10分钟确保完全溶解。 - 酶标仪在570 nm处测定吸光度,通过GraphPad Prism拟合剂量-反应曲线计算50%抑制浓度(IC50)[1] 2. Western blot实验: - MKN-45/EBC-1细胞以2×10⁵细胞/孔接种于6孔板,过夜孵育。 - Tepotinib(10~100 nM)处理细胞2小时,吸弃培养基后用冷PBS洗涤细胞2次。 - 含蛋白酶和磷酸酶抑制剂的RIPA裂解液冰上裂解细胞30分钟,4°C下12,000×g离心15分钟收集上清液。 - BCA蛋白定量试剂盒测定蛋白浓度,每泳道上样30 μg蛋白进行10% SDS-PAGE电泳(120 V,90分钟)。 - 转印蛋白至PVDF膜(300 mA,60分钟),用含5%脱脂牛奶的TBST缓冲液(0.1% Tween-20)室温封闭1小时。 - 4°C下用一抗(抗p-MET、抗MET、抗p-AKT、抗p-ERK1/2、抗切割型caspase-3、抗GAPDH)孵育膜过夜,TBST缓冲液洗涤3次(每次10分钟)。 - 室温下用辣根过氧化物酶(HRP)标记二抗孵育1小时,增强化学发光(ECL)试剂检测蛋白信号,ImageJ软件定量信号强度 [1] 3. 凋亡实验(Annexin V-FITC/PI双染色法): - Tepotinib(100 nM)处理MKN-45细胞24或48小时,收集漂浮和贴壁细胞,冷PBS洗涤2次。 - 细胞重悬于100 μL Annexin V结合缓冲液,加入5 μL Annexin V-FITC和5 μL碘化丙啶(PI),室温避光孵育15分钟。 - 每样本加入400 μL Annexin V结合缓冲液,1小时内用流式细胞仪分析凋亡率(激发波长488 nm;FITC发射波长530 nm,PI发射波长610 nm)[1] 4. 软琼脂集落形成实验: - 制备底层胶:0.6%琼脂与RPMI 1640培养基按1:1体积比混合,每孔(6孔板)加入1.5 mL,室温放置至凝固。 - 制备顶层胶:EBC-1细胞重悬于含0.3%琼脂的RPMI 1640培养基(密度1×10⁴细胞/mL),向细胞-琼脂混合物中加入Tepotinib(10~100 nM),每孔加入1.5 mL(覆盖底层胶)。 - 37°C、5% CO₂培养箱孵育14天,室温下用0.05%结晶紫染色集落1小时。 - 显微镜下计数直径>50 μm的集落,计算较溶媒对照组的集落抑制率 [1] |
| 动物实验 |
人胃癌异种移植模型 Hs746T
\n15 mg/kg \n每日 \n抗肿瘤疗效异种移植模型[1] \n在小鼠异种移植模型中研究了 EMD 1214063 或 EMD 1204831 的抗肿瘤疗效。将人癌细胞系 KP-4、U87MG(10 × 10⁶ 个细胞/100 μL)、Hs746T、EBC-1(5 × 10⁶ 个细胞/100 μL)皮下注射到 CD-1 或 BALB/C 裸鼠体内。当肿瘤达到线性生长期(70–150 mm³)时,荷瘤小鼠(每组 10 只)每日注射指定剂量的 EMD 1214063 或 EMD 1204831 或载体。每周测量两次体重和肿瘤大小[长度 (L) 和宽度 (W)]。肿瘤体积采用公式 L × W²/2 计算。统计学显著性采用单因素方差分析 (ANOVA) 确定。P ≤ 0.05 被认为具有统计学意义。 \n药代动力学和药效学研究[1] \n采用高效液相色谱 (HPLC) 和质谱 (MS) 法测定血浆和肿瘤药物浓度。简而言之,血浆样本在甲醇中进行蛋白质沉淀,肿瘤样本在乙醇/水 (80:20, v/v) 混合溶液中用 Precellys 24 均质器进行均质。HPLC/串联质谱 (MS-MS) 系统由安捷伦 1100 系列 HPLC 系统、CTC HTC PAL 自动进样器和 Applied Biosystems API4000 质谱仪组成。采用反相色谱柱(Chromolith SpeedROD RP-18e,50–3 mm)进行高效液相色谱分离,流动相A为0.1%甲酸溶液,流动相B为乙腈。使用多反应监测(MRM)进行MS/MS检测,以实现化合物的选择性。体内药效学研究中的所有动物实验均按照当地动物福利机构批准的标准程序进行。将5 × 10⁶个Hs746T细胞(100 μL)皮下注射到小鼠体内。待肿瘤体积达到600至1000 mm³后,将小鼠随机分为不同的实验组,分别单次口服3、10、30和100 mg/kg的EMD 1214063、EMD 1204831或溶剂对照。分别于治疗后 3、6、12、24、48、72 和 96 小时采集肿瘤和血浆样本。每个实验组每个剂量和时间点均包含 4 只小鼠。肿瘤组织样本经速冻用于药代动力学和生物标志物分析,或经福尔马林固定用于免疫组织化学分析。 \n1. MKN-45 胃癌异种移植模型: \n-动物:雌性裸鼠(6-8 周龄,体重 18-22 g),每组 n=6。 \n-肿瘤诱导:将 5×10⁶ 个 MKN-45 细胞(悬浮于 0.2 mL PBS 与 Matrigel 以 1:1 比例混合的溶液中)皮下注射到每只小鼠的右侧腹部。 \n - 药物制剂:替泊替尼溶于 0.5% 甲基纤维素 + 0.2% Tween 80(最终 DMSO 浓度 < 1%)。 \n - 给药途径:每日一次灌胃,连续 21 天,剂量分别为 30 mg/kg 和 60 mg/kg;对照组给予赋形剂(0.5% 甲基纤维素 + 0.2% Tween 80)。 \n - 监测:每 2 天使用数字游标卡尺测量肿瘤体积(计算方法为长 × 宽² / 2),每周记录体重,并追踪生存时间直至肿瘤体积超过 2000 mm³ [1]。 \n2. EBC-1 肺癌异种移植模型: \n - 动物:雌性裸鼠(6-8 周龄),每组 n=6。 \n - 肿瘤诱导:将 4×10⁶ 个 EBC-1 细胞(0.2 mL PBS/Matrigel 1:1 混合液)皮下注射至小鼠右侧腹部。 \n - 给药:替泊替尼(60 mg/kg,口服,每日一次,连续 18 天);对照组给予溶剂。 \n - 终点:治疗结束后,处死小鼠,切除肿瘤并称重,然后提取肿瘤蛋白进行 Western blot 分析,检测 p-MET 和 MET 的表达 [1] \n3. 18F-FLT PET 成像方案(MKN-45 模型): \n - 动物:荷 MKN-45 肿瘤(肿瘤体积约 200 mm³)的裸鼠,每组 n=4。 \n - 给药途径:替泊替尼(60 mg/kg,口服,每日一次,连续7天);首次给药前1天进行基线PET成像。 \n - 成像流程:经尾静脉注射18F-FLT(每只小鼠100 μCi),注射后1小时进行微型PET扫描。计算肿瘤的最大标准化摄取值(SUVmax)以评估增殖情况[1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服替泊替尼的绝对生物利用度约为72%。推荐剂量为每日一次450mg,中位达峰时间(Tmax)为8小时,平均稳态血药浓度峰值(Cmax)和24小时药时曲线下面积(AUC0-24h)分别为1291 ng/mL和27438 ng·h/mL。与高脂肪、高热量食物同服可使替泊替尼的AUC和Cmax分别增加约1.6倍和2倍。 口服后,约85%的给药剂量经粪便排出,其余部分经尿液排出。原药约占粪便排泄剂量的一半,其余部分包括去甲基化的M478代谢物、一种葡萄糖醛酸苷代谢物、外消旋的M506代谢物以及一些少量的氧化代谢物。原药也约占尿液排泄剂量的一半,其余部分包括一种葡萄糖醛酸苷代谢物和一对N-氧化物非对映异构体代谢物。 平均表观分布容积为1038升。 替泊替尼的表观清除率为23.8升/小时。 代谢/代谢物 替泊替尼主要由CYP3A4和CYP2C8代谢,部分未明确的UGT酶也有代谢作用。代谢物 M506 是主要的循环代谢物,约占血浆中观察到的药物总量的 40.4%,而葡萄糖醛酸代谢物 M668 在血浆中的含量则低得多(约占口服剂量的 4%)。在服用替泊替尼后,共检测到 10 种 I 期和 II 期代谢物,其中大部分经粪便排泄。 生物半衰期 口服给药后,替泊替尼的半衰期约为 32 小时。 1. 小鼠口服药代动力学: - 雄性 C57BL/6 小鼠(每个时间点 n=3)以 60 mg/kg 的剂量经口灌胃给予 替泊替尼。 - 分别于给药后 0.25、0.5、1、2、4、8、12 和 24 小时采集血样,并通过离心(3500 rpm,4°C,10 分钟)分离血浆。 - 使用经验证的 LC-MS/MS 方法分析血浆药物浓度(流动相:含 0.1% 甲酸的乙腈/水;色谱柱:C18)。 - 主要参数: - 血浆峰浓度 (Cmax) = 950 ng/mL - 达峰时间 (Tmax) = 1.2 小时 - 血浆浓度-时间曲线下面积 (AUC0-24h) = 5200 ng·h/mL - 消除半衰期 (t1/2) = 7.5 小时 - 口服生物利用度 = 48% [1] 2. 组织分布: - 口服给药 (60 mg/kg) 2 小时后,处死小鼠并收集主要组织(肝脏、肿瘤、肾脏、脾脏、脑)。 - 替泊替尼浓度(ng/g):肝脏 (3520)、肿瘤 (3180)、肾脏 (2850)、脾脏 (2360)、脑 (62) [1] 3. 血浆蛋白结合率: - 使用超滤法:将 替泊替尼 分别以 10 ng/mL 和 1000 ng/mL 的浓度加入小鼠、大鼠和人血浆中。 - 将样品在 37°C 下孵育 1 小时,然后使用超滤装置(截留分子量 30 kDa)以 3000 rpm 的转速离心 30 分钟。 - 使用 LC-MS/MS 测定游离药物和总药物的浓度;所有物种和浓度下的血浆蛋白结合率均 > 99% [1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在替泊替尼(tepotinib)上市前针对携带MET突变的实体瘤患者的临床试验中,肝功能异常较为常见,但通常为自限性且程度较轻。44%的替泊替尼治疗患者出现不同程度的ALT升高,其中4%的患者ALT升高超过正常值上限(ULN)的5倍。在这些纳入255例患者的试验中,3%的患者因ALT或AST升高而中断治疗,但永久停药的患者不足1%。肝功能异常的中位发病时间为治疗开始后30天。虽然血清转氨酶偶尔会升高至相当高的水平(正常值上限的5至20倍),但未出现血清胆红素升高,也没有患者出现伴有黄疸的临床明显肝损伤。替泊替尼的产品说明书建议在开始治疗前、治疗的前3个月每2周进行一次常规肝功能检查,之后根据临床需要每月进行一次。 可能性评分:E(未经证实但怀疑是临床上明显的肝损伤的罕见原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于替泊替尼在哺乳期临床应用的信息。由于替泊替尼与血浆蛋白的结合率高达98%,因此其在乳汁中的含量可能很低。然而,由于其对母乳喂养婴儿的潜在毒性以及其32小时的半衰期,制造商建议在接受替泊替尼治疗期间以及末次给药后1周内停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 替泊替尼在血浆中的蛋白结合率约为98%,主要与血清白蛋白和α1-酸性糖蛋白结合。在临床相关暴露量下,血浆蛋白结合与药物浓度无关。 1. 小鼠急性毒性: - 雄性/雌性 C57BL/6 小鼠(每性别每剂量组 n=3)经口灌胃给予 替泊替尼,剂量分别为 100 mg/kg、200 mg/kg、300 mg/kg 和 400 mg/kg。 - 所有剂量组均未观察到死亡;400 mg/kg 剂量组出现短暂嗜睡(48 小时内恢复);口服 LD50 > 400 mg/kg [1] 2. 亚急性毒性(小鼠 28 天研究): - 剂量:30 mg/kg、60 mg/kg(口服,每日一次)。 - 两个剂量组的体重、食物摄入量、血清生化指标(ALT、AST、肌酐)或血液学指标(白细胞计数、血小板计数、血红蛋白水平)均无显著变化。 - 组织病理学检查显示肝脏、肾脏、心脏或肺脏均未受损[1] |
| 参考文献 | |
| 其他信息 |
Tepotinib 是一种 MET 酪氨酸激酶抑制剂,旨在治疗多种 MET 过表达的实体瘤。它最初由 EMD Serono 和德克萨斯大学 MD 安德森癌症中心于 2009 年合作开发,此后一直在研究用于治疗神经母细胞瘤、胃癌、非小细胞肺癌和肝细胞癌。MET 是某些实体瘤治疗的理想靶点,因为它似乎在肿瘤的生长和增殖中发挥着关键作用,无论是直接的还是间接的,尤其是在其过表达和/或发生突变的肿瘤中。Tepotinib 于 2020 年 3 月在日本首次获批用于治疗 MET 基因改变的非小细胞肺癌 (NSCLC),随后于 2021 年 2 月获得美国 FDA 的加速批准,以商品名 Tepmetko 用于治疗携带 MET 14 号外显子跳跃突变的转移性 NSCLC 成人患者。它是首个可每日一次给药的口服MET靶向酪氨酸激酶抑制剂,这一优势有助于减轻化疗方案通常伴随的服药负担。2022年2月,tepotinib获准在欧洲上市。
Tepotinib是一种激酶抑制剂。其作用机制是作为间质上皮转化抑制剂和P-糖蛋白抑制剂。 Tepotinib是一种口服小分子间质上皮转化(MET)因子酪氨酸激酶受体抑制剂,用于治疗部分非小细胞肺癌(NSCLC)病例。接受替泊替尼治疗期间,血清转氨酶升高较为常见,但尚未发现与出现临床上明显的肝损伤和黄疸病例相关。 替泊替尼是一种口服生物利用度高的MET酪氨酸激酶抑制剂,具有潜在的抗肿瘤活性。替泊替尼选择性地与MET酪氨酸激酶结合,并破坏MET信号转导通路,这可能诱导过度表达该激酶的肿瘤细胞凋亡。受体酪氨酸激酶MET(也称为肝细胞生长因子受体或HGFR)是原癌基因c-Met的产物,在多种肿瘤细胞类型中过度表达或发生突变;这种蛋白质在肿瘤细胞增殖、存活、侵袭和转移以及肿瘤血管生成中发挥关键作用。 另见:盐酸替普替尼(活性成分)。 药物适应症 替普替尼适用于治疗伴有间质-上皮转化因子(MET)14号外显子跳跃突变的转移性非小细胞肺癌(NSCLC)成人患者。 替普替尼单药治疗适用于治疗伴有导致间质-上皮转化因子基因14号外显子(METex14)跳跃突变的晚期非小细胞肺癌(NSCLC)成人患者,这些患者在接受过免疫疗法和/或铂类化疗后需要全身治疗。 非小细胞肺癌(NSCLC)的治疗 作用机制 间质-上皮转化因子(MET) MET是一种受体酪氨酸激酶,在多种肿瘤类型中均存在过表达和/或突变,因此是肿瘤治疗的理想靶点。MET在肿瘤细胞的增殖、存活、侵袭和迁移中发挥着关键作用,异常的MET激活被认为会导致更具侵袭性、预后更差的癌症的发生。Tepotinib是一种靶向MET的激酶抑制剂,包括外显子14跳跃的MET变体。它通过抑制MET磷酸化及其下游信号通路,从而抑制MET依赖性肿瘤细胞的增殖、非锚定依赖性生长和迁移。研究还发现,在c-MET扩增的胃癌细胞中,替泊替尼可下调上皮-间质转化(EMT)促进基因(例如MMP7、COX-2、WNT1、MUC5B和c-MYC)的表达,并上调EMT抑制基因(例如MUC5AC、MUC6、GSK3β和E-钙黏蛋白)的表达,这表明替泊替尼的抑癌活性至少部分是由c-MET诱导的EMT的负调控驱动的。此外,研究还表明,替泊替尼在临床相关浓度下可抑制褪黑素1B和尼沙林,但这种活性与替泊替尼的作用机制之间的关联尚不明确。治疗背景:Tepotinib(EMD 1214063;MSC 2156119)是一种强效、选择性的MET酪氨酸激酶抑制剂,用于治疗MET驱动的实体瘤,包括MET扩增的胃癌和MET过表达的非小细胞肺癌(NSCLC)[1] 2. 作用机制:它通过与MET的ATP结合口袋竞争性结合发挥抗肿瘤作用,抑制MET的自身磷酸化以及随后下游信号通路(PI3K-AKT、RAS-ERK1/2)的激活。这导致肿瘤细胞增殖受到抑制、侵袭能力下降并诱导细胞凋亡[1] 3.研究意义:本研究为MET作为实体瘤的有效治疗靶点提供了重要的临床前证据,其对MET突变体(例如METΔ14)的活性拓展了其在MET基因改变患者中的潜在应用[1] 4. 临床意义:在研究进行时,Tepotinib已进入针对MET驱动的晚期癌症的早期临床试验(I/II期),初步数据显示其毒性可控且具有良好的抗肿瘤活性[1] |
| 分子式 |
C29H28N6O2
|
|---|---|
| 分子量 |
492.57
|
| 精确质量 |
492.227
|
| 元素分析 |
C, 70.71; H, 5.73; N, 17.06; O, 6.50
|
| CAS号 |
1100598-32-0
|
| 相关CAS号 |
1100598-32-0; 1103508-80-0 (HCl);1946826-82-9
|
| PubChem CID |
25171648
|
| 外观&性状 |
White to light yellow solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
626.5±65.0 °C at 760 mmHg
|
| 闪点 |
332.7±34.3 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.660
|
| LogP |
2.72
|
| tPSA |
96.93
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
37
|
| 分子复杂度/Complexity |
880
|
| 定义原子立体中心数目 |
0
|
| SMILES |
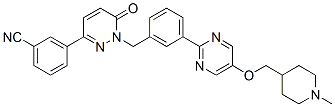
O(C1=C([H])N=C(C2=C([H])C([H])=C([H])C(=C2[H])C([H])([H])N2C(C([H])=C([H])C(C3=C([H])C([H])=C([H])C(C#N)=C3[H])=N2)=O)N=C1[H])C([H])([H])C1([H])C([H])([H])C([H])([H])N(C([H])([H])[H])C([H])([H])C1([H])[H]
|
| InChi Key |
AHYMHWXQRWRBKT-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C29H28N6O2/c1-34-12-10-21(11-13-34)20-37-26-17-31-29(32-18-26)25-7-3-5-23(15-25)19-35-28(36)9-8-27(33-35)24-6-2-4-22(14-24)16-30/h2-9,14-15,17-18,21H,10-13,19-20H2,1H3
|
| 化学名 |
3-[1-[[3-[5-[(1-methylpiperidin-4-yl)methoxy]pyrimidin-2-yl]phenyl]methyl]-6-oxopyridazin-3-yl]benzonitrile
|
| 别名 |
EMD-1214063; MSC-2156119; EMD1214063; EMD 1214063; MSC2156119; MSC 2156119; Tepotinib
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0302 mL | 10.1508 mL | 20.3017 mL | |
| 5 mM | 0.4060 mL | 2.0302 mL | 4.0603 mL | |
| 10 mM | 0.2030 mL | 1.0151 mL | 2.0302 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03940703 | Active Recruiting |
Drug: Tepotinib Drug: Osimertinib |
Non-small Cell Lung Cancer | EMD Serono Research & Development Institute, Inc. |
September 19, 2019 | Phase 2 |
| NCT02864992 | Active Recruiting |
Drug: Tepotinib | Lung Adenocarcinoma Stage IIIB/IV Amplification |
EMD Serono Research & Development Institute, Inc. |
September 13, 2016 | Phase 2 |
| NCT05120960 | Recruiting | Drug: tepotinib plus osimertinib Drug: tepotinib |
Brain Tumor | M.D. Anderson Cancer Center | February 27, 2023 | Phase 1 |
| NCT04647838 | Recruiting | Drug: Tepotinib | Solid Tumor MET Amplification |
Chungbuk National University Hospital |
January 16, 2020 | Phase 2 |
| NCT05782361 | Recruiting | Drug: Tepotinib Drug: Pembrolizumab |
Non Small Cell Lung Cancer Advanced Cancer |
Institute of Cancer Research, United Kingdom |
May 3, 2023 | Phase 1 |
Dose-dependent inhibition of c-Met auto-phosphorylation in vivo. Clin Cancer Res. 2013 Jun 1;19(11):2941-51. |
EMD 1214063 and EMD 1204831 effectively inhibit tumor c-Met auto-phosphorylation and cyclin D1 expression while inducing p27 expression. Clin Cancer Res. 2013 Jun 1;19(11):2941-51. |
EMD 1214063 and EMD 1204831 display antitumor activity in HGF-dependent and HGF-independent xenograft tumor models. Clin Cancer Res. 2013 Jun 1;19(11):2941-51. |