| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在健康受试者中,口服伊沙康唑胶囊(相当于每日600 mg伊沙康唑,即6粒胶囊)后,伊沙康唑的药代动力学呈剂量比例关系。在66名空腹健康男性受试者中,口服相当于200 mg伊沙康唑的伊沙康唑胶囊后,单次服用两粒186 mg伊沙康唑胶囊和五粒74.5 mg伊沙康唑胶囊,其平均(标准差)Cmax和AUC分别为3.3 (0.6) mg/L和112.2 (30.3) mg·hr/L,以及3.3 (0.6) mg/L和118.0 (33.1) mg·hr/L。在健康志愿者中口服伊沙康唑后,活性成分伊沙康唑通常在单次或多次给药后2至3小时达到最大血浆浓度(Cmax)。口服伊沙康唑后,伊沙康唑的绝对生物利用度为98%。口服给药后,血浆中未检测到显著浓度的前药或非活性裂解产物。静脉注射伊沙康唑后,输注期间可检测到前药和非活性裂解产物的最大血浆浓度,并在给药结束后迅速下降。在1小时输注开始后1.25小时,前药浓度已低于检测限。基于AUC计算的前药总暴露量不到伊沙康唑的1%。在部分受试者中,输注开始后8小时内仍可定量检测到非活性裂解产物。基于AUC的非活性裂解产物的总暴露量约为伊沙康唑的1.3%。经鼻胃管静脉输注的伊沙康唑溶液可提供与口服胶囊相似的全身伊沙康唑暴露量。与高脂餐同时服用相当于400 mg口服剂量的伊沙康唑可使伊沙康唑的Cmax降低9%,AUC增加9%。伊沙康唑可空腹或与食物同服。 健康志愿者口服放射性标记的硫酸伊沙康唑后,平均46.1%的总放射性剂量从粪便中回收,45.5%从尿液中回收。伊沙康唑本身的肾脏排泄量不到给药剂量的1%。无活性裂解产物主要通过代谢及其代谢产物的肾脏排泄消除。完整裂解产物的肾脏排泄量不到给药总剂量的1%。静脉注射放射性标记的裂解产物后,95%的总放射性剂量经尿液排出。 伊沙康唑分布广泛,平均稳态分布容积(Vss)约为450 L。 在健康受试者中,伊沙康唑的清除率估计为2.4至4.1 L/h。研究发现,中国受试者的平均清除率比西方受试者低40%(中国受试者为1.6 L/hr,西方受试者为2.6 L/hr)。 代谢/代谢物 体外研究表明,硫酸异沙康唑在血液中会被酯酶(主要是丁基胆碱酯酶)迅速水解为异沙康唑。异沙康唑是细胞色素P450酶3A4和3A5的底物。在人体单次服用[氰基14C]异沙康唑和[吡啶甲基14C]异沙康唑后,除了活性成分(异沙康唑)和非活性裂解产物外,还鉴定出几种次要代谢物。除活性成分异沙康唑外,未观察到任何单一代谢物的AUC超过药物相关物质的10%。体内研究表明,CYP3A4、CYP3A5 以及随后的尿苷二磷酸葡萄糖醛酸转移酶 (UGT) 参与了伊沙康唑的代谢。 生物半衰期 基于对健康受试者和患者的群体药代动力学分析,伊沙康唑的平均血浆半衰期为 130 小时。 |
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
服用伊沙康唑的患者中,1%至5%会出现血清转氨酶水平短暂升高。这些升高通常无症状且可自行消退,但少数患者因ALT升高而需要停用伊沙康唑。伊沙康唑尚未见临床表现明显的肝毒性报道,但其应用范围有限。其他三唑类药物,如氟康唑和伏立康唑,已上市十余年并广泛使用,但与罕见的临床表现明显的肝损伤病例相关。这种损伤通常在治疗的最初几个月内出现,血清酶升高的模式从胆汁淤积型到肝细胞型不等。已有数例由其他三唑类药物引起的急性肝衰竭病例报道。免疫过敏反应和自身抗体并不常见。停止治疗后通常需要 6 至 10 周才能恢复,但在某些情况下,完全康复的时间可能会延长。 可能性评分:E(未经证实但怀疑是临床上明显的肝损伤的原因)。 蛋白结合 伊沙康唑与蛋白质高度结合(大于 99%),主要与白蛋白结合。 |
| 参考文献 |
1: LiverTox: Clinical and Research Information on Drug-Induced Liver Injury [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases; 2012–. Isavuconazonium. 2018 Apr 27. PMID: 31643955. 2: McCormack PL. Isavuconazonium: first global approval. Drugs. 2015 May;75(7):817-22. doi: 10.1007/s40265-015-0398-6. PMID: 25902926. 3: Walker RC, Zeuli JD, Temesgen Z. Isavuconazonium sulfate for the treatment of fungal infection. Drugs Today (Barc). 2016 Jan;52(1):7-16. doi: 10.1358/dot.2016.52.1.2404002. PMID: 26937491. 4: Isavuconazonium sulfate (Cresemba)--a new antifungal. Med Lett Drugs Ther. 2016 Mar 14;58(1490):37-8. PMID: 26963156. 5: McCreary EK, Nguyen MH, Davis MR, Borlagdan J, Shields RK, Anderson AD, Rivosecchi RM, Marini RV, Sacha LM, Silveira FP, Andes DR, Lepak AJ. Achievement of clinical isavuconazole blood concentrations in transplant recipients with isavuconazonium sulphate capsules administered via enteral feeding tube. J Antimicrob Chemother. 2020 Oct 1;75(10):3023-3028. doi: 10.1093/jac/dkaa274. PMID: 32710097; PMCID: PMC7778376. 6: Murrell D, Bossaer JB, Carico R, Harirforoosh S, Cluck D. Isavuconazonium sulfate: a triazole prodrug for invasive fungal infections. Int J Pharm Pract. 2017 Feb;25(1):18-30. doi: 10.1111/ijpp.12302. Epub 2016 Aug 29. PMID: 27569742. 7: Adamsick ML, Elshaboury RH, Gift T, Mansour MK, Kotton CN, Gandhi RG. Therapeutic drug concentrations of isavuconazole following the administration of isavuconazonium sulfate capsules via gastro-jejunum tube: A case report. Transpl Infect Dis. 2019 Apr;21(2):e13048. doi: 10.1111/tid.13048. Epub 2019 Jan 29. PMID: 30636363. 8: Peyton LR, Gallagher S, Hashemzadeh M. Triazole antifungals: a review. Drugs Today (Barc). 2015 Dec;51(12):705-18. doi: 10.1358/dot.2015.51.12.2421058. PMID: 26798851. 9: Kovanda LL, Maher R, Hope WW. Isavuconazonium sulfate: a new agent for the treatment of invasive aspergillosis and invasive mucormycosis. Expert Rev Clin Pharmacol. 2016 Jul;9(7):887-97. doi: 10.1080/17512433.2016.1185361. Epub 2016 May 21. PMID: 27160418. 10: Reid G, Lynch JP 3rd, Fishbein MC, Clark NM. Mucormycosis. Semin Respir Crit Care Med. 2020 Feb;41(1):99-114. doi: 10.1055/s-0039-3401992. Epub 2020 Jan 30. PMID: 32000287.
|
| 其他信息 |
伊沙康唑是一种有机阳离子,是硫酸伊沙康唑(一种用于治疗侵袭性曲霉病和侵袭性毛霉病的抗真菌药物,是伊沙康唑的前药)的阳离子部分。它具有多种功能,包括作为前药、麦角甾醇生物合成抑制剂、EC 1.14.13.70(甾醇14α-脱甲基酶)抑制剂和抗真菌药物。
伊沙康唑是一种第二代三唑类抗真菌药物,于2015年3月6日获得美国食品药品监督管理局(FDA)批准,并于2015年7月获得欧洲药品管理局(EMA)批准,用于治疗成人侵袭性曲霉病和侵袭性毛霉病,由安斯泰来公司以商品名Cresemba销售。它是活性成分伊沙康唑的前药形式,有口服和注射剂两种剂型。由于伊沙康唑本身在水中的溶解度较低,因此异沙康唑铵制剂因其水溶性高而更受青睐,并可进行静脉给药。该制剂还避免了使用环糊精作为增溶剂(其他抗真菌药物如伏立康唑和泊沙康唑静脉给药所需的溶剂),从而消除了环糊精相关的肾毒性风险。异沙康唑铵具有优异的口服生物利用度、可预测的药代动力学和良好的安全性,使其成为市场上其他少数同类药物的合理替代品。2023年12月8日,FDA批准异沙康唑铵扩大用于儿科患者,适应症与上述药物相同。 伊沙康唑铵是一种三唑类抗真菌药物,主要用于治疗侵袭性曲霉病和毛霉病感染。伊沙康唑治疗期间出现短暂且无症状的血清转氨酶升高的发生率较低,但尚未发现与临床上明显的急性药物性肝损伤病例相关。 药物适应症 伊沙康唑适用于治疗成人和1岁及以上儿童的侵袭性曲霉病和毛霉病,胶囊剂适用于治疗成人和体重16公斤及以上的6岁及以上儿童的侵袭性曲霉病和毛霉病,注射剂适用于治疗成人和体重16公斤及以上的儿童的侵袭性曲霉病和毛霉病。 FDA标签 作用机制 硫酸伊沙康唑是唑类抗真菌药伊沙康唑的前体药物。伊沙康唑通过抑制细胞色素P-450依赖性酶羊毛甾醇14-α-脱甲基酶(Erg11p)来抑制真菌细胞膜关键成分麦角甾醇的合成。该酶负责将羊毛甾醇转化为麦角甾醇。真菌细胞膜内甲基化甾醇前体的积累和麦角甾醇的消耗会削弱细胞膜的结构和功能。哺乳动物细胞的脱甲基作用对伊沙康唑的抑制作用不太敏感。 药效学 在一项对照试验中,接受伊沙康唑治疗侵袭性曲霉病的患者,其血浆AUC或血浆伊沙康唑浓度与疗效之间无显著相关性。研究还评估了多次服用伊沙康唑胶囊对QTc间期的影响。在一项随机、安慰剂和活性对照(莫西沙星400 mg单剂量)、四组平行治疗研究中,160名健康受试者接受了伊沙康唑治疗。在第1天和第2天,受试者每日三次服用2粒伊沙康唑胶囊(相当于200 mg伊沙康唑),随后连续13天每日一次服用2粒或6粒伊沙康唑胶囊(相当于600 mg伊沙康唑)。结果显示,伊沙康唑可导致QTc间期呈剂量依赖性缩短。对于2粒胶囊的给药方案,给药后2小时,其QTc间期与安慰剂相比的最小二乘均值(LSM)差异为-13.1毫秒[90% CI:-17.1,-9.1毫秒]。将剂量增加至 6 粒胶囊后,给药后 2 小时,最小二乘均值 (LSM) 与安慰剂相比差异为 -24.6 毫秒 [90% 置信区间:-28.7,-20.4]。伊沙康唑尚未与其他可缩短 QTc 间期的药物联合使用进行评估,因此其叠加效应尚不清楚。与其他唑类抗真菌药物一样,伊沙康唑的耐药机制可能涉及多种机制,包括靶基因 CYP51 的氨基酸替换。观察到甾醇谱的变化和外排泵活性的升高;然而,这些发现的临床意义尚不明确。体外和动物研究表明,伊沙康唑与其他唑类药物之间存在交叉耐药性。交叉耐药性与临床结局的相关性尚未完全明确;然而,既往唑类药物治疗失败的患者可能需要其他抗真菌治疗。 |
| 分子式 |
C35H37F2N8O5S+
|
|---|---|
| 分子量 |
719.78
|
| 精确质量 |
717.242
|
| 元素分析 |
C, 58.40; H, 5.18; F, 5.28; N, 15.57; O, 11.11; S, 4.45
|
| CAS号 |
742049-41-8
|
| 相关CAS号 |
338990-84-4 (chloride);497235-79-7 (chloride HCl);742049-41-8 (cation);946075-13-4 (sulfate);
|
| PubChem CID |
6918606
|
| 外观&性状 |
Solid powder
|
| LogP |
4.975
|
| tPSA |
187.61
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
13
|
| 可旋转键数目(RBC) |
15
|
| 重原子数目 |
51
|
| 分子复杂度/Complexity |
1210
|
| 定义原子立体中心数目 |
2
|
| SMILES |
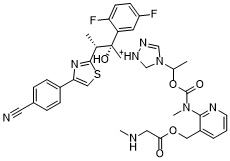
S1C=C(C2C=CC(C#N)=CC=2)N=C1[C@H](C)[C@@](C1C=C(C=CC=1F)F)(CN1C=[N+](C=N1)C(C)OC(N(C)C1C(=CC=CN=1)COC(CNC)=O)=O)O
|
| InChi Key |
AWANULZDKHTBBZ-QXLBVTBOSA-O
|
| InChi Code |
InChI=1S/C35H36F2N8O5S/c1-22(33-42-30(18-51-33)25-9-7-24(15-38)8-10-25)35(48,28-14-27(36)11-12-29(28)37)19-45-21-44(20-41-45)23(2)50-34(47)43(4)32-26(6-5-13-40-32)17-49-31(46)16-39-3/h5-14,18,20,22-23,39,48H,16-17,19,21H2,1-4H3/p+1/t22-,23?,35+/m0/s1
|
| 化学名 |
Glycine, N-methyl-, (2-(((1-(1-((2R,3R)-3-(4-(4-cyanophenyl)-2-thiazolyl)-2-(2,5-difluorophenyl)-2-hydroxybutyl)-1H-1,2,4-triazolium-4-yl)ethoxy)carbonyl)methylamino)-3-pyridinyl)methyl ester
|
| 别名 |
Isavuconazonium Free Base; BAL8557; BAL 8557; BAL-8557
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.3893 mL | 6.9466 mL | 13.8931 mL | |
| 5 mM | 0.2779 mL | 1.3893 mL | 2.7786 mL | |
| 10 mM | 0.1389 mL | 0.6947 mL | 1.3893 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。