| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 体外研究 (In Vitro) |
阿莫地喹(10–20 μM;4 小时)治疗以剂量依赖性方式抑制脂多糖 (PLS) 引起的促炎细胞因子(IL-1β、白细胞介素 6、TNF-α 和 iNOS)的表达 [1 ]。 TH+ 神经元数量和多巴胺摄取分析表明,阿莫地喹(5 μM;24 小时)可有效防止神经毒性 (6-OHDA) 诱导的原发性多巴胺细胞死亡。此外,在大鼠 PC12 细胞中观察到阿莫地喹。莫迪喹的神经保护作用[1]
|
|---|---|
| 体内研究 (In Vivo) |
阿莫地喹(40 mg/kg;腹膜内;每日;持续 3 天)治疗可减少雄性 ICR 小鼠的星形胶质细胞和小胶质细胞/巨噬细胞的血肿周围激活。除了改善小鼠的运动障碍外,阿莫地喹还可以降低 ICH 诱导的 IL-1β、CCL2 和 CXCL2 mRNA 表达 [2]。
|
| 细胞实验 |
RT-PCR[1]
细胞类型:原代小胶质细胞 测试浓度: 10 µM、15 µM、20 µM 孵育时间:4小时 实验结果:抑制LPS诱导的促炎细胞因子(IL-1β、白细胞介素6、TNF-α和iNOS) )以剂量依赖性方式。 |
| 动物实验 |
动物/疾病模型:雄性ICR小鼠(8-10周龄)诱导脑出血(ICH)[2]
剂量:40 mg/kg 给药途径:腹腔注射(ip);每日一次;持续3天 实验结果:血肿周围的小胶质细胞/巨噬细胞和星形胶质细胞活化减少。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服后迅速吸收。 盐酸阿莫地喹易于从胃肠道吸收。它在肝脏中迅速转化为活性代谢物去乙基阿莫地喹,后者几乎贡献了全部的抗疟作用 (10)。关于去乙基阿莫地喹的终末血浆消除半衰期的数据不足。给药数月后,在尿液中均可检测到阿莫地喹和去乙基阿莫地喹。 口服后,盐酸阿莫地喹迅速吸收…… 7 名健康成年男性口服阿莫地喹 (600 mg) 后……阿莫地喹的峰浓度为 32 ± 3 ng/mL,时间为 0.5 ± 0.03 小时。全血和浓缩红细胞中阿莫地喹的峰浓度分别为 60 ± 10 ng/mL 和 42 ± 6 ng/mL,均在 0.5 ± 0.1 小时达到。此后,阿莫地喹的浓度迅速下降,且在 8 小时内无法检测到。代谢物(去乙基阿莫地喹)的平均血浆峰浓度为 181 ± 26 ng/mL。全血和浓缩红细胞的达峰时间分别为 2.2 ± 0.5 小时和 3.6 ± 1.1 小时。 有关阿莫地喹(共 10 项)的更多吸收、分布和排泄(完整)数据,请访问 HSDB 记录页面。 代谢/代谢物 阿莫地喹的主要清除途径是经肝脏生物转化生成去乙基阿莫地喹(主要生物活性代谢物),由于首过效应显著,口服的阿莫地喹几乎没有未转化的药物进入体循环。 ……盐酸阿莫地喹……迅速且广泛地代谢为去乙基阿莫地喹,后者在血细胞中浓缩。去乙基阿莫地喹而非阿莫地喹很可能是大部分观察到的抗疟活性的来源,口服阿莫地喹的毒性作用可能部分归因于去乙基阿莫地喹。 口服阿莫地喹后,血液中母体化合物的含量相对较低。阿莫地喹的主要清除途径是经肝脏生物转化生成去乙基阿莫地喹(主要的生物活性代谢物),由于首过效应显著,口服的阿莫地喹几乎没有未转化的代谢物进入体循环。 为了进一步了解限制阿莫地喹使用的肝毒性的假定代谢原因,我们对阿莫地喹的肝脏代谢进行了研究。麻醉大鼠经门静脉注射(54 μmol/kg)后,药物主要以硫醚结合物的形式经胆汁排泄(5小时内排出23 ± 3%的剂量;平均值 ± 标准差,n = 6)。门静脉注射后,24小时内,20%的剂量以母体化合物以及N-脱烷基化和氧化脱氨产物的形式经尿液排泄。去乙基阿莫地喹在肝脏中蓄积,但通过检测胆汁中谷胱甘肽加合物的排泄情况,发现它并非生物活化的底物。预先给予P450抑制剂酮康唑,可使胆汁排泄减少50%,并相应降低与肝脏蛋白不可逆结合的药物量。这表明P450在阿莫地喹生物活化为活性代谢物的过程中发挥作用,该活性代谢物可与谷胱甘肽和蛋白质结合。在体外使用雄性大鼠肝微粒体观察到了去乙基化和不可逆结合,且酮康唑再次抑制了这些反应。然而,尽管阿莫地喹大量转化为去乙基阿莫地喹,但在人(6名受试者)肝微粒体中并未观察到此类结合。阿莫地喹醌亚胺在人或大鼠肝微粒体存在下均发生快速还原。因此,体外研究可能低估了阿莫地喹在体内的生物活化。这些数据表明,肝脏中蛋白质加合物的形成程度取决于阿莫地喹氧化和其醌亚胺还原的相对速率。这反过来可能是阿莫地喹特异性肝毒性的一个诱发因素。用氟取代阿莫地喹中的酚羟基可阻断该药物在体内的生物活化。引入N-羟乙基官能团可使阿莫地喹及其脱羟氟类似物通过O-葡萄糖醛酸化部分清除,并改变阿莫地喹I相氧化和直接II相结合之间的平衡。 阿莫地喹(AQ)代谢为N-去乙基阿莫地喹(DEAQ)是其在人体内的主要代谢途径。作者利用人肝微粒体和两组重组人细胞色素P450同工酶(分别来自淋巴母细胞和酵母)开展研究,以鉴定参与AQ代谢的CYP同工酶。CYP2C8是清除AQ并催化DEAQ生成的主要肝脏同工酶。肝外P450酶1A1和1B1也清除AQ,并催化一种未知代谢物M2的生成。重组CYP2C8对AQ N-去乙基化的Km和Vmax值分别为1.2 μM和2.6 pmol/min/pmol CYP2C8,而人肝微粒体(HLM)的相应值分别为2.4 μM和1462 pmol/min/mg蛋白。采用相对活性因子法估算CYP2C8在DEAQ生成中的相对贡献为100%。对10个不同的HLM样本进行了AQ代谢与8种肝脏P450酶活性的相关性分析。DEAQ的生成和AQ的清除均与CYP2C8的标志性底物紫杉醇的6α-羟基化表现出极好的相关性(r²分别为0.98和0.95)。槲皮素对DEAQ生成的抑制作用呈竞争性,其对CYP2C8和HLM的Ki值分别为1.96 μM和1.56 μM。将AQ对接至CYP2C同工酶的活性位点同源模型显示,AQ与CYP2C8存在有利的相互作用,这支持了N-去乙基化反应的可能性。这些数据表明,CYP2C8是负责AQ代谢的主要肝脏同工酶。AQ去乙基化反应具有特异性、高亲和力和高周转率,使其成为CYP2C8活性的优良标志反应。 生物半衰期 5.2 ±口服阿莫地喹 600 毫克后,阿莫地喹的表观末端半衰期为 5.2 + 1.7(范围 0.4 至 5.5)分钟,估计的消除相半衰期的几何平均值为 2.1(范围 0.5 至 5.7)小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
阿莫地喹与少数患者(1%)的血清转氨酶升高有关。更重要的是,已有多个关于阿莫地喹引起特异性急性肝损伤的报道。损伤通常在1至4个月内出现,且常伴有粒细胞缺乏症。血清酶升高模式最常见的是肝细胞性,典型症状类似于急性病毒性肝炎。超敏反应和自身抗体并不常见。肝炎可能很严重,已有数例死亡或需要紧急肝移植的病例报道。严重肝损伤的发生率估计约为1/15,000。由于存在粒细胞缺乏症和肝损伤的风险,阿莫地喹不再推荐用于疟疾预防,主要用于美国以外疟疾流行地区的治疗。关于疟疾治疗的一般建议,包括诊断、治疗、药物剂量和安全性方面的具体细节,可在美国疾病控制与预防中心 (CDC) 网站获取:http://www.cdc.gov/malaria/。 可能性评分:A(已确定的临床明显肝损伤病因)。 药物相互作用 由于已知同时服用三硅酸镁和高岭土会降低氯喹的胃肠道吸收,因此很可能也会降低阿莫地喹的吸收。 在皮内注射狂犬疫苗进行狂犬病暴露前预防期间,同时服用推荐剂量的氯喹(用于抑制疟疾化学预防)可能会干扰疫苗的抗体反应。然而,这种相互作用的临床意义尚待明确,但应予以考虑,并且可能与阿莫地喹的情况相关。 应避免与其他抗疟药同时使用,并应定期进行实验室检查,以确保血液指标和肝功能检查结果保持在正常范围内。 |
| 参考文献 |
[1]. Chun-Hyung Kim, et al. Nuclear receptor Nurr1 agonists enhance its dual functions and improve behavioral deficits in an animal model of Parkinson's disease. Proc Natl Acad Sci U S A. 2015 Jul 14;112(28):8756-61.
[2]. Keita Kinoshita, et al. A Nurr1 agonist amodiaquine attenuates inflammatory events and neurological deficits in a mouse model of intracerebral hemorrhage. J Neuroimmunol. 2019 May 15;330:48-54. [3]. Akira Yokoyama, et al. Effect of amodiaquine, a histamine N-methyltransferase inhibitor, on, Propionibacterium acnes and lipopolysaccharide-induced hepatitis in mice. Eur J Pharmacol. 2007 Mar 8;558(1-3):179-84. [4]. M T HOEKENGA. The treatment of acute malaria with single oral doses of amodiaquin, chloroquine, hydroxychloroquine and pyrimethamine. Am J Trop Med Hyg. 1954 Sep;3(5):833-8. |
| 其他信息 |
治疗用途
治疗类别:抗疟药 关于卵形疟原虫和疟原虫对疟疾药物的体内敏感性,近期数据非常有限。尽管近期有一份关于疟原虫对氯喹产生耐药性的报告,但两种疟原虫均被认为对氯喹非常敏感。经验表明,卵形疟原虫和疟原虫也对阿莫地喹、甲氟喹和青蒿素衍生物敏感。 关于治疗无并发症间日疟的建议总结:对于氯喹耐药的间日疟,应使用阿莫地喹(30 mg/kg 体重,分 3 天服用,每日一次,每次 10 mg/kg 体重)联合伯氨喹。 /适应症/用于/治疗/非免疫人群的急性疟疾发作。它至少与氯喹一样有效,并且对某些氯喹耐药株也有效,尽管已有关于阿莫地喹耐药性的报道。 药物警告 与使用阿莫地喹预防疟疾相关的粒细胞缺乏症 近期有报道称,英国旅行者中使用阿莫地喹(卡莫喹)后出现7例粒细胞缺乏症(1)。另有16例来自西欧的与使用阿莫地喹相关的粒细胞缺乏症病例近期已报告给药品生产商,美国疾病控制与预防中心(CDC)也收到了2例美国病例的报告。这25例病例中有23例发生在1985年或1986年,据报道其中7例死亡。在已知阿莫地喹预防用药持续时间的20例病例中,用药时间从3周到24周不等。在25例病例中,除4例以外,其余病例均按适当剂量(成人每周400毫克碱基)使用阿莫地喹进行预防。已知其中14例患者同时使用了其他抗疟药进行预防……现在看来,阿莫地喹可能带来的任何预防优势都无法抵消其可能导致的粒细胞缺乏症风险。因此,美国疾病控制与预防中心(CDC)不再建议使用阿莫地喹进行预防。 由于阿莫地喹可能在肝脏中蓄积,因此肝病患者、酒精中毒患者以及正在服用肝毒性药物的患者应谨慎使用该药。 儿童对4-氨基喹啉衍生物尤其敏感。由于儿童体内治疗浓度和中毒浓度之间的范围很窄,因此不应在该年龄组中进行阿莫地喹的肠外给药。 对4-氨基喹啉衍生物过敏的患者禁用阿莫地喹。 有关阿莫地喹(共14条)的更多药物警告(完整)数据,请访问HSDB记录页面。 药效学 阿莫地喹是一种4-氨基喹啉类药物,其结构和活性与氯喹相似,已用作抗疟药和抗炎药超过40年。阿莫地喹的疗效至少与氯喹相当,并且对某些氯喹耐药株有效,但已有阿莫地喹耐药的报道。阿莫地喹的作用机制尚未确定。 4-氨基喹啉类药物可抑制心肌,损害心脏传导,并引起血管舒张,从而导致低血压。它们还会抑制呼吸,并引起复视、头晕和恶心。 |
| 精确质量 |
355.145
|
|---|---|
| CAS号 |
86-42-0
|
| 相关CAS号 |
Amodiaquine dihydrochloride dihydrate;6398-98-7;Amodiaquine-d10;1189449-70-4;Amodiaquine dihydrochloride;69-44-3
|
| PubChem CID |
2165
|
| 外观&性状 |
Crystals from absolute ethanol
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
478.0±45.0 °C at 760 mmHg
|
| 熔点 |
208°C
|
| 闪点 |
242.9±28.7 °C
|
| 蒸汽压 |
0.0±1.2 mmHg at 25°C
|
| 折射率 |
1.669
|
| LogP |
4.77
|
| tPSA |
48.39
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
25
|
| 分子复杂度/Complexity |
406
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
OVCDSSHSILBFBN-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C20H22ClN3O/c1-3-24(4-2)13-14-11-16(6-8-20(14)25)23-18-9-10-22-19-12-15(21)5-7-17(18)19/h5-12,25H,3-4,13H2,1-2H3,(H,22,23)
|
| 化学名 |
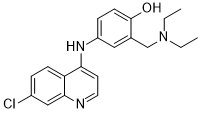
4-[(7-chloroquinolin-4-yl)amino]-2-(diethylaminomethyl)phenol
|
| 别名 |
Camochin Camoquin Camoquinal Camoquine Flavoquine Miaquin NSC 13453 SN-10751
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~66.67 mg/mL (~187.35 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT02741024 | COMPLETED | Drug: Amodiaquine-Artesunate (ASAQ) Drug: Artemether-Lumefantrine (AL) |
Malaria | Medecins Sans Frontieres, Netherlands | 2013-10 | Phase 4 |
| NCT01704508 | COMPLETED | Drug: Artemether-lumefantrine Drug: Dihydroartemisinin-piperaquine |
Malaria | Bandim Health Project | 2012-11 | Phase 4 |
| NCT02627456 | COMPLETED | Biological: PfSPZ Vaccine Biological: PfSPZ Challenge Material Drug: PBS and HSA Diluent |
Malaria | National Institute of Allergy and Infectious Diseases (NIAID) | 2015-12-09 | Phase 1 |
|