| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
IC50: 10.5 μM (TRPP3 channel)[1] NHE[2] Macropinocytosis[3]
|
|---|---|
| 体外研究 (In Vitro) |
在 X 中,TRPP3 介导的 Ca2+ 吸收被 EIPA 盐酸盐(100 μM,30 分钟)抑制。滑鼠卵[1]。 EIPA 盐酸盐 (10-100 μM) 可逆地抑制基础 Na+ 电流 (IC50: 19.5 μM) [1]。通过 NHE3(Na+/H+-交换器 3),EIPA 盐酸盐(300 μM,6 小时)可增强 IEC-18 细胞中的自噬 [2]。 EIPA 盐酸盐(20 μM,2 小时)可抑制 HT-29 细胞和 MIA PaCa-2 细胞通过巨胞饮作用摄取 CA-PZ [3]。 EIPA 盐酸盐(30 μM,3 小时)可通过减少 Zn2+ 进入小脑颗粒神经元来减轻锌/红藻氨酸的毒性 [4]。通过上调 p21 表达,EIPA 盐酸盐(5-100 μM,48 小时)抑制 MKN28 细胞增殖 [5]。 EIPA 盐酸盐(3 μM,6 小时)可防止 LPS 引起的 COX-2 蛋白水平升高 [7]。
|
| 体内研究 (In Vivo) |
在 ddY 品系小鼠中,静脉注射 1 mg/kg EIPA 盐酸盐可剂量依赖性地减少由 I/R(缺血/再灌注)引起的肾损伤[6]。 ?在球囊型 LPS 诱导的炎症范例中,EIPA 盐酸盐 (10 mg/kg) 可减轻 LPS 诱导的炎症 [7]。
|
| 酶活实验 |
方法:在表达MKN28的NHE暴露于EIPA 48小时后,研究EIPA对增殖、pH(c)、[Cl(-)](c)以及调节细胞周期和MAPKs的蛋白质表达的影响。 结果:EIPA通过引起G(0)/G(1)阻滞来抑制MKN28细胞的增殖,对pH(c)没有任何显著影响,但与[Cl(-)](c)的减少有关。尽管单独使用EIPA对pH(c)没有影响,但EIPA与DIDS(Cl(-)/HCO(3)(-)交换剂的抑制剂)联合使用;也就是说,阴离子交换剂(AE)和Na+驱动的Cl(-)/HCO(3)(-)交换剂(NDCBE))降低了pH(c),这表明DIDS敏感的Cl(-]/HCO(3-)转运蛋白,如AE和/或NDCBE,在NHE抑制条件下通过刺激HCO(3-)摄取和Cl(-”释放来保持pH(c”正常”。EIPA诱导[Cl(-)]降低(c)上调与MAPKs磷酸化相关的p21表达,抑制与G(0)/G(1)阻滞相关的增殖。 结论:在NHE抑制条件下,DIDS敏感的Cl(-)/HCO(3)(-)交换器介导的补偿使pH(c)保持正常,EIPA通过降低[Cl(-)](c)来上调p21表达,从而抑制MKN28细胞的增殖。这是第一项表明NHE抑制剂通过减少[Cl(-)](c)而不是pH(c)来抑制癌症细胞增殖的研究[5]。
|
| 细胞实验 |
细胞增殖测定 [5]
细胞类型: MKN28 细胞 测试浓度: 5、10、25、50 和 100 μM 孵育时间:48小时 实验结果:以剂量和时间依赖性方式抑制细胞增殖。 蛋白质印迹分析[2] 细胞类型: IEC-18 细胞 测试浓度: 300 μM 孵育持续时间:6 小时 实验结果:LC3-II 总蛋白水平和 P62 通量增加。 ATG5、7、12和P62的表达增加。 |
| 动物实验 |
动物/疾病模型:雄性ddY品系小鼠[6]
剂量:1 mg/kg 给药途径:静脉注射 实验结果:减轻肾脏组织学损伤,改善缺血/再灌注损伤引起的肾脏ET-1含量升高。 动物/疾病模型:气囊型LPS诱导炎症模型[7] 剂量:10 mg/kg 给药途径:口服 实验结果:抑制LPS诱导的白细胞浸润气囊。抑制造口袋液中PGE2的含量。 |
| 参考文献 |
[1]. Inhibition of TRPP3 channel by MK-870 and analogs. Mol Pharmacol. 2007 Dec;72(6):1576-85.
[2]. Na+/H+ Exchanger Regulates Amino Acid-Mediated Autophagy in Intestinal Epithelial Cells. Cell Physiol Biochem. 2017;42(6):2418-2429. [3]. A new HDAC inhibitor cinnamoylphenazine shows antitumor activity in association with intensive macropinocytosis.Oncotarget. 2017 Feb 28;8(9):14748-14758. [4]. Acidosis and 5-(N-ethyl-N-isopropyl)amiloride (EIPA) Attenuate Zinc/Kainate Toxicity in Cultured Cerebellar Granule Neurons. Biochemistry (Mosc). 2015 Aug;80(8):1065-72. [5]. An inhibitor of Na(+)/H(+) exchanger (NHE), ethyl-isopropyl amiloride (EIPA), diminishes proliferation of MKN28 human gastric cancer cells by decreasing the cytosolic Cl(-) concentration via DIDS-sensitive pathways. Cell Physiol Biochem. 2012;30(5):1241-53. [6]. Role of Na+/H+ exchanger in the pathogenesis of ischemic acute renal failure in mice. J Cardiovasc Pharmacol. 2007 Mar;49(3):154-60. [7]. Inhibition of lipopolysaccharide-induced prostaglandin E2 production and inflammation by the Na+/H+ exchanger inhibitors. J Pharmacol Exp Ther. 2007 Apr;321(1):345-52. |
| 其他信息 |
TRPP3是瞬时受体电位(TRP)阳离子通道超家族的成员,是一种Ca²⁺激活通道,可通透Ca²⁺、Na⁺和K⁺。TRPP3与舌双极细胞的酸味感知以及脊髓神经元pH敏感性动作电位的调节有关。TRPP3也存在于其他组织的兴奋性和非兴奋性细胞中,包括视网膜、脑、心脏、睾丸和肾脏,但其功能尚不清楚。本研究利用非洲爪蟾卵母细胞表达、电生理和放射性示踪技术,研究了阿米洛利及其类似物(已知可抑制多种离子通道和转运蛋白,并对所有味觉刺激均有反应)对TRPP3通道的功能调节作用。我们发现,阿米洛利及其类似物对TRPP3通道活性的抑制亲和力各不相同。放射性标记的 (45)Ca2+ 摄取实验表明,阿米洛利、苯那米、苯扎米和 5-(N-乙基-N-异丙基)阿米洛利 (EIPA) 可抑制 TRPP3 介导的 Ca2+ 转运。双微电极电压钳实验显示,阿米洛利类似物可显著抑制 TRPP3 介导的 Ca2+ 激活电流,其抑制效力顺序为苯那米 > 苯扎米 > EIPA > 阿米洛利,IC50 值分别为 0.14、1.1、10.5 和 143 μM。抑制效力与抑制剂分子大小呈正相关。利用细胞贴附式膜片钳技术,我们发现阿米洛利类似物可降低通道开放概率和平均开放时间,但对单通道电导无影响。在先前报道的抑制剂四戊基铵存在的情况下,对苯那米尔的抑制作用的研究表明,阿米洛利和有机阳离子抑制剂竞争结合 TRPP3 上的同一位点。TRPP3 可能与先前报道的体内阿米洛利敏感阳离子转运有关。[1]
|
| 分子式 |
C11H19CL2N7O
|
|---|---|
| 分子量 |
336.220858812332
|
| 精确质量 |
335.1
|
| 元素分析 |
C, 39.30; H, 5.70; Cl, 21.09; N, 29.16; O, 4.76
|
| CAS号 |
1345839-28-2
|
| 相关CAS号 |
EIPA;1154-25-2
|
| PubChem CID |
56935648
|
| 外观&性状 |
Typically exists as Light yellow to yellow solids at room temperature
|
| tPSA |
137Ų
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
372
|
| 定义原子立体中心数目 |
0
|
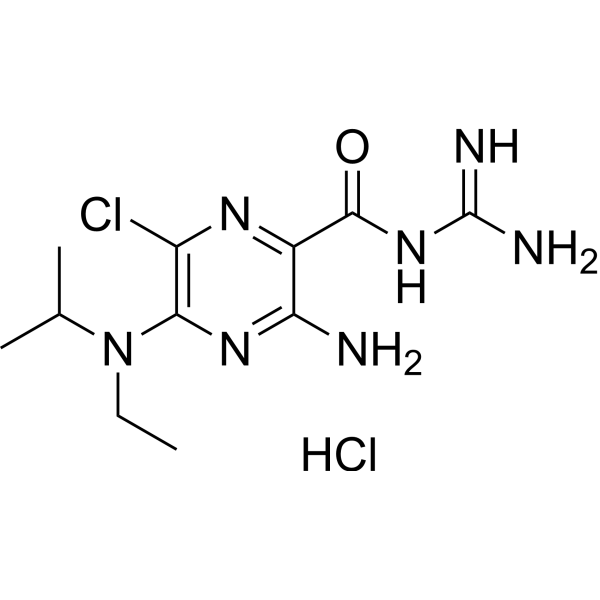
| SMILES |
CCN(C1=NC(=C(N=C1Cl)C(=O)N=C(N)N)N)C(C)C.Cl
|
| InChi Key |
BGHBOQNLQNKPFO-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C11H18ClN7O.ClH/c1-4-19(5(2)3)9-7(12)16-6(8(13)17-9)10(20)18-11(14)15;/h5H,4H2,1-3H3,(H2,13,17)(H4,14,15,18,20);1H
|
| 化学名 |
3-amino-6-chloro-N-(diaminomethylidene)-5-[ethyl(propan-2-yl)amino]pyrazine-2-carboxamide;hydrochloride
|
| 别名 |
EIPA hydrochloride; EIPA (hydrochloride); 1345839-28-2; CHEMBL1909809; 3-amino-6-chloro-N-(diaminomethylidene)-5-[ethyl(propan-2-yl)amino]pyrazine-2-carboxamide;hydrochloride; L593754 hydrochloride; 5-(N-Ethyl-N-isopropyl)amiloridehydrochloride; MH 12-43 hydrochloride; .
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~130 mg/mL (~386.65 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.9742 mL | 14.8712 mL | 29.7424 mL | |
| 5 mM | 0.5948 mL | 2.9742 mL | 5.9485 mL | |
| 10 mM | 0.2974 mL | 1.4871 mL | 2.9742 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。