| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 500mg |
|
| 靶点 |
JAK1 (IC50 = 10 nM); JAK2 (IC50= 28 nM); Tyk2 (IC50= 116 nM); JAK3 (IC50= 810 nM)
|
||
|---|---|---|---|
| 体外研究 (In Vitro) |
Filgotinib (GLPG0634) 剂量依赖性地抑制由 IL-4(一种通过 JAK1 和 JAK3 发出信号的细胞因子)介导的 Th2 细胞分化。此外,filgotinib 还在 1 μM 或更低的浓度下有效抑制 Th1 分化 [1]。 PRL 或 EPO 产生的 JAK2 同二聚体介导的信号传导 (IC50 > 10 μM) 不受 filgotinib (GLPG0634) 抑制 [2]。
|
||
| 体内研究 (In Vivo) |
Filgotinib(马来酸盐)(1–10 mg/mL;口服和静脉注射;患有胶原诱导性关节炎的大鼠)具有良好的药代动力学特征,可减少炎症细胞、骨和软骨退化以及爪子肿胀。因素大小[1]。
在经过修改的大鼠 CIA 模型中,filgotinib(GLPG0634;3、10、30 mg/kg,口服)剂量依赖性地抑制病程。 Filgotinib(50 mg/kg,op)抑制骨骼和软骨的恶化,有效减少足部T细胞(CD3+细胞)和巨噬细胞(F4/80+细胞)的浸润,并降低血液中细胞因子和趋化因子的水平,例如 IL-6、IP-10、XCL1 和 MCP-1[1]。在 CIA 大鼠模型中,filgotinib(GLPG0634;0.1 和 0.3 mg/kg)显示出有效性 [2]。 |
||
| 酶活实验 |
生化实验[1]
IC50测定。[1] 重组JAK1、TYK2、JAK2和JAK3 分别在50 mM HEPES (pH 7.5)、1 mM EGTA、10 mM MgCl2、2 mM DTT和0.01% Tween 20中进行活性测定。测定每组分中JAK蛋白的量,保持初始速度和随时间的线性。ATP浓度相当于实验Km值的4倍,底物浓度(光共轭的JAK-1(Tyr1023)肽)与实验测定的Km值对应。室温孵育90 min后,在Lance检测缓冲液中加入2 nM的euroium -anti-phosphotyrosine Ab 和10 mM的EDTA,测定磷酸化底物的量。在加入ATP之前,将酶与化合物在RT下预孵育60分钟,测定化合物的IC50值。 Kd的测定。[1] 解离常数在一家CRO公司测定。将具有快速解离率的荧光标记ATP模拟物(分别为JAK1、JAK2和JAK3的PRO13、PRO14和PRO13)与纯化的jak的JH1结构域一起在20 mM MOPS (pH 7.5)、1 mM DTT、0.01% Tween 20和500 mM hydroxyectoine(仅限JAK3)中孵育30分钟。将化合物(浓度范围为520 pM至1.1 μM)添加到100% DMSO中,并测量报告位移的时间依赖性。得到探针位移50%时对应的IC50值,并根据Cheng-Prusoff方程计算Kd值。 |
||
| 细胞实验 |
细胞分析[1]
IL-4诱导STAT6磷酸化[1] 将THP-1细胞(ATCC TIB-202)与化合物在室温下预孵育1 h,与IL-4 (10 ng/ml)在室温下孵育60 min,并进行流式细胞术处理。细胞在Cytofix/Cytoperm缓冲液中固定,在Phosflow perm缓冲液III中冰透30分钟。阻断(Fc阻断试剂)后,用小鼠抗人pe标记的抗pSTAT6 Ab检测pSTAT6。 IL-2、IL-3和促红细胞生成素诱导STAT5磷酸化[1] NK-92细胞(ATCC CRL-2407) IL-2饥饿过夜,与化合物在37℃预孵育1小时,RT下IL-2 (1 ng/ml)刺激20分钟,并进行alphasgreen分析。将TF1细胞在含0.1% FBS的RPMI 1640中饥饿过夜,在室温下用化合物预孵育1小时,在室温下用IL-3 (30 ng/ml)刺激20分钟,并进行AlphaScreen分析。UT-7-红细胞生成素(EPO)细胞(UT-7的EPO依赖性衍生物;Centocor)与化合物在RT下预孵育1小时,用EPO (1 U/ml)刺激20分钟,然后进行alphasgreen分析。pSTAT5的测量基本上是根据制造商的协议使用AlphaScreen技术。 IFN-α和IFN-γ诱导STAT1磷酸化[1] STAT1 U2OS细胞(Invitrogen,目录号:K1469)与化合物在37℃下预孵育1 h,用30,000 U/ml IFN-αB2 (PBL IFN来源,目录号:11115-1)或20 ng/ml IFN-γ在37℃下裂解1小时(裂解缓冲液含有2 nM Tb-Ab),根据制造商的方案,在RT下孵育60分钟。pSTAT1通过时间分辨荧光共振能量转移检测。 催乳素诱导STAT5磷酸化[1] 22Rv1细胞(ATCC CW22Rv)饥饿过夜,用化合物预孵育,用催乳素(PRL)触发;500 ng/ml人PRL 20 min),用10 mM Tris-HCl (pH 7.5)、5 mM EDTA、150 mM NaCl、0.5% Triton X-100、50 mM NaF、30 mM焦磷酸钠、10%甘油缓冲液(含磷酸酶/蛋白酶抑制剂鸡尾酒)裂解,离心。细胞裂解液(180 μg)用于STAT5免疫沉淀(anti-STAT5 polyclonal Abs, C-17;蛋白A-Sepharose珠)。Western blotting后用密度分析法测定总STAT5和磷酸化STAT5。 IL-3/ jak2诱导Ba/F3细胞增殖[1] Ba/F3细胞(由V. Lacronique, Paris, France提供)依赖于IL-3和JAK2信号,与化合物在37℃孵育40 h,之后通过测量ATP含量来分析细胞增殖。 肿瘤抑制素m诱导的HeLa细胞STAT1报告基因检测[1] 用pSTAT1报告基因构建体转染HeLa细胞(ATCC CCL-2)。LR0127)。转染24 h后,用化合物孵育1 h,用抑癌素M (OSM)触发;33 ng / ml)。孵育20 h后,裂解细胞,根据供应商推荐使用荧光素酶SteadyLite试剂盒测定荧光素酶活性。同时,测定4 mg/ml 2-硝基苯β-d-半乳糖苷存在时β-半乳糖苷酶活性。 可拆卸的实验。[1] 从American Type Culture Collection中获得的HeLa和HCT116细胞用50 nM的ON-TARGETplus SMARTpool小干扰RNA (siRNA)转染人JAK1、JAK2、JAK3或TYK2,或用非靶向或gapdh阴性对照siRNA转染Invitrogen公司的Lipofectamine RNAiMAX转染试剂。转染4天后,将细胞饥饿过夜,用IL-6/sIL-6R(均为250 ng/ml)刺激20分钟,并根据制造商的方案使用alphasgreen技术检测pSTAT1水平。 T细胞分化的研究进展[1] 利用淋巴细胞密度梯度离心从健康供体的肉色被毛中分离PBMCs。使用初始CD4+ T细胞分离试剂盒II,通过消耗非T辅助细胞和记忆CD4+ T细胞进一步分离初始CD4+ T细胞。分离的初始CD4+ T细胞在细胞因子存在的情况下,用板结合的抗cd3 (3 μg/ml)和抗cd28 (5 μg/ml)抗体刺激其分化为Th1、Th2或Th17 Th亚群。在10 μg/ml抗il -4 Ab、10 ng/ml IL-2和10 ng/ml IL-12的作用下培养Th1细胞。在10 μg/ml抗ifn -γ Ab (Becton Dickinson)、25 ng/ml IL-4和10 ng/ml IL-2的作用下培养Th2细胞极化。对于Th17细胞极化,使用以下细胞因子的混合物:10 ng/ml IL-6, 10 ng/ml IL-1β, 1 ng/ml TGF-β和100 ng/ml IL-23。为了监测化合物对T细胞分化的影响,在T细胞分化开始时按指定浓度添加化合物。5 d后,使用RNeasy Mini试剂盒提取RNA,进行逆转录,并通过实时检测IFN-γ (Th1标记物)、IL-13 (Th2标记物)或IL-17F (Th17标记物)的表达来监测Th亚群分化程度。 |
||
| 动物实验 |
|
||
| 药代性质 (ADME/PK) |
吸收
口服后,菲戈替尼吸收迅速。菲戈替尼的血浆峰浓度中位数出现在给药后2-3小时,而GS-829845的血浆峰浓度中位数出现在给药后5小时。菲戈替尼可在2-3天内达到稳态血药浓度,而GS-829845则需4天。食物似乎对菲戈替尼的吸收没有显著影响;因此,服用该药不受进食影响。重复口服200 mg菲戈替尼后,菲戈替尼的Cmax和AUCτ值分别为2.15 μg/mL和6.77 μg·h/mL。对于GS-829845(主要代谢物),报告的Cmax为4.43 μg/mL,报告的AUCτ为83.2 μg·h/mL。 排泄途径 在给药的总剂量中,约 87% 经肾脏排泄,15% 经粪便排泄。 代谢/代谢物 羧酸酯酶参与 filgotinib 的代谢。羧酸酯酶 2 (CES2) 同工酶主要负责将 filgotinib 代谢为其主要代谢物 GS-829845。虽然羧酸酯酶 1 (CES1) 在 filgotinib 的生物转化中作用较小,但体外研究表明,当 CES2 饱和时,CES1 可部分补偿。GS-829845 是迄今为止唯一被鉴定的主要循环代谢物。 生物半衰期 filgotinib 的半衰期估计为 7 小时,而其活性代谢物 GS-829845 的半衰期估计为 19 小时。 |
||
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概述 菲戈替尼尚未获得美国食品药品监督管理局 (FDA) 的批准。目前尚无关于菲戈替尼在哺乳期临床应用的信息。欧洲生产商建议在菲戈替尼治疗期间停止哺乳。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合率 菲戈替尼的蛋白结合率约为 55-59%,而其活性代谢物 GS-829845 的蛋白结合率为 39-44%。 |
||
| 参考文献 | |||
| 其他信息 |
药物适应症
类风湿性关节炎:Jyseleca适用于治疗对一种或多种改善病情抗风湿药(DMARDs)疗效不佳或不耐受的中重度活动性类风湿性关节炎成人患者。Jyseleca可作为单药治疗,也可与甲氨蝶呤(MTX)联合使用。溃疡性结肠炎:Jyseleca适用于治疗对传统疗法或生物制剂疗效不佳、疗效丧失或不耐受的中重度活动性溃疡性结肠炎成人患者。 |
| 分子式 |
C25H27N5O7S
|
|---|---|
| 分子量 |
541.5762
|
| 精确质量 |
541.163
|
| 元素分析 |
C, 55.44; H, 5.03; N, 12.93; O, 20.68; S, 5.92
|
| CAS号 |
1802998-75-9
|
| 相关CAS号 |
Filgotinib;1206161-97-8
|
| PubChem CID |
131801100
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
180
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
38
|
| 分子复杂度/Complexity |
834
|
| 定义原子立体中心数目 |
0
|
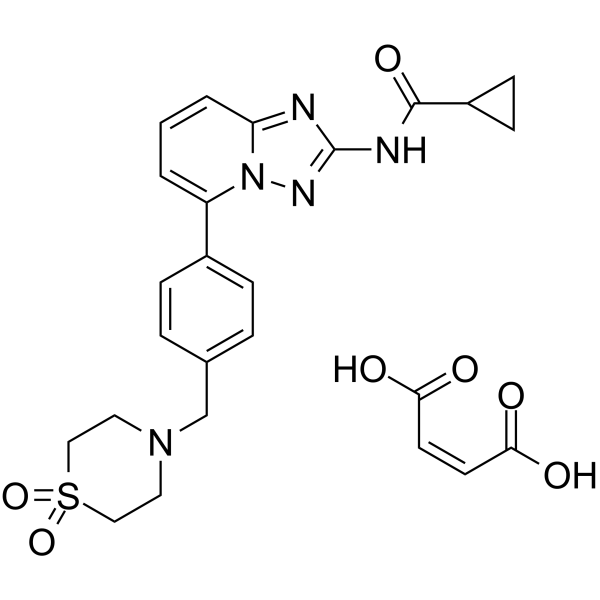
| SMILES |
C1CC1C(=O)NC2=NN3C(=N2)C=CC=C3C4=CC=C(C=C4)CN5CCS(=O)(=O)CC5.C(=C\C(=O)O)\C(=O)O
|
| InChi Key |
BFENHEAPFWQJFL-BTJKTKAUSA-N
|
| InChi Code |
InChI=1S/C21H23N5O3S.C4H4O4/c27-20(17-8-9-17)23-21-22-19-3-1-2-18(26(19)24-21)16-6-4-15(5-7-16)14-25-10-12-30(28,29)13-11-25;5-3(6)1-2-4(7)8/h1-7,17H,8-14H2,(H,23,24,27);1-2H,(H,5,6)(H,7,8)/b;2-1-
|
| 化学名 |
(Z)-but-2-enedioic acid;N-[5-[4-[(1,1-dioxo-1,4-thiazinan-4-yl)methyl]phenyl]-[1,2,4]triazolo[1,5-a]pyridin-2-yl]cyclopropanecarboxamide
|
| 别名 |
Filgotinib maleate; 1802998-75-9; Filgotinib (maleate); JG8OB4UL9Y; Filgotinib maleate [USAN]; GS-6034; (Z)-but-2-enedioic acid;N-[5-[4-[(1,1-dioxo-1,4-thiazinan-4-yl)methyl]phenyl]-[1,2,4]triazolo[1,5-a]pyridin-2-yl]cyclopropanecarboxamide; Cyclopropanecarboxamide, N-(5-(4-((1,1-dioxido-4-thiomorpholinyl)methyl)phenyl)(1,2,4)triazolo(1,5-a)pyridin-2-yl)-, (2Z)-2-butenedioate (1:1);
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8464 mL | 9.2322 mL | 18.4645 mL | |
| 5 mM | 0.3693 mL | 1.8464 mL | 3.6929 mL | |
| 10 mM | 0.1846 mL | 0.9232 mL | 1.8464 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05817942 | Recruiting | Drug: Filgotinib | Ulcerative Colitis | Galapagos NV | June 12, 2023 | |
| NCT05323591 | Recruiting | Drug: Filgotinib | Rheumatoid Arthritis | Galapagos NV | May 3, 2022 | |
| NCT04871919 | Recruiting | Drug: Filgotinib | Rheumatoid Arthritis | Galapagos NV | May 11, 2021 | |
| NCT05785611 | Recruiting | Drug: Filgotinib Drug: Placebo |
Axial Spondyloarthritis | Galapagos NV | April 5, 2023 | Phase 3 |