| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
FTase (farnesyl transferase)
|
||
|---|---|---|---|
| 体外研究 (In Vitro) |
当在辐射前用 FTI-277 (20 μM) 处理 48 小时时,表达 24-kDa 同工型 (HeLa 3A) 的放射抗性细胞的存活率显着下降;然而,这种治疗对对照细胞(HeLa PINA)的存活没有影响。除了减少两种细胞类型的 G(2)/M 期停滞并刺激 HeLa 3A 细胞有丝分裂后细胞死亡外,FTI-277 还具有放射增敏作用[1]。使用 GGTI-298 和 FTI-277 处理后,PC-3 细胞迁移和侵袭以时间和剂量依赖性方式减少[3]。
|
||
| 体内研究 (In Vivo) |
与单独使用载体相比,FTI-277疗法可抑制烧伤小鼠中 PTP-1B 和 PTEN 蛋白表达的升高。另一方面,在假烧伤动物中,FTI-277 对 PTP-1B 或 PTEN 蛋白表达没有明显影响 [2]。
与假烧伤相比,烧伤后3天,小鼠肌肉中的FTase表达和法尼酰化蛋白增加。同时,胰岛素刺激的胰岛素受体(IR)、胰岛素受体底物(IRS)-1、Akt和GSK-3β的磷酸化降低。烧伤后PTP-1B(IR-IRS-1信号传导的负调节因子)、PTEN(Akt介导的信号传导的阴性调节因子)的蛋白质表达、肌肉的蛋白质降解和乳酸释放以及血浆乳酸水平升高。烧伤引起的胰岛素信号传导受损和代谢功能障碍与炎症基因表达增加有关。这些烧伤引起的改变被FTI-277逆转或改善。[2] 结论:我们的数据表明,烧伤增加了小鼠骨骼肌中的FTase表达和蛋白法尼酰化,同时也增加了胰岛素抵抗、代谢改变和炎症反应,所有这些都可以通过FTI-277治疗来预防。这些结果表明,蛋白质法尼酰化的增加在烧伤诱导的代谢功能障碍和炎症反应中起着关键作用。我们的研究确定FTase是一种新的潜在分子靶点,可以逆转或改善烧伤患者的代谢紊乱。[2] |
||
| 酶活实验 |
FTI-277抑制病毒颗粒的产生。[4]
如上所述,从转染后的第一天开始,每天用含有0.2%二甲亚砜(DMSO)、400μM二硫苏糖醇(DTT)和不同浓度FTI-277的Huh7培养基替换培养基。在第10天,用1倍磷酸盐缓冲盐水(PBS)洗涤细胞数次,以去除DTT的痕迹,并通过XTT测定法测量其存活率,如别处所述。使用基于酶联免疫吸附试验的测定法测定培养基HBsAg浓度。然后按照制造商的说明,用1×PBS洗涤细胞两次,并刮入2ml Trizol试剂以纯化其RNA含量。将上清液低速预冷,装载在2毫升20%蔗糖的1×PBS缓冲垫上,在SW41Ti转子中以30000转/分的速度在4°C下超速离心15小时。去除上清液后,将沉淀物小心地重新悬浮在水中,并按照下文所述进行提取,以进行Northern分析。 |
||
| 细胞实验 |
在这篇论文中,描述了法尼基转移酶抑制剂(FTI-277)对表达野生型RAS的人细胞中由24 kDa FGF2亚型诱导的放射抗性的影响。在照射前用FTI-277(20微M)处理48小时导致表达24 kDa亚型的放射抗性细胞(HeLa 3A)的存活率显著降低,但对对照细胞(HeLa PINA)的存活没有影响。FTI-277的放射增敏作用伴随着HeLa 3A细胞有丝分裂后细胞死亡的刺激,以及两种细胞类型G(2)/M期阻滞的减少。这些结果清楚地表明,至少有一种法尼酰化蛋白参与了FGF2 24kDa亚型诱导的放射抗性的调节。此外,辐射诱导的G(2)/M相阻滞也受法尼酰化蛋白的控制。这项工作还表明,FTase抑制剂可能是某些具有野生型RAS的人类肿瘤的有效放射增敏剂。[1]
PC-3细胞的生长速度[3] 将细胞铺在24孔板中,3000个细胞/孔,并在含有iFBS(10%)的DMEM中培养24小时。用不同浓度的FTI-277、GGTI-298或NE-10790处理细胞24小时,用含有10%iFBS的DMEM洗涤,并在没有化合物的情况下再培养75小时。在处理前后用库尔特计数器计数细胞数量。 荧光染色[3] PC-3细胞在涂有Matrigel的盖玻片上用10μM GGTI-298、10μMFTI-277、1 mM NE-10790或含有1%BSA的DMEM(作为对照)预处理24小时。细胞用4%多聚甲醛固定,用0.5%Triton X-100渗透5分钟,用TRITC(异硫氰酸四甲基罗丹明)标记的鬼笔环肽(0.2μg/ml)染色20分钟,可染色F-actin。使用Hoechst 33342对DNA进行可视化。通过用0.1%BSA在PBS中固定和阻断细胞1小时,并用抗filin抗体再孵育1小时,进行cofilin的免疫染色。PBS洗涤后,将细胞与Alexa Fluor®488鸡抗abbit IgG(h+L)作为第二抗体孵育1 h。用PBS和H2O洗涤后,安装盖玻片,用蔡司LSM510 META共聚焦显微镜获取共聚焦图像。Hoechst 33342、Alexa Fluor®488和TRITC–phalloidin分别用405、488和543 nm激光线激发,并通过420–480、500–550 nm和560LP滤光片收集发射数据。 FRAP(光漂白后的荧光恢复)[3] 在玻璃底细胞培养皿中,使用3μg载体DNA和7μl TransFectin脂质试剂,用pEGFP-actin、pEGFP-cofilin或pEGFP-paxillin转染PC-3细胞。将细胞孵育5小时,然后更换培养基。将细胞再培养48小时以实现GFPs的表达。转染的细胞用DMEM+1%BSA(阴性对照)、10μMFTI-277、10μM GGTI-298或1 mM NE-10790处理。FRAP实验(Sprague和McNally,2005年综述)是在37°C、5%CO2的加湿室中,用蔡司LSM510 META共聚焦显微镜进行的。用488nm激光束激发瞬时表达EGFP-actin/paxillin/-cofilin 1的细胞,用500-550nm带通滤光片收集发射。在光漂白之前,收集了三张图像。选择ROI(感兴趣区域),并对其进行光漂白(488nm;100%强度)。每隔2秒进行一次恢复。计算了回收半衰期(t½)和流动分数(Mf)。数据通过FCalc®进行评估。简而言之,对采集的数据进行了光漂白引起的图像采集校正,并将得到的数据拟合到方程y=(1-exp(kt))中。 |
||
| 动物实验 |
|
||
| 参考文献 |
|
||
| 其他信息 |
甲羟戊酸合成途径产生小GTP酶异戊二烯化的中间体,这些小GTP酶参与肌动蛋白细胞骨架和细胞运动的调控。本研究探讨了异戊二烯化转移酶在调控PC-3前列腺癌细胞骨架组织和运动中的作用。我们使用了FTase(法尼基转移酶)、GGTase(牻牛儿基牻牛儿基转移酶)-I和-II的特异性抑制剂FTI-277、GGTI-298或NE-10790。用GGTI-298和FTI-277处理PC-3细胞后,细胞迁移和侵袭能力呈时间和剂量依赖性地受到抑制。这与F-肌动蛋白结构的破坏和GFP-肌动蛋白的恢复减少有关。免疫印迹分析显示,GGTI-298 和 FTI-277 处理的细胞中,最显著的变化是总 cofilin 和磷酸化 cofilin 水平显著降低,而 cofilin mRNA 水平并未降低。GGTI-298 处理 PC-3 细胞还影响了 GFP-paxillin 的动态变化,并降低了总 paxillin 和磷酸化 paxillin 的水平。GGTI-298 也降低了磷酸化 FAK(黏着斑激酶)和 PAK(p-21 相关激酶)-2 的水平,但 paxillin 或 FAK mRNA 的水平未受影响。此外,GGTI-298 对 MMP-9 的活性影响较小。RNAi 敲低 GGTase-Iβ 可抑制 PC-3 细胞的侵袭,破坏 F-肌动蛋白的组织结构,并降低 cofilin 的水平。 NE-10790 对 PC-3 前列腺癌细胞的运动性或细胞骨架的组织结构均无影响。总之,我们的结果表明 GGTase-I 和 FTase 催化的异戊二烯化反应参与调控前列腺癌细胞的细胞骨架完整性和运动性,并提示它们可能是开发前列腺癌转移抑制剂的潜在药物靶点。[3]
丁型肝炎病毒 (HDV) 是全球范围内引起急性和慢性肝病的主要病原体。目前尚缺乏有效的治疗方法。先前的研究表明,法尼基转移酶抑制剂 BZA-5B 可以抑制 HDV 病毒样颗粒 (VLP) 的组装。本文中,我们发现另一种法尼基转移酶抑制剂 FTI-277 可以阻止两种不同基因型的完整、具有感染性的 HDV 病毒颗粒的产生。因此,尽管与病毒样颗粒(VLP)相比,感染性HDV病毒颗粒的结构和组装决定因素更为复杂,但前者同样对药物性异戊二烯化抑制剂敏感。此外,与临床病情尤为严重的HDV III型病毒颗粒的产生,与HDV I型病毒颗粒一样,对异戊二烯化抑制剂同样敏感。因此,法尼基转移酶抑制剂是一类极具吸引力的新型抗病毒药物,可用于治疗HDV感染,包括与最严重疾病相关的基因型。[4] |
| 分子式 |
C₂₂H₂₉N₃O₃S₂
|
|---|---|
| 分子量 |
447.61
|
| 精确质量 |
447.165
|
| 元素分析 |
C, 59.03; H, 6.53; N, 9.39; O, 10.72; S, 14.32
|
| CAS号 |
170006-73-2
|
| 相关CAS号 |
FTI-277 hydrochloride;180977-34-8; 1217447-06-7 (TFA)
|
| PubChem CID |
3005532
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| LogP |
4.844
|
| tPSA |
194.85
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
12
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
532
|
| 定义原子立体中心数目 |
2
|
| SMILES |
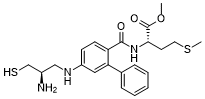
S(C([H])([H])[H])C([H])([H])C([H])([H])[C@@]([H])(C(=O)OC([H])([H])[H])N([H])C(C1C([H])=C([H])C(=C([H])C=1C1C([H])=C([H])C([H])=C([H])C=1[H])N([H])C([H])([H])[C@]([H])(C([H])([H])S[H])N([H])[H])=O
|
| InChi Key |
GKFPROVOIQKYTO-UZLBHIALSA-N
|
| InChi Code |
InChI=1S/C22H29N3O3S2/c1-28-22(27)20(10-11-30-2)25-21(26)18-9-8-17(24-13-16(23)14-29)12-19(18)15-6-4-3-5-7-15/h3-9,12,16,20,24,29H,10-11,13-14,23H2,1-2H3,(H,25,26)/t16-,20+/m1/s1
|
| 化学名 |
L-Methionine, N-((5-((2-amino-3-mercaptopropyl)amino)(1,1'-biphenyl)-2-yl)carbonyl)-, methyl ester, (R)-
|
| 别名 |
FTI277; methyl (2S)-2-[[4-[[(2R)-2-amino-3-sulfanylpropyl]amino]-2-phenylbenzoyl]amino]-4-methylsulfanylbutanoate; CID 3005532; CHEMBL135561; L-Methionine, N-((5-((2-amino-3-mercaptopropyl)amino)(1,1'-biphenyl)-2-yl)carbonyl)-, methyl ester, (R)-; GKFPROVOIQKYTO-UZLBHIALSA-N; SCHEMBL8365606; FTI-277; FTI 277
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2341 mL | 11.1704 mL | 22.3409 mL | |
| 5 mM | 0.4468 mL | 2.2341 mL | 4.4682 mL | |
| 10 mM | 0.2234 mL | 1.1170 mL | 2.2341 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。