| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25g |
|
||
| 50g |
|
||
| 100g |
|
||
| Other Sizes |
|

| 靶点 |
TGR5 (GPCR19); Microbial Metabolite; Human Endogenous Metabolite
|
|---|---|
| 体外研究 (In Vitro) |
猪去氧胆酸是由破坏菌群在小肠中形成的次级亲水性胆汁酸,作为TGR5的激动剂,在CHO细胞中的EC50为31.6 μM[1]。猪去氧胆酸(50,100 μM)增加参与RAW 264.7 细胞切除的基因 (Abca1、Abcg1 和 Apoe) 的表达[2]。
HDCA增加了RAW 264.7细胞中与胆固醇外流相关的基因的表达[2] 我们研究了HDCA是否影响巨噬细胞系RAW 264.7中胆固醇流出相关基因的表达。在我们的研究中,用于治疗RAW细胞的HDCA浓度为50和100μM,接近在饮食中补充1.25%HDCA的LDLRKO小鼠的循环HDCA水平(平均42.4μM,范围31-66μM)。HDCA处理以剂量反应的方式显著增加了RAW细胞中ATP结合盒亚家族A成员1(Abca1)、ATP结合盒子家族G成员1(Abcg1)和载脂蛋白E(Apoe)的表达。因此,与赋形剂治疗组相比,在50μM HDCA剂量下,Abca1、Abcg1和Apoe的表达分别显著增加了57%、54%和106%(图5E)。此外,与赋形剂治疗组相比,在100μM HDCA剂量下,Abca1、Abcg1和Apoe的表达分别显著增加了201%、112%和189%(图5E)。载体处理组和HDCA处理组之间Srb1的表达相似(图5E)。与对照组相比,在50和100μM剂量下,HDCA治疗使核受体Lxrα的表达适度增加了36%,但Lxrβ或过氧化物酶体增殖物激活受体γ1(Pparγ1)的表达没有增加(图5E)。 |
| 体内研究 (In Vivo) |
猪去氧胆酸 (HDCA;1.25% (wt/wt)) 在 LDLRKO 中明显减少脂肪量并增加瘦体重,但不会提高任何器官毒性标志物的血清水平。猪去氧胆酸在 LDLRKO 的多个部位阻断动脉粥样淋巴瘤病变的,改善便秘脂蛋白谱系,降低胆固醇水平并阻止胆固醇吸收效率,并通过粪便呼吸增加每日胆固醇排泄。猪去氧胆酸还可以改善HDL功能,这可通过胆固醇中断测定法来简单[2]。
研究了天然次生胆汁酸猪去氧胆酸(HDCA)对LDL受体缺失(LDLRKO)小鼠脂质代谢和动脉粥样硬化的影响。雌性LDLRKO小鼠在西方饮食中维持8周,然后分为2组,接受食物或食物+1.25%HDCA饮食15周。我们观察到,喂食HDCA饮食的小鼠更瘦,空腹血糖水平降低了37%(P<0.05)。与周粮组相比,补充HDCA显著降低了主动脉根部、整个主动脉和无名动脉的动脉粥样硬化病变大小,分别降低了44%(P<0.0001)、48%(P<0.01)和94%(P<0.01)。与周粮组相比,HDCA组血浆VLDL/IDL/LDL胆固醇水平显著降低了61%(P<0.05)。与食物组相比,补充HDCA使肠道胆固醇吸收降低了76%(P<0.0001)。此外,与饮食组的HDL相比,从HDCA组分离的HDL在体外介导胆固醇流出的能力显著增强。此外,HDCA显著增加了巨噬细胞系中与胆固醇流出相关的基因的表达,如Abca1、Abcg1和Apoe。因此,HDCA是抗动脉粥样硬化药物治疗的候选者[2]。 补充HDCA显著提高了循环中的HDCA水平,并没有影响小鼠的整体健康。 HDCA抑制LDLRKO多部位动脉粥样硬化病变的形成。 HDCA改善了血浆脂蛋白谱,降低了血糖水平。 补充HDCA会降低肠道胆固醇吸收效率,并通过粪便排出增加每日胆固醇排泄量。 HDCA对肝脏脂质含量、肝脏基因表达和胆汁成分的影响[2]。 |
| 细胞实验 |
细胞培养和处理条件[2]
RAW 264.7细胞是一种小鼠巨噬细胞系,在含有DMEM的生长培养基中培养,DMEM补充了10%FBS(Hyclone,South Logan,UT,USA)、100 U/ml青霉素和100μg/ml链霉素。治疗时,将RAW 264.7细胞铺在生长培养基中的6孔板(7.5×10−5个细胞/孔)中2天。用PBS洗涤后,将细胞在含有各种化学物质或二甲亚砜(DMSO)作为载体对照的治疗培养基(DMEM补充了1%FBS、100 U/ml青霉素和100μg/ml链霉素)中孵育24小时。然后用PBS洗涤细胞,然后如下所述分离总RNA。 胆固醇外排测定[2] 将RAW 264.7细胞铺在24孔板中(300000个细胞/孔)并生长1天。然后将每个孔中的细胞与1ml含有25μg/ml人乙酰化LDL和1μCi 3H-胆固醇/ml的生长培养基在CO2培养箱中孵育48小时。用PBS洗涤后,将细胞与DMEM+0.2%无脂肪酸的牛血清白蛋白一起孵育过夜。用PBS洗涤后,将细胞与0.5ml测试样品(DMEM中的小鼠HDL+0.2%BSA)在37°C下孵育4小时。然后,收集上清液,用0.1N NaOH裂解细胞。然后通过液体闪烁测量分别与上清液和细胞相关的放射性。 |
| 动物实验 |
小鼠:为进行动脉粥样硬化研究,对8周龄雌性LDLRKO小鼠喂食8周的西式饮食(21%脂肪,0.15%胆固醇;TD.88137)。为了测量无名动脉和主动脉根部的病变,此时处死一组小鼠(基线组)。基线组不研究累及整个主动脉的动脉粥样硬化病变。在处死前,将存活的小鼠分为两组,并分别喂食以下两种饮食,持续15周:第1组喂食含5%脂肪的普通饲料(AIN-76A啮齿动物饲料);第2组喂食添加1.25%(w/w)羟基胆酸的普通饲料。在其他研究中,8周龄的雌性LDLRKO小鼠在表型测量前3周分别喂食标准饲料或添加1.25%脱氧胆酸的标准饲料。每周记录食物摄入量和体重。使用Bruker Minispec软件和Eco Medical Systems软件,通过磁共振成像(MRI)测量动物的瘦体重和总体脂量[2]。
本研究使用了雌性LDLRKO小鼠。在动脉粥样硬化研究中,8周龄的雌性LDLRKO小鼠喂食高脂饮食(21%脂肪,0.15%胆固醇)8周。一组小鼠(基线组)在此时间点被安乐死,用于测量主动脉根部和无名动脉的病变。基线组未检查整个主动脉的动脉粥样硬化病变。剩余的小鼠随后被分为两组,并分别喂食以下饲料15周后处死:第1组,标准饲料(5%脂肪);第2组,标准饲料+1.25%(w/w)HDCA。在其他研究中,8周龄的雌性LDLRKO小鼠在表型测量前喂食标准饲料或标准饲料+1.25%HDCA 3周。本研究中使用的HDCA购自xxx。每周记录食物消耗量和体重。[2] 脂质、总胆汁酸、HDCA测定、血清生化检测、凝胶过滤色谱、二氯荧光素(DCF)测定和免疫印迹[2] 为了测定血浆脂质和脂蛋白水平,小鼠在采血前禁食16小时。采用酶比色法测定总胆固醇、高密度脂蛋白胆固醇、游离胆固醇、甘油三酯和游离脂肪酸水平。磷脂酰胆碱水平采用酶比色法测定。血浆样品按先前所述方法通过快速高效液相色谱(FPLC)进行分离。为测定高密度脂蛋白样品的脂质氧化程度,将2 μg高密度脂蛋白胆固醇溶于175 μl磷酸盐缓冲液(PBS)中,加入96孔板的每个孔中,并在37°C下孵育1小时。然后向每个孔中加入5 μg DCFH溶于25 μl PBS中,并在37°C下继续孵育1小时。然后使用酶标仪在激发波长485 nm和发射波长530 nm下测定DCF荧光强度,方法如前所述。对于免疫印迹分析,FPLC分离的组分或高密度脂蛋白样品通过SDS-PAGE进行分离;将蛋白转移至尼龙膜上;与兔抗小鼠载脂蛋白A1 (apoA1)、apo B-48/100或apoE抗体孵育;洗涤;与二抗孵育;并使用电化学发光法检测。总胆汁酸水平采用Diazyme Laboratories公司的试剂盒,按照制造商的说明书进行测定。为测定高密度脂蛋白(HDL)中的总胆汁酸水平,使用Amicon超滤离心管浓缩FPLC分离的HDL。将含有等量血浆HDL胆固醇的HDL样品与血浆样品(HDL制备的来源)一起测定,以比较总胆汁酸水平。血浆HDCA水平采用下述LC/MS/MS方法测定。标准品用甲醇:水(2:1)配制,HDCA浓度为1.00–1000 ng/ml。样品和标准品的提取采用蛋白质沉淀法,取100 μl样品或标准品,加入400 μl含内标d4-熊去氧胆酸(UDCA;100 ng/ml)的甲醇溶液。涡旋混匀后离心,取上清液400 μl,与400 μl水合并。HDCA在Supelco Ascentis Express C-18色谱柱(50×2.1 mm,2.7 μm)上分离,流速为0.200 ml/min,流动相为两种:一种是含0.1%氢氧化铵的10 mM乙酸铵水溶液(pH 9);另一种是含0.1%氢氧化铵的10 mM乙酸铵甲醇溶液。初始流动相为50% B,保持0.5 min;随后线性梯度洗脱至80% B,持续4 min;最后线性梯度洗脱至95% B,持续5 min。该流动相保持2分钟,随后重新平衡至50% B相,总运行时间为8分钟。洗脱液直接导入Sciex API5000质谱仪,通过MS/MS监测Q1和Q3通道中m/z 391.1的峰,并使用40 eV碰撞电压以降低背景干扰,检测HDCA。内标物在m/z 395.1处被检测到。HDCA在4.26分钟处洗脱,内标物在4.08分钟处被检测到。利用该系统,HDCA与同量异位素UDCA、脱氧胆酸(5.3分钟)和鹅脱氧胆酸(5.1分钟)实现了基线分离。 |
| 药代性质 (ADME/PK) |
代谢/代谢物
6α-羟基石胆酸是已知的石胆酸的人体代谢物。 |
| 参考文献 |
|
| 其他信息 |
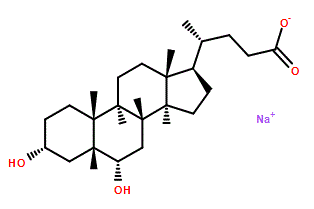
猪脱氧胆酸属于5β-胆烷酸类化合物,是(5β)-胆烷-24-酸在3位和6位被α-羟基取代的化合物。它既是人体的代谢产物,也是小鼠的代谢产物。它是一种胆汁酸,属于5β-胆烷酸类化合物,也是一种6α,20xi-鼠脱氧胆酸和C24甾体。它在功能上与胆酸相关。它是猪脱氧胆酸盐的共轭酸。
猪脱氧胆酸已被用于高胆固醇血症治疗的研究试验中。 TGR5是一种代谢型受体,它与腺苷酸环化酶的诱导存在G蛋白偶联,被认为是连接胆汁酸与能量和葡萄糖稳态调控的分子纽带。为了揭示该受体的新型选择性调节剂,并阐明TGR5激活的分子机制,我们在此报告了对一系列天然胆汁酸、胆汁酸衍生物和一些类固醇激素的生物学筛选,结果发现了新型高效选择性TGR5配体。我们利用这些化合物的生物学结果,扩展了TGR5激动剂的构效关系,并构建了TGR5活性的二元分类模型。该模型尤其能够揭示胆汁酸和类固醇激素分子结构中一些与TGR5激活相关的潜在特性,从而可用于设计新型高效选择性TGR5激动剂。[1] 研究表明,胆汁酸能够激活G蛋白偶联受体TGR5,从而增加能量消耗、减少肥胖并提高胰岛素敏感性。体外实验表明,HDCA能够激活TGR5,但不能激活FXR。我们发现,补充HDCA 15周后,小鼠肥胖程度降低(表2),且空腹血糖水平显著低于普通饲料组(表4)。已知糖异生基因Pepck和G6pase的表达可通过激活FXR,进而被TGR5和SHP抑制,而HDCA组的Pepck和G6pase表达水平显著低于普通饲料组(图4C)。由于HDCA组小鼠肝脏中Shp mRNA水平显著低于对照组,因此HDCA处理组小鼠Pepck和G6pase表达降低不太可能是FXR和SHP的作用所致。更可能的原因是HDCA激活了TGR5。与此一致,已知分别受FXR下调和上调的两个基因Cyp7a1和Bsep在肝脏中的表达不受HDCA补充的影响(图4C),表明HDCA并未激活小鼠肝脏中的FXR。在小肠中,HDCA也未显著增加或减少FXR靶基因Ostα、Ostβ和Mrp2的表达(图3C)。因此,我们的数据表明,HDCA在体内是TGR5的激动剂,而非FXR的激动剂。我们的数据不支持HDCA作为FXR拮抗剂的观点。 总之,我们的研究表明HDCA影响LDLRKO小鼠的胆固醇和葡萄糖稳态。HDCA补充抑制了肠道胆固醇的吸收,降低了血浆VLDL/IDL/LDL胆固醇水平,改善了HDL功能,并降低了小鼠的肥胖程度和血浆葡萄糖水平。 HDCA的降血糖和预防肥胖作用很可能是由于TGR5的激活所致。此外,HDCA不仅显著缩小了动脉粥样硬化病变的面积,还减少了病变内炎症成分、巨噬细胞的含量以及钙化的发生率。我们的研究结果表明,HDCA有望成为治疗肥胖、糖尿病和动脉粥样硬化的候选药物。[1] |
| 分子式 |
C24H40O4
|
|---|---|
| 分子量 |
392.58
|
| 精确质量 |
414.274
|
| 元素分析 |
C, 73.43; H, 10.27; O, 16.30
|
| CAS号 |
10421-49-5
|
| 相关CAS号 |
Hyodeoxycholic acid;83-49-8
|
| PubChem CID |
23720132
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| 沸点 |
547.1ºC at 760 mmHg
|
| 熔点 |
357-365°C
|
| 闪点 |
298.8ºC
|
| 蒸汽压 |
2.98E-14mmHg at 25°C
|
| 折射率 |
3.5 ° (C=2, H2O)
|
| LogP |
3.143
|
| tPSA |
80.59
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
29
|
| 分子复杂度/Complexity |
612
|
| 定义原子立体中心数目 |
10
|
| SMILES |
[Na+].O([H])[C@]1([H])C([H])([H])[C@@]2([H])[C@@]([H])(C([H])([H])C([H])([H])[C@@]3(C([H])([H])[H])[C@]([H])([C@@]([H])(C([H])([H])[H])C([H])([H])C([H])([H])C(=O)[O-])C([H])([H])C([H])([H])[C@@]32[H])[C@]2(C([H])([H])[H])C([H])([H])C([H])([H])[C@@]([H])(C([H])([H])[C@@]21[H])O[H]
|
| InChi Key |
DUYSCILLIVEITB-ADQIWYCWSA-M
|
| InChi Code |
InChI=1S/C24H40O4.Na/c1-14(4-7-22(27)28)17-5-6-18-16-13-21(26)20-12-15(25)8-10-24(20,3)19(16)9-11-23(17,18)2;/h14-21,25-26H,4-13H2,1-3H3,(H,27,28);/q;+1/p-1/t14-,15-,16+,17-,18+,19+,20+,21+,23-,24-;/m1./s1
|
| 化学名 |
sodium;(4R)-4-[(3R,5R,6S,8S,9S,10R,13R,14S,17R)-3,6-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthren-17-yl]pentanoate
|
| 别名 |
Sodium hyodeoxycholate; HDCA sodium; 10421-49-5; Sodium hyodeoxycholate; Sodium hyodesoxycholate; HBY71R8HO2; UNII-HBY71R8HO2; 5beta-Cholan-24-oic acid, 3alpha,6alpha-dihydroxy-, monosodium salt; Cholan-24-oic acid, 3,6-dihydroxy-, monosodium salt, (3alpha,5beta,6alpha)-; CHOLAN-24-OIC ACID, 3,6-DIHYDROXY-, SODIUM SALT (1:1), (3.ALPHA.,5.BETA.,6.ALPHA.)-; Hyodeoxycholic acid sodium salt
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5473 mL | 12.7363 mL | 25.4725 mL | |
| 5 mM | 0.5095 mL | 2.5473 mL | 5.0945 mL | |
| 10 mM | 0.2547 mL | 1.2736 mL | 2.5473 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。