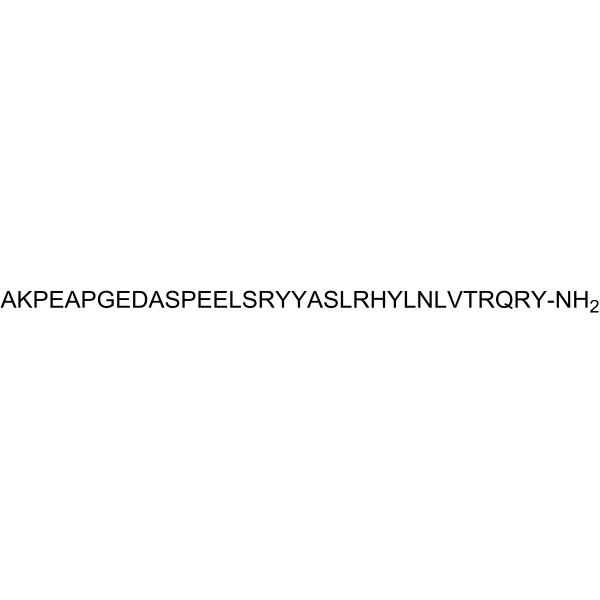
| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Y2 receptor (selective agonist) [1]
|
|---|---|
| 体外研究 (In Vitro) |
肽 YY (PYY) (3-36) 是一种猪 Y2 受体激动剂,由二肽基肽酶-IV (DPP-IV) 裂解 PYY1-36 N 末端的前两个氨基酸产生,可能会降低食物摄入量。 1]。
将 2 nmol 的 PYY(3-36) 与 200 ng 重组人脑啡肽酶 (NEP) 在 37°C 下孵育 60 分钟,导致 7 ± 1% 的降解。 [1] 将 2 nmol 的 PYY(3-36) 与 200 ng 重组人 meprin β 亚基在 37°C 下孵育 30 分钟,导致 53 ± 5% 的降解。 [1] 将 2 nmol 的 PYY(3-36) 与 1.25 mg/ml 的大鼠肾脏刷状缘 (KBB) 膜在 37°C 下孵育 30 分钟,导致约 82% 的降解。该降解作用具有剂量和时间依赖性。 [1] 质谱分析显示,meprin β 在多个位点切割 PYY(3-36):Glu10-Asp11、Asp11-Ala12 和 Ala12-Ser13,产生 PYY(11-36)、PYY(12-36) 和 PYY(13-36) 片段。 [1] KBB 膜在包括 Glu10-Asp11 和 Pro14-Glu15 的位点切割 PYY(3-36),产生 PYY(11-36) 和 PYY(15-36) 片段。 [1] NEP 抑制剂磷酰二肽 (phosphoramidon, 10 nmol) 使 NEP 诱导的 PYY(3-36) 降解减少了 95%。磷酰二肽 (100 nmol) 使 KBB 诱导的降解减少了 36%。 [1] Meprin 抑制剂 actinonin (10 nmol) 使 meprin β 诱导的 PYY(3-36) 降解减少了 96%。Actinonin (100 nmol) 完全阻止了 KBB 诱导的 PYY(3-36) 降解。 [1] |
| 体内研究 (In Vivo) |
与单独使用 PYY3-36 治疗相比,放线菌素显着延长了 PYY3-36 对小鼠厌食作用的持续时间 (50 nmol/kg),并保持了更高的 PYY3-36 血浆水平 [1]。
在禁食过夜的雄性 C57/BL6 小鼠中,单次皮下注射 PYY(3-36) (50 nmol/kg) 与生理盐水对照相比,在注射后 0-1 小时和 1-2 小时显著减少了摄食量。 [1] 当与 meprin 抑制剂 actinonin (20 mg/kg,腹腔注射预处理) 共同给药时,PYY(3-36) (50 nmol/kg) 不仅在注射后 0-1 小时和 1-2 小时,而且在 2-3 小时和 2-4 小时也显著减少了摄食量,延长了其厌食效应。 [1] 在注射后 0-6 小时内,PYY(3-36) (50 nmol/kg) 单独给药显著减少了累积摄食量。当与 actinonin (40 mg/kg) 共同给药时,减少程度显著更大。 [1] 在黑暗期自由摄食的小鼠中,较低剂量的 PYY(3-36) (5 nmol/kg,皮下注射) 与 actinonin (40 mg/kg,腹腔注射) 共同给药,在注射后 0-1 小时显著减少了摄食量。 [1] 在同一黑暗期摄食模型中,PYY(3-36) (5 nmol/kg,皮下注射) 与 NEP 抑制剂磷酰二肽 (phosphoramidon, 0.75 mg/kg,腹腔注射) 共同给药,显著减少了注射后 0-4 小时的累积摄食量。 [1] 在禁食小鼠皮下注射 PYY(3-36) (50 nmol/kg) 后测量血浆 PYY 免疫反应性 (PYY-IR) 水平。与单独使用 PYY(3-36) 相比,与 actinonin (20 mg/kg,腹腔注射) 共同给药导致注射后 20 分钟和 60 分钟的循环 PYY-IR 水平显著更高。 [1] |
| 酶活实验 |
重组酶降解实验: 将 2 nmol 的 PYY(3-36) 与或不与 200 ng 重组人 NEP 或 200 ng 重组人 meprin β 亚基在消化缓冲液 (50 mmol/L Tris-HCl, 50 mmol/L NaCl, pH 7.5) 中,总体积 120 µL,于 37°C 下孵育。在抑制剂研究中,反应混合物中包含 10 nmol 的磷酰二肽 (NEP 抑制剂) 或 actinonin (meprin 抑制剂)。反应在指定时间点通过加入 10 µL 10% 三氟乙酸终止。样品离心后,上清液通过反相 HPLC 和 MALDI-ToF 质谱分析,以定量降解并鉴定切割产物。 [1]
肾脏刷状缘膜降解实验: 通过匀浆和离心制备大鼠肾脏刷状缘 (KBB) 膜。将 2 nmol 的 PYY(3-36) 与 KBB 膜(终浓度 1.25 mg/mL)在消化缓冲液 (300 mmol/L 甘露醇,溶于 12 mmol/L HEPES,pH 7.4) 中于 37°C 孵育 30 分钟。在抑制剂研究中,加入 100 nmol 的磷酰二肽或 actinonin。孵育后,样品离心,上清液通过 HPLC 和质谱分析。 [1] |
| 动物实验 |
磷酰胺酮对禁食小鼠厌食作用的影响:成年雄性C57/BL6小鼠(20-25 g)禁食过夜。随后将其分为四组,分别进行皮下注射(最大注射量100 µL):1)生理盐水组(n=10),2)磷酰胺酮组(10 mg/kg)(n=10),3)PYY(3-36)组(50 nmol/kg,溶于生理盐水)(n=10),4)PYY(3-36)组(50 nmol/kg)+磷酰胺酮组(10 mg/kg)。在指定时间间隔内测量小鼠体重和食物摄入量,持续24小时。[1]
放线菌素对禁食小鼠厌食作用的影响:禁食过夜的小鼠被分为六组。首先,他们接受腹腔注射(最大体积 100 µL)赋形剂(20% 乙醇,80% 生理盐水)或放线菌素(20 或 40 mg/kg,溶于赋形剂)。15 分钟后,他们接受皮下注射(最大体积 100 µL)生理盐水或 PYY(3-36)(50 nmol/kg,溶于生理盐水)。分组:1) 载体腹腔注射 + 生理盐水皮下注射 (n=11),2) 放线菌素 (20 mg/kg) 腹腔注射 + 生理盐水皮下注射 (n=10),3) 放线菌素 (40 mg/kg) 腹腔注射 + 生理盐水皮下注射 (n=9),4) 载体腹腔注射 + PYY(3-36) 皮下注射 (n=9),5) 放线菌素 (20 mg/kg) 腹腔注射 + PYY(3-36) 皮下注射 (n=9),6) 放线菌素 (40 mg/kg) 腹腔注射 + PYY(3-36) 皮下注射 (n=8)。监测食物摄入量和体重。[1] 抑制剂对黑暗期进食小鼠的影响:在小鼠的黑暗期(活跃期)对其进行研究,小鼠可自由摄食。受试者被分为六组,分别接受以下注射:1)腹腔注射赋形剂+皮下注射生理盐水(n=8),2)腹腔注射赋形剂+皮下注射PYY(3-36)(5 nmol/kg)(n=8),3)腹腔注射磷酰胺酮(0.75 mg/kg,溶于赋形剂)+皮下注射PYY(3-36)(5 nmol/kg)(n=8),4)腹腔注射磷酰胺酮+皮下注射生理盐水(n=8),5)腹腔注射放线菌素(40 mg/kg,溶于赋形剂)+皮下注射PYY(3-36)(5 nmol/kg)(n=8),6)腹腔注射放线菌素+皮下注射生理盐水(n=8)。测量食物摄入量。 [1] 放线菌素药代动力学研究:禁食过夜的小鼠被分为三组,分别接受:1)放线菌素(20 mg/kg,腹腔注射)+生理盐水(皮下注射);2)赋形剂(腹腔注射)+ PYY(3-36)(50 nmol/kg,皮下注射);3)放线菌素(20 mg/kg,腹腔注射)+ PYY(3-36)(50 nmol/kg,皮下注射)。分别在皮下注射后20、60和90分钟处死小鼠。通过心脏穿刺采集血液,分离血浆,并用放射免疫分析法测定PYY免疫反应性水平。[1] |
| 药代性质 (ADME/PK) |
PYY(3-36) 在体外可被金属内肽酶 meprin β 迅速降解,其次可被脑啡肽酶 (NEP) 降解。[1]
在体内,小鼠皮下注射 PYY(3-36) (50 nmol/kg) 后,血浆中 PYY 免疫反应性水平先达到峰值,然后下降。与单独注射 PYY(3-36) 相比,同时注射 meprin 抑制剂放线菌素 (20 mg/kg) 可显著提高注射后 20 分钟和 60 分钟的血浆 PYY 免疫反应性水平,表明抑制降解可延长循环水平。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
文献指出,超生理水平的PYY(3-36)可导致人类出现恶心症状。[1]
|
| 参考文献 | |
| 其他信息 |
肽YY(3-36)是一种合成的人源肽YY 3-36,目前正在评估其治疗肥胖症的疗效。它能降低肥胖患者的食欲并增加饱腹感。
药物适应症 已研究用于代谢性疾病和肥胖症的治疗。 作用机制 PYY 3-36通过下丘脑弓状核(ARC)的突触前Y2受体发挥作用。它能减少静止下丘脑外植体中神经肽Y(NPY)的释放,从而减少食物摄入。 PYY(3-36)是一种由36个氨基酸组成的肠道激素,餐后由远端肠道的L细胞释放。它是由PYY(1-36)经二肽基肽酶-IV (DPP-IV)切割前两个N端氨基酸而生成的。 [1] PYY 是一种选择性 Y2 受体激动剂,可通过中枢 Y2 受体减少食物摄入。[1] 肥胖人群对其厌食作用敏感,但餐后 PYY 水平升高幅度较小。减肥手术可提高循环中 PYY 的水平。[1] 由于其循环半衰期短,因此作为抗肥胖疗法的应用受到限制。[1] 该研究表明,抑制其被 meprin β 降解(例如使用放线菌素等抑制剂)或设计对 meprin 裂解具有抗性的类似物可能是开发抗肥胖疗法的有效策略。[1] |
| 分子式 |
C176H272N52O54
|
|---|---|
| 分子量 |
3980.35891914368
|
| 精确质量 |
3979.017
|
| CAS号 |
126339-09-1
|
| 相关CAS号 |
Peptide YY (PYY) (3-36), porcine TFA
|
| PubChem CID |
90479816
|
| 外观&性状 |
Solid powder
|
| LogP |
-15.7
|
| tPSA |
1740
|
| 氢键供体(HBD)数目 |
61
|
| 氢键受体(HBA)数目 |
61
|
| 可旋转键数目(RBC) |
130
|
| 重原子数目 |
282
|
| 分子复杂度/Complexity |
9680
|
| 定义原子立体中心数目 |
34
|
| SMILES |
O=C([C@H](CCCCN)NC([C@H](C)N)=O)N1CCC[C@H]1C(N[C@H](C(N[C@@H](C)C(N1CCC[C@H]1C(NCC(N[C@H](C(N[C@@H](CC(=O)O)C(N[C@@H](C)C(N[C@@H](CO)C(N1CCC[C@H]1C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@@H](C)C(N[C@@H](CO)C(N[C@H](C(N[C@H](C(N[C@@H](CC1=CNC=N1)C(N[C@@H](CC1C=CC(=CC=1)O)C(N[C@H](C(N[C@@H](CC(N)=O)C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N[C@H](C(N)=O)CC1C=CC(=CC=1)O)=O)CCCNC(=N)N)=O)CCC(N)=O)=O)CCCNC(=N)N)=O)[C@@H](C)O)=O)C(C)C)=O)CC(C)C)=O)=O)CC(C)C)=O)=O)=O)CCCNC(=N)N)=O)CC(C)C)=O)=O)=O)CC1C=CC(=CC=1)O)=O)CC1C=CC(=CC=1)O)=O)CCCNC(=N)N)=O)CO)=O)CC(C)C)=O)CCC(=O)O)=O)CCC(=O)O)=O)=O)=O)=O)=O)CCC(=O)O)=O)=O)=O)=O)CCC(=O)O)=O
|
| InChi Key |
AIYOBVCUSVSXOL-NYGOYQSZSA-N
|
| InChi Code |
InChI=1S/C176H272N52O54/c1-84(2)67-114(155(265)202-104(27-19-61-192-174(184)185)148(258)218-121(75-98-78-190-83-196-98)160(270)217-120(74-97-39-47-102(236)48-40-97)158(268)212-115(68-85(3)4)156(266)219-122(76-131(180)238)161(271)213-117(70-87(7)8)162(272)224-138(88(9)10)168(278)225-139(93(15)232)169(279)208-106(29-21-63-194-176(188)189)145(255)204-108(49-54-130(179)237)150(260)201-103(26-18-60-191-173(182)183)146(256)210-113(140(181)250)71-94-33-41-99(233)42-34-94)214-164(274)124(80-229)221-142(252)90(12)197-153(263)118(72-95-35-43-100(234)44-36-95)216-159(269)119(73-96-37-45-101(235)46-38-96)215-147(257)105(28-20-62-193-175(186)187)203-163(273)125(81-230)222-157(267)116(69-86(5)6)211-152(262)110(52-57-135(244)245)205-151(261)111(53-58-136(246)247)207-167(277)129-32-24-66-228(129)172(282)126(82-231)223-143(253)91(13)198-154(264)123(77-137(248)249)220-149(259)107(50-55-133(240)241)200-132(239)79-195-165(275)127-30-22-64-226(127)170(280)92(14)199-144(254)109(51-56-134(242)243)206-166(276)128-31-23-65-227(128)171(281)112(25-16-17-59-177)209-141(251)89(11)178/h33-48,78,83-93,103-129,138-139,229-236H,16-32,49-77,79-82,177-178H2,1-15H3,(H2,179,237)(H2,180,238)(H2,181,250)(H,190,196)(H,195,275)(H,197,263)(H,198,264)(H,199,254)(H,200,239)(H,201,260)(H,202,265)(H,203,273)(H,204,255)(H,205,261)(H,206,276)(H,207,277)(H,208,279)(H,209,251)(H,210,256)(H,211,262)(H,212,268)(H,213,271)(H,214,274)(H,215,257)(H,216,269)(H,217,270)(H,218,258)(H,219,266)(H,220,259)(H,221,252)(H,222,267)(H,223,253)(H,224,272)(H,225,278)(H,240,241)(H,242,243)(H,244,245)(H,246,247)(H,248,249)(H4,182,183,191)(H4,184,185,192)(H4,186,187,193)(H4,188,189,194)/t89-,90-,91-,92-,93+,103-,104-,105-,106-,107-,108-,109-,110-,111-,112-,113-,114-,115-,116-,117-,118-,119-,120-,121-,122-,123-,124-,125-,126-,127-,128-,129-,138-,139-/m0/s1
|
| 化学名 |
(4S)-5-[[(2S)-1-[[(2S)-1-[[(2S)-1-[(2S)-2-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S)-1-[[(2S)-1-[[(2S,3R)-1-[[(2S)-1-[[(2S)-5-amino-1-[[(2S)-1-[[(2S)-1-amino-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-1,5-dioxopentan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-(1H-imidazol-4-yl)-1-oxopropan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-hydroxy-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-3-hydroxy-1-oxopropan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-4-carboxy-1-oxobutan-2-yl]amino]-4-carboxy-1-oxobutan-2-yl]carbamoyl]pyrrolidin-1-yl]-3-hydroxy-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-3-carboxy-1-oxopropan-2-yl]amino]-4-[[2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-2-aminopropanoyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-4-carboxybutanoyl]amino]propanoyl]pyrrolidine-2-carbonyl]amino]acetyl]amino]-5-oxopentanoic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.2512 mL | 1.2562 mL | 2.5123 mL | |
| 5 mM | 0.0502 mL | 0.2512 mL | 0.5025 mL | |
| 10 mM | 0.0251 mL | 0.1256 mL | 0.2512 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。