| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
PKA
|
|---|---|
| 体外研究 (In Vitro) |
Rp-8-Br-cAMPS (1 mM; 4-6 小时) 可以完全阻断 2-氯腺苷抑制 LAK 细胞毒性的能力,并显著减轻 2-氯腺苷对细胞因子产生的抑制作用 [1]。Rp-8-Br-cAMPS (50-100 μM; 2 分钟) 抑制 832/13 细胞 (源自 INS-1 细胞) 中的胰岛素分泌 [2]。
在2型糖尿病中,β细胞对葡萄糖无反应,导致高血糖。为了解决这个问题,我们最近从INS-1胰岛素瘤系中创建了克隆的胰岛素生产细胞系,其葡萄糖反应性从差到强不等。在这里,通过功能性比较葡萄糖反应性832/13β细胞和葡萄糖无反应性832/2β细胞,确定了决定分泌性能的机制。因此,832/13细胞的胰岛素分泌对葡萄糖的反应最大增加了8倍,而832/2细胞的反应仅为1.5倍。两个品系的胰岛素含量相似,表明刺激-分泌耦合的差异是导致分泌性能差异的原因。毛喉素或异丁基甲基黄嘌呤显著增强了832/13细胞的胰岛素分泌,但没有增强832/2细胞的分泌,这表明cAMP对于增强832/13电池的分泌性能至关重要。事实上,蛋白激酶A(PKA)抑制剂8-溴腺苷-3',5'-环单硫代磷酸酯,rp异构体(rp-8-Br-cAMPS)在有或没有福司克林的情况下,抑制了葡萄糖对胰岛素分泌的反应。有趣的是,虽然毛喉素显著增加了832/2细胞中的cAMP,但832/13细胞中cAMP仅略有上升。这表明832/13细胞对cAMP更敏感。事实上,贴片钳夹832/13细胞中cAMP诱导的外切细胞反应是832/2细胞的2倍。此外,免疫印迹显示,832/13细胞中PKA催化亚基的表达高出2倍。此外,当PKA的调节亚基在832/13细胞中过表达时,为了降低未结合和催化活性激酶的水平,胰岛素分泌和PKA活性会减弱。我们的研究结果表明,cAMP-PKA信号传导与β细胞的分泌性能相关。[2] 当832/13细胞被15 mM葡萄糖刺激时,Rp-8-Br-cAMPS抑制分泌21%(P<0.01;图3C);当细胞被毛喉素和葡萄糖刺激时,高浓度的Rp-8-Br-cAMPS完全阻断了毛喉素的增强作用(P<0.001;图3C)。在832/2细胞中,无论是否存在福司柯林,Rp-8-Br-cAMPS浓度均未对胰岛素分泌产生显著影响[2]。 |
| 体内研究 (In Vivo) |
Rp-8-Br-cAMPS(1mg;腹腔注射;10天)可以提高小鼠逆转录病毒感染模型中的小鼠免疫功能[3]。
进行了初步实验以评估Rp-8-Br-cAMPS的生物分布。通过HPLC在植入渗透泵的动物的肝脏、脾脏和血浆上测量化合物的浓度,渗透泵设置为每24小时输送0.7mg Rp-8-Br-cAMPS。如表1所示,在所有分析的器官中发现Rp-8-Br-cAMPS的浓度很高,表明该化合物已被递送到脾脏等相关组织。还评估了Rp-8-Br-cAMPS的毒性,如表2所示,研究期间没有意外死亡。此外,在不同实验的整个给药过程中,小鼠没有观察到临床症状(表2)。所有动物都被认为在研究中实现了令人满意的体重增加。动物处死时的肉眼检查没有发现任何异常。因此,我们得出结论,Rp8-Br-cAMPS在对照组非感染动物和感染小鼠中具有良好的耐受性。在接下来的10天内反复注射Rp-8-Br-cAMPS的实验中,我们评估了该化合物对已确诊RadLV Rs感染的小鼠的影响。通常,每个实验包括四组七到十只小鼠(两组小鼠在八周前接种了RadLV Rs,两组为年龄匹配的假注射对照组)。用Rp-8-Br-cAMPS治疗小鼠10天(每天腹腔注射1mg/只小鼠),或用300μl PBS进行等效假注射。在10天注射期结束时,处死小鼠。用Rp-8-Br-cAMPS治疗对RadLV Rs逆转录病毒感染的典型淋巴结病和脾肿大的程度没有显著影响。事实上,用Rp-8-Br-cAMPS治疗的感染小鼠和接受PBS的感染小鼠的淋巴器官重量总是相似的(图1)。两组的大小和细胞数也相似(数据未显示)。在从不同实验组的每只小鼠的外周淋巴结制备细胞悬液后,我们测量了对可溶性抗CD3单克隆抗体的增殖反应。在抗CD3单克隆抗体(2C11:4μg/ml)存在下培养细胞72小时。在72小时的培养期内,将Rp-8-Br-cAMPS(1 mM)加入到用该化合物处理的小鼠分离的细胞中。给予Rp-8-Br-cAMPS对非感染小鼠对抗CD3单克隆抗体的反应没有影响(未显示)。正如预期的那样,在RadLV Rs逆转录病毒感染的小鼠中,对抗CD3单克隆抗体的增殖反应几乎被消除,刺激指数(定义为刺激/非刺激CPM)通常约为正常小鼠细胞达到的值的10%(图2)。用Rp-8-BrcAMPS治疗未感染的小鼠没有显著改变其对抗CD3单克隆抗体的增殖反应(未显示)。相比之下,对RadLV Rs感染的小鼠腹腔注射PKA i型抑制剂Rp-8-Br-cAMPS显著增加了它们对抗CD3单克隆抗体的反应(31.97±4.21 n=10 vs 5.979±0.882 n=8,p<0.0001)。事实上,在大多数实验中,刺激指标值达到了对照值的50%以上(图2)。当感染和治疗的小鼠的细胞在缺乏Rp-8-Br-cAMPS的情况下在体外被激活时,治疗的效果部分丧失,在某些实验中变得不显著(未显示)。当来自未经治疗的逆转录病毒感染小鼠的细胞在体外与Rp-8-Br-cAMPS一起孵育时,T细胞反应也发生了显著改善(12.45±2.02 n=8 vs 5.98±0.88 n=8)(p=0.013),如我们之前的研究所示,但刺激指数仍然远低于用IP注射该化合物治疗的感染小鼠的刺激指数(p=0.0014),这表明PKA I型抑制对感染小鼠增殖反应恢复的体内影响。[3] 尽管MAIDS具有特定的病毒学特征,并且RadLV Rs对B细胞而非CD4 T细胞具有优先取向,但MAIDS与HIV感染具有惊人的相似性,例如涉及CD4和CD8 T细胞的多克隆和持续免疫激活,并导致T细胞反应受损。事实上,最近的证据表明,异常的免疫激活而不是HIV的直接细胞病变效应在HIV感染的发病机制中起着重要作用,至少在早期阶段是这样。PGE2-cAMP-PKA I型通路最有可能参与这种异常激活,如塞来昔布治疗的HIV感染患者中活化的CD8 CD38 T细胞减少所示,以及体外数据显示与Rp-8-BrcAMPS孵育后T细胞反应部分恢复所示。尽管COX-2在HIV感染中确实过表达,但其他可溶性因子可能在腺苷酸环化酶的激活中发挥作用。CCR5在HIV感染的发病机制中起着至关重要的作用,这可能部分独立于其作为HIV进入辅助受体的功能。有趣的是,CCR5和CXCR4等HIV辅助受体与G蛋白偶联,配体结合激活腺苷酸环化酶。因此,Gp120与其共受体的结合可以通过PGE2非依赖性机制直接增加cAMP浓度。因此,设计作用于腺苷酸环化酶激活下游的药理学方法非常重要[3]。 |
| 酶活实验 |
PKA活性[2]
如上所述,用等滴度的AdCMV PKAreg或AdCMV-βGal感染RPMI-1640培养基中保存的12孔培养皿中的汇合832/13细胞。移除培养基,用HBSS-3 mM葡萄糖洗涤细胞,随后在含有15 mM葡萄糖和2.5μM毛喉素的HBSS中孵育10分钟。然后,将细胞在冰冷的PBS中洗涤一次,并置于冰上,加入150μl匀浆缓冲液[50 mM N-[三羟甲基]-2-氨基乙烷磺酸(TES),1 mM EDTA,0.1 mM EGTA,250μM蔗糖;加入含有蛋白酶抑制剂(1μg/ml pepstatin、10μg/ml leupeptin、1μg/ml antipain)、磷酸酶抑制剂(0.1μM冈田酸)和磷酸二酯酶抑制剂(1.67mM IBMX)的pH 7.4。通过注射器抽吸细胞五次,然后在4℃下以5000 rpm离心10分钟来制备匀浆。允许10-μl匀浆等分试样中的PKA在39 mM TES、0.5 M蔗糖、0.1 M MgSO4、10 mM二硫代赤藓醇、0.4 mM ATP(pH 7.4)和15μCi[γ32P]ATP的混合物中磷酸化合成肽底物(13μg Kemptide);在有或没有蛋白激酶抑制剂(17μM)的情况下,在30℃下进行两次反应。30分钟后,通过加入10μl 1%BSA-1 mM ATP和10μl 12.5%三氯乙酸终止反应,随后在冰上放置10分钟。将反应混合物在3000 rpm下离心3分钟,然后将10μl匀浆转移到Whatman P81膜上。将膜在H3PO4中洗涤三次,在丙酮中洗涤一次。通过闪烁计数测定活性。PKA活性是通过减去添加了蛋白激酶抑制剂的反应中的活性来计算的。在每个实验中,PKA活性以对照组的百分比表示。 |
| 细胞实验 |
胰岛素分泌研究[2]
为了测定胰岛素分泌,将细胞在24孔培养皿中生长至汇合,并在测定前18小时将培养基中的葡萄糖浓度切换至5mM。当进行测定时,将细胞在37℃下在补充有3 mM葡萄糖的HEPES平衡盐溶液(HBSS;114 mM NaCl;4.7 mM KCl;1.2 mM KH2PO4;1.16 mM MgSO4;20 mM HEPES;2.5 mM CaCl2;25.5 mM NaHCO3;0.2%BSA,pH 7.2)中洗涤2小时。然后通过在含有图例中所示葡萄糖浓度的0.8 ml HBSS中静态孵育细胞1小时来测量胰岛素分泌。当检查KATP非依赖性葡萄糖传感时,静态培养期间HBSS中的K+浓度增加到35 mM,而Na+浓度降低到89.8 mM,并加入250μM二氮氧化物。胰岛素由Coat-a-Count试剂盒(DPC)测量,该试剂盒可识别人胰岛素,并与大鼠胰岛素发生约20%的交叉反应。在酸乙醇提取激素后测定细胞的胰岛素含量。 蛋白质印迹分析[2] 细胞在0.25M蔗糖中均质化;1mM EDTA,pH 7.0;1 mM二硫代赤藓醇(DTE);20μg/ml亮肽;20μg/ml抗癫痫药;在4℃下以110000×g离心45分钟制备细胞质组分。蛋白质通过SDS-PAGE解析并电印迹到硝化纤维膜上。使用多克隆兔抗人PKAcat或PKAreg抗体(分别为sc-903和sc-907)通过增强化学发光系统进行蛋白质印迹分析。在定量实验中,将来自每个细胞系的5μg蛋白质(由BCA蛋白质检测试剂盒测定;Pierce)装载到凝胶上。通过蛋白质印迹的密度分析确定表达(每条线n=5)。 cAMP的测定[2] 为了测定cAMP的积累,如上所述,将细胞在完全RPMI-1640培养基中的12孔培养皿中生长至融合。然后将细胞在含有5 mM葡萄糖的RPMI-1640培养基中保存12小时,然后在补充了3 mM葡萄糖的HBSS中孵育2小时。在切换到含有3或15 mM葡萄糖(含或不含2.5μM毛喉素)的HBSS两分钟后,通过向细胞中加入0.5 ml 80%乙醇从细胞中提取cAMP。通过RIA测定细胞提取物离心后的cAMP水平。 |
| 动物实验 |
动物/疾病模型: 小鼠白血病逆转录病毒 RadLV-Rs 处理的雄性 C57BL/6 小鼠[3]
剂量: 1 mg 给药途径: 腹腔注射 (ip);10 天 实验结果: 对 RadLV-Rs 逆转录病毒感染的典型淋巴结肿大和脾肿大程度没有显著影响。对 CD3 抗体的免疫应答显著增强。T 细胞应答得到改善。 雄性 C57BL/6 小鼠由本实验室饲养。小鼠在 4 周龄和 5 周龄时,腹腔注射 (ip) 两次,每次注射 0.25 ml 无细胞病毒提取物。同龄对照组小鼠腹腔注射两次,每次注射 0.25 ml 磷酸盐缓冲液 (PBS)。感染后不同时间点,用二氧化碳窒息法处死小鼠。将外周淋巴结(腹股沟、腋窝和颈部)用注射器抽吸,制成单细胞悬液,并通过尼龙细胞筛过滤,用完全RPMI 1640培养基洗涤三次,经台盼蓝染色排除后,在Thoma流式细胞仪上进行计数,之后进行进一步分析或细胞培养。在体内实验中,将Rp-8-Br-cAMPS 1 mg qd 腹腔注射到小鼠体内,持续10天。在旨在评估Rp-8-Br-cAMPS生物分布的初步实验中,将感染组和健康组小鼠皮下植入装有10 mg Rp-8-Br-cAMPS(溶于PBS)的Alzet渗透泵,设定24小时释放0.7 mg。在处死前14天植入渗透泵。 [3] Rp-8-Br-cAMPS浓度的定量测定 本研究开发了适用于定量测定小鼠组织和血清样本中Rp-8-Br-cAMPS浓度的样品前处理和高效液相色谱(HPLC)方法,可用于评估体内实验中的药物浓度。使用Rp-8-Br-cAMPS和8-Br-cAMP进行校准。两种化合物在0 ng/ml至1000 ng/ml范围内均具有良好的线性关系。将每份小鼠样本转移至硼硅酸盐微型研钵(1000×1000 L)中,然后加入250×1000 L水。手动均质后,再加入750×1000 L水,将所得悬浮液转移至1.5 mL带螺旋盖的Sarstedt管中。所有样品在-70℃下至少4小时后,置于Speed-Vac真空冷冻干燥机中,在油泵真空下冷冻干燥过夜。将冷冻干燥后的样品悬浮于1000 μL甲醇/水(1:1,v/v)混合溶液中,置于超声波浴中处理15分钟,然后以13000 rpm离心15分钟。取0.85 mL上清液上样至阴离子交换固相萃取柱(Chromafix 400 mg SB/货号:731835/Machery-Nagel),用2 mL水洗涤两次,然后用1 mL 0.6 M NaCl溶液洗脱。所得溶液直接用于高效液相色谱(HPLC)分析。为确保完全上样,将300 μL溶质上样至200 μL进样环中。该体积的溶质在 HPLC 方法校准过程中产生了可重复的数据 [3]。 |
| 参考文献 |
|
| 其他信息 |
腺苷抑制多种细胞因子/趋化因子的产生,并抑制经IL-2或Ly49D、NKp46受体交联激活的小鼠和人NK细胞的细胞毒活性。这些作用是通过A2A型腺苷受体介导的,其机制包括刺激腺苷酸环化酶、增加cAMP的产生以及激活PKA。PKA I而非PKA II参与腺苷的抑制作用。阻断PKA I的调节亚基(而非催化亚基)可消除腺苷的抑制作用。这些发现表明,肿瘤产生的腺苷抑制NK细胞和其他效应细胞的活性,从而保护肿瘤免受免疫介导的破坏。 [1]
鼠艾滋病(MAIDS)是由鼠白血病逆转录病毒RadLV-Rs感染引起的,其特征是T细胞无反应性和严重的免疫缺陷,并伴有对多种实验性机会性感染的易感性增加,这与HIV感染的情况类似。T细胞无反应性与细胞内cAMP水平升高有关,cAMP水平升高会触发一个多步骤通路,该通路涉及I型蛋白激酶A(PKA I)的激活,最终导致近端T细胞受体(TCR)信号传导受到抑制。我们之前已证明,使用选择性抑制剂Rp-8-Br-cAMPS阻断PKA I可以恢复MAIDS小鼠以及HIV感染小鼠的体外T细胞功能。在本报告中,我们研究了肠外途径给予Rp-8-Br-cAMPS对MAIDS小鼠的影响。我们发现该化合物无毒,并能部分恢复体外抗CD3单克隆抗体的增殖反应,但对MAIDS综合征的特征性淋巴结肿大和脾肿大无影响。[3]这是首篇报道在逆转录病毒感染模型中,短期肠外给予PKA I型抑制剂后免疫功能得到改善的报告。我们的观察结果为通过直接作用于T细胞信号传导近端步骤的新型药物逆转逆转录病毒诱导的免疫缺陷提供了原理验证。有必要进一步研究PKA I型阻断是否也能改善感染小鼠的抗原特异性免疫反应和其他免疫参数,例如CD4细胞因子分泌和CD8功能。[3] |
| 分子式 |
C10H10BRN5NAO5PS
|
|---|---|
| 分子量 |
446.15
|
| CAS号 |
925456-59-3
|
| 相关CAS号 |
Sp-8-Br-cAMPS sodium;1573115-90-8;Rp-8-Br-cAMPS;129735-00-8
|
| 外观&性状 |
Typically exists as solids at room temperature
|
| LogP |
0
|
| SMILES |
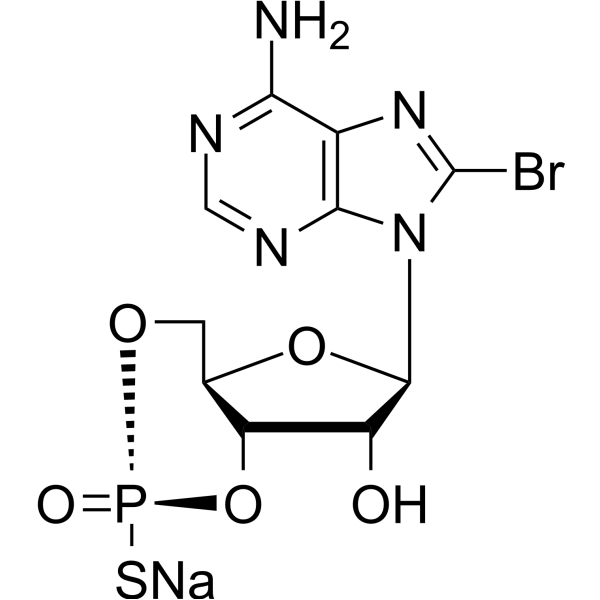
BrC1=NC2=C(N=CN=C2N1[C@@H]1O[C@]2([H])CO[P@](S)(=O)O[C@@]2([H])[C@H]1O)N.[NaH]
|
| 别名 |
925456-59-3; 1573115-90-8; Rp-8-bromo-Cyclic AMPS (sodium salt); Rp-8-bromo-Cyclic AMPS sodium salt; 8-Bromoadenosine 3',5'-cyclic monophosphothiaoate, Sp-isomer sodium salt; sodium;(4aR,6R,7R,7aS)-6-(6-amino-8-bromopurin-9-yl)-2-oxido-2-sulfanylidene-4a,6,7,7a-tetrahydro-4H-furo[3,2-d][1,3,2]dioxaphosphinin-7-ol; 8-Bromoadenosine3',5'-CyclicMonophosphothioateSp-IsomerSodiumSalt; 8-bromo-adenosinecyclic3',5'-[hydrogen[P(R)]-phosphorothioate],monosodiumsalt;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2414 mL | 11.2070 mL | 22.4140 mL | |
| 5 mM | 0.4483 mL | 2.2414 mL | 4.4828 mL | |
| 10 mM | 0.2241 mL | 1.1207 mL | 2.2414 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。