| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
β-adrenoceptor
|
|---|---|
| 体外研究 (In Vitro) |
体外活性:盐酸索他洛尔是一种有效的、非选择性的 β-肾上腺素受体拮抗剂。索他洛尔也是一种钾通道抑制剂,在 HEK 细胞系中的 IC50 值为约 1.2mM。
|
| 体内研究 (In Vivo) |
一种抗心律失常药物是索他洛尔。高达 100 mg/kg 的索他洛尔对电惊厥阈值没有影响。当剂量为 80-100 mg/kg 时,索他洛尔不会干扰拉莫三嗪、普瑞巴林、托吡酯或奥卡西平的抗电击作用。索他洛尔无论是单独使用还是与抗癫痫药物联合使用,都不会妨碍长期记忆和运动功能。索他洛尔(100 mg/kg)会大大降低拉莫三嗪的脑浓度,但托吡酯和奥卡西平的脑浓度会增加。普瑞巴林水平不受影响[3]。
|
| 细胞实验 |
II类抗心律失常药或β受体阻滞剂是通过阻断β肾上腺素受体起作用的抗交感神经系统药物。尽管β受体阻滞剂在临床上很常见,但人们对其对游离细胞内钙(Ca2+i)的影响知之甚少,Ca2+i是一种重要的细胞质第二信使,也是细胞功能的关键调节因子。我们研究了四种化学类似物,即常用的β-受体阻滞剂(阿替洛尔、美托洛尔、普萘洛尔和索他洛尔)对哺乳动物癌症细胞(PC3前列腺癌症和MCF7乳腺癌症细胞系)中Ca2+i释放和全细胞电流的作用。我们发现,只有普萘洛尔以不同的动力学激活游离Ca2+i的释放,而阿替洛尔、美托洛尔和索他洛尔则没有。普萘洛尔诱导的Ca2+i释放被细胞外钙与乙二醇四乙酸(EGTA)的螯合作用和内质网(ER)ryanodine受体通道抑制剂丹曲林显著抑制,并被ER肌醇-1,4,5-三磷酸(IP3)受体通道抑制剂2-氨基乙氧基二苯硼酸酯完全消除。使用ryanodine受体激活剂4-氯间甲酚或肌氨酸/ER Ca2+ATP酶抑制剂thapsigargin耗尽ER储存,可以阻止普萘洛尔诱导的Ca2+i释放。最后,用索他洛尔或噻吗洛尔(β肾上腺素受体的非选择性阻断剂)预孵育细胞也减少了普萘洛尔激活的Ca2+i释放。我们的研究结果表明,不同的β受体阻滞剂对全细胞电流和游离Ca2+i释放具有不同的影响,普萘洛尔通过一种涉及钙诱导的钙释放和推定的下游转导子(如IP3)的机制激活储存操作的Ca2+i释放。II类抗心律失常药对Ca2+i分泌的不同作用可能对这些药物的药理学产生影响[1]。
|
| 动物实验 |
动物/疾病模型: 20-25 克雌性瑞士小鼠[3]
剂量: 100 毫克/千克 给药途径: 腹腔注射 (ip) 实验结果: 显著降低了拉莫三嗪的脑浓度,并增加了奥卡西平和托吡酯的脑浓度。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
索他洛尔的生物利用度为90-100%。与食物同服时,吸收率降低18%。肌酐清除率>80mL/min的患者,其最大浓度为6.25±2.19 mL/min。 80-90%的给药剂量以原形索他洛尔经尿液排出。少量剂量以原形索他洛尔经粪便排出。 表观分布容积为1.2-2.4L/kg。 肌酐清除率>80mL/min的患者,其血浆清除率为6.78±2.72L/h,肾清除率为4.99±1.43L/h。肌酐清除率为 30-80 mL/min 的患者,血浆清除率为 2.74±0.53 L/h,肾清除率为 2.00±0.67 L/h。肌酐清除率为 10-30 mL/min 的患者,血浆清除率为 1.56±0.44 L/h,肾清除率为 0.65±0.31 L/h。肌酐清除率 <10 mL/min 的患者,血浆清除率为 0.65±0.20 L/h,肾清除率为 0.27±0.13 L/h。 代谢/代谢物 索他洛尔不发生代谢。 生物半衰期 健康患者的末端消除半衰期为 10-20 小时。肌酐清除率>80mL/min的患者,半衰期为17.5±0.97h;肌酐清除率30-80mL/min的患者,半衰期为22.7±6.4h;肌酐清除率10-30mL/min的患者,半衰期为64±27.2h;肌酐清除率<10mL/min的患者,半衰期为97.9±57.3h。 |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
服用索他洛尔的患者中,血清转氨酶水平轻度至中度升高的发生率低于2%,通常为短暂且无症状,即使继续治疗也能恢复正常。索他洛尔曾与一例临床表现明显的肝损伤病例相关,该患者在开始服用索他洛尔12周后出现急性肝炎样综合征,并伴有持续性黄疸。停用索他洛尔后,肝损伤有所改善但并未完全消失。在大型药物性肝病和急性肝衰竭病例系列研究中,索他洛尔并未被列为病因。其他β受体阻滞剂与罕见的急性临床表现肝损伤病例相关,其潜伏期为4至24周,血清酶升高呈肝细胞型,病程轻微且可自愈,无超敏反应或自身免疫反应的证据。 可能性评分:E(不太可能是临床表现肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 由于索他洛尔会大量分泌到乳汁中,且主要经肾脏排泄,因此,尤其是在哺乳新生儿或早产儿时,应优先选择其他β受体阻滞剂而非索他洛尔。一些作者建议,哺乳期使用索他洛尔时,应密切监测婴儿的β受体阻滞反应。预计婴儿在出生4周或更大后接触药物的机会将减少。 ◉ 对母乳喂养婴儿的影响 一项针对哺乳期服用β受体阻滞剂的母亲的研究发现,服用任何β受体阻滞剂的母亲出现不良反应的例数在数值上有所增加,但未达到统计学意义。尽管婴儿的年龄与对照组婴儿相匹配,但未说明受影响婴儿的年龄。其中一位母亲正在服用索他洛尔。 在一位母亲每日服用600毫克索他洛尔期间,一名出生即开始母乳喂养的12天大的婴儿未出现心动过缓。另一例母乳喂养的婴儿,其母亲每日服用80毫克,每日2至3次,持续3个月以上,未观察到心动过缓,且发育里程碑均正常达成。 具有相似乳汁排泄特性和肾脏清除的β-肾上腺素能阻滞剂已对母乳喂养的新生儿造成不良影响。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到关于β受体阻滞剂或索他洛尔在正常哺乳期影响的相关已发表信息。一项针对6名高催乳素血症和溢乳患者的研究发现,使用普萘洛尔进行β-肾上腺素能阻滞后,血清催乳素水平未发生变化。 蛋白结合 0%。 |
| 参考文献 |
[1]. Marta Reyes-Corral, et al. Differential Free Intracellular Calcium Release by Class II Antiarrhythmics in Cancer Cell Lines. J Pharmacol Exp Ther. 2019 Apr;369(1):152-162.
[2]. Xiaomei Li, et al. Pediatric Dosing of Intravenous Sotalol Based on Body Surface Area in Patients with Arrhythmia. Pediatr Cardiol. 2017 Oct;38(7):1450-1455. [3]. Kinga K Borowicz-Reutt, et al. Sotalol does not interfere with the antielectroshock action of selected second-generation antiepileptic drugs in mice.Pharmacol Rep. 2021 Apr;73(2):516-524. |
| 其他信息 |
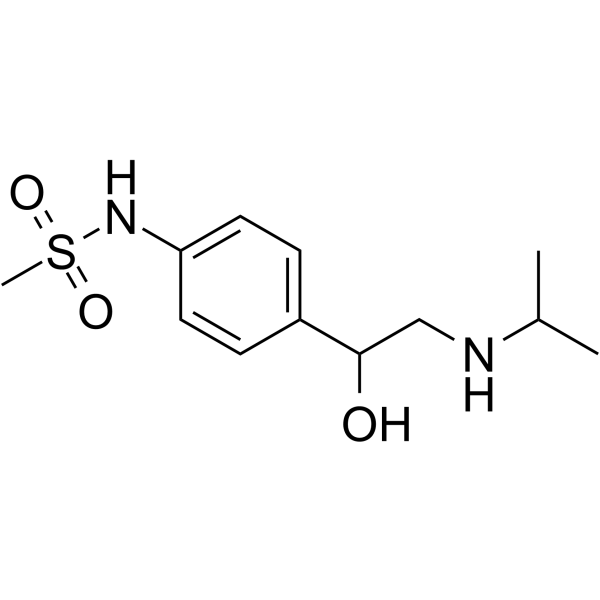
索他洛尔是一种磺酰胺类化合物,其结构为N-苯基甲磺酰胺,其中苯基在4位被1-羟基-2-(异丙基氨基)乙基取代。它具有β-肾上腺素能受体阻滞(Vaughan Williams II类)和延长心肌动作电位时程(Vaughan Williams III类)的抗心律失常作用。它(通常以盐酸盐形式)用于治疗室性和室上性心律失常。它是一种β-肾上腺素能拮抗剂、抗心律失常药物、环境污染物和外源性物质。它属于乙醇胺类、仲氨基化合物、仲醇类和磺酰胺类化合物。它是索他洛尔(1+)的共轭碱。
索他洛尔是一种甲磺酰苯胺类化合物,于1960年研制成功。它是首个III类抗心律失常药物。索他洛尔于1992年10月30日首次获批上市,剂型为口服片剂。目前,索他洛尔的消旋混合物被制成片剂、口服溶液和静脉注射剂,用于治疗危及生命的心室性心律失常,以及在房颤或房扑中维持正常窦性心律。 索他洛尔是一种抗心律失常药。其作用机制是作为β-肾上腺素能受体拮抗剂。索他洛尔的生理效应是通过改变心律来实现的。 索他洛尔是一种非选择性β-肾上腺素能阻滞剂,主要用于治疗心律失常。索他洛尔至少与一例临床上明显的肝损伤有关。 索他洛尔是一种乙醇胺衍生物,具有III类抗心律失常和抗高血压特性。索他洛尔是一种非选择性β-肾上腺素能受体和钾通道拮抗剂。在心脏中,该药物抑制正性变时性和正性变力性作用,从而减慢心率并降低心肌收缩力。该药物还能降低窦性心率,减慢心房和房室结的传导速度,并延长房室结的功能性不应期。 一种用于治疗危及生命的心律失常的β受体阻滞剂。 另见:盐酸索他洛尔(有盐形式)。 药物适应症 索他洛尔适用于治疗危及生命的室性心律失常,并维持房颤或房扑患者的正常窦性心律。对于需要索他洛尔但不适合服用片剂的患者,也有口服溶液和静脉注射剂可供选择。 FDA标签 作用机制 索他洛尔抑制心肌中的β1肾上腺素能受体以及快速钾通道,从而减慢复极化,延长QT间期,并减慢和缩短动作电位在心房的传导。索他洛尔对β肾上腺素能受体的作用可延长窦房结周期、房室结传导时间、不应期和动作电位持续时间。 药效学 索他洛尔是快速钾通道的竞争性抑制剂。这种抑制作用可延长心房和心室的动作电位持续时间和不应期。随着心率降低,对快速钾通道的抑制作用增强,因此在较低心率下更容易出现尖端扭转型室性心动过速等不良反应。左索他洛尔在血浆浓度高于 800 ng/L 时也具有β肾上腺素能受体阻滞活性。索他洛尔的β受体阻滞作用会进一步延长动作电位。右索他洛尔不具有β受体阻滞活性,但也能降低患者站立或运动时的心率。这些作用共同产生负性肌力效应,降低心肌细胞的收缩力。QT间期延长也与患者发生心律失常的风险增加相关。非胰岛素依赖型糖尿病患者发生高血糖的风险高于胰岛素依赖型糖尿病患者。β受体阻滞剂抑制胰岛素分泌,这可能导致II型糖尿病患者出现高血糖。胰岛素依赖型糖尿病患者发生低血糖的风险高于非胰岛素依赖型糖尿病患者。β受体阻滞剂减少胰岛素分泌,这可能会掩盖胰岛素依赖型患者的低血糖症状。β受体阻滞剂还会增加细胞对葡萄糖的摄取,这可能会延长或加剧低血糖。有关不良反应的更多信息,请点击此处查看。 |
| 分子式 |
C12H20N2O3S
|
|---|---|
| 分子量 |
272.3638
|
| 精确质量 |
272.119
|
| CAS号 |
3930-20-9
|
| 相关CAS号 |
Sotalol hydrochloride;959-24-0;Sotalol-d6;1246912-17-3
|
| PubChem CID |
5253
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| 密度 |
1.239 g/cm3
|
| 沸点 |
443.3ºC at 760 mmHg
|
| 熔点 |
206.5 - 207 °C
|
| 闪点 |
221.9ºC
|
| 折射率 |
1.57
|
| LogP |
2.634
|
| tPSA |
86.81
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
18
|
| 分子复杂度/Complexity |
330
|
| 定义原子立体中心数目 |
0
|
| SMILES |
CS(=O)(NC1=CC=C(C(O)CNC(C)C)C=C1)=O
|
| InChi Key |
ZBMZVLHSJCTVON-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C12H20N2O3S/c1-9(2)13-8-12(15)10-4-6-11(7-5-10)14-18(3,16)17/h4-7,9,12-15H,8H2,1-3H3
|
| 化学名 |
N-[4-[1-hydroxy-2-(propan-2-ylamino)ethyl]phenyl]methanesulfonamide
|
| 别名 |
beta-Cardone; DL-Sotalol; Sotalolum; Darob mite; Sotalolum [INN-Latin]; N-(4-(1-Hydroxy-2-(isopropylamino)ethyl)phenyl)methanesulfonamide;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.6716 mL | 18.3581 mL | 36.7161 mL | |
| 5 mM | 0.7343 mL | 3.6716 mL | 7.3432 mL | |
| 10 mM | 0.3672 mL | 1.8358 mL | 3.6716 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT02347111
Conditions:Atrial FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT02624765
Conditions:Fetal Atrial Flutter Without Hydrops|Fetal Supraventricular Tachycardia Without Hydrops|Fetal Supraventricular Tachycardia With HydropsLink: https://clinicaltrials.gov/ct2/show/NCT05279833
Conditions:Atrial Fibrillation
Title:Study of the Effects of BMS-919373 on the Electrical Activity of the Heart Using Pacemakers
Status:Terminated
updateDate:2023-12-19
Ctid:NCT02153437
Link: https://clinicaltrials.gov/ct2/show/NCT02153437
Conditions:Atrial FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT05247320
Conditions:Atrial ArrhythmiaLink: https://clinicaltrials.gov/ct2/show/NCT03845010
Conditions:Ventricular Premature BeatsLink: https://clinicaltrials.gov/ct2/show/NCT05418036
Conditions:Supraventricular Arrhythmia|Ventricular Arrythmia|Proarrhythmia|Antiarrhythmic Drug Adverse ReactionLink: https://clinicaltrials.gov/ct2/show/NCT04128878
Conditions:Atrial FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT03799536
Conditions:BioequivalenceLink: https://clinicaltrials.gov/ct2/show/NCT03895411
Conditions:ArrhythmiaLink: https://clinicaltrials.gov/ct2/show/NCT02294955
Conditions:Atrial Fibrillation|Quality of LifeLink: https://clinicaltrials.gov/ct2/show/NCT00000531
Conditions:Arrhythmia|Cardiovascular Diseases|Death, Sudden, Cardiac|Heart Diseases|Tachycardia, Ventricular|Ventricular FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT00000556
Conditions:Arrhythmia|Atrial Fibrillation|Cardiovascular Diseases|Heart DiseasesLink: https://clinicaltrials.gov/ct2/show/NCT00000518
Conditions:Arrhythmia|Cardiovascular Diseases|Death, Sudden, Cardiac|Heart Diseases|Tachycardia, Ventricular|Ventricular Arrhythmia|Ventricular FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT01576042
Conditions:Ventricular TachycardiaLink: https://clinicaltrials.gov/ct2/show/NCT02145546
Conditions:Atrial FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT00000464
Conditions:Arrhythmia|Cardiovascular Diseases|Heart Arrest|Heart Diseases|Myocardial Infarction|Ventricular FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT00773201
Conditions:Healthy VolunteersLink: https://clinicaltrials.gov/ct2/show/NCT00035451
Conditions:Atrial FibrillationLink: https://clinicaltrials.gov/ct2/show/NCT00007605
Conditions:Atrial Fibrillation|Cerebrovascular Accident|Death, SuddenLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2007-005780-99
Condition:volontaires sainsLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2004-004337-33
Condition:APPLICATION OF CIRCUMFERENTIAL PULMONARY VEIN ABLATION IN THE TREATMENT OF PAROXYSMAL ATRIAL FIBRILLATION