| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 50g |
|
||
| 100g |
|
||
| 200g |
|
||
| 500g |
|
||
| Other Sizes |
|
| 药代性质 (ADME/PK) |
吸收、分布和排泄
三丁酸甘油酯可被大鼠肠黏膜吸收,但不能被豚鼠皮肤吸收。 在人体中,每日一次口服注射50-400 mg/kg三丁酸甘油酯,持续3周,血浆峰浓度出现在给药后0.25-3小时。200 mg/kg剂量组的血浆峰浓度范围为0.1-0.45 mM。更高剂量组未观察到更高的血浆浓度。 小鼠和大鼠口服10.3 g/kg三丁酸甘油酯后,血浆丁酸盐浓度峰值分别为1.75 mM和3.07 mM。小鼠给药后10-60分钟,大鼠给药后30-90分钟,血药浓度≥1 mM。 ……雌性CD2F1小鼠分别经口灌胃给予三丁酸甘油酯,或经静脉推注或口灌胃给予丁酸钠。小鼠口服三丁酸甘油酯的剂量分别为3.1、5.2、7.8和10.3 g/kg。静脉注射丁酸钠的剂量分别为0.31、0.62、0.94和1.25 g/kg。小鼠口服丁酸钠的剂量为5 g/kg。随后,在雌性Sprague-Dawley大鼠中进行了类似的研究。大鼠经口灌胃给予三丁酸甘油酯,剂量分别为3.6、5.2或10.3 g/kg,或静脉注射丁酸钠,剂量为500 mg/kg。采用气相色谱法测定血浆丁酸浓度。结果:小鼠口服三丁酸甘油酯后,最早在给药后5分钟即可检测到血浆丁酸浓度,并在给药后15至60分钟达到血浆丁酸浓度峰值。血浆丁酸浓度峰值随三丁酸甘油酯剂量的增加呈比例增加,但随着口服三丁酸甘油酯剂量的增加,血浆丁酸浓度-时间曲线下面积(AUC)的增加幅度大于剂量比例。当三丁酸甘油酯剂量为10.3 g/kg时,血浆丁酸浓度峰值约为1.75 mM,并在给药后10至60分钟内维持在1 mM以上。然而,约10%接受该剂量治疗的小鼠发生急性死亡。在给予7.8 g/kg剂量的三丁酸甘油酯后,血浆丁酸浓度在给药后15分钟达到约1 mM,并维持在0.8至1 mM之间直至给药后60分钟。接受该剂量治疗的小鼠均未出现急性死亡。给予5.2 g/kg和3.1 g/kg剂量的三丁酸甘油酯的小鼠,在给药后45分钟分别达到约0.9 mM和0.5 mM的血浆丁酸峰值浓度。这些小鼠的血浆丁酸浓度分别在给药后120分钟和90分钟内维持在0.1 mM以上。四次静脉注射丁酸钠的实验结果显示,血浆浓度-时间曲线也呈现非线性药代动力学特征,且可用具有饱和消除的单室模型很好地描述。记录的米氏常数 (Km) 和最大反应速率 (Vmax) 值分别在 1.02 至 5.65 mM 和 0.60 至 1.82 mmol/min 之间。中心室容积 (Vc) 的值在 0.48 至 0.72 L/kg 之间。静脉注射 1.25 g/kg 丁酸钠后,血浆丁酸峰值浓度为 10.5 至 17.7 mM,且血浆丁酸浓度在 20 至 30 分钟内保持在 1 mM 以上。口服 5 g/kg 丁酸钠后,小鼠在给药后 15 分钟血浆丁酸峰值浓度约为 9 mM,且血浆丁酸浓度在给药后 90 分钟内保持在 1 mM 以上。在大鼠中,口服10.3 g/kg的丁酸甘油酯后,75分钟时血浆丁酸浓度峰值约为3 mM,30至90分钟时血浆丁酸浓度超过1 mM。5.2 g/kg和3.6 g/kg剂量组大鼠血浆丁酸浓度均低于10.3 g/kg剂量组,且未观察到非线性关系。静脉注射500 mg/kg丁酸钠后,大鼠血浆丁酸浓度峰值约为11 mM,给药后血浆丁酸浓度随时间下降,符合饱和清除规律。 ……血浆丁酸浓度峰值出现在给药后0.25至3小时之间,随剂量增加而升高,浓度范围为0至0.45 mM。在三名接受剂量递增治疗的患者中,血药峰浓度并未升高。第1天和第15天的丁酸盐药代动力学无差异。由于达到了接近体外有效浓度(0.5-1 mM)的血浆峰浓度,但丁酸盐在给药后5小时内从血浆中消失,我们目前正在进行剂量递增治疗,每日三次给药,起始剂量为450 mg/kg/天。 代谢/代谢物 ……三丁酸酶……是一种特异性水解三丁酸的酶。该酶可被某些有机化合物抑制,特别是某些氟磷酸盐。……已从大鼠脂肪组织中分离出一种对氟化物敏感的三丁酸酶,该酶可从1-单丁酸、1,2-二丁酸或三丁酸中释放丁酸。 猪肝和肾微粒体对三丁酸的水解活性最高。青蛙、猪、大鼠、猫、兔、豚鼠、绵羊、鸽子、狗(但不包括鱼)的肝微粒体也具有对三丁酸甘油酯的酯酶活性。 对甘油脂肪酸酯(包括三丁酸甘油酯……)水解的研究表明,它们完全水解为甘油和相应的脂肪酸,分别为丁酸、5-羟基癸酸和5-羟基十二烷酸。 |
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
相互作用
喂食三丁酸甘油酯对小鼠体内二异丙基氟磷酸酯 (DFP) 毒性的影响。喂食三丁酸甘油酯 36 小时后,DFP 毒性为正常值的 1.7 倍;喂食 14 天后,毒性仅为正常值的 1.15 倍。 非人类毒性值 大鼠口服 LD50:3.2 g/kg 小鼠口服 LD50:12.8 mg/kg |
| 参考文献 |
|
| 其他信息 |
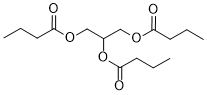
三丁酸甘油酯是一种甘油三酯,由丁酸酰化甘油的三个羟基制得。它具有多种功能,包括作为EC 3.5.1.98(组蛋白去乙酰化酶)抑制剂、保护剂、细胞凋亡诱导剂、前药和抗肿瘤剂。它是一种甘油三酯和丁酸酯,在功能上与丁酸相关。
三丁酸甘油酯已用于前列腺癌和特定成人实体瘤(方案特定)的治疗试验。 据报道,三丁酸甘油酯存在于眼虫和秀丽隐杆线虫中,并有相关数据。 三丁酸甘油酯是一种具有潜在抗肿瘤活性的丁酸甘油三酯前药。丁酸是三丁酸甘油酯的活性代谢产物,它能抑制组蛋白去乙酰化酶,从而导致某些肿瘤细胞系分化增加、增殖减少、细胞周期阻滞和凋亡。(NCI04) 作用机制 ……将人胃癌SGC-7901细胞暴露于浓度为0.5、1、2、5、10和50 mmol/L的三丁酸甘油酯中24-72小时。采用MTT/2H-四唑,2-(4,5-二甲基-2-噻唑-3)法检测细胞增殖。测定[(3)H]-TdR的摄取量以确定DNA合成。通过电镜和Hoechst-33258染色观察细胞凋亡形态。采用流式细胞术和末端脱氧核苷酸转移酶介导的dUTP缺口末端标记法(TUNEL)检测三丁酸甘油酯诱导的细胞凋亡。通过Western blot检测PARP/聚ADP核糖聚合酶、Bcl-2和Bax的表达。三丁酸甘油酯能够以剂量和时间依赖的方式抑制SGC-7901细胞的生长。与对照组相比,经2 mmol/L三丁酸甘油酯处理48 h后,SGC-7901细胞对[(3)H]-TdR的摄取量降低至33.6%(P<0.05)。TUNEL检测显示细胞凋亡形态。流式细胞术结果表明,三丁酸甘油酯能够以剂量依赖的方式诱导SGC-7901细胞凋亡。在2 mmol/L(-1)的三丁酸甘油酯孵育48小时后,SGC-7901细胞中Bcl-2蛋白水平降低,Bax蛋白水平升高,并伴有PARP裂解。 ……HT-29结肠癌细胞暴露于PB(苯丁酸)和TB(三丁酸甘油酯)后,生长受到抑制,并伴有caspase-3活性激活介导的细胞凋亡诱导。PB和TB暴露后,还观察到G1/S期细胞周期阻滞,伴有CDK2(细胞周期蛋白依赖性激酶)蛋白水平降低和视网膜母细胞瘤蛋白低磷酸化。 我们研究了三丁酸甘油酯诱导MCF-7人乳腺癌细胞生长停滞和凋亡的作用。用三丁酸甘油酯处理细胞4小时后,即可观察到线粒体相关蛋白Bax的瞬时增加、线粒体膜电位(Δψm)的耗散以及不依赖于caspase-3的聚(ADP-核糖)聚合酶的裂解。随后,胞质溶胶中线粒体细胞色素c的瞬时积累,最终导致亚二倍体DNA含量细胞的生成和积累。在与线粒体相关的Bax水平升高、δψm通道紊乱且胞质中检测到细胞色素c的时期,我们发现p21WAF1/Cip1在p53未升高的情况下被诱导表达,且细胞停滞于G2-M期。 治疗用途 ……本研究纳入了20例晚期实体瘤患者,这些患者无其他治疗方案,预期生存期超过12周,且器官功能正常。他们接受了三丁酸甘油酯治疗,剂量为150至200 mg/kg,每日三次。在给药前以及给药后15分钟、30分钟、1小时、1.5小时、2小时、2.5小时、3小时、3.5小时和4小时采集血样进行药代动力学分析。入组患者共15名男性和5名女性,中位年龄61岁(范围30-74岁)。既往治疗方案包括:化疗(中位数为2个疗程,范围0-5个疗程)、放疗(1例)和未接受过任何治疗(1例)。未出现剂量限制性毒性。由于所需胶囊数量较多,剂量递增至每日三次,每次200 mg/kg时停止。丁酸盐浓度中位数为52 μM,但患者间差异较大。未观察到客观缓解。4例患者病情稳定期延长,持续时间为3至23个月;中位无进展生存期为55天。截至本报告撰写之时,2例化疗难治性非小细胞肺癌患者已生存超过1年,且无疾病进展迹象。 |
| 分子式 |
C15H26O6
|
|---|---|
| 分子量 |
302.36334
|
| 精确质量 |
302.172
|
| 元素分析 |
C, 59.58; H, 8.67; O, 31.75
|
| CAS号 |
60-01-5
|
| 相关CAS号 |
60-01-5
|
| PubChem CID |
6050
|
| 外观&性状 |
COLORLESS
Oily liquid |
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
307.5±0.0 °C at 760 mmHg
|
| 熔点 |
-75 °C
|
| 闪点 |
173.9±0.0 °C
|
| 蒸汽压 |
0.0±0.6 mmHg at 25°C
|
| 折射率 |
1.448
|
| LogP |
2.95
|
| tPSA |
78.9
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
14
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
304
|
| 定义原子立体中心数目 |
0
|
| SMILES |
CCCC(=O)OCC(COC(=O)CCC)OC(=O)CCC
|
| InChi Key |
UYXTWWCETRIEDR-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C15H26O6/c1-4-7-13(16)19-10-12(21-15(18)9-6-3)11-20-14(17)8-5-2/h12H,4-11H2,1-3H3
|
| 化学名 |
2,3-di(butanoyloxy)propyl butanoate
|
| 别名 |
Tributyrin; NSC 661583; NSC-661583; NSC661583
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~100 mg/mL (~330.7 mM)
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.3073 mL | 16.5366 mL | 33.0732 mL | |
| 5 mM | 0.6615 mL | 3.3073 mL | 6.6146 mL | |
| 10 mM | 0.3307 mL | 1.6537 mL | 3.3073 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05446168 | Recruiting | Drug: tributyrin | Parkinson Disease | Nicolaas Bohnen, MD, PhD | July 1, 2022 | Phase 1 |
| NCT05951153 | Not yet recruiting | Combination Product: Tributyrin | Hematopoietic Cell Transplantation (HCT) |
Duke University | November 2023 | Early Phase 1 |
| NCT00002677 | Completed | Drug: tributyrin Drug: chemotherapy |
Prostate Cancer Unspecified Adult Solid Tumor, Protocol Specific |
University of Maryland, Baltimore | August 1995 | Phase 1 |
| NCT02264951 | Completed | Dietary Supplement: Tributyrin Dietary Supplement: Carrot |
Type 2 Diabetes | Glostrup University Hospital, Copenhagen |
October 2013 | Not Applicable |