| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
Survivin (IC50 = 0.54 nM)
|
|---|---|
| 体外研究 (In Vitro) |
生存基因启动子驱动的荧光素酶报告基因活性不影响司潘溴铵 (YM155;30 μM)。通过对生存素基因启动子的转录抑制,sepantronium bromide 可显着降低 p53 缺陷的 PC-3 和 PPC-1 人 HRPC 细胞中内源性生存素的表达。 c-IAP2、XIAP、Bcl-2、Bcl-xL、Bad、α-肌动蛋白和 β-微管蛋白的蛋白表达不受 sepatrium bromide (100 nM) 的影响。 Sepatrium bromide 的 IC50 范围为 2.3 至 11 nM,可有效抑制人类癌细胞系(突变或截短的 p53),包括 PC-3、PPC-1、DU145、TSU-Pr1、22Rv1、SK-MEL-5 和 A375,分别。 1]。溴化隔膜 (YM155) 可增加 NSCLC 细胞的伽马射线敏感性。当分离溴化物和伽玛射线联合使用时,凋亡细胞的数量和 caspase-3 活性会增加。此外,溴化庚烷无法快速修复由辐射引起的核 DNA 双链断裂 [2]。
|
| 体内研究 (In Vivo) |
在 PC-3 异种移植物中,sepantronium bromide(YM155;3 和 10 mg/kg)可抑制肿瘤生长,而不会导致明显的体重减轻或血细胞计数降低。溴化蛇纹石广泛分散在人体的肿瘤组织中。在 PC-3 原位异种移植物中,溴化蛇在 5 mg/kg 剂量下显示出 80% TGI [1]。当与伽马射线结合时,spentronium bromide (YM155) 对裸鼠中的 H460 或 Calu6 异种移植物表现出强大的抗癌功效 [2]。在原位肾肿瘤和转移性肺肿瘤模型中,Sepantronium bromide (YM-155) 和 IL-2 进一步降低了肿瘤重量、肺转移和荧光素染色的肿瘤图片 [3]。
|
| 酶活实验 |
使用 Pyrobest 聚合酶和以下引物,通过 PCR 从人类基因组 DNA 中分离出 2,767 bp 的人类生存素基因启动子序列:5
γ-H2AX免疫荧光染色。[2] 细胞在两孔Lab Tec小室载玻片(Nunc)中生长至50%融合,然后在50 nmol/LYM155或载体存在下培养48小时,然后暴露于3 Gy的γ辐射。在此后的不同时间,它们在室温下用4%多聚甲醛固定10分钟,在4°C下用0.1%Triton X-100渗透10分钟,并在室温下暴露于5%脱脂奶粉中10分钟。用PBS洗涤载玻片,然后在室温下首先用1:300稀释的组蛋白γ-H2AX小鼠单克隆抗体孵育2小时,然后用1:700稀释的Alexa 488标记的小鼠IgG山羊抗体孵育1小时。将载玻片安装在荧光安装介质中,用配备LSM5 PASCAL系统的共聚焦激光扫描显微镜观察荧光信号。以×100的放大倍数检查了三个随机区域,每个区域包含=50个细胞。如前所述,将含有≥10个免疫反应灶的核计数为γ-H2AX阳性,并计算阳性细胞的百分比[2]。 |
| 细胞实验 |
将细胞以 5-40 × 103 的密度接种在 96 孔板中。将溶解有 YM155 的 DMSO 给予细胞 48 小时。然后,使用磺基罗丹明 B 测定法计算细胞计数。台盼蓝排斥染色用于测定细胞活力。[1]
在有或没有YM155的情况下培养48小时后,通过胰蛋白酶消化和离心(0.05%胰蛋白酶-EDTA)收集PC-3和PPC-1细胞,并将其重新悬浮在DMEM中。将细胞悬浮液用等体积的台盼蓝(0.4%工作溶液)稀释。在血细胞计数器上计数活细胞(未染色)和死细胞(染色),活细胞与细胞总数的比率表示为活细胞百分比。 半胱氨酸天冬氨酸蛋白酶-3活性的测量。[1] 根据制造商的说明,用CPP32/SCaspase-3荧光蛋白酶检测试剂盒(MBL)测量半胱氨酸天冬氨酸蛋白酶-3活性。在用YM155孵育48小时后,PC-3和PPC-1细胞在100μL细胞裂解缓冲液(随试剂盒提供)中裂解,得到等体积(50μL)的细胞裂解液(100μg蛋白质)。加入2倍反应缓冲液后,将混合物加入黑色96孔板中。然后以5 mL/孔的速度加入DEVD-AFC底物(附有试剂盒),并将混合物在37°C下孵育30分钟。用荧光分光光度计在390 nm的激发波长和460 nm的发射波长下对荧光发射进行定量。 体外细胞生长抑制试验。[1] YM155的抗增殖活性通过国家癌症研究所使用的方法进行测量。用YM155处理48小时后,通过磺基罗丹明B测定细胞计数。GI50值通过逻辑分析计算,即药物浓度导致对照细胞在药物孵育过程中净蛋白质增加(通过硫罗丹明B染色测量)减少50%。该测定一式三份,平均GI50值由四次独立测定的结果得出。 体外抗肿瘤活性的时间依赖性。[1] A549细胞用YM155、甲氨蝶呤或阿霉素处理。通过用新鲜培养基洗涤五次,在不同长度的暴露时间后去除每种化合物。在细胞处理开始后的72小时温育时,用Alamar Blue测定法(Serotec;参考文献22)测定所选化合物对细胞增殖的影响,每种浓度(n=1)两次。通过逻辑分析计算IC50。为了了解每种化合物的体外作用模式和药效学特性,以对数标度绘制了YM155、阿霉素(作为曲线下面积依赖性药物)和甲氨蝶呤(作为时间相关药物)的对数斜率(暴露时间)和对数斜率的倒数(A549抗增殖作用的IC50),并比较了三种药物的IC50暴露时间曲线的斜率。 |
| 动物实验 |
在雄性裸鼠(BALB/c nu/nu)中建立PC-3皮下(原位)异种移植瘤模型
5 mg/kg 通过植入式微型渗透泵,每周皮下注射3天,持续3周。 体内实验中,YM155在给药前立即溶解并稀释于生理盐水中。 针对PC-3皮下异种移植瘤模型的体内抗肿瘤活性。[1] 使用5周龄雄性裸鼠(BALB/c nu/nu)。将PC-3细胞(2 × 10⁶–3 × 10⁶)注射到小鼠侧腹部,使其肿瘤体积(长×宽2 × 0.5)>100 mm³。 YM155采用皮下注射给药,每周3天,持续2周,使用植入式微型渗透泵(Alzet 1003D型,Durect公司)进行持续输注;或采用静脉注射给药,每周5次,持续2周。首次给药YM155后14天,使用以下公式计算各组的肿瘤生长抑制率:MTV = 100 × {1 − [(治疗组第14天的MTV) − (治疗组第0天的MTV)] / [(对照组第14天的MTV) − (对照组第0天的MTV)]},其中MTV为平均肿瘤体积。对于冷冻肿瘤和血浆样本,采用Western blotting分析survivin表达水平,并采用高效液相色谱/三重四极杆质谱(LC/MS/MS)结合已验证的方法分析YM155药物浓度。 针对PC-3原位异种移植模型的体内抗肿瘤活性。[1] 对于原位移植,将PC-3细胞悬液(每只小鼠1 × 10⁶/20 μL)注射到7周龄雄性裸鼠(BALB/c nu/nu)的前列腺背外侧叶(右侧)。移植两周后,使用植入式微型渗透泵(Alzet 1003D型,Durect)以5 mg/kg/d的剂量,每周连续3天皮下输注YM155,持续3周。从首次给予YM155给药开始,定期测量体重。三周后,取出附着于前列腺和精囊的肿瘤并称重,作为肿瘤重量。YM155的抗肿瘤活性以肿瘤生长抑制百分比表示,计算公式如下:MTW = 100 × [1 − (治疗组第21天的MTW) / (对照组第21天的MTW)]。 体内肿瘤生长评估。[2] 将肿瘤细胞(2 × 10⁶)皮下注射到6周龄雌性无胸腺裸鼠(BALB/c nu/nu)的右后肢。根据公式LW²/2,用游标卡尺测量肿瘤长度(L)和宽度(W)计算肿瘤体积。当各组动物的肿瘤平均体积达到约 200 至 250 mm³ 时开始治疗。治疗组(每组 8 只小鼠)包括:载体对照组(生理盐水)、YM155 单独治疗组、载体联合放射治疗组和 YM155 联合放射治疗组。载体或 YM155 的剂量为 5 mg/kg 体重,连续 7 天(第 1-7 天)通过植入式微型渗透泵(Alzet 1003D 型;Durect 公司)给药。放射治疗组的小鼠接受钴辐照器提供的 10 Gy γ 射线照射,照射方式为:在给药第 3 天一次性照射,或在连续 5 天(第 3-7 天)分次照射;照射靶向肿瘤,其余身体部位用铅屏蔽。生长延迟 (GD) 的计算方法为:治疗组肿瘤体积增长 5 倍所需时间减去对照组肿瘤体积增长 5 倍所需时间。增强因子随后被确定为:(GDcombination − GDYM155)/GDradiation。[2] 将表达荧光素酶的RENCA细胞分别植入左肾肾包膜下和尾静脉,以构建具有原位肿瘤和肺转移瘤的小鼠肾细胞癌(RCC)模型。将小鼠随机分为四组,各组的IVIS值分布均匀。第1组腹腔注射100 μL磷酸盐缓冲液(PBS)作为载体对照;第2组单独接受YM155治疗(1 mg/kg体重/天,腹腔注射,持续1周);第3组单独接受IL-2治疗(在治疗的第0、4和8天腹腔注射6000 U重组IL-2);第 4 组(联合治疗组)接受 YM155 和 IL-2 治疗(剂量和给药方案与第 2 组相同,加上第 3 组)。所有组均在治疗后第 14 天进行肿瘤成像并分析肿瘤体积。处死小鼠,测量左肾原位肿瘤和双侧肺转移组织切片的重量。[3] |
| 参考文献 |
|
| 其他信息 |
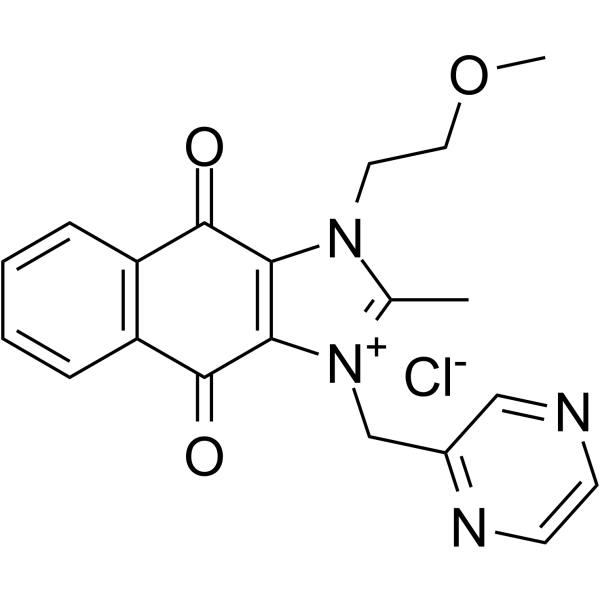
溴化塞潘曲铵是一种有机溴化物盐,由塞潘曲铵阳离子和溴离子阴离子组成。研究发现,它能选择性抑制survivin(BIRC5)基因启动子活性,并在体外下调survivin表达,从而诱导细胞凋亡。它具有抗肿瘤、抑制survivin和诱导细胞凋亡的双重作用。其分子结构中包含塞潘曲铵基团。
溴化塞潘曲铵是一种具有潜在抗肿瘤活性的小分子促凋亡剂。溴化塞潘曲铵选择性抑制肿瘤细胞中survivin的表达,从而抑制survivin的抗凋亡活性(通过外源性或内源性凋亡途径),最终诱导肿瘤细胞凋亡。Survivin是凋亡抑制蛋白(IAP)基因家族的成员,在胚胎发育过程中表达,但在大多数正常的终末分化组织中不表达。 Survivin在多种人类癌症中表达上调,其在肿瘤中的表达与更具侵袭性的表型、更短的生存期以及化疗反应降低相关。 越来越多的证据表明,作为凋亡抑制蛋白(IAP)家族成员的Survivin在多种癌症(包括激素难治性前列腺癌(HRPC))的耐药性和癌细胞存活中发挥着重要作用。本研究采用Survivin基因启动子活性检测方法,对一种新型小分子Survivin抑制剂YM155进行了表征。YM155在10 nmol/L浓度下即可抑制PC-3和PPC-1人HRPC细胞系中Survivin的表达并诱导细胞凋亡。相反,浓度高达100 nmol/L的YM155对其他IAP或Bcl-2相关蛋白的表达水平几乎没有影响。在小鼠皮下移植PC-3肿瘤模型中,连续3天以3至10 mg/kg的剂量输注YM155可诱导肿瘤显著消退,并伴有肿瘤内survivin表达的抑制。YM155还能完全抑制原位移植PC-3肿瘤的生长。在实验期间,接受YM155治疗的小鼠体重未见明显下降。药代动力学分析表明,YM155在肿瘤部位分布广泛,其浓度约为血浆浓度的20倍。我们的研究首次尝试通过单一小分子化合物治疗,证实了p53缺陷型人HRPC细胞的肿瘤消退和survivin表达的抑制。对YM155在多种癌症类型(包括去势抵抗性前列腺癌[HRPC])中的进一步广泛研究,对于开发这种新型治疗方法而言似乎很有价值。[1] 目的:Survivin是凋亡抑制蛋白家族的成员,是癌症治疗的一个有吸引力的靶点。我们现在研究了Survivin表达的小分子抑制剂YM155对人非小细胞肺癌(NSCLC)细胞系γ射线敏感性的影响。实验设计:基于细胞死亡、克隆形成存活率和肿瘤异种移植瘤的进展来评估YM155的放射增敏作用。基于组蛋白H2AX磷酸化和DNA聚焦形成来评估辐射诱导的DNA损伤。结果:YM155以浓度和时间依赖的方式诱导NSCLC细胞中Survivin表达的下调。克隆形成存活实验表明,YM155 可提高非小细胞肺癌 (NSCLC) 细胞在体外对 γ 射线的敏感性。YM155 与 γ 射线联合应用可协同增加凋亡细胞的数量和 caspase-3 的活性。组蛋白 γ-H2AX 的免疫荧光分析也显示,YM155 可延缓核 DNA 中辐射诱导的双链断裂的修复。最后,YM155 与 γ 射线联合治疗可显著延缓裸鼠体内 NSCLC 肿瘤异种移植瘤的生长,其效果优于单独使用任一治疗方式。结论:这些结果表明,YM155 可在体外和体内增强 NSCLC 细胞对辐射的敏感性,并且 YM155 的这种作用可能至少部分归因于其通过下调 survivin 表达而抑制 DNA 修复并增强细胞凋亡。 YM155与放射治疗联合治疗作为一种潜在的抗癌策略,值得在临床试验中进行研究。[2]YM155是一种小分子抗凋亡蛋白survivin抑制剂,已被开发为一种潜在的抗癌药物。我们利用肾细胞癌(RCC)小鼠模型研究了YM155与白细胞介素-2(IL-2)的联合治疗。YM155可诱导肾癌(RENCA)细胞的细胞周期阻滞和凋亡。随后,我们将表达荧光素酶的RENCA细胞移植到BALB/c小鼠的左肾和肺中,构建RCC转移模型。在这些原位肾癌和肺转移瘤模型中,YM155和IL-2均能协同降低肿瘤重量、肺转移灶和荧光素染色肿瘤的显像强度。此外,与单药治疗相比,联合用药显著抑制了调节性T细胞和髓源性抑制细胞的增殖。我们建议,YM155 和 IL-2 的组合可以作为 RCC 患者的潜在治疗方式进行测试。[3] |
| 分子式 |
C20H19N4O3+.CL-
|
|---|---|
| 分子量 |
398.84286
|
| 精确质量 |
398.115
|
| 元素分析 |
C, 60.23; H, 4.80; Cl, 8.89; N, 14.05; O, 12.03
|
| CAS号 |
355406-09-6
|
| 相关CAS号 |
Sepantronium bromide;781661-94-7
|
| PubChem CID |
23108256
|
| 外观&性状 |
Light brown to brown solid powder
|
| tPSA |
77.96
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
571
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
NUZWGSASIPTGSA-UHFFFAOYSA-M
|
| InChi Code |
InChI=1S/C20H19N4O3.ClH/c1-13-23(9-10-27-2)17-18(24(13)12-14-11-21-7-8-22-14)20(26)16-6-4-3-5-15(16)19(17)25;/h3-8,11H,9-10,12H2,1-2H3;1H/q+1;/p-1
|
| 化学名 |
1-(2-methoxyethyl)-2-methyl-3-(pyrazin-2-ylmethyl)benzo[f]benzimidazol-3-ium-4,9-dione;chloride
|
| 别名 |
YM-155 hydrochloride; 355406-09-6; YM-155 (hydrochloride); 1-(2-methoxyethyl)-2-methyl-4,9-dioxo-3-(pyrazin-2-ylmethyl)-4,9-dihydro-1H-naphtho[2,3-d]imidazol-3-ium chloride; Sepantronium (hydrochloride); 1-(2-methoxyethyl)-2-methyl-3-(pyrazin-2-ylmethyl)benzo[f]benzimidazol-3-ium-4,9-dione;chloride; YM-155hydrochloride; YM-155 (chloride);
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5073 mL | 12.5364 mL | 25.0727 mL | |
| 5 mM | 0.5015 mL | 2.5073 mL | 5.0145 mL | |
| 10 mM | 0.2507 mL | 1.2536 mL | 2.5073 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05263583 | Recruiting | Drug: Sepantronium Bromide | Burkitt Lymphoma Lymphoma, B-Cell |
Cothera Bioscience, Inc | December 9, 2022 | Phase 2 |
| NCT01023386 | Completed | Drug: YM155 | Cancer | Astellas Pharma Inc | November 2009 | Phase 1 |
| NCT01007292 | Completed | Drug: YM155 Biological: Rituximab |
Non-Hodgkin's Lymphoma | Novartis Pharmaceuticals | November 2009 | Phase 2 |
| NCT01009775 | Completed | Drug: YM155 Drug: Docetaxel |
Melanoma | Astellas Pharma Inc | November 2009 | Phase 2 |
| NCT01038804 | Completed | Drug: YM155 Drug: Docetaxel |
Breast Cancer | Astellas Pharma Inc | December 2009 | Phase 2 |