| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
CSF-1R (IC50 = 1 nM); c-Kit (IC50 = 3.2 μM); PDGFRβ (IC50 = 4.8 μM); Flt3 (IC50 = 9.1 μM)
|
|---|---|
| 体外研究 (In Vitro) |
体外活性:在骨髓源性巨噬细胞 (BMDM) 中,BLZ945 特异性抑制 CSF-1 依赖性增殖,EC50 为 67nM,并降低 CSF-1R 磷酸化。 BLZ945 阻断巨噬细胞和神经胶质瘤细胞之间对彼此存活、增殖和/或极化的相互作用,从而促进肿瘤发生。激酶测定:BLZ945 是一种有效的、口服生物活性的、选择性的 CSF-1R(集落刺激因子 1 受体)抑制剂,IC50 为 1 nM,对其最接近的受体酪氨酸激酶同源物的选择性超过 1000 倍。细胞测定:使用MTT细胞增殖试剂盒测定细胞生长速率。简而言之,将细胞一式三份接种在 96 孔板中:神经胶质瘤细胞系每孔 1,000 个细胞,BMDM 和 CRL-2467 每孔 5 x 1,000 个细胞,HUVEC 和 HBMEC 细胞系每孔 2.5 x 1,000 个细胞。对于所有实验,介质每 48 小时更换一次。细胞在存在或不存在 6.7–6,700 nM BLZ945 或 8 μg/mL CSF-1R 中和抗体的情况下生长。 BMDM 和 CRL-2467 细胞分别补充 10 ng/mL 和 30 ng/mL 重组小鼠 CSF-1。根据制造商的方案,使用读板器通过比色分析检测 MTT 底物的还原,并在 SpectraMax 340pc 读板器上在 595 nm 和 750 nm 处进行测量。
|
| 体内研究 (In Vivo) |
在患有神经胶质瘤的小鼠中,BLZ945 通过抑制 CSF-1R 来阻止肿瘤进展并显着提高生存率。 BLZ945 还在体内抑制患者源性原神经肿瘤球和细胞系的原位肿瘤生长。 BLZ945(200 mg/kg,口服)可降低小鼠乳腺肿瘤病毒驱动的多瘤病毒中 T 抗原 (MMTV-PyMT) 乳腺癌模型和表达角蛋白 14 的人乳头瘤病毒 16 型 (K14-HPV- 16)宫颈癌转基因模型。
|
| 酶活实验 |
BLZ945 是一种有效的、口服生物活性的、选择性的 CSF-1R(集落刺激因子 1 受体)抑制剂,IC50 为 1 nM,对其最接近的受体酪氨酸激酶同源物的选择性超过 1000 倍。
BLZ945, CSF-1R酪氨酸激酶的高选择性小分子抑制剂(比其他酪氨酸激酶高3200倍);参考文献27)。在体外阻断实验中,将BLZ945和GW2580分别溶于10 mmol/L和1 mmol/L的DMSO中制备原液。在体内治疗方面,根据先前的研究,BLZ945溶解在20% Captisol中,剂量为16 mg/mL,每日灌胃剂量为200 mg/kg。[3] 细胞因子分析:在卡罗林斯卡大学医院的核心设施中,通过27参数Luminex多路试验 分析从SK-N-BE(2)、SK-N-AS或SK-N-FI神经母细胞瘤细胞系中收集的培养基或上清液中的细胞因子含量。采用ELISA法测定中药中人或鼠M-CSF (CSF-1)的浓度。[3] |
| 细胞实验 |
CD34+造血祖细胞的分化[3]
采用含有50 ng/mL GM-CSF和5 ng/mL tnf - α的900 μL培养基,24孔板培养CD34+细胞。或者,从上述三种人类神经母细胞瘤细胞系中收集的上清液以2:1的比例添加到祖细胞中。以培养液中维持的CD34+细胞为对照。为了阻断CSF-1R信号,将Sotuletinib (BLZ945) (500 nmol/L)添加到细胞因子成熟的细胞中或细胞因子与SK-N-BE(2)结合的上清液中。7天后,通过清洗和轻轻刮拭收集所有细胞,并通过流式细胞术或基于cfse的t细胞增殖试验评估细胞的表型和功能。 人单核细胞-肿瘤共培养[3] 原代人单核细胞与人神经母细胞瘤细胞系共培养。简而言之,将单核细胞与4×105 SK-N-BE(2)、SK-N-AS或6×105 SK-N-FI神经母细胞瘤细胞在3ml培养基中的6孔板中共培养。未培养肿瘤细胞的单核细胞作为对照。64小时后,通过大力清洗细胞,然后轻轻刮板收获细胞。流式细胞术评价细胞表型变化,用微珠和质谱柱对HLA-DR+细胞进行分选。为了研究CSF-1R的作用,将500 μmol/L Sotuletinib (BLZ945) 或1 μmol/L GW2580加入到单核细胞或共培养中。 小鼠骨髓细胞的分化[3] 抑制性骨髓细胞是根据先前描述的方案,从负基因型TH-MYCN小鼠的骨髓细胞中诱导的。简言之,将1×106分离的骨髓细胞在NHO2A肿瘤条件培养基(中药,1:1稀释至新鲜培养基)存在的6孔板中培养。作为对照,细胞在新鲜培养基或M-CSF (20 ng/mL)中培养。为了阻断CSF-1R信号,在培养物中加入1 μmol/L的Sotuletinib (BLZ945) 或GW2580,并加入DMSO作为对照。4天后,通过收集浮细胞和仔细刮拭孔贴壁细胞的方法收获细胞,随后进行流式细胞术分析或t细胞抑制实验。 |
| 动物实验 |
小鼠:使用游标卡尺测量肿瘤体积,计算公式为:体积 = (宽度)² × 长度/2。在 MMTV-PyMT 小鼠研究中,56-63 日龄雌性小鼠分别接受 200 mg/kg 的 sotuletinib 或 20% Captisol 溶剂。根据肿瘤大小将小鼠随机分组。每周测量两次肿瘤体积,每日灌胃给药一次。每五天腹腔注射一次大鼠 IgG 对照或 5A1 大鼠抗小鼠 CSF1 中和抗体,剂量为 10 mg/kg。将 MMTV-PyMT 转基因小鼠的福尔马林固定石蜡包埋肺组织进行连续切片,并用苏木精-伊红染色,以确定肺转移情况。肿瘤区域的评估基于肿瘤大小(肿瘤直径)、肿瘤负荷(肿瘤总面积除以肺总面积)以及以单盲方式计数的单个转移灶总数。最终值取自整个肺深度的平均值。
原位同种异体移植模型[2] 使用6-7周龄的雌性FVB/NJ小鼠和6-7周龄的雌性BALB/c裸鼠(CAnN.Cg-Foxn1nu/Crl)。对于乳腺肿瘤病毒驱动的多瘤病毒中T抗原(MMTV-PyMT)原位同种异体移植模型,将10-13周龄雌性转基因MMTV-PyMT小鼠的自发性肿瘤混合,并用Liberase™(Roche)进行酶消化。将所得单细胞悬液立即按指定细胞剂量原位注射到同基因雌性FVB/NJ受体小鼠的单个乳腺脂肪垫中。对于CD45同种异型研究,从10-13周龄的MMTV-PyMT转基因雌性小鼠中取出自发性肿瘤,通过钝性分离法将其分割成3 mm的立方体。在雌性BALB/c裸鼠受体小鼠的乳腺脂肪垫上做一个小切口,将2个肿瘤样本放入脂肪垫内,并用手术钉封闭。5天后,重新打开伤口取出肿瘤样本。肿瘤按以下所述进行消化和分析。供体和受体小鼠在切除和植入前5天分别接受Sotuletinib (BLZ945)或载体处理,具体方法如下所述。 CSF1信号拮抗剂在自发性肿瘤模型中的药理学研究[2] 使用游标卡尺测量肿瘤大小,并根据公式:体积 = (宽度)² × 长度/2 计算肿瘤体积。在MMTV-PyMT小鼠研究中,将56-63日龄的雌性小鼠根据肿瘤体积随机分组,并分别给予20% Captisol®溶剂或200 mg/kg的Sotuletinib (BLZ945)。每日一次灌胃给药,每周两次测量肿瘤体积。每5天腹腔注射10 mg/kg的5A1大鼠抗小鼠CSF1中和抗体或大鼠IgG对照。为了计算MMTV-PyMT转基因小鼠的肺转移情况,将福尔马林固定、石蜡包埋的肺组织进行连续切片,并用苏木精-伊红(H&E)染色。肿瘤区域的评分依据肿瘤负荷(肿瘤总面积除以肺总面积)、大小(肿瘤直径)以及以单盲方式计数的单个转移灶总数。将这些值在整个肺组织深度范围内取平均值,得到最终值。在K14-HPV16小鼠研究中,每2个月给雌性小鼠植入缓释17β-雌二醇颗粒,以诱导宫颈和阴道上皮发生鳞状细胞癌。43,44 小鼠在6月龄时(即报道的宫颈癌发病年龄)进行随机分组,并用Sotuletinib (BLZ945)治疗1个月。为了确定 K14-HPV16 转基因小鼠的宫颈肿瘤体积,将福尔马林固定石蜡包埋的宫颈组织和肿瘤进行连续切片,以单盲方式对肿瘤面积进行评分,并将这些值乘以肿瘤深度。 |
| 参考文献 |
|
| 其他信息 |
索妥替尼是一种口服生物利用度高的集落刺激因子1受体(CSF-1R;CSF1R)抑制剂,具有潜在的抗肿瘤活性。CSF1R抑制剂BLZ945选择性地与肿瘤相关巨噬细胞(TAM)上表达的CSF1R结合,阻断CSF1R的活性,并抑制CSF1R介导的信号转导通路。这抑制了TAM的活性和增殖,并重编程了现有TAM的免疫抑制特性。总之,这降低了肿瘤微环境中TAM介导的免疫抑制,重新激活了免疫系统,并增强了T细胞介导的抗肿瘤细胞反应。CSF1R,也称为巨噬细胞集落刺激因子受体(M-CSFR)和CD115(分化簇115),是其配体集落刺激因子1(CSF1)的细胞表面受体。该受体在肿瘤微环境中由肿瘤相关巨噬细胞(TAM)过度表达,并在免疫抑制和诱导肿瘤细胞增殖中发挥重要作用。
目的:神经母细胞瘤是儿童最常见的颅外实体瘤,高危患者即使接受积极的多模式治疗,预后仍然很差。神经母细胞瘤引起的炎症会导致抑制性髓系细胞的诱导,从而阻碍有效的抗肿瘤免疫反应。因此,我们试图通过消除髓系细胞介导的免疫抑制来增强抗肿瘤免疫。 实验设计:通过分析神经母细胞瘤患者的基因组数据集,证实了髓系细胞的预后价值。利用新鲜分离的人类CD34+造血干细胞、原代人单核细胞和鼠骨髓细胞,通过体外培养模型,解析了肿瘤来源因子对髓系造血和抑制性髓系细胞局部诱导的影响。为了测试 BLZ945 作为单药疗法或与免疫检查点抑制剂联合疗法的治疗效果,我们使用了一种会自发形成侵袭性神经母细胞瘤的转基因小鼠模型 (TH-MYCN)。 结果:我们发现,浸润的 CSF-1R+ 髓系细胞预示着神经母细胞瘤患者预后不良。体外实验表明,神经母细胞瘤来源的因子会干扰髓系细胞的早期发育,并通过 M-CSF/CSF-1R 相互作用赋予其对人单核细胞的抑制功能。在一种类似于高危人类神经母细胞瘤的转基因小鼠模型 (TH-MYCN) 中,使用选择性抑制剂 (BLZ945) 拮抗 CSF-1R 可以调节人和小鼠抑制性髓系细胞的诱导,并有效限制肿瘤进展。尽管免疫检查点抑制剂不足以控制肿瘤生长,但将BLZ945与PD-1/PD-L1阻断抗体联合使用可显著提高肿瘤控制效果。 结论:我们的研究结果表明CSF-1R信号通路在诱导抑制性髓系细胞过程中发挥着至关重要的作用,并强调了其作为人类癌症免疫疗法的临床潜力。[3] 肿瘤浸润巨噬细胞数量的增加与多种癌症(包括乳腺癌和前列腺癌)患者的不良预后相关。集落刺激因子1受体(CSF1R)信号通路驱动肿瘤相关巨噬细胞(TAM)募集至肿瘤微环境,并促进TAM向促肿瘤表型分化。目前有12项临床试验正在评估靶向CSF1/CSF1R信号通路的药物作为治疗多种恶性肿瘤(包括乳腺癌、白血病和胶质母细胞瘤)的疗效。研究表明,阻断 CSF1R 信号通路能够以组织特异性的方式显著降低巨噬细胞的数量。然而,为了理解巨噬细胞的耗竭机制以及 CSF1R 抑制对其他肿瘤浸润免疫细胞的整体影响,还需要进一步的机制研究。我们使用高选择性 CSF1R 小分子抑制剂 BLZ945,发现 CSF1R 抑制能够降低肿瘤相关巨噬细胞 (TAM) 的周转率,同时增加浸润宫颈癌和乳腺癌的 CD8+ T 细胞的数量。具体而言,我们发现 BLZ945 能够抑制小鼠乳腺肿瘤病毒驱动的多瘤病毒中 T 抗原 (MMTV-PyMT) 乳腺癌模型中恶性细胞的生长。此外,我们发现BLZ945能够抑制表达角蛋白14的人乳头瘤病毒16型(K14-HPV-16)转基因宫颈癌模型中的肿瘤进展。我们的结果表明,肿瘤相关巨噬细胞(TAMs)以CSF1R依赖的方式持续更新,并提示持续抑制CSF1R通路对于维持有效的巨噬细胞清除作为抗癌疗法至关重要。[2]胶质母细胞瘤(GBM)包含多种分子亚型,包括前神经型GBM。大多数靶向胶质瘤细胞的治疗方法均以失败告终。一种替代策略是靶向胶质瘤微环境中的细胞,例如肿瘤相关巨噬细胞和小胶质细胞(TAMs)。巨噬细胞的分化和存活依赖于集落刺激因子-1(CSF-1)。我们使用 CSF-1 受体 (CSF-1R) 抑制剂靶向小鼠前神经胶质母细胞瘤 (GBM) 模型中的肿瘤相关巨噬细胞 (TAM),结果显著延长了小鼠的生存期并使已形成的肿瘤消退。此外,CSF-1R 阻断还减缓了患者来源的胶质瘤异种移植瘤的颅内生长。令人惊讶的是,在接受治疗的小鼠中,TAM 并未减少。相反,胶质瘤分泌的因子,包括粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 和干扰素-γ (IFN-γ),在 CSF-1R 抑制的情况下促进了 TAM 的存活。存活的 TAM 中替代激活的 M2 标志物的表达降低,这与肿瘤促进功能的受损相一致。这些基因特征与前神经胶质母细胞瘤患者的生存期延长相关。我们的研究结果表明,TAM 是前神经胶质瘤的一个有前景的治疗靶点,并证实了 CSF-1R 抑制在 GBM 治疗中的转化应用潜力。[1] |
| 精确质量 |
434.11793
|
|---|---|
| 元素分析 |
C, 50.96; H, 5.13; Cl, 15.04; N, 11.89; O, 10.18; S, 6.80
|
| CAS号 |
2222138-40-9
|
| 相关CAS号 |
Sotuletinib;953769-46-5;Sotuletinib hydrochloride;2222138-31-8
|
| PubChem CID |
141759984
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| LogP |
125Ų
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
540
|
| 定义原子立体中心数目 |
2
|
| InChi Key |
ZIHWHYXECXSBNA-LVVRIOTCSA-N
|
| InChi Code |
InChI=1S/C20H22N4O3S.2ClH/c1-21-19(26)16-10-13(8-9-22-16)27-12-6-7-15-18(11-12)28-20(24-15)23-14-4-2-3-5-17(14)25;;/h6-11,14,17,25H,2-5H2,1H3,(H,21,26)(H,23,24);2*1H/t14-,17-;;/m1../s1
|
| 化学名 |
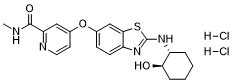
4-((2-(((1R,2R)-2-hydroxycyclohexyl)amino)benzo[d]thiazol-6-yl)oxy)-N-methylpicolinamide dihydrochloride
|
| 别名 |
Sotuletinib dihydrochloride; BLZ945; Sotuletinib hydrochloride; 2222138-31-8; Sotuletinib (hydrochloride); 4-((2-(((1R,2R)-2-Hydroxycyclohexyl)amino)benzo[d]thiazol-6-yl)oxy)-N-methylpicolinamide hydrochloride; Sotuletinib HCl?; BLZ945 HCl; BLZ945 HYDROCHLORIDE; BLZ 945; BLZ-945.Sotuletinib;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。