| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
PBP/penicillin-binding proteins
|
|---|---|
| 体外研究 (In Vitro) |
氯化头孢吡肟与青霉素结合的蛋白质结合,产生抗菌作用 [2]。
|
| 体内研究 (In Vivo) |
氯化头孢吡肟(80 mg/kg;腹腔注射)显着延长了半衰期,小鼠得以存活[4]。
|
| 动物实验 |
动物/疾病模型:雄性CD-1小鼠[4]
剂量:80 mg/kg 给药途径:腹腔注射(ip) 实验结果:在所有接受顺铂18-22 mg/kg和26 mg/kg治疗的小鼠中,头孢吡肟的半衰期均显著延长,且所有小鼠在预处理期间均存活。在接受顺铂18-22 mg/kg和26 mg/kg治疗的小鼠中,存活率显著降低,且头孢吡肟的半衰期并未显著延长。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
9名健康成年男性志愿者单次静脉输注500 mg、1 g和2 g头孢吡肟后,其血药浓度峰值(Cmax)分别为39.1、81.7和163.9 μg/mL,相应的AUC分别为70.8、148.5和284.8 h⋅μg/mL。另一方面,9名健康成年男性志愿者单次肌注500 mg、1 g和2 g头孢吡肟后,其血药浓度峰值(Cmax)分别为13.9、29.6和57.5 μg/mL,相应的AUC分别为60、137和262 h⋅μg/mL,相应的达峰时间(Tmax)分别为1.4、1.6和1.5 h。一项针对健康成年男性志愿者(n=7)的研究表明,在接受临床相关剂量头孢吡肟治疗9天后,头孢吡肟不会在体内蓄积。在250 mg至2 g剂量范围内,头孢吡肟的药代动力学符合线性模型。在接受50 mg/kg肌注的儿科患者(n=8)中,头孢吡肟的绝对生物利用度为82.3%。头孢吡肟主要经肾脏排泄,且大部分以原形排出。正常受试者服用的头孢吡肟约85%以原形经尿液排出。尿液中回收的N-甲基吡咯烷(NMP)不足1%,NMP-N-氧化物占6.8%,差向异构体占2.5%。由于肾脏排泄在头孢吡肟的清除中起着重要作用,肾功能不全患者或接受血液透析的患者需要调整剂量。 头孢吡肟的平均稳态分布容积为 18.0 L。在儿科患者中,平均稳态分布容积为 0.3 L/kg。 在健康志愿者中,头孢吡肟的总清除率为 120 mL/min;在儿科患者中,平均总清除率为 3.3 mL/min/kg。在老年患者(65 岁及以上)和肾功能异常的患者中,头孢吡肟的总清除率与肌酐清除率成正比下降。 代谢/代谢物 不到 1% 的头孢吡肟在肝脏代谢。头孢吡肟代谢为N-甲基吡咯烷(NMP),后者迅速氧化生成更稳定的化合物NMP-N-氧化物。NMP-N-氧化物是头孢吡肟的主要代谢产物,而NMP和头孢吡肟的7-差向异构体是次要的副产物。有研究表明,含黄素的混合功能加氧酶介导了NMP氧化为NMP-N-氧化物的过程。 生物半衰期 9名健康成年男性志愿者服用头孢吡肟后,其平均半衰期为2小时。在需要血液透析的患者中,平均半衰期为 13.5 小时;在需要持续腹膜透析的患者中,平均半衰期为 19 小时。 吸收 9 名健康成年男性志愿者单次静脉输注 500 mg、1 g 和 2 g 头孢吡肟后,相应的 Cmax 分别为 39.1、81.7 和 163.9 μg/mL,相应的 AUC 分别为 70.8、148.5 和 284.8 h⋅μg/mL。另一方面,健康成年男性志愿者单次肌注500 mg、1 g和2 g头孢吡肟后,其血药浓度峰值(Cmax)分别为13.9、29.6和57.5 μg/mL,曲线下面积(AUC)分别为60、137和262 h·μg/mL,达峰时间(Tmax)分别为1.4、1.6和1.5 h。一项针对7名健康成年男性志愿者进行的为期9天的临床相关剂量研究表明,头孢吡肟不会在体内蓄积。在 250 mg 至 2 g 的剂量范围内,头孢吡肟遵循线性药代动力学模型。在接受 50 mg/kg 肌注的儿科患者(n=8)中,头孢吡肟的绝对生物利用度为 82.3%。 消除途径 头孢吡肟主要经肾脏排泄,大部分以原形排出。正常受试者服用的头孢吡肟约 85% 以原形经尿液排出。不到 1% 的给药剂量以 N-甲基吡咯烷 (NMP) 的形式从尿液中回收,6.8% 以 NMP-N-氧化物的形式回收,2.5% 以差向异构体的形式回收。由于肾脏排泄在头孢吡肟的清除中起着重要作用,肾功能不全患者或接受血液透析的患者需要调整剂量。 分布容积 头孢吡肟的平均稳态分布容积为 18.0 L。在儿科患者中,平均稳态分布容积为 0.3 L/kg。 清除率 在健康志愿者中,头孢吡肟的总清除率为 120 mL/min;在儿科患者中,平均总清除率为 3.3 mL/min/kg。在老年患者(65岁及以上)和肾功能异常的患者中,头孢吡肟的总清除率与肌酐清除率成正比下降。 蛋白结合 头孢吡肟的血清蛋白结合率约为20%,与其血清浓度无关。 代谢/代谢物 不到1%的头孢吡肟在肝脏代谢。头孢吡肟代谢为N-甲基吡咯烷(NMP),NMP随后迅速氧化生成更稳定的化合物NMP-N-氧化物。NMP-N-氧化物是头孢吡肟的主要代谢物,而NMP和头孢吡肟的7-差向异构体是次要的副产物。有研究表明,含黄素的混合功能加氧酶介导NMP氧化为NMP-N-氧化物。 生物半衰期 接受头孢吡肟治疗的健康成年男性志愿者(n=9)的平均半衰期为2小时。需要血液透析的患者的平均半衰期为13.5小时,需要持续腹膜透析的患者的平均半衰期为19小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概述 虽然目前尚无关于哺乳期使用头孢吡肟的公开信息,但其在母乳中的浓度似乎较低,通常情况下,头孢菌素类药物不会对母乳喂养的婴儿造成严重不良反应。有报道称,头孢菌素类药物偶尔会扰乱婴儿的胃肠道菌群,导致腹泻或鹅口疮,但这些影响尚未得到充分评估。哺乳期妇女可以安全使用头孢吡肟。尚未在哺乳期妇女中研究过头孢吡肟和恩美他唑巴坦的联合用药,但其不良反应应与哺乳期妇女相同。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 头孢吡肟的血清蛋白结合率约为20%,与其血清浓度无关。 毒性概述 如怀疑过量用药,临床医生应停药或调整剂量。确定症状是由头孢吡肟过量还是由既有的合并症引起可能较为困难。如果高度怀疑或调整剂量或停药后症状未消退,应进行血液和脑脊液检测,以评估毒性是否由头孢吡肟水平升高引起。头孢吡肟引起的神经毒性 (CIN) 可导致脑电图出现广泛性周期性放电和三相波模式。严重病例可能需要透析。 不良反应 成人和儿童患者通常对头孢吡肟耐受性良好。成人最常见的不良反应是腹泻和皮疹。儿童最常见的不良反应是发热、腹泻和皮疹。 根据受影响的系统,还有许多其他不太常见的不良反应: 神经系统:头痛、发热和神经毒性 胃肠道:恶心、呕吐、腹痛、肝损伤、结肠炎(包括假膜性结肠炎)、口腔念珠菌病 泌尿生殖系统:阴道炎、肾损伤 皮肤:局部注射部位刺激、瘙痒、荨麻疹、Stevens-Johnson综合征和多形性红斑 血液系统:Coombs试验阳性但无溶血、全血细胞减少症和再生障碍性贫血 不良反应通常在停药后消退。 神经毒性是一种严重的、危及生命的不良反应,值得特别关注。症状可能包括精神状态改变、脑病、癫痫发作、肌阵挛、幻觉、昏迷和类似中风的症状。症状通常在开始使用头孢吡肟后4天出现。危险因素包括肾功能衰竭(肌酐≤60 mL/min)、老年患者、ICU危重患者、中风、阿尔茨海默病、脑恶性肿瘤、癫痫病史以及血脑屏障(BBB)受损。推测的机制是头孢吡肟可以穿过血脑屏障并拮抗γ-氨基丁酸受体。 治疗方法包括停药、使用苯二氮卓类药物控制癫痫发作,或在严重难治性病例中进行肾脏替代治疗。临床团队必须监测肾功能并根据肾功能调整剂量;然而,肾功能正常的患者也有神经毒性的报道。 药物相互作用 使用头孢吡肟时存在显著的药物相互作用。头孢吡肟与氨基糖苷类抗生素合用会增加细胞毒性和肾毒性的风险。头孢菌素类(如头孢吡肟)与强效利尿剂(如呋塞米)合用可导致肾毒性。当患者服用这些药物时,应监测肾功能。 头孢吡肟可导致尿糖假阳性;建议采用基于葡萄糖氧化酶反应的尿糖检测方法。 不建议将头孢吡肟与膀胱癌的膀胱内灌注卡介苗同时使用,因为这可能会对膀胱癌的治疗效果产生不利影响。 不建议同时接种霍乱疫苗和伤寒疫苗,因为疫苗效力会降低。 |
| 参考文献 |
|
| 分子式 |
C19H25CLN6O5S2
|
|---|---|
| 分子量 |
517.022000074387
|
| 精确质量 |
516.101638
|
| CAS号 |
107648-79-3
|
| 相关CAS号 |
Cefepime;88040-23-7; Cefepime Dihydrochloride Monohydrate;123171-59-5; Cefepime chloride;107648-79-3; 107648-78-2 (sulfate); 103296-32-8 (compound E); 123171-59-5 (2HCl hydrate);107648-80-6 (2HCl)
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| tPSA |
201 Ų
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
11
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
33
|
| 分子复杂度/Complexity |
874
|
| 定义原子立体中心数目 |
2
|
| SMILES |
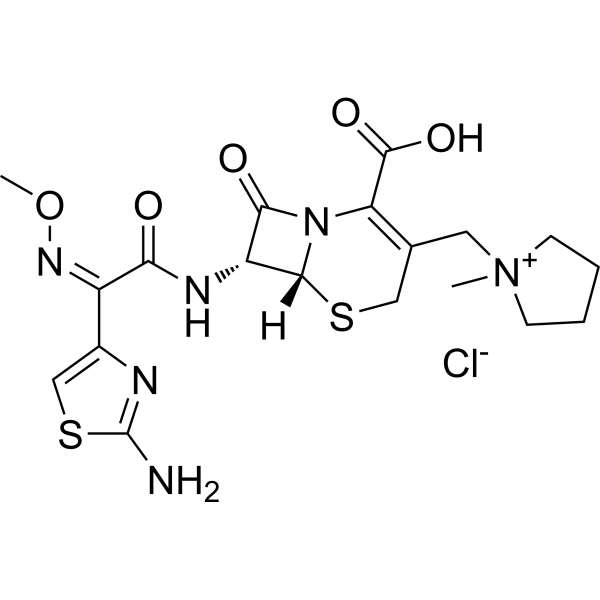
[Cl-].S1CC(=C(C(=O)O)N2C([C@H]([C@@H]12)NC(/C(/C1=CSC(N)=N1)=N\OC)=O)=O)C[N+]1(C)CCCC1
|
| InChi Key |
MMRINLZOZVAPDZ-LSGRDSQZSA-N
|
| InChi Code |
InChI=1S/C19H24N6O5S2.ClH/c1-25(5-3-4-6-25)7-10-8-31-17-13(16(27)24(17)14(10)18(28)29)22-15(26)12(23-30-2)11-9-32-19(20)21-11;/h9,13,17H,3-8H2,1-2H3,(H3-,20,21,22,26,28,29);1H/b23-12-;/t13-,17-;/m1./s1
|
| 化学名 |
(6R,7R)-7-[[(2Z)-2-(2-amino-1,3-thiazol-4-yl)-2-methoxyiminoacetyl]amino]-3-[(1-methylpyrrolidin-1-ium-1-yl)methyl]-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid chloride
|
| 别名 |
Cefepime (chloride); 107648-79-3; 1-(((6R,7R)-7-((Z)-2-(2-Aminothiazol-4-yl)-2-(methoxyimino)acetamido)-2-carboxy-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-en-3-yl)methyl)-1-methylpyrrolidin-1-ium chloride; orb1744769;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9342 mL | 9.6708 mL | 19.3416 mL | |
| 5 mM | 0.3868 mL | 1.9342 mL | 3.8683 mL | |
| 10 mM | 0.1934 mL | 0.9671 mL | 1.9342 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Comparative Study To Determine The Efficacy, Safety, And Tolerability Of Ceftolozane-Tazobactam
CTID: NCT03485950
Phase: Phase 2 Status: Completed
Date: 2022-03-15