| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
Cannabinoid receptor
|
|---|---|
| 体外研究 (In Vitro) |
CP55940以独立的浓度方式恢复线粒体膜电位(ΔΨm)并抑制PSEN1 E280A ChLN中ROS的产生。[2]
CP55940以CB1受体非依赖的方式恢复ΔΨm,但减少PSEN1 E280A ChLN中部分依赖CB1受体的ROS产生。[2] CP55940以CB1Rs非依赖的方式减少细胞内sAβPPβf聚集,但它减少了PSEN1 E280A ChLN中部分依赖CB1Rs的氧化DJ-1。[2] CP55940以独立于CB1Rs的方式阻断PSEN1 E280A ChLN的凋亡。[2] CP55940以独立于CB1Rs的方式抑制tau磷酸化PSEN1 E280A ChLN。[2] CP55940降低了PSEN 1 E280A ChLN中独立于CB1Rs的eAβ42蛋白片段的水平。[2] CP55940不能恢复PSEN1 E280A ChLN中的Ca2+失调。[2] BAY 59-3074[3-[2-氰基-3-(三氟甲基)苯氧基]苯基-4,4,4-三氟-1-丁烷磺酸盐]是一种结构新颖的大麻素CB1/CB2受体部分激动剂,具有镇痛作用。[1] 在两种反向激动剂(以下简称SR)存在的情况下,CP几乎完全抑制了细胞内sAβPPβf和p-Tau的聚集,增加了ΔΨm,减少了DJ-1Cys106-SH残基的氧化,并阻断了突变ChLN中c-Jun、p53、PUMA和caspase-3的激活,与CB1Rs信号传导无关。CP还抑制部分依赖CB1R的活性氧物种的产生。尽管CP降低了细胞外Aβ42,但它无法逆转突变ChLN对乙酰胆碱刺激的Ca2+内流失调反应。在SR加CP存在或不存在的情况下,暴露于抗Aβ抗体6E10(1:300)完全恢复了突变ChLN对乙酰胆碱的瞬时[Ca2+]i信号。[2] |
| 体内研究 (In Vivo) |
本研究旨在通过高灵敏度的体内试验确认其受体结合谱。在28次训练后,大鼠(n=10)学会了以固定比例(10,食物强化双杠杆程序)区分BAY 59-3074(0.5mg/kg,口服,t-1h)和载体。BAY 59-3074呈全身剂量依赖性(ED(50):0.081 mg/kg,口服),给药后0.25至4小时可检测到提示。选择性大麻素CB1受体拮抗剂SR 141716A[N-(哌啶-1-基)-5-(4-氯苯基)-1-(2,4-二氯苯基)-4-甲基-1H-吡唑-3-甲酰胺盐酸盐]阻断了BAY 59-3074的鉴别作用(ID50:1.79mg/kg,i.p.)。
腹腔注射BAY 59-3074(ED50值:0.41 mg/kg)和参考大麻素BAY 38-7271[(-)-(R)-3-(2-羟基甲基茚基-4-氧基)苯基-4,4,4-三氟-1-丁磺酸酯,0.011 mg/kg]、CP 55940[(-”-顺-3-[2-羟基-4(1,1-二甲基庚基)苯基]-反-4-(3-羟基丙基)环己醇,0.013 mg/kg]、HU-210[(-WIN55212-2[(R)-4,5-二氢-2-甲基-4(4-吗啉基甲基)-1-(1-萘羰基)-6H-吡咯并[3,2,1-ij]喹啉-6-酮,0.41mg/kg]和(-)-Delta9-四氢大麻酚(0.41mg/kg)。具有镇痛作用的非大麻素,如吗啡、阿米替林、卡马西平、加巴喷丁和巴氯芬,并没有推广到这一线索。结果表明,BAY 59-3074的鉴别刺激作用是由大麻素CB1受体激活特异性介导的[1]。
|
| 酶活实验 |
受体结合试验。[3]
1.CB1测定。使用中国仓鼠卵巢(CHO)细胞的膜制剂测定CB1受体亲和力,其中人大麻素CB1受体与[3H]CP 55940作为放射性配体稳定转染19。在将新制备的细胞膜制剂与[3H]-放射性配体孵育后,加入或不加入测试化合物,通过玻璃纤维过滤器过滤进行结合配体和游离配体的分离。通过液体闪烁计数测量过滤器上的放射性。将至少三次独立测量的IC50值合并,并使用Cheng和Prusoff的假设转换为Ki值。 CB2测定。[3] 使用中国仓鼠卵巢(CHO)细胞的膜制剂测定CB2受体亲和力,其中人大麻素CB2受体与[3H]CP 55940作为放射性配体稳定转染。在将新制备的细胞膜制剂与[3H]-放射性配体孵育后,加入或不加入测试化合物,通过玻璃纤维过滤器过滤进行结合配体和游离配体的分离。通过液体闪烁计数测量过滤器上的放射性。将至少两次独立测量的IC50值合并,并使用Cheng和Prusoff的假设转换为Ki值。 体外药理学。[3] 花生四烯酸释放的测量。用克隆在中国仓鼠卵巢(CHO)细胞中的人CB1受体评估CB1受体拮抗作用。CHO细胞在添加了10%热灭活胎牛血清的Dulbecco改良Eagle培养基(DMEM)培养基中生长。吸取培养基,用DMEM代替,不含胎牛血清,但含有[3H]-花生四烯酸,并在细胞培养炉中孵育过夜(5%CO2/95%空气;37°C;水饱和气氛)。在此期间,[3H]-花生四烯酸被掺入膜磷脂中。在测试日,吸出培养基,用0.5mL含0.2%牛血清白蛋白(BSA)的DMEM洗涤细胞三次。WIN 55212-2刺激CB1受体导致PLA2激活,随后[3H]-花生四烯酸释放到培养基中。这种WIN 55212-2诱导的释放被CB1受体拮抗剂浓度依赖性地拮抗。试验化合物的CB1拮抗效力表示为pA2值。 P-糖蛋白测定。[3] 评估了人MDR1 P-糖蛋白泵在PK1 LLC MDR细胞单层上转移化合物的能力。使用文献31中基本描述的运输方法。在实验开始时,以1μg/mL的浓度将化合物添加到细胞层的一侧。测量了底部到顶部的运输以及顶部到底部的运输。P-糖蛋白(Pgp)因子表示为自下而上运输和自上而下运输的比率。膜通过率表示为在添加化合物后3小时从底部到顶部和从顶部到底部运输的化合物的平均百分比。使用LC/MS法进行化合物检测。 |
| 细胞实验 |
细胞分析[2]
检测方案[2] WT和PSEN1 E280A ChLNs细胞培养测定的方法是相同的。初始CP 55940筛选在10 nM和1μM之间进行了至少两次,一式三次。随后,确定CP 55940(1μM)为进一步实验的最佳浓度。ChLN分为四组:1)未治疗组;2) 分别用终浓度为1μM的SR141716(CB1受体反向激动剂)和SR144528(CB2受体反向激动器)治疗(以下简称SR);3) CP 55940(或CP);4) RS+CP55940(也称为SR+CP鸡尾酒)。为了阻断eAβ42,在分化后,在有或没有CP或CP+RS的情况下,将野生型和突变型ChLN与抗Aβ42抗体6E10(RCm中1:300)一起孵育四天。 野生型(WT)和PSEN1 ChLN仅暴露于CP(1μM)或在CB1和CB2受体(CB1R、CB2Rs)反向激动剂SR141716(1μM)和SR144528(1μM.)存在的情况下暴露24小时。对未治疗或治疗的神经元进行生化和功能分析评估[2]。 |
| 动物实验 |
体内药理学。1. CP 55940 诱导大鼠低血压。雄性正常血压大鼠(225-300 g;Harlan,荷兰霍斯特)用戊巴比妥钠(80 mg/kg,腹腔注射)麻醉。通过插入左侧颈动脉的套管,使用 Spectramed DTX-plus 压力传感器(Spectramed BV,荷兰比尔特霍芬)测量血压。经 Nihon Kohden 载波放大器(AP-621G 型;Nihon Kohden BV,荷兰阿姆斯特丹)放大后,血压信号通过 Po-Ne-Mah 数据采集程序(Po-Ne-Mah Inc.,美国斯托尔斯)记录到个人电脑(Compaq Deskpro 386s)上。心率由脉动压力信号计算得出。所有化合物均以1%甲基纤维素微混悬液的形式口服给药,于麻醉诱导前30分钟给药,麻醉诱导后60分钟给予CB1受体激动剂CP-55,940。注射体积为10 mL/kg。血流动力学稳定后,静脉注射CB1受体激动剂CP-55,940(0.1 mg/kg),并观察到降压作用22。与溶媒对照组相比,CP-55,940给药后的典型血压约为60%[3]。
|
| 参考文献 |
[1]. Eur J Pharmacol.2004 Nov 28;505(1-3):127-33.
[2]. J Alzheimers Dis. 2021; 82(Suppl 1): S359–S378. [3]. J Med Chem. 2004 Jan 29;47(3):627-43. |
| 其他信息 |
合成了一系列新型3,4-二芳基吡唑啉类化合物,并对其在人CB1和人CB2受体活性进行了评价。这些3,4-二芳基吡唑啉类化合物表现出强效的体外CB1受体拮抗活性,且总体上对CB1和CB2受体亚型具有较高的选择性。一些关键化合物在口服给药后,在CB1受体激动剂诱导的血压升高模型和CB2受体激动剂诱导的体温过低模型中均显示出显著的体内药理活性。通过对消旋体67进行手性分离,并结合结晶和X射线衍射分析,确定了其对映体80(SLV319)在C4位的绝对构型为4S。生物分析研究显示,候选药物 80 的中枢神经系统/血浆浓度比值较高。分子建模研究表明,80 与已知的 CB(1) 受体拮抗剂利莫那班 (SR141716A) 具有较为接近的三维结构重叠。对 80 的 X 射线衍射数据进行进一步分析,发现其分子内存在氢键,这一发现也得到了计算方法的证实。计算模型和 X 射线衍射数据表明,体内无活性化合物 6 的分子内氢键模式与 80 不同。此外,对 6 的 X 射线衍射研究表明,其分子间堆积比 80 更紧密,这可能也是其体内吸收较差的原因之一。用 -NHCH(3) 基团取代脒基 -NH(2) 部分被证明是提高该系列化合物口服生物利用度的关键改变,最终鉴定出化合物 80。[3]
背景:阿尔茨海默病 (AD) 的特征是胆碱能神经元 (ChN) 的结构损伤、死亡和功能障碍,这是由于细胞内淀粉样β蛋白 (Aβ) 聚集、细胞外神经炎性斑块以及 tau 蛋白 (p-Tau) 的过度磷酸化所致。目的:评估合成大麻素 CP 55940 (CP) 对 PSEN1 E280A 胆碱能样神经细胞 (PSEN1 ChLN)(一种家族性 AD 的天然模型)的影响。方法:将野生型 (WT) 和 PSEN1 ChLN 单独暴露于 CP (1μM) 或在存在以下情况时暴露于 CP:分别用CB1和CB2受体(CB1R、CB2R)的反向激动剂SR141716(1μM)和SR144528(1μM)处理24小时。对未经处理或已处理的神经元进行生化和功能分析。结果:在两种反向激动剂(以下简称SR)存在的情况下,CP几乎完全抑制了细胞内sAβPPβf和p-Tau的聚集,增加了线粒体膜电位(ΔΨm),降低了DJ-1Cys106-SH残基的氧化,并阻断了突变型ChLN中c-Jun、p53、PUMA和caspase-3的激活,且该作用独立于CB1R信号通路。CP还抑制了活性氧的产生,该作用部分依赖于CB1R。尽管CP降低了细胞外Aβ42水平,但它无法逆转突变型ChLNs中乙酰胆碱刺激引起的Ca2+内流失调。在有或无SR加CP的情况下,用抗Aβ抗体6E10(1:300)处理突变型ChLNs,可完全恢复乙酰胆碱刺激引起的瞬时[Ca2+]i信号。结论:综上所述,我们的研究结果表明,大麻素、CB1R反向激动剂和抗Aβ抗体的联合应用可能是一种有前景的家族性AD治疗方法。[2] BAY 59-3074 [3-[2-氰基-3-(三氟甲基)苯氧基]苯基-4,4,4-三氟-1-丁烷磺酸盐]是一种结构新颖的大麻素CB1/CB2受体部分激动剂,具有镇痛作用。本研究旨在通过高灵敏度的体内实验验证其受体结合特性。大鼠(n=10)在固定比例为10的食物强化双杆实验中,经过平均28次训练后,学会区分BAY 59-3074(0.5 mg/kg,口服,t-1 h)和溶剂对照。BAY 59-3074的泛化作用呈剂量依赖性(ED50:0.081 mg/kg,口服),且给药后0.25至4小时内均可检测到信号。选择性大麻素 CB1 受体拮抗剂 SR 141716A [N-(哌啶-1-基)-5-(4-氯苯基)-1-(2,4-二氯苯基)-4-甲基-1H-吡唑-3-甲酰胺盐酸盐] 阻断了 BAY 59-3074 的辨别作用(ID50:1.79 mg/kg,腹腔注射)。腹腔注射 BAY 59-3074(ED50 值:0.41 mg/kg)后,以及参考大麻素 BAY 38-7271 [(-)-(R)-3-(2-羟甲基茚基-4-氧基)苯基-4,4,4-三氟-1-丁烷磺酸盐,0.011 mg/kg]、CP 55940 [(-)-顺式-3-[2-羟基-4-(1,1-二甲基庚基)苯基]-反式-4-(3-羟基丙基)环己醇,0.013 mg/kg]、HU-210 [(-)-11-OH-Δ8-四氢大麻酚二甲基庚基,0.022 mg/kg]、WIN 55,212-2 后,均获得了完全泛化。 [(R)-4,5-二氢-2-甲基-4(4-吗啉基甲基)-1-(1-萘基羰基)-6H-吡咯并[3,2,1-ij]喹啉-6-酮,0.41 mg/kg] 和 (-)-Δ9-四氢大麻酚 (0.41 mg/kg)。具有镇痛作用的非大麻素类药物,如吗啡、阿米替林、卡马西平、加巴喷丁和巴氯芬,均未泛化至该线索。由此得出结论,BAY 59-3074 的辨别性刺激效应是由大麻素 CB1 受体激活特异性介导的。[1] |
| 分子式 |
C24H40O3
|
|---|---|
| 分子量 |
376.57
|
| 精确质量 |
376.297
|
| 元素分析 |
C, 76.55; H, 10.71; O, 12.75
|
| CAS号 |
83002-04-4
|
| PubChem CID |
104895
|
| 外观&性状 |
Typically exists as solid at room temperature
|
| 密度 |
1.0±0.1 g/cm3
|
| 沸点 |
494.4±45.0 °C at 760 mmHg
|
| 闪点 |
209.2±23.3 °C
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
| 折射率 |
1.526
|
| LogP |
5.97
|
| tPSA |
60.69
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
408
|
| 定义原子立体中心数目 |
3
|
| SMILES |
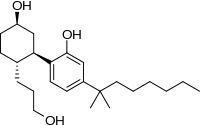
CCCCCCC(C)(C)C1=CC(=C(C=C1)[C@@H]2C[C@@H](CC[C@H]2CCCO)O)O
|
| InChi Key |
YNZFFALZMRAPHQ-SYYKKAFVSA-N
|
| InChi Code |
InChI=1S/C24H40O3/c1-4-5-6-7-14-24(2,3)19-11-13-21(23(27)16-19)22-17-20(26)12-10-18(22)9-8-15-25/h11,13,16,18,20,22,25-27H,4-10,12,14-15,17H2,1-3H3/t18-,20-,22-/m1/s1
|
| 化学名 |
2-[(1R,2R,5R)-5-hydroxy-2-(3-hydroxypropyl)cyclohexyl]-5-(2-methyloctan-2-yl)phenol
|
| 别名 |
CP55940; CP-55940; 83003-12-7; 83002-04-4; 2-[(1r,2r,5r)-5-hydroxy-2-(3-hydroxypropyl)cyclohexyl]-5-(2-methyloctan-2-yl)phenol; CP55,940; CP-55,940; 8YX8JK1BQG;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6555 mL | 13.2777 mL | 26.5555 mL | |
| 5 mM | 0.5311 mL | 2.6555 mL | 5.3111 mL | |
| 10 mM | 0.2656 mL | 1.3278 mL | 2.6555 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。